卡培他滨联合常规化疗对乳腺肿瘤患者淋巴结转移及肿瘤标志物水平的影响
边志清,白晓慧,王甜甜
1.陕西省榆林市第二医院肿瘤科/放疗科,陕西榆林 719000;2.陕西省宝鸡市妇幼保健院药剂科,陕西宝鸡 721000
乳腺肿瘤是一种女性恶性肿瘤,内分泌治疗、手术、放化疗等是临床通常采用的治疗手段,但是有复发或转移发生的患者占总数的50%左右[1],对患者的生命安全造成了严重威胁,极易引发乳腺癌患者死亡。目前,临床重点研究了乳腺癌患者治疗后降低转移率、复发率的方法[2]。卡培他滨片继承了氟尿嘧啶(5-FU)广谱的抗肿瘤活性,同时又具备了口服化疗安全方便的优越性。卡培他滨是治疗癌症和恶性肿瘤常用药物之一,是由瑞士罗氏公司研制的一种新型选择性靶向口服抗肿瘤药。卡培他滨片治疗乳腺癌的效果较好,安全性高。本文研究了乳腺肿瘤治疗中卡培他滨联合常规化疗对患者淋巴结转移及肿瘤标志物水平的影响。
1 资料与方法
1.1一般资料 回顾性选取2017年2月至2021年2月榆林市第二医院肿瘤科/放疗科乳腺肿瘤患者100例,分为两组。联合治疗组50例患者年龄32~69岁,平均(53.14±9.25)岁。在病程方面,1~<4年24例(46.00%),4~7年26例(52.00%);在病理分期方面,Ⅱ期33例(66.00%),Ⅲ+Ⅳ期17例(34.00%);在淋巴结转移情况方面,有转移19例,无转移31例;在绝经情况方面,绝经前患者23例(46.00%),绝经后患者27例(54.00%)。常规化疗组50例患者年龄33~70岁,平均(54.06±9.46)岁。在病程方面,1~<4年23例(46.00%),4~7年27例(54.00%);在病理分期方面,Ⅱ期32例(64.00%),Ⅲ+Ⅳ期18例(36.00%);在淋巴结转移情况方面,有20例,无30例;在绝经情况方面,绝经前患者24例(48.00%),绝经后患者26例(52.00%)。两组患者的一般资料比较差异无统计学意义(P>0.05)。本研究通过医院医学伦理委员会批准,患者均知情同意。
1.2纳入和排除标准 纳入标准:(1)均符合乳腺肿瘤的诊断标准[3];(2)内分泌指标和人表皮生长因子受体-2(HER2)指标均为阴性。排除标准:(1)复发乳腺癌;(2)合并其他部位原发肿瘤;(3)有药物过敏史。
1.3方法
1.3.1常规化疗组 采用CMF化疗方案,化疗前6、12 h分别让患者口服0.75 mg地塞米松,化疗前30 min给予患者静脉注射20 mg苯海拉明+10 mg地塞米松。化疗第1天给予患者静脉注射80 mg/m2表柔比星+75 mg/m2多西紫杉醇。
1.3.2联合治疗组 同时让患者口服卡培他滨片(上海罗氏制药有限公司,产品规格:0.5 g×12片),体表面积<1.25 m2、1.25~1.5 m2、>1.5 m2患者的剂量分别为1 000、1 500、2 000 mg,每天2次。两组均治疗3周为1个周期,共治疗6个周期。
1.4观察指标 随访6个月。(1)淋巴结转移情况;(2)肿瘤标志物水平。运用酶联免疫吸附法对血清癌胚抗原(CEA)、糖类抗原125(CA125)、糖类抗原153(CA153)水平进行测定;(3)雌激素水平。抽取患者的10 mL静脉血,分离血清,采用全自动生化分析仪对其雌酮(E1)、雌二醇(E2)、黄体生成素(LH)水平进行测定;(4)不良反应发生情况。采用不良反应量表(TESS)对治疗后的不良反应发生情况进行调查。

2 结 果
2.1两组患者的淋巴结转移情况比较 联合治疗组患者的淋巴结转移率低于常规化疗组(P<0.05),见表1。

表1 两组患者的淋巴结转移情况比较[n(%)]
2.2两组患者治疗前后的肿瘤标志物水平比较 治疗后,联合治疗组患者的CEA、CA125、CA153水平均低于常规化疗组(P<0.05),见表2。
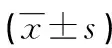
表2 两组患者治疗前后的肿瘤标志物水平比较
2.3两组患者治疗前后的雌激素水平比较 治疗后,联合治疗组E1、E2、LH水平均低于常规化疗组(P<0.05),见表3。
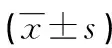
表3 两组患者治疗前后的雌激素水平比较
2.4两组患者的不良反应发生情况比较 联合治疗组和常规化疗组患者的不良反应发生率比较差异无统计学意义(P>0.05),见表4。

表4 两组患者的不良反应发生情况比较[n(%)]
3 讨 论
乳腺肿瘤是一种女性恶性肿瘤,患者具有较高的发病率及病死率,对患者的生命安全造成了严重威胁。相关医学研究表明,乳腺肿瘤具有较高的转移率、复发率,进而使临床很难有效降低患者的病死率[4]。要想降低乳腺肿瘤患者的复发率,对患者治疗预后进行改善,关键是要对其淋巴结转移进行有效抑制。近年来,在抗肿瘤治疗中,卡培他滨日益广泛地应用于临床。相关医学研究表明,在乳腺肿瘤的治疗中,卡培他滨能够发挥积极作用[5]。
卡培他滨属于氟尿嘧啶类抗肿瘤药物,给药方式为口服,能够增强抗癌效果。相关医学学者应用卡培他滨治疗结直肠癌患者[6],发现其能够使化疗效果得到有效保证,促进患者转移率、复发率的降低、生存率的提升。以此认为在结直肠癌的治疗中,卡培他滨的作用机制为对结直肠癌细胞的转移进行了有效抑制,使化疗药物效果得到有效保证[7]。本研究结果表明,联合治疗组患者的淋巴结转移率低于常规化疗组,和上述研究结果一致,原因为卡培他滨是一种抗癌药物,能够使化疗效果得到有效保证[8]。
肿瘤标志物指肿瘤细胞对周围组织进行刺激将相关物质分泌出来,肿瘤的发生发展和肿瘤标志物水平关系密切。CEA是一种广谱抗肿瘤标志物,临床在监测肿瘤发生发展的过程中将其作为重要的血清学指标。CA125是大分子糖蛋白,合成主体为上皮细胞,主要在细胞中储存,乳腺细胞癌变会破坏细胞结构,使大量CA125进入血液,从而提高了血液中CA125水平。因此,在预测肿瘤发生发展的过程中,CA125也能够将重要依据提供给临床。CA153的产生途径为乳腺细胞表面包膜异变,大量CA153在乳腺癌发生后进入外周血中,从而显著提高外周血中CA153水平。因此,在早期诊断乳腺癌、监测乳腺肿瘤细胞浸润性的过程中,对CA153水平进行检测能够给临床提供重要依据[9]。本研究结果表明,治疗后,联合治疗组患者的血清CEA、CA125、CA153水平均低于常规化疗组(P<0.05),说明能卡培他滨能够在肝脏内向5-氟尿嘧啶转变,进而对肿瘤活性进行抵抗,对RNA、蛋白质合成造成干扰,从而对肿瘤细胞分裂进行抑制,最终促进肿瘤标志物水平的降低。
在乳腺肿瘤发病的影响因素中,高水平雌激素是一个重要危险因素[10]。本研究结果表明,治疗后,联合治疗组患者的血清E1、E2、LH水平均低于常规化疗组(P<0.05),说明卡培他滨能够促进乳腺肿瘤患者雌激素水平的降低,从而发挥抗肿瘤作用。本研究结果还表明,联合治疗组和常规化疗组患者的不良反应发生率之间的差异无统计学意义(P>0.05),说明卡培他滨不会引发严重不良反应。原因为卡培他滨的激活机制独特,对抗肿瘤的作用靶向性明确,肿瘤组织会将其选择性激活,促进较高浓度活性细胞毒物质的产生,进而对患者的耐受力进行改善,从而促进消化道等不良反应的减轻[11-12]。
综上所述,乳腺肿瘤治疗中,与常规化疗相比,卡培他滨联合常规化疗更能有效降低患者的淋巴结转移率及肿瘤标志物水平,值得推广。

