响应曲面法优化绿原酸明胶微球的制备工艺研究*
费文玲,陈庆庆,2,秦 兰,2,杨 宽,秦 蓓,2
(1.西安医学院 药学院 药物研究所,陕西 西安 710021;2.成都医学院 药学院,四川 成都 610500)
绿原酸是一种苯丙素类化合物,是山银花、金银花、杜仲等药材的主要活性成分,具有清除自由基、抗菌、抗肿瘤、降糖降脂、保肝利胆等活性作用[1]。但稳定性差、代谢快、生物利用度低等限制了其临床应用[2]。研究发现,将绿原酸制备成微球制剂,可有效提高其药物稳定性,增加生物利用度[3]。李辉等[4]研究者通过沉淀聚合法制备了绿原酸分子印迹聚合物微球;顾晓红等[5]研究者采用多重乳液悬浮聚合法制备了绿原酸磁性印迹聚合微球,但是分子印迹技术存在产率低、成本高、实用性欠佳等缺陷,难以投入生产[6]。明胶是一种廉价、生物相容性优良的高分子材料,以明胶为载体制备的明胶微球具有稳定性好、工艺简单、价格低廉和产率高等优势,在生物、医学、化工等领域应用广泛[7]。本研究以明胶为载体材料,绿原酸作为模型药物,制备绿原酸微球。本文采用响应曲面法[8]考察影响微球制备工艺的各因素,进行响应面分析,得到绿原酸微球的最佳制备工艺,为绿原酸微球的推广应用奠定了一定的理论基础。
1 实验部分
1.1 原料、试剂与仪器
绿原酸原料药(99.4%上海源叶生物科技公司);绿原酸标准品(中国食品药品检定研究院);明胶(A型明胶,阿拉丁试剂公司);乙醇、液体石蜡、Span-80、戊二醛、乙醚,均为分析纯,天津科密欧化学试剂公司;实验用水为蒸馏水。
SQP QUINTIX24-1CN型电子分析天平(德国赛多利斯公司);HITACHI TM4000型扫描电镜(日本日立公司);U-2910型紫外-可见分光光度计(日本日立公司);FD-1A-50型冷冻干燥机(北京博医康实验仪器公司);DF-101S型集热式恒温加热磁力搅拌水浴锅(巩义市予华仪器公司)。
1.2 实验方法
1.2.1 绿原酸明胶微球的制备方法 采用乳化-化学交联法[9]制备绿原酸微球。将一定量绿原酸溶解到适量的配好的明胶溶液中作为水相,以液体石蜡作为油相,以Span-80作为油相乳化剂;将水相缓慢均匀滴入油相,油浴温度55℃,磁力搅拌,乳化30min,形成均匀白色乳液;将该体系迅速移至4℃的冰水浴,搅拌,乳化30min;快速滴加定量25%戊二醛溶液,交联30min后反应结束;离心,采用乙醚和蒸馏水各洗涤3次[10],冷冻干燥后备用。
1.2.2 含量测定方法的建立
(1)波长的选择 采用紫外分光光度法检测,取绿原酸的乙醇溶液,以乙醇作为空白对照,于200~600nm波长范围进行扫描得绿原酸紫外吸收光谱,确定最大吸收波长。并对辅料明胶的乙醇溶液进行紫外扫描,确定辅料有无干扰。
(2)标准曲线的建立 称取10mg的绿原酸标准品配制成100μg·mL-1的绿原酸对照品母液,用乙醇稀释至浓度为2,4,6,8,10,12,14μg·mL-1的系列对照品溶液。采用紫外-可见分光光度法,以乙醇溶液为空白对照,在328nm处测吸光度值(A),以A为纵坐标,绿原酸浓度C为横坐标进行线性回归,绘制标准曲线。
(3)精密度实验 准确称取绿原酸,分别配制高、中、低3种浓度的绿原酸乙醇溶液,于328nm处连续测定5次吸光度,计算RSD。
(4)回收率实验 称取适量已知含量的绿原酸明胶微球到10mL容量瓶,加乙醇溶解至刻度。取1mL上述溶液9份分别于9个10mL的容量瓶中。取(2)中的对照品母液,稀释到一定浓度作为储备液,取1、1.5、2mL于上述容量瓶中,每个浓度设置3组平行,用乙醇定容至刻度线摇匀。于328nm处测定吸光度值,代入回归方程求出药物浓度,并计算回收率、RSD。
1.2.3 微球粒径分析 取微量样品黏贴于贴有导电胶带的样品台上,用吸耳球吹去未黏贴的样品,喷金镀膜后,扫描电子显微镜观察微球形态,根据标尺,分析微球粒径,计算平均粒径。
1.2.4 微球载药量和包封率的测定 精密称定一定量样品粉末,用80%乙醇充分溶解后[11],稀释到一定浓度,以空白明胶微球悬浮液做空白对照,紫外法测定其吸光度。根据绿原酸标准曲线,计算绿原酸浓度,结合溶液的稀释倍数,计算微球中绿原酸的含量。依据公式(1)和(2)计算微球载药量和包封率[12]。

1.2.5 实验因素水平确定 在工艺优化前,本研究进行了单因素实验,挑选出对绿原酸微球产率、包封率和平均粒径影响较显著的3个因素,即明胶浓度(A)、水油体积比(B)、搅拌速度(C)作为考察对象,每个因素3水平,用代码-1,0,1表示,采用响应曲面法优化[13,14],见表1。

表1 响应曲面分析因素与水平Tab.1 Analytical factors and levels for response surface method
以绿原酸微球的产率Y1、包封率Y2和平均粒径Y3为评价指标,采用综合评分法对其影响因素排序。设定Y1、Y2、Y3最高为10分,最低为0分,评分标准见表2。
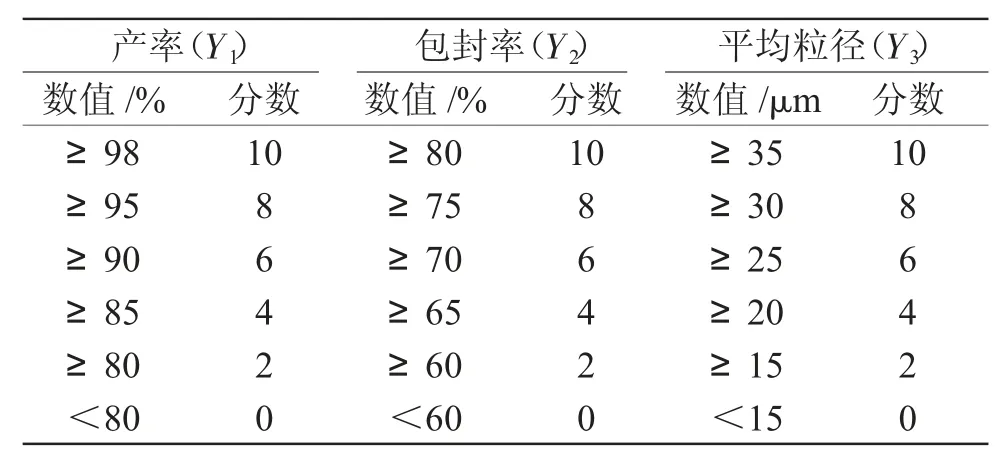
表2 评分标准Tab.2 Standard of scores
2 结果与讨论
2.1 含量测定方法的建立
绿原酸在(328±1)nm处有最大吸收,且辅料明胶无干扰,故确定检测波长为328nm。以绿原酸浓度C对吸光度A进行线性回归,得到线性回归方程:A=0.0633C-0.0129,R2=0.9997。绿原酸在2.0~14.0μg·mL-1范围内与吸光度线性关系良好。精密度实验的RSD均小于2%,此方法对不同浓度的绿原酸平均回收率为99.60%,RSD为2.13%,说明紫外分光光度法灵敏度和精确度均较高,可用于绿原酸的含量测定。
2.2 响应面实验安排及结果
根据响应面分析设计实验,进行三因素三水平共17次实验,结果见表3。

表3 响应曲面实验分析及结果Tab.3 Analysis and results of RSA experiment
由表3可见,计算各组实验得分,将Y1、Y2和Y3得分相加得出经验得分Y0;运用SPSS22.0软件把经验得分Y0作为因变量,将各指标经验得分分别作为自变量Y1、Y2和Y3,得出综合评分值Y的回归线性方程式为Y=0.391Y1+0.426Y2+0.339Y3-58.077,把各实验指标实测值代入回归方程,得到该实验的线性回归综合得分(Y),以综合得分作为效应值,进行评价。
2.3 模型的建立及显著性检验
通过Design-Expert 12.0软件对数据回归分析,得出二次多元回归模型方程:Y=30.02+5.08X1+2.00X2+1.22X3-0.28X1X2-0.63X1X3+0.46X2X3-9.11X12-8.51X22-8.18X32,该模型的校正系数R2=0.9930,修正相关系数Radj2=0.9839,说明因变量和自变量之间相关性较强,可以用该结果分析绿原酸微球制备工艺与明胶浓度、水油体积比和搅拌速度这3个因素的相关性。
表4为回归分析结果。
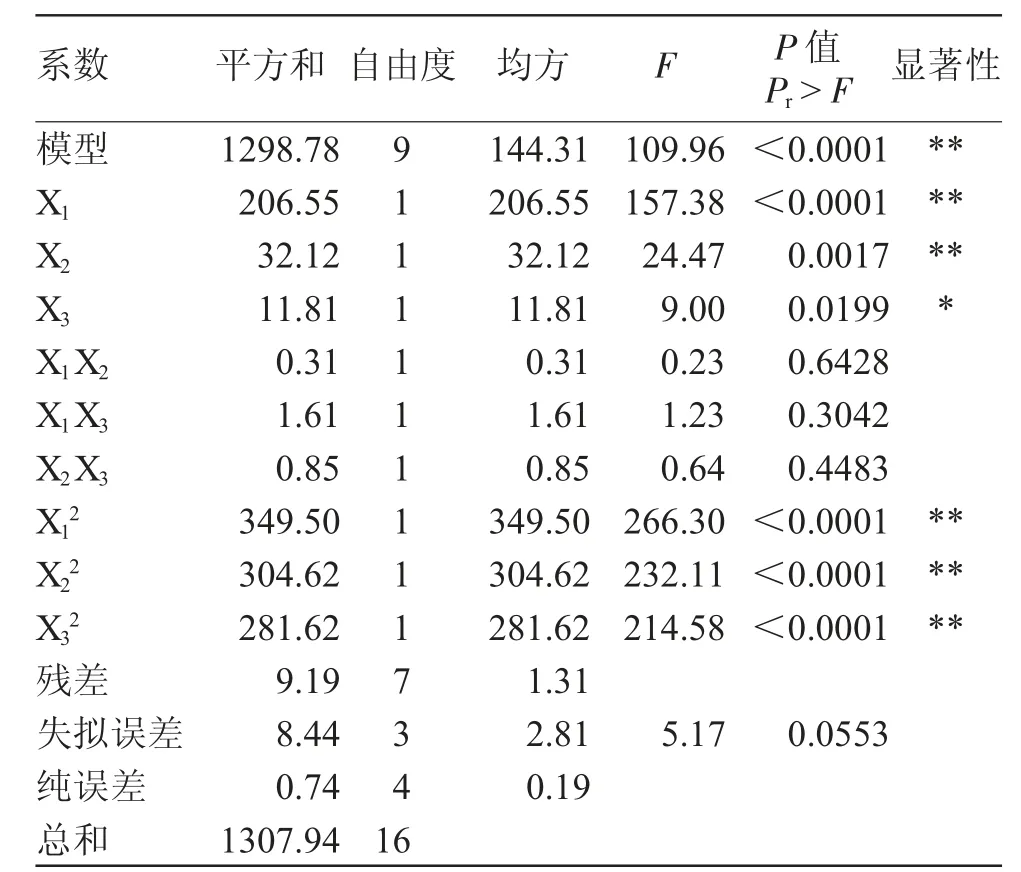
表4 回归分析结果Tab.4 Results of regression analysis
由表4中模型P小于0.0001,说明该模型极显著,实验结果分析具有统计学意义。各项P值显示,一次项X1、X2、X3与二次项X12、X22、X32均达到显著性水平,即说明明胶浓度、水油体积比、搅拌速度这3个因子对响应值有影响。根据各项F值大小可知,各因素影响大小依次为A>B>C,即3个因素中对综合评分影响最大的是明胶浓度,水油体积比次之,搅拌速度影响最小。失拟误差是反映实验数据与模型不相符的情况,P大于0.05,说明失拟误差不显著,不相关的其他因素对实验结果影响很小。
2.4 响应曲面优化及预测
图1为根据回归方程作出不同因子的响应曲面分析及等高线图。图(a)、(b)、(c)分别是搅拌速度、水油体积比、明胶浓度各因素取零水平时,其他两因素对综合得分的影响,3个因素对实验的交互影响见图(d)、(e)、(f)。

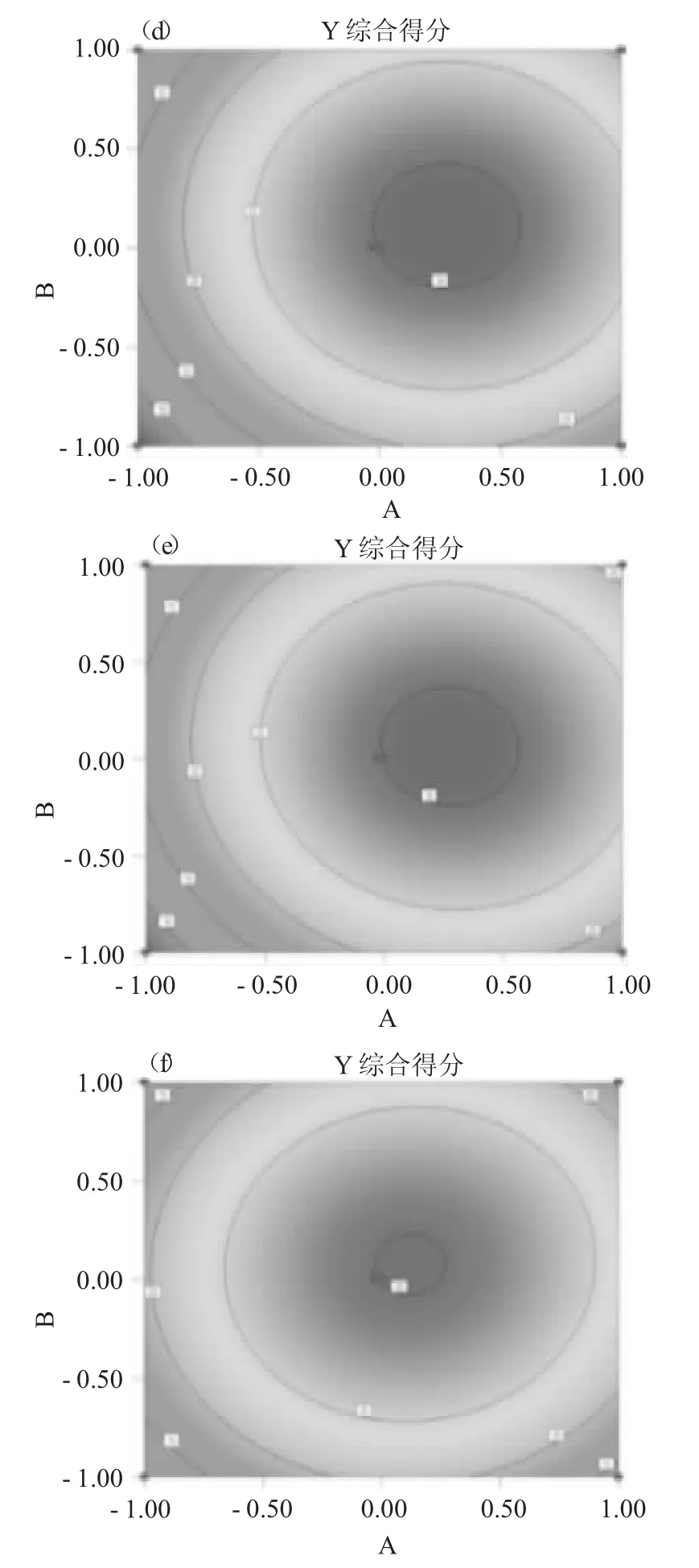
图1 综合得分的响应曲面及等高线图Fig.1 Response surface plots and contours of composite score
由图1可知,观察综合得分的响应曲面及等高线图可以发现,响应曲面的弧度越大,等高线图颜色变化越快,该因素对响应值的影响越显著。3个因素中明胶浓度对综合得分的影响最明显。明胶浓度越大,形成的液滴越大,微球粒径就越大,黏连的机会就越小,产率增加[10];其次是水油体积比,水油比例会影响乳化的难易程度,进而导致微球的形态和性质差异。增大水油比例,乳液的乳化程度提高,液滴能够得到均匀分散,微球的流动性增强,得到的微球圆整,产率增加,包封率提高[15];搅拌速度对微球工艺影响最小。提高搅拌速度,可以增大乳液各部位受到的剪切力,形成较均匀的液滴,并且被搅拌离心力所稳定,不易发生聚集[16],得到的微球均匀、分散性好、产率高。由图1可知,在实验范围内,综合得分随3个因素的变化趋势都是先增大后减小。为进一步确证最佳点的位置,对模型回归方程的3个自变量分别取一阶偏导,并令偏导方程等于零,整理可得:
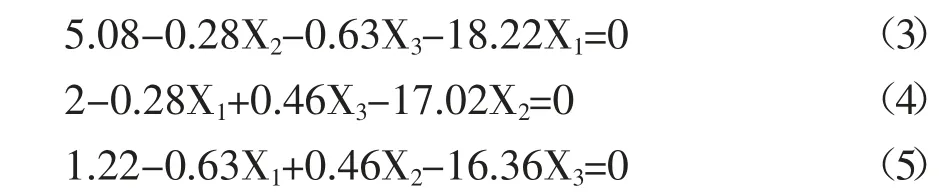
由式(3)~(5)解得X1=0.270、X2=0.115、X3=0.067。代入变换公式得优化的制备条件为:明胶浓度为0.23g·mL-1、水油体积比1∶5.58(mL∶mL)、搅拌速度1220.10r·min-1。
2.5 最佳工艺的验证
为验证响应曲面法结果的可靠性并考虑到实验的可操作性,调整最优合成方案为:明胶浓度为0.23g·mL-1、水油体积比1∶5.6(mL∶mL)、搅拌速度1220r·min-1。以最佳工艺条件进行验证实验,结果见表5。

表5 预测值与实验值比较(n=3)Tab.5 Comparison of predicted and experimental values(n=3)
由表5可知,得到的3批绿原酸明胶微球平均产率为99.5%,包封率89.5%,平均粒径为36μm,综合得分为30分。预测值和实验值的偏差值小于5%,表明响应曲面分析获得的最佳点比较准确,由此可见,该多元二次回归模型可以较好地反映各因素与响应值之间的真实关系,可以通过该回归方程来确定绿原酸明胶微球的最佳制备工艺。
2.6 绿原酸微球的电镜分析
最佳制备工艺制得的绿原酸明胶微球外观均匀较疏松,在水中的分散性较好。扫描电子显微镜观察的形态见图2。

图2 绿原酸明胶微球电镜图(×1800)Fig.2 Scanning electron micrograph of chlorogenic acid gelatin microspheres(×1800)
由图2可知,绿原酸明胶微球表面光滑圆整,没有过多的微球黏连,平均粒径为36μm。
3 结论
(1)本研究采用响应曲面法,得到绿原酸明胶微球最佳制备工艺为:明胶浓度为0.23g·mL-1、水油体积比为1∶5.6(mL∶mL)、搅拌速度为1220r·min-1。
(2)最佳工艺条件下得到的微球表面光滑圆整,大小较均匀,分散性好,平均粒径为36μm,产率为99.5%,包封率为89.5%。经验证,采用响应曲面法得到的绿原酸明胶微球制备工艺可行。

