经皮椎体后凸成形术对新鲜与陈旧性骨质疏松性椎体压缩骨折的临床疗效分析
芦怀旺 田霖 胡鹏 刘彬 张玉红
滨州医学院附属医院脊柱外科,滨州 256603
骨质疏松症是一种系统性骨骼退变性疾病,由于骨微结构的破坏和骨量的减少,导致骨脆性增加,从而导致身体各个部位骨折[1-2]。其中,脊柱压缩性骨折较为常见[3]。骨折后,患者活动受限,常伴有脊柱疼痛,需要及时有效的治疗。否则,会出现骨折愈合延迟和骨不连等并发症,严重影响患者的生活质量[4-6]。由于骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fracture,OVCF)是一种低能损伤,所以损伤后疼痛容易与疲劳疼痛混淆。而且,多数老年患者对疼痛不敏感,容易使病情发展,最终发展为陈旧性骨折。对于陈旧性OVCF,保守治疗,如卧床休息、佩戴腰围、抗骨质疏松等药物治疗,对多数患者无明显疗效[7]。有研究证实椎体成形术(PVP)和经皮椎体后凸成形术(percutaneous kyphoplasty,PKP)均能有效改善老年OVCF患者的疼痛和功能障碍[8],恢复椎体高度,矫正后凸畸形,但PKP具有更好的疗效和更高的安全性,值得推广[9]。本研究分析了滨州医学院附属医院采用PKP治疗的62例新鲜性及42例陈旧性OVCF患者的临床疗效,现具体报道如下。
资料与方法
1、一般资料
选取滨州医学院附属医院脊柱外科2019年6月至2021年1月收治的104例经PKP治疗的OVCF患者的143个椎体。根据患者病程及MRI的T1、T2信号强度分为陈旧组与新鲜组。新鲜组共62例71个椎体,男11例,女51例,年龄(70.21±8.05)岁;伤椎节段:胸椎35个,腰椎36个。陈旧组共42例72个椎体,男4例,女38例,年龄(70.05±5.17)岁;伤椎节段:胸椎32个,腰椎40个。两组患者性别、年龄、伤椎节段差异均无统计学意义(均P>0.05)。两组术前均进行CT和MRI检查来确定伤椎并明确椎管情况,并根据MRI上T1、T2信号高低及症状持续时间区分新鲜性及陈旧性,新鲜组T1WI低信号,T2WI高信号;陈旧组T1WI高信号,T2WI低信号[10],且陈旧组病史均大于3周。
本研究经滨州医学院附属医院医学伦理委员会审批通过(2019KT-042),患者和家属知情同意并签署知情同意书。
2、纳入与排除标准
纳入标准:⑴伴有顽固性胸腰部疼痛,保守治疗不缓解;⑵术前双能X线测定骨密度T值小于-2.5,证实存在骨质疏松;⑶术前X线、CT、MR明确胸腰椎压缩骨折,且椎体前缘高度压缩超过30%,且后壁完整,未累及椎管;⑷无脊髓和神经根受损的症状和体征。
排除标准:⑴经保守治疗疼痛明显缓解或椎体前缘高度丢失小于30%;⑵影像学证实椎体后壁或周壁骨折,并累及椎管;⑶严重胸腰椎畸形;⑷伴有脊髓和神经根受损症状,需要椎管或神经根减压者;⑸系统性疾病不能耐受手术者。
3、手术方法
患者取俯卧位,透视定位责任椎体椎弓根,局部麻醉后在透视下以穿刺针经责任椎体椎弓根进入相应椎体前方中央。球囊扩张椎体,透视见椎体撑开后复位良好。抽出穿刺针内芯,向椎体内打入适量骨水泥。再次透视见椎体复位良好,骨水泥弥散均匀,位置良好,无明显外漏。敷料包扎切口。
4、术后处理
术后即刻可以在腰围保护下离床活动。术后第2天即可出院休养。术后常规应用钙剂、双膦酸盐类、性激素等抗骨质疏松和促进骨折愈合药物辅助治疗。术后定期来医院复查,根据复查相关指标,调整抗骨质疏松药物。
5、观察指标
5.1、围术期指标比较两组手术时间、术中出血量及单椎体骨水泥注入量。
5.2、疼痛评分根据视觉模拟评分法(VAS)对患者术前、术后3 d、末次随访的疼痛程度进行评分(0~10分),分数越高疼痛程度越高。
5.3、椎体形态恢复通过测量胸腰椎矢状位X线片比较术前、术后3 d、末次随访的椎体前缘高度及矢状位后凸Cobb角来评价椎体形态的恢复情况。
5.4、椎体功能障碍指数对两组患者术前、术后3 d、末次随访的椎体功能障碍采用Oswestry功能障碍指数(Oswestry disability index,ODI)进行评价,分数与障碍严重程度呈正比。
5.5、并发症比较比较两组患者的骨水泥渗漏率及相邻椎体骨折情况。
6、统计学方法
数据用SPSS 22.0统计学软件进行数据处理并分析,年龄、手术时间、出血量、单椎体骨水泥用量等计量资料均符合正态分布,用(±s)表示,两组比较采用独立样本t检验。两组术前、术后3 d、末次随访VAS评分、ODI、Cobb角、椎体前缘高度计量资料符合正态分布,不同时点比较采用重复测量方差分析。性别、手术椎体、骨水泥渗漏率等计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
结 果
1、围术期指标
两组患者均顺利完成手术,术后穿刺部位无感染及不愈合等情况。陈旧组手术时间长于新鲜组,单椎体骨水泥注入量少于新鲜组,差异均有统计学意义(P<0.05);两组出血量差异无统计学意义(P>0.05)。见表1。
表1 两组骨质疏松性椎体压缩骨折患者围术期指标比较(±s)

表1 两组骨质疏松性椎体压缩骨折患者围术期指标比较(±s)
注:两组均采用经皮椎体后凸成形术治疗
组别新鲜组陈旧组t值P值例数62 42手术时间(min)44.24±17.32 56.12±30.05-2.552 0.012出血量(ml)4.60±3.40 5.83±4.08-1.676 0.097单椎体骨水泥注入量(ml)3.90±1.07 3.53±0.90 2.262 0.025
2、疼痛评分
两组术后3 d、末次随访VAS评分较术前明显改善(P<0.05);两组间VAS评分差异无统计学意义(P=0.839)。见表2。
表2 两组骨质疏松性椎体压缩骨折患者各时间点VAS评分比较(分,±s)
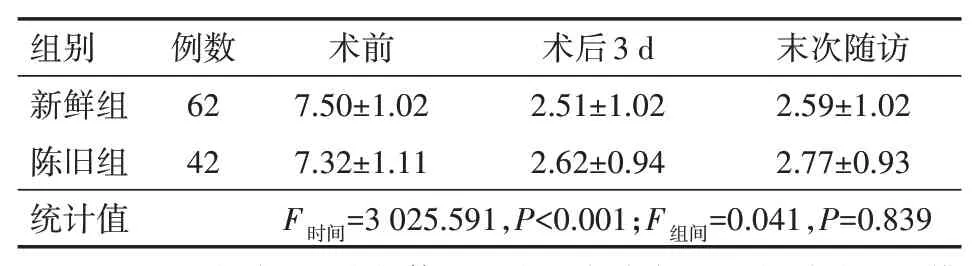
表2 两组骨质疏松性椎体压缩骨折患者各时间点VAS评分比较(分,±s)
注:两组均采用经皮椎体后凸成形术治疗;VAS评分为视觉模拟疼痛评分。
组别新鲜组陈旧组统计值例数62 42术前7.50±1.02 7.32±1.11 F时间=3 025.591,P<0.001;F组间=0.041,P=0.839术后3 d 2.51±1.02 2.62±0.94末次随访2.59±1.02 2.77±0.93
3、椎体形态恢复
两组术后3 d、末次随访Cobb角、椎体前缘高度较术前明显改善(P<0.05);两组间Cobb角、椎体前缘高度改善情况差异均有统计学意义(均P<0.05)。见表3。
表3 两组骨质疏松性椎体压缩骨折患者各时间点椎体形态恢复情况比较(±s)
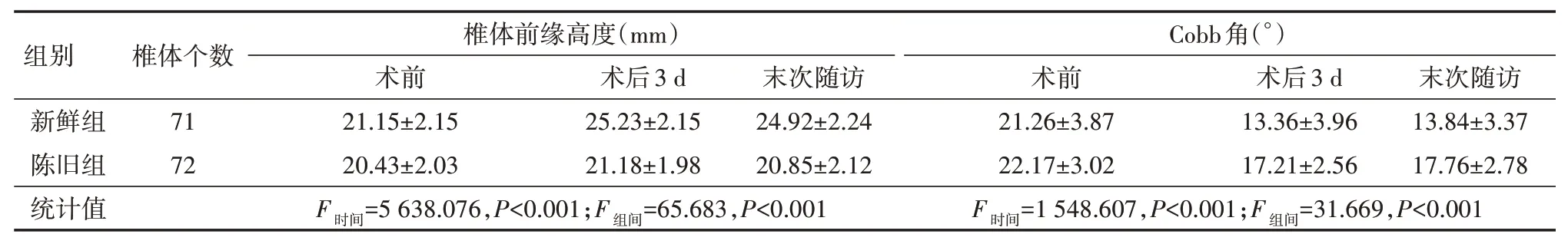
表3 两组骨质疏松性椎体压缩骨折患者各时间点椎体形态恢复情况比较(±s)
注:两组均采用经皮椎体后凸成形术治疗
组别新鲜组陈旧组统计值椎体个数71 72椎体前缘高度(mm)术前21.15±2.15 20.43±2.03 F时间=5 638.076,P<0.001;F组间=65.683,P<0.001术后3 d 25.23±2.15 21.18±1.98末次随访24.92±2.24 20.85±2.12 Cobb角(°)术前21.26±3.87 22.17±3.02 F时间=1 548.607,P<0.001;F组间=31.669,P<0.001术后3 d 13.36±3.96 17.21±2.56末次随访13.84±3.37 17.76±2.78
4、椎体功能障碍指数
两组术后3 d、末次随访ODI指数较术前明显改善(P<0.05);两组间ODI指数差异无统计学意义(P=0.347)。见表4。
表4 两组骨质疏松性椎体压缩骨折患者各时间点Oswestry功能障碍指数比较(±s)
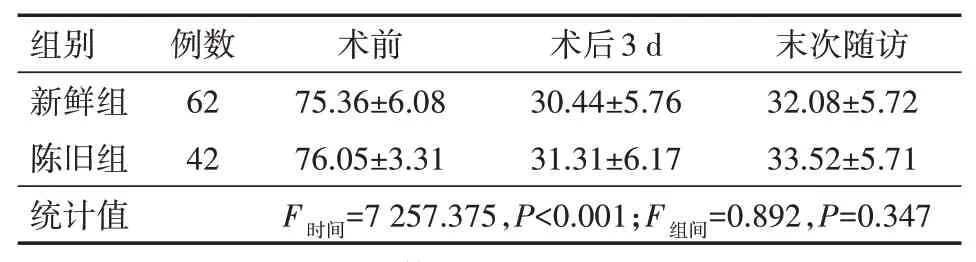
表4 两组骨质疏松性椎体压缩骨折患者各时间点Oswestry功能障碍指数比较(±s)
注:两组均采用经皮椎体后凸成形术治疗
组别新鲜组陈旧组统计值例数62 42术前75.36±6.08 76.05±3.31 F时间=7 257.375,P<0.001;F组间=0.892,P=0.347术后3 d 30.44±5.76 31.31±6.17末次随访32.08±5.72 33.52±5.71
5、并发症比较
新鲜组9例骨水泥渗漏,陈旧组1例骨水泥渗漏;术后1年相邻椎体骨折,新鲜组1例,陈旧组5例;两组间差异均有统计学意义(χ2=4.243,P=0.046;χ2=4.878,P=0.038)。典型病例见图1。

图1 新鲜与陈旧骨质疏松性椎体压缩骨折典型病例影像学资料。A、B分别为患者Ⅰ术前磁共振T1WI低信号、T2WI高信号,证实为新鲜L1椎体压缩骨折;C、D为患者Ⅰ术后复查腰椎侧正位片,见骨水泥分布良好。E、F分别患者Ⅱ为术前磁共振T1WI高信号、T2WI低信号,证实为陈旧L2椎体压缩骨折;G、H为患者Ⅱ术后复查腰椎侧正位片,见骨水泥扩散良好
讨 论
骨质疏松症是一种低骨密度的代谢性骨病,以全身骨骼疼痛和易骨折为特征[11]。OVCF是其最常见的并发症之一,已成为老龄化社会亟待解决的公共卫生问题[12]。OVCF作为骨质疏松症的主要并发症,保守治疗效果有限,并发症较多,尤其是对老年人。PKP治疗老年OVCF疗效明显,速度快。术后并发症少,能促进功能恢复和生活质量的提高[13]。近年来,随着脊柱微创手术的发展,PKP治疗OVCF的快速改善效果已被大量学者所接受。
本研究发现:PKP术后,新鲜组及陈旧组患者胸腰背部疼痛均得到了明显缓解,生活质量得到改善;术后VAS评分及ODI功能障碍指数较术前均明显改善(均P<0.05);两组手术时间、骨水泥注入量、椎体前缘高度和矢状位Cobb角改善差异有统计学意义(均P<0.05);考虑陈旧性骨折由于病史长,椎体内骨质部分愈合甚至硬化,球囊扩张不充分、不均匀,增加了手术时间,而新鲜组球囊更容易实现均匀有效扩张,从而可注入更多的骨水泥量,使椎体前缘高度和矢状位Cobb角改善方面优于陈旧组。在工作中我们也发现应用球囊扩张的PKP对于陈旧性OVCF复位效果不佳,为解决这一问题,我们建议应用带有金属扩张器的骨囊袋来治疗陈旧性OVCF,它对椎体前缘高度及Cobb角的恢复会较好一些。虽然两组患者PKP术后均取得了良好的临床疗效,但其骨水泥的渗漏情况也需要我们关注。Lv等[14]发现骨水泥渗漏率高的患者表现为单一分散或单一致密的椎体,而集中分布的高黏度骨水泥可降低骨水泥渗漏发生率[15]。为进一步证实高粘度和低粘度骨水泥在PKP中的临床疗效,Wang等[16]研究发现,在PKP中高粘度骨水泥的水泥渗漏率低于低粘度骨水泥,并认为高粘度骨水泥可能是改善OVCF渗漏的一种潜在选择。本研究中骨水泥渗漏共10例,均为椎间隙或椎旁渗漏,未发现椎管内渗漏等其他严重并发症。其中新鲜组9例,陈旧组1例,两组间差异有统计学意义(P<0.05),考虑陈旧性OVCF存在不同程度的骨质愈合,一定程度上限制了骨水泥的扩散有关。鉴于以上研究,为了减少骨水泥的渗漏,笔者建议在PKP手术时,尽可能应用高粘度的骨水泥,并使水泥集中分布在椎体中,而非单一分散或单一致密的分布在骨折椎体中。
相邻椎体的骨折也是我们不容忽视的PKP另一重要并发症。生物力学研究已经被用来评估骨水泥增强术对邻近椎体的影响。最近的一项荟萃分析显示,骨水泥加固骨折椎体并不会增加新骨折的风险,尤其是邻近椎体骨折[17]。但也有学者认为PKP容易诱发位于增强椎体的再骨折,尤其是椎体成形术邻近的椎体的压缩骨折[18],并认为可能与患者PKP术后,骨水泥可在短时间内改变骨折椎体局部生物力学性质,影响相邻椎体的力学传导,增加术后相邻节段复发的风险。近年来大量研究表明,骨水泥的注入量及骨水泥的状态与相邻椎体骨折密切相关。有研究发现,随着骨水泥用量的增加,骨水泥节段上、下终板的应力显著增加。当单个椎体骨水泥量增加到11.5 ml以上时,有发生邻近骨折的潜在风险。中央注射骨水泥可以降低PKP术后邻近骨折的风险[19]。而PKP中湿砂相骨水泥注射有利于骨水泥均匀分布,强化责任椎体,减少责任椎体再骨折及邻近椎体骨折发生率,且不增加相关并发症的发生[20]。鉴于以上研究,笔者更倾向于PKP能增加相邻椎体骨折的观点。本研究中术后1年随访共有6例,其中新鲜组1例,陈旧组5例,两组间差异有统计学意义(P<0.05),考虑与陈旧组由于球囊扩张欠佳,骨水泥分布相对集中,而新鲜组在球囊扩张后骨水泥能够相对均匀分布于骨折椎体,使之受力更均匀有关,当然这有待于进一步相关研究证实。
综上所述,PKP治疗新鲜和症状性陈旧OVCF均能减轻患者疼痛,提高生活质量。新鲜组术后1年相邻椎体骨折、改善椎体前缘高度及Cobb角优于陈旧组,但骨水泥渗漏率高于陈旧组。本研究具有样本量少、来自同一中心、随访时间短等局限,具体临床疗效需要大样本量的前瞻性随机对照研究来进一步证实。

