mRNA疫苗技术:疫情下的高速赛道
□文/ 杨 瑾 杭州市科技信息研究院

mRNA,即Messenger RNA(信使核糖核酸),是把遗传信息从DNA 传递到蛋白质的信使。通俗来讲,mRNA复制了细胞核中双链DNA 的一条链的遗传信息,随即离开细胞核在细胞质中生成蛋白质。在细胞质中,核糖体沿着mRNA 移动,读取其碱基序列,并翻译成其相应的氨基酸,最终形成蛋白质(如图1)。
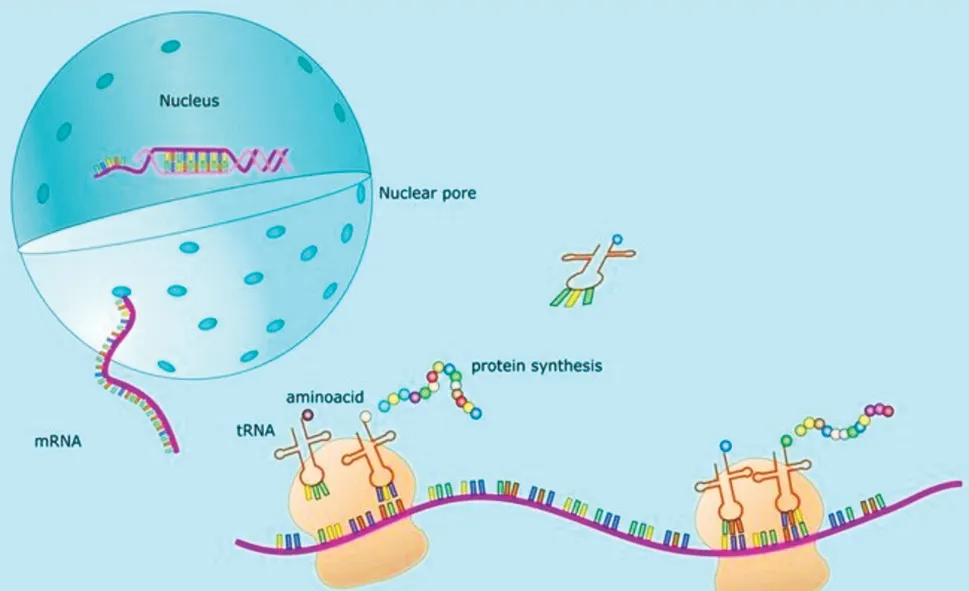
图1 mRNA工作过程
一般的疫苗是通过病原体本身、病原体的一部分或者病原体的免疫分子注射进入机体,引起免疫反应来保护机体。而mRNA 疫苗是将编码疾病特异性抗原的mRNA 引入体内,利用宿主细胞的蛋白质合成机制产生靶标蛋白(即抗原),从而触发免疫应答,抵抗相应的病毒。
通常可根据不同疾病构建特异性抗原的mRNA序列,由新型脂质纳米载体颗粒包裹运送至细胞内,再利用人体核糖体翻译mRNA 序列产生疾病的抗原蛋白,分泌后被自身免疫系统识别产生免疫反应,从而达到预防疾病作用(如图2)。
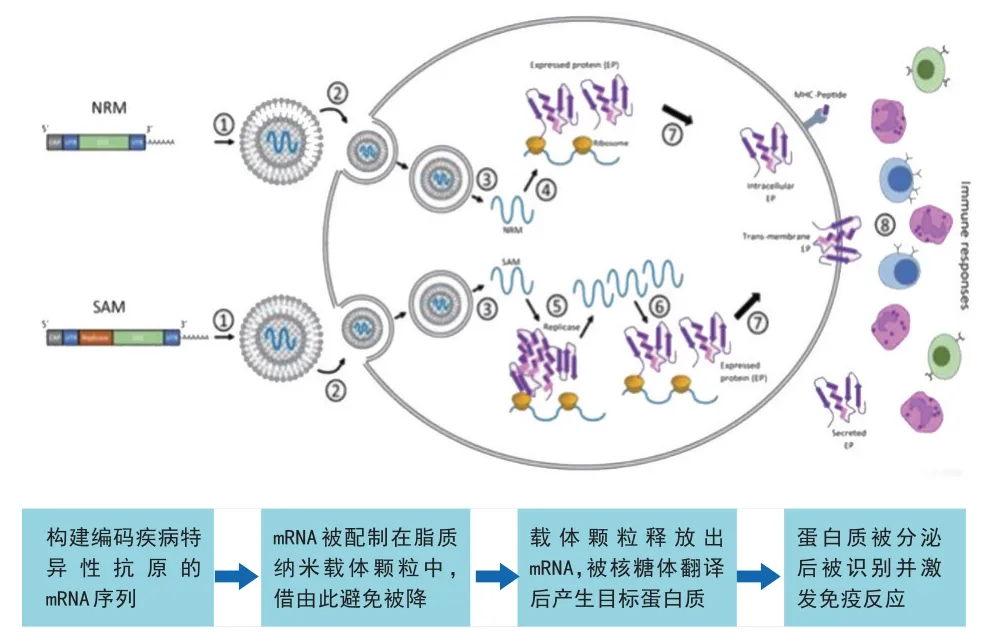
图2 mRNA疫苗在体内作用
mRNA 分子量大,亲水性强,生物活性是小分子药物的上千倍,工业生产比较容易。但它自身的单链结构致使其极为不稳定,易被降解,自身携带负电荷,穿过表面同为负电荷的细胞膜递送亦是难题。所以,mRNA需要特殊的修饰或包裹递送系统才能实现胞内表达,改变mRNA 胞内的生物分布、细胞靶向和摄取机制,发挥疫苗的效果。
脂质体纳米颗粒(LNP)是目前最先进的mRNA 疫苗递送系统。LNP 最初用于siRNA 的递送,已被证明是安全有效的。LNP 是一种稳定的,由阳离子脂质、辅助脂质、胆固醇和包裹水核的聚乙二醇组成的脂质双分子层壳,在水核中可以携带mRNA。但LNP 制造工艺复杂,成品剂型的稳定性有限(只有6 个月),且需要冷链储存及运输。除LNP 以外,mRNA 疫苗的递送系统还有阳离子脂质复合物(LPX)、脂质多聚复合物(LPP)、聚合物纳米颗粒(PNP)、无机纳米颗粒(INP)、阳离子纳米乳(CNE)等。
mRNA疫苗的优势
从生产疫苗的技术路线来讲,目前主要生产疫苗的技术路线有第一代传统疫苗、第二代新型疫苗和第三代前沿疫苗。
第一代传统疫苗主要包括灭活疫苗和减毒活疫苗,应用最为广泛。灭活疫苗是指先对病毒或细菌进行培养,然后用加热或化学剂(通常是福尔马林)将其灭活;减毒活疫苗是指病原体经过各种处理后,发生变异,毒性减弱,但仍保留其免疫原性。将其接种到身体内,不会引起疾病的发生,但病原体可在机体内生长繁殖,引发机体免疫反应,起到获得长期或终生保护的作用。
第二代新型疫苗包括亚单位疫苗和重组蛋白疫苗。亚单位疫苗是将致病菌主要的保护性免疫原存在的组分制成的疫苗,即通过化学分解或有控制性的蛋白质水解方法,提取细菌、病毒的特殊蛋白质结构,筛选出具有免疫活性的片段制成的疫苗;重组蛋白疫苗是将某种病毒的目的抗原基因构建在表达载体上,将已构建的表达蛋白载体转化到细菌、酵母或哺乳动物或昆虫细胞中,在一定的诱导条件下,表达出大量的抗原蛋白,通过纯化后制备的疫苗。

第三代前沿疫苗包括DNA 疫苗和mRNA 疫苗,是将编码某种抗原蛋白的病毒基因片段(DNA 或RNA)直接导入动物体细胞内(注射到人体),并通过宿主细胞的蛋白质合成系统产生抗原蛋白,诱导宿主产生对该抗原蛋白的免疫应答,以达到预防和治疗疾病的目的。两者的区别在于DNA 是先转录成mRNA 再合成蛋白质,mRNA则直接合成蛋白质。
相比减毒、灭活、重组亚单位等疫苗,mRNA 疫苗生产工艺简单,无需细胞培养或动物源基质,合成速度快,成本低。相比同属核酸疫苗的DNA 疫苗,mRNA 疫苗发挥作用无需进入细胞核,没有整合至宿主基因组的风险,且为一过性表达,半衰期可以通过修饰进行调整。
mRNA 疫苗从基因测序至生产只需要数周的时间,因此在对时间要求比较紧急的疫情中有望发挥重要作用。与传统疫苗不同的是,mRNA 疫苗对非感染性疾病也可以发挥作用,肿瘤是mRNA 疫苗应用的重要领域之一。全球领先的3 家mRNA 疫苗公司(CuerVac、Moderna、BioNTech)均在肿瘤领域建立了自己的产品线,包括针对个体的个性化肿瘤疫苗以及通用的肿瘤疫苗,部分已经开展Ⅰ/Ⅱ期临床应用。

mRNA疫苗在新冠病毒疫情中的应用
新冠疫情在全球扩散,随着疫苗的上市,每日新增患者数量有所降低,但考虑到新冠病毒的变异性,疫情的未来走势仍扑朔迷离。相较于传统疫苗,mRNA 疫苗生产工艺简单,开发速度快,无需细胞培养,成本低,更适合应对新冠病毒的快速变异。
全球的机构投资者已经意识到了mRNA 技术领域中的机会,随着mRNA 技术逐步成熟,资本将进一步集中。2020年mRNA技术领域的投资金额大幅增加,增幅约780%。大部分投资对象为专注于针对COVID-19 新冠病毒疫苗开发的医药公司。2020 年12 月后,mRNA新冠疫苗陆续投产,给全球mRNA 药物行业带来超690亿美元的市场规模增幅,考虑到新冠病毒的变异性与疫苗的保护期,mRNA 新冠疫苗将持续为全球mRNA 药物市场规模增长带来动力。
新冠mRNA 疫苗是人类首次在体外进行超大规模mRNA 合成与制备并应用于临床的疫苗,其过程涉及生物、化学、工程等多学科,同时mRNA 药物的生产在过程控制、工程保证、大规模制备工艺、质量控制与质量体系等多方面面临复杂挑战。在应对挑战的同时,对mRNA药物进行生产成本控制并构建稳定的供应链成为其是否能够成功商业化的关键。2021年,BioNTech 和Moderna两家企业凭借这一疫苗跃入超级大药企行列。
mRNA 新冠疫苗的广泛关注给mRNA 产业链带来历史性的机遇,国内产业链力量也在迅速崛起。
mRNA疫苗的应用风险
在mRNA 疫苗接种过程中,部分人会产生不良反应,比如出现低烧或者发炎,这就意味着疫苗还有潜在要解决的问题。而mRNA 疫苗对人类的长期影响,也需要更多时间来观察。至于mRNA 疫苗接种后是否感染重症率较低,这一问题目前还不能得到清晰的结论。因为当前突破感染的数据量偏小,要想下结论则需要更大规模的真实世界数据。现在,有很多新冠病毒的突变株出现,有可能会让新冠病毒的感染率更强,也有可能会导致更高的重症率,这是需要警惕的。

2021年6月23日,美国疾控中心公布了新冠mRNA疫苗安全性的更新数据,并着重讨论了可能带来的心肌炎、心包炎副作用。当前美国接种mRNA 疫苗已经超过3 亿剂,VAERS 介导的心肌炎、心包炎报告案例超过1200 例,其中791 例接受辉瑞、BioNtech 疫苗,435 例接受Moderna 疫苗,大部分发生在第二剂接种以后。疾控中心强调继续监测心肌炎、心包炎副作用,并适当延长随访时间(如3—6个月)。
国际mRNA疫苗技术发展现状
mRNA 技术起步于1987 年。1990 年,Wolff 等人发现在小鼠肌肉组织中注射含有特定基因的质粒DNA 或mRNA,小鼠组织局部会产生该基因编码的蛋白产物,此后多项研究发现用核酸免疫动物,可以诱导机体产生针对该核酸编码抗原的免疫力。但由于mRNA 不稳定、在组织内易被降解、细胞吸收率较低等缺陷,其研发进展缓慢,更多研究放在DNA疫苗领域。
近年来的新冠疫情使得mRNA 疫苗和药物受到全球广泛的关注,带动了mRNA 领域的研究快速发展。根据Nature 相关统计,截至2021 年7 月底,全球mRNA 疫苗和药物在研管线共180 条,虽大多数处于早期阶段,但其中新冠相关应用仅有22 条,传染病、罕见病和肿瘤相关则多达158 条,充分说明虽然新冠疫情推动了mRNA技术的研发,但其应用场景在持续拓宽,并不局限于单一领域。综合考虑临床管线成功概率、推出时间及潜在市场需求等因素,预计2035 年全球mRNA 医药市场规模约230 亿美元。而在mRNA 疫苗赛道,根据Market Study Report LLC 的测算,预计全球mRNA 预防性和治疗性疫苗的市场规模在2020 年至2025 年的年复合增长率为32.0%,预计到2025 年市场规模将达到59.8 亿美元。
基于mRNA 技术平台的代表企业主要位于欧美地区(如表1),其中CuerVac、Moderna、BioNTech 被称为“mRNA 国际三巨头”。CuerVac 是全球第一家成功地将mRNA用于医疗目的的公司,主要关注肿瘤、感染性疾病和罕见病。Moderna 一直专注于mRNA 相关药物和疫苗的研发,治疗领域涵盖了感染性疾病、肿瘤免疫治疗、罕见病、心血管疾病和自身免疫疾病等,在新冠疫情中,Moderna 研发的mRNA-1273 是全球首个进入临床I 期试验的疫苗。BioNTech拥有四大技术平台,mRNA疗法平台就是其中1 个,其余3 个平台为细胞和基因治疗平台、蛋白质疗法平台和小分子治疗平台。BioNTech 于2020 年启动“光速(Light Speed)计划”,着力研究新冠病毒疫苗,同年3 月,BioNTech 成功与美国医药巨头辉瑞(Pfizer)和中国医药巨头复星医药达成合作。其Arcturus Therapeutics 研发的专有LUNAR®递送系统可更快、更简单地生产疫苗。

表1 全球主要mRNA平台型企业相关情况
我国mRNA疫苗技术发展现状
我国mRNA 技术虽然起步较晚,但发展快速。从投融资情况来看,2016-2019年,我国mRNA 领域投融资金额并不高,但从2020 年开始大幅增加至7.66 亿美元,2021年我国mRNA领域投融资金额达13.61 亿美元。受到mRNA 新冠疫苗商业化巨大成功的激励,国内已有众多企业纷纷投入mRNA 赛道,涌现了斯微生物、艾博生物、丽凡达生物等重点企业(如表2)。其中斯微生物是我国最早成立的mRNA药物研发企业,专注于LPP 纳米递送技术和冻干制剂工艺,拥有全球领先的高通量技术。艾博生物与中国人民解放军军事医学研究院、沃森生物共同研制的新冠mRNA 疫苗ARCoVaX 是国内首个获批开展临床试验的mRNA 疫苗。艾博生物也因此在2021 年顺利完成3 轮融资,累计融资超11亿美元。
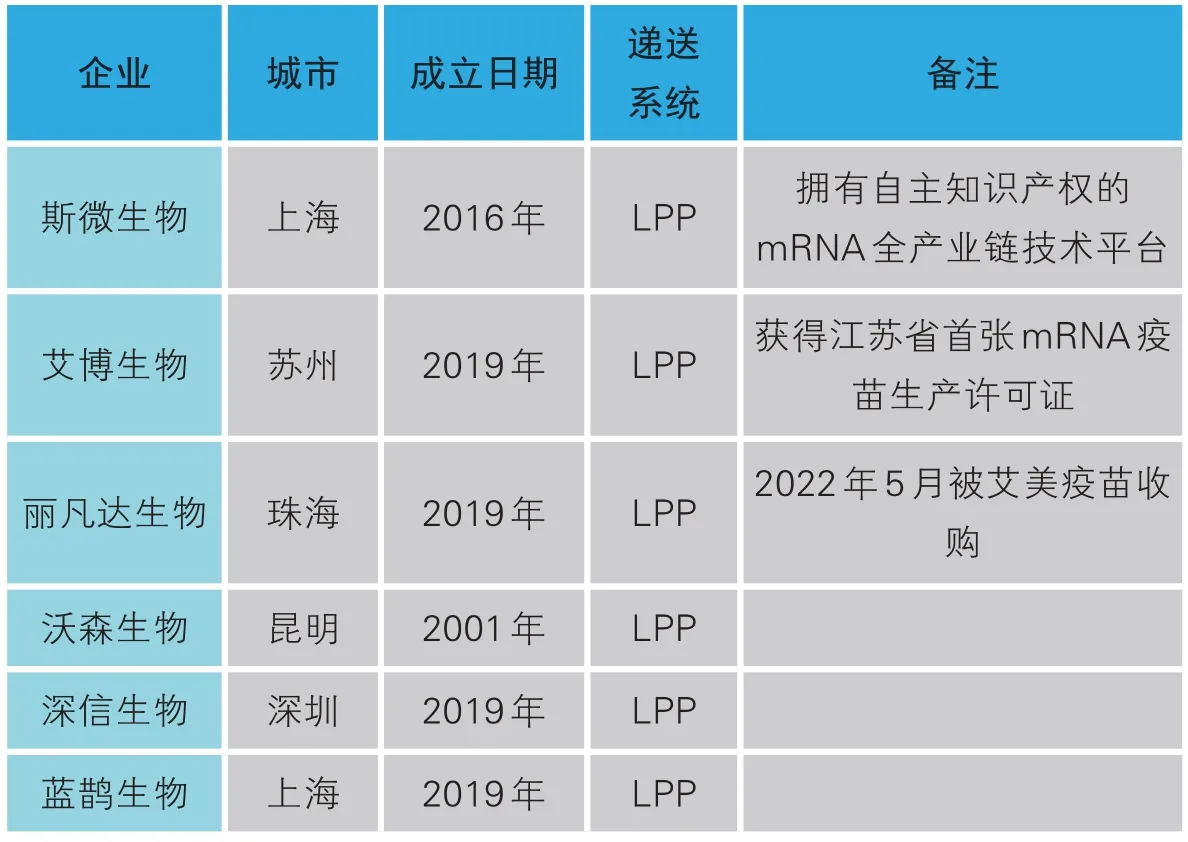
表2 我国主要mRNA技术相关企业
我国mRNA 疫苗研发热情高涨,临床试验持续推进。截至2022 年4 月,国内mRNA 疫苗在研管线有23 条,10 条与非新冠疫苗相关,显示mRNA 的疫苗应用场景也在不断拓宽。目前国内虽未有产品获得正式上市批准,但已经有多个mRNA 疫苗候选药物进入到临床阶段(如表3)。在国内临床进展最快的属艾博生物、军科院和沃森生物共同研制的ARCoVaX,全球和国内均已进入Ⅲ期临床试验。据沃森生物2022 年3 月发布的调研活动信息显示,ARCoVaX 国内三期临床的现场工作基本结束,正在进行数据整理和持续血清检测。进入我国Ⅱ期临床阶段的mRNA 疫苗还有复星医药与BioNTech 合作的Tozinameran及丽凡达生物的LVRNA009。■

表3 我国重点mRNA疫苗临床进展

