纳米金和ZIF-8改性的复合棉纤维的构建及其在染料分离/检测中的应用
董夏晓,叶勇,周吉
(湖北大学化学化工学院,湖北 武汉 430062)
0 引言
近年来,随着全球工业的快速发展,水资源污染极大地破坏了人类赖以生存的生态系统,并严重威胁到人类的健康.有机染料广泛应用在纺织、印刷、塑料、制药等行业,大量的有机染料废水的滥排造成了水体的严重污染,有机染料成为水体中主要的污染物之一[1-2].废水污染已经成为当今社会一个严重的问题,对废水中有机污染物的检测和监测至关重要.
表面增强拉曼散射(SERS)是一种依赖于活性基底表面附近分子的增强拉曼散射的检测技术,能实现超痕量分子的检测,其中金纳米粒子(gold nanoparticles,Au NPs)具有优异的光学特性而被广泛用作SERS活性基底[3].但面对目标分子的扩散、基质干扰等问题,SERS技术受到了挑战[4].金属有机框架(metal-organic frameworks,MOFs)材料相比于传统吸附材料如活性炭[5]、沸石[6]、金属氧化物纳米颗粒[7],它具有更高孔隙率和吸附容量,以及孔隙可调实现的高选择性,是废水处理及分离纯化应用领域的明星材料[8].在众多的MOFs材料中,ZIFs材料以其优异的水稳定性、毒性低而备受关注,能有效应用于水介质中[9-10]. MOFs与SERS技术的结合,能通过选择性捕获目标分子、电荷转移共振效应大幅度提高SERS检测灵敏度,在痕量呼出气体检测、食品和环境安全分析等领域取得巨大进展[11-12].但粉末状MOFs材料在实际应用中具有局限性,将MOFs原位生长或组装在其他材料载体上成为一个重要的发展方向.常见的载体有纤维素气凝胶[13]、混合基质膜[14]或杂化刚性[15]/柔性薄膜[16]等.
天然纤维材料大的比表面积有利于MOFs晶体的原位生长[17],大孔结构还能为MOFs提供吸附质的传输孔道,有利于分子扩散至MOFs空隙中发挥其吸附分离性能[18],是良好的支撑基体材料.棉纤维易获取、环保、成本低,含有多羟基活性位点.功能化棉纤维在保留吸湿、生物相容性等自身优势的前提下,其表面多羟基活性位点还可以与多种纳米材料组装或用于原位生长,进而赋予棉纤维光、电、热等更多方面的功能,其应用领域也不断地被拓展.如负载了金纳米粒子的柔性SERS棉纤维方便开展SERS采样和检测[19]、负载了UiO-66等疏水材料的棉纤维可以用于有机污染物的分离和回收利用[20]等.
本研究选取具有良好渗透性和较大比表面积的非织造棉纤维(non-woven fabric,NWFs)[19]作为支撑基体,通过水浴加热的方式原位负载了Au NPs,制备了NWFs@Au NPs复合纤维.然后,在NWFs@Au NPs复合纤维上利用剩余的羟基活性位点采用共沉淀法原位沉积ZIF-8获得NWFs@Au NPs@ZIF-8功能性复合纤维,材料的复合有效克服了单一材料的应用缺陷,并成功应用于混合染料的分离和SERS检测.
1 实验部分
1.1 试剂与仪器主要仪器:Sigma500热场发射扫描电子显微镜(德国Zeiss公司)、D8 Advance X线小角衍射仪(德国Bruker公司)、Diamond热重分析仪(瑞士梅特勒公司)、InVia型共聚焦显微镜拉曼光谱仪(英国Renishaw公司)、UV-3600紫外可见光分光光度计(日本岛津公司).
主要试剂:非织造布购于深圳全棉时代科技有限公司;HAuCl4、2-甲基咪唑、六水合硝酸锌、硝酸钠、孔雀石绿(Malachite green,MG)、亚甲基蓝(Methylene blue,MB)、甲基橙(Methyl orange,MO)、苏丹红I(Sudan1,SD1)均购于上海阿拉丁试剂有限公司;无水甲醇(>99%)、无水乙醇(>99%)购于上海国药集团化学试剂有限公司.以上试剂均为分析纯,实验用水来自杭州娃哈哈集团有限公司.
1.2 实验方法
1.2.1 NWFs@Au NPs的制备 金纳米粒子利用棉纤维的羟基还原性加热还原实现原位负载[21],具体实验步骤如下:将非织造布在50 ℃温水中洗涤3 min后用去离子水冲洗,室温下晾干;将洗净的织物浸入0.40 mmol/L HAuCl4水溶液中15 min,其中织物与溶液的浴比为1∶100,将混合溶液置于85 ℃的水浴中,振荡90 min后取出并用去离子水冲洗织物3次,室温晾干备用.
1.2.2 NWFs@Au NPs@ZIF-8的制备 将制备好的NWFs@Au NPs剪成1.5 cm×1.5 cm大小,浸入50 mmol/L 2-甲基咪唑和25 mmol/L硝酸锌甲醇混合溶液(二者摩尔比为40∶1),静置40 min后,取出用乙醇溶液冲洗并晾干.上述原位沉积步骤重复3次.
1.2.3 NWFs@Au NPs@ZIF-8的染料吸附性能 取质量均为14 mg NWFs@Au NPs@ZIF-8分别浸入2 mL浓度为5.0×10-5mol/L MG、MB、MO、SD1染料溶液中,用紫外可见分光光度计监测浸入不同时间时剩余溶液中染料分子的浓度变化,依据公式(1)计算该复合纤维材料对不同染料的吸附效果:
(1)
其中C0、Ct分别为染料的起始溶液浓度和吸附tmin后溶液浓度.
以5.0×10-5mol/L MG为吸附对象,用紫外可见分光光度计监测采用3种纤维(NWFs、NWFs@Au NPs和NWFs@Au NPs@ZIF-8)材料吸附不同时间染料溶液的浓度变化,计算不同纤维的吸附容量:
(2)
其中qt为几种不同纤维的吸附容量,C0、Ct分别为MG的起始溶液浓度和吸附tmin时溶液浓度,V为MG体积,这里我们取2 mL计算,M为MG相对分子质量(364.92 g/mol),m为几种不同纤维的质量.
1.2.4 NWFs@Au NPs@ZIF-8用于混合染料吸附和选择性分离 将NWFs@Au NPs@ZIF-8复合纤维浸泡在混合染料溶液(浓度均为1.0×10-4mol/L MG和MO等体积混合)中,记录随时间变化混合染料的吸收光谱.将NWFs@Au NPs@ZIF-8作为吸附分离垫层,填充到微量注射器中,垂直推动注射器过滤混合染料后,将复合纳米纤维垫层取出后,用去离子水清洗晾干后测试拉曼光谱,对吸附物质进行定性检测.
为了评估复合纤维材料的可重复使用性,以纤维材料作为吸附分离垫层对5×10-5mol/L MG染料溶液实现过滤吸附后,将NWFs@Au NPs@ZIF-8浸入NaNO3饱和溶液中,在室温下浸泡5 h,用去离子水清洗3遍晾干后继续进行了4个循环的过滤再生,记录吸收光谱.
1.2.5 NWFs@Au NPs@ZIF-8的SERS性能考察 将NWFs@Au NPs@ZIF-8浸入10-5、10-6、10-7、10-8、10-9mol/L MG溶液中1 h,用去离子水冲洗并晾干,采用同样的测试条件对MG进行SERS检测.光谱条件如下:785 nm激光,激光功率为10%,采集600~1 700 cm-1区间内光谱信号.
2 结果与讨论
2.1 NWFs@Au NPs@ZIF-8合成条件优化金纳米粒子和ZIF-8的负载量是该复合纤维实现吸附分离和痕量检测的关键要素.通过调整HAuCl4浓度和ZIF-8原位沉积的次数考察了该复合纤维的SERS增强性能.将0.13 mmol/L、0.30 mmol/L、0.40 mmol/L、0.50 mmol/L 4种不同浓度HAuCl4中原位热还原得到的复合纤维和未经修饰的非织造布浸泡在浓度为1.0×10-4mol/L MG溶液中1 h后,用去离子水洗掉表面物理吸附的MG分子并晾干后进行SERS测试.
如图1(a)所示,随着前体溶液HAuCl4浓度的增大,复合纤维颜色由浅红色逐渐加深为深紫色,当氯金酸浓度增大到0.50 mmol/L时,纤维颜色变成灰金色.当氯金酸浓度为0.40 mmol/L时SERS信号最强,这可能是因为该浓度下,原位生长的金纳米粒子尺寸和分散密度与测试条件最为匹配[21].如图1(b)展示的是ZIF-8沉积不同层数与SERS增强性能的依赖关系。随着沉积次数的增加,SERS信号不断增强,但当沉积次数过多时(>4次),由于紧密堆叠的ZIF-8纳米粒子包裹了首先沉积的金纳米粒子,即使ZIF-8层吸附了更多的染料分子,但染料分子却不在金纳米粒子产生增强电磁场的空间范围中,导致了SERS信号大幅降低[22].由此可见,当HAuCl4溶液浓度为0.40 mmol/L,ZIF-8沉积次数为3次时,该复合纳米纤维材料的SERS性能最优.

图1 NWFs@Au NPs@ZIF-8复合纤维材料在不同(a)HAuCl4浓度;(b)ZIF-8沉积次数制备条件下,1.0×10-4mol/L MG在1 172 cm-1处SERS信号强度变化
2.2 NWFs@Au NPs@ZIF-8表征扫描电子显微镜可以观察复合纤维材料表面纳米级的形貌和元素分布.如图2(a)所示,非织造布纤维表面呈现与棉纤维一致的多层次的凹槽和单纤维结构,表面光滑,没有附着纳米粒子.原位合成金纳米粒子后(图2(b)),光滑的单纤维表面均匀分布着约30~40 nm的金纳米粒子,继续沉积ZIF-8后,纤维表面紧密堆积着更大尺度的纳米粒子.为了更好地观察和分辨沉积的Au NPs和ZIF-8纳米粒子,我们对NWFs@Au NPs@ZIF-8复合纤维材料进行了选区的EDX能谱测试,如图3(a)所示,可以观察到纤维表面上均匀分散着Au、Zn、C和O元素,其中金元素的分布呈现多层次的单纤维结构,与非织造布本征特性相似,也进一步证明了金纳米粒子沿着纤维表面的原位沉积.来自于ZIF-8的Zn元素的分布浓度较高也很均匀,元素分析结果证明了金纳米粒子和ZIF-8的分层沉积.

图2 (a)NWFs;(b)NWFs@Au NPs;(c)NWFs@Au NPs@ZIF-8纤维的SEM图
图3(b)为不同样品的XRD衍射图. 14.6°、26.8°、22.8°和34.3°处的衍射峰为纤维素的特征峰[23].在氯金酸溶液中加热处理后,在38.2°处出现了一个新的衍射峰,对应于Au NPs的(111)晶面,表明Au NPs原位还原并沉积在纤维上.继续沉积ZIF-8后,在7.3°、10.4°、18.3°出现衍射峰,与ZIF-8的(011)、(002)、(222)晶面一致.非织造布的晶体衍射峰在两种纳米粒子负载前后没有明显改变,表明在原位热还原和溶剂沉积过程中不会破坏纤维的结构,也不会影响纤维本身的一些性质.
图3(c)是3种不同纤维材料的热失重分析曲线,以NWFs残余量为基准,NWFs@Au NPs和NWFs@Au NPs@ZIF-8的残余量分别为3.9%、7.8%,NWFs@Au NPs@ZIF-8残余量稍大是因为高温下未灰化的无机质含量的增多,这也间接证明了Au NPs和ZIF-8的逐层负载.
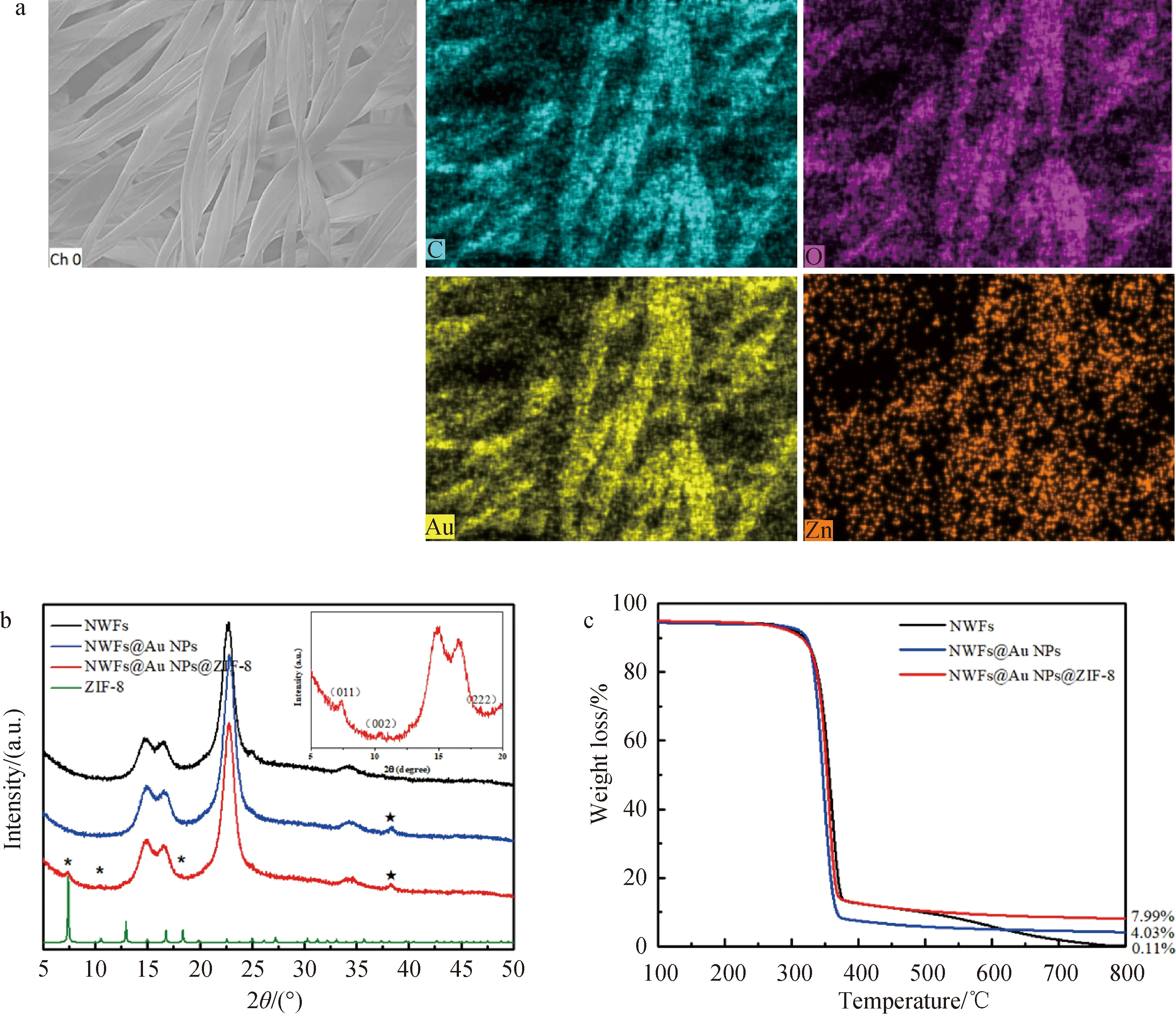
图3 (a)NWFs@Au NPs@ZIF-8复合纤维EDX元素分析;(b)3种纤维材料的XRD图谱及(c)TG分析曲线
2.3 NWFs@Au NPs@ZIF-8的吸附性能为了探究NWFs@Au NPs@ZIF-8复合纤维对不同染料的吸附性能,选择了两种代表性的阳离子染料MG、MB,一种阴离子染料MO和一种非离子染料SD1进行探究,4种染料分子结构及尺寸见表1.等质量复合纤维浸泡在等浓度的染料水溶液中,其中SD1为醇溶液,在给定时间内取染料溶液进行吸收光谱测试.4种染料分子吸收光谱随时间变化结果如图4所示,并根据公式1分别计算了NWFs@Au NPs@ZIF-8复合纤维对MG、MB、MO及SD1分子的去除效率,分别为86.44%、31.56%、22.44%和12%,如图4e所示,影响吸附去除效率的影响因素可能有分子尺寸效应、水溶性及其在水溶液中的粒子带电性. NWFs@Au NPs@ZIF-8复合纤维对MG分子去除效率最高,一方面,ZIF-8的孔径大小为3.4×10-1nm,MG分子与ZIF-8的微孔尺寸更加匹配[24],另一方面是MG分子有良好的水溶性有助于吸附的发生.相比于SD1分子,其水溶性较差,不利于吸附,因而去除效率最低. MB、MO分子均能溶于水,但分子尺寸较大,去除效率明显弱于MG分子,他们的差异更多来源于水溶液中粒子带电性差异.随后我们以MG为研究对象,还考察了NWFs、NWFs@Au NPs和NWFs@Au NPs@ZIF-8 3种纤维对MG的吸附容量,由图4(f)可知,未修饰的非织造布具有吸湿特性,并且表面的多羟基结构对正电荷染料具有静电吸附作用,原位合成Au NPs后,由于表面羟基被部分消耗导致吸附性能下降,而沉积了ZIF-8多孔材料后对MG的吸附容量明显增大,并且在前10 min,吸附速率极快.
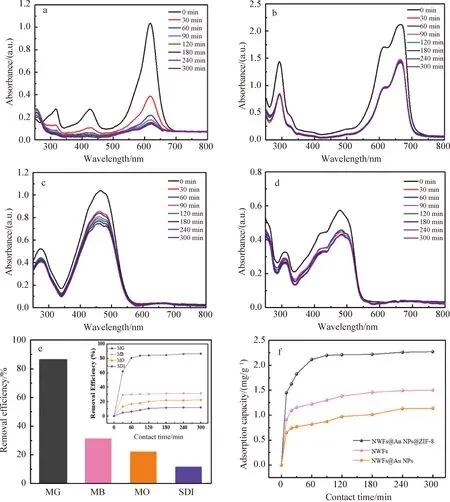
图4(a~d)NWFs@Au NPs@ZIF-8复合纳米纤维依次对MG、MB、MO、SD1吸附的紫外-可见光谱图及(e)在室温下6 h内染料移除效率(插图:不同吸附时间间隔染料去除效率);(f)不同纤维对MG的吸附效果
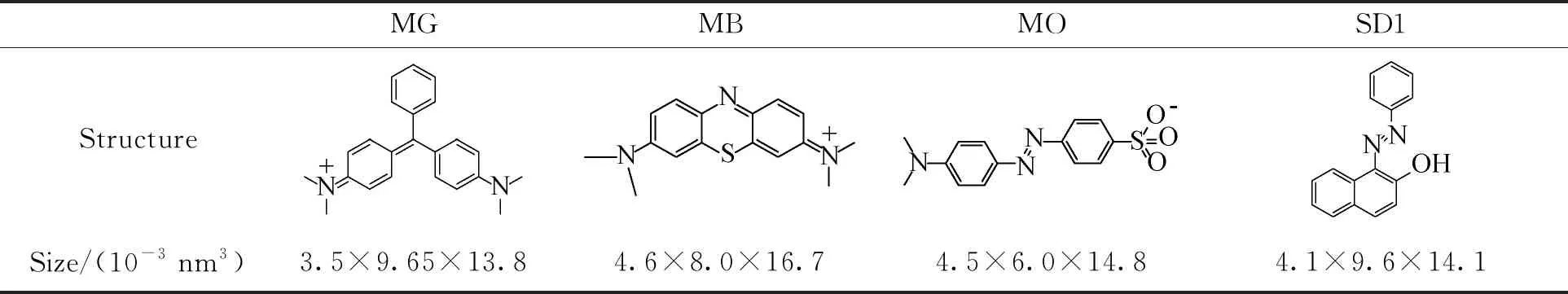
表1 染料分子的结构及尺寸
2.4 NWFs@Au NPs@ZIF-8用于混合染料吸附和选择性分离依据NWFs@Au NPs@ZIF-8复合纤维对不同染料吸附作用不同,选择MG+和MO-混合溶液为研究对象考察了该复合纤维材料对混合染料的分离效果,如图5(a)所示,混合溶液的吸收光谱存在两个明显的吸收峰,其中464 nm和617 nm分别对应于MO、MG的紫外可见吸收的最大吸收波长.在10 min内617 nm的吸收峰强度迅速下降,而464 nm吸收峰强度没有明显变化,2 h后对应于MG的吸收峰强度几乎不再下降达到吸附平衡,说明该复合纳米纤维对MG具有明显的吸附,而对MO没有明显的吸附作用.混合染料吸附前后颜色变化如图5(a)所示,随着吸附过程的进行,混合染料颜色由黄绿色逐渐变成黄色.进一步地,我们将NWFs@Au NPs@ZIF-8复合纤维作为分离垫层填充到微量注射器底部,如图5(b)所示,混合溶液流经纤维垫层后,MG分子被快速吸附在复合纳米纤维中,而MO溶液流经纤维并最终被回收,实现了混合染料的快速分离,将纤维垫层取出后冲洗后进行拉曼检测,其SERS光谱如图5(c)所示,与MG粉末样品的拉曼光谱一致,表面复合纤维成功对MG-MO混合染料实现快速分离,有效排除检测干扰.该分离模型未来有望拓展用于废水样品中多种染料的吸附分离和鉴定,具有较好的应用潜力.
进一步地,我们还研究了该复合纤维材料的吸附再生性能,以浓度为5×10-5mol/L MG为研究对象,将过滤吸附MG后的复合纤维浸泡在饱和NaNO3溶液中5 h,当Na+浓度足够大时,Na+可以和MG+进行离子交换实现材料再生[16],结果如图5(d)所示,经过4次过滤-解吸循环,复合纤维材料对MG的移除率始终达到80%以上,去除效率的缓慢降低可能由于非织造布结构松散,反复浸泡在溶液中有微小的质量损失导致的.
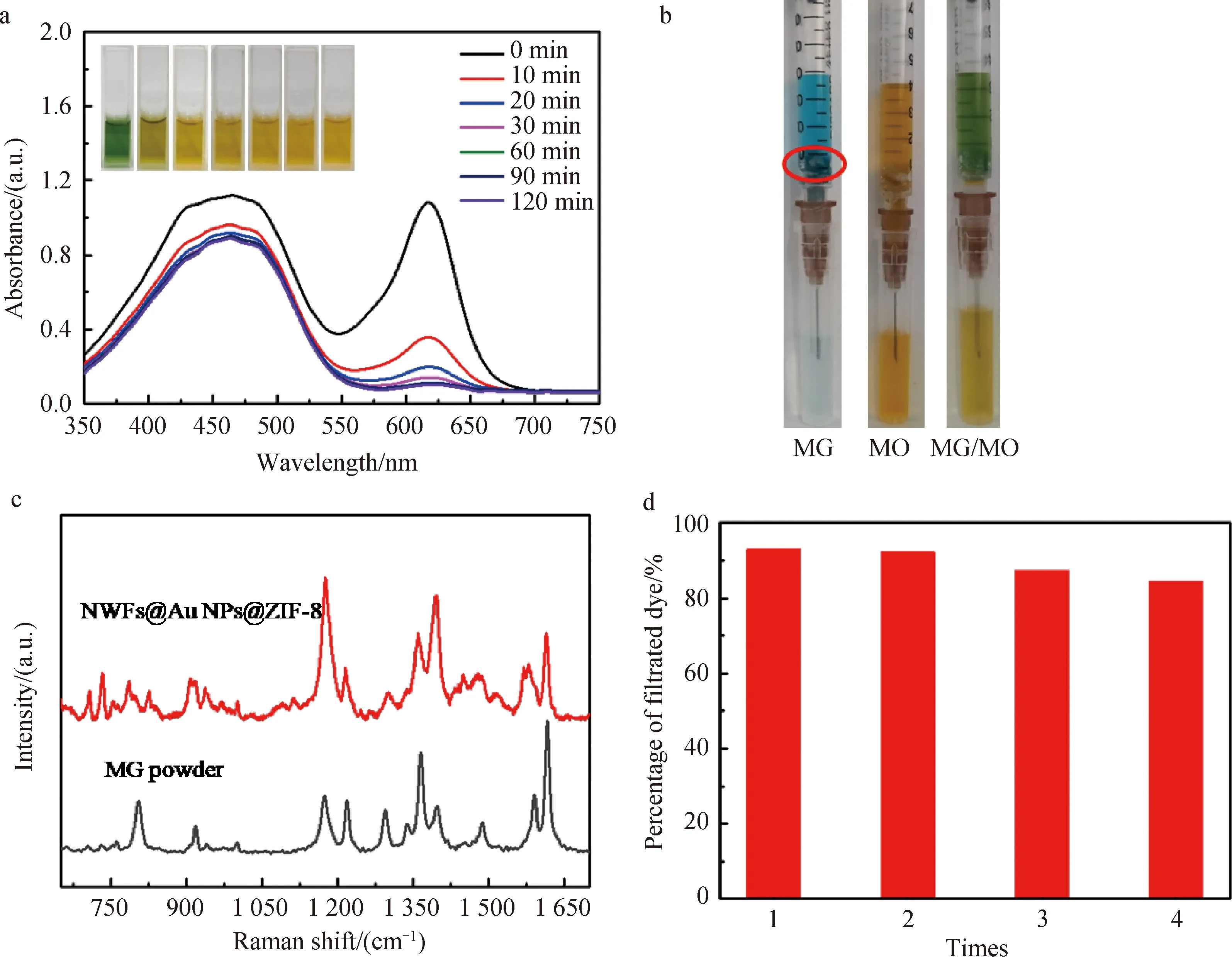
图5 NWFs@Au NPs@ZIF-8复合纤维(a)分离MO-MG混合染液的紫外-可见光谱图(插图:分离过程混合染料溶液的颜色变化);(b)作为吸附分离垫层的柱分离实验;(c)实现分离后的SERS检测图谱;(d)以5×10-5 mol/L MG为吸附对象,复合纤维循环再生性能
2.5 NWFs@Au NPs@ZIF-8 SERS性能为了更好地实现该复合纤维对不同场景废水中有机染料吸附分离和鉴定,我们还考察了该复合纤维的SERS性能,探究其对染料分子的最低检测浓度.以MG为研究对象,探究了复合纤维对不同浓度MG分子的检测效果,结果如图6所示,随着MG浓度的降低,棉纤维的特征拉曼峰1 095 cm-1逐渐增强,而MG的1 172、1 615 cm-1等特征振动峰逐渐减弱,该SERS基底对MG分子的最低检测浓度为1.0×10-9mol/L.
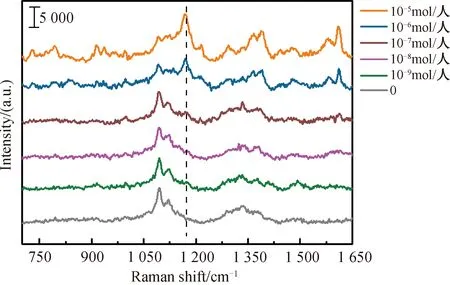
图6 NWFs@Au NPs@ZIF-8复合纤维检测不同浓度MG的SERS谱图
3 结论
采用原位合成和共沉淀方法制备了NWFs@Au NPs@ZIF-8复合纤维材料,利用SEM、EDX、XRD、TG等手段证实了在没有破坏纤维原有结构的基础上,Au NPs和ZIF-8纳米粒子的成功负载.非织造布所具有大孔结构以及吸湿特性,与ZIF-8纳米粒子的多孔结构结合,赋予织物良好的选择吸附特性,能有效选择性吸附MG,成功实现对MG-MO混合溶液的快速分离.结合Au NPs优异的SERS特性,实现对吸附质MG的快速检测,实验表明该复合纤维基底可实现对1.0×10-9mol/L MG的检测.此外,该复合纤维可实现循环再生,在实际水污染处理中具有较好的应用潜力.

