人工智能自动检测系统辅助超声诊断乳腺结节的临床应用
吴 墅, 赵佳琦,2, 陈 蕊
(1. 上海中医药大学附属曙光医院超声中心,上海 201203; 2. 海军军医大学(第二军医大学)第二附属医院超声诊断科,上海 200003)
最新的中国癌症数据显示,乳腺癌为女性发病首位的恶性肿瘤,早期准确诊断与评估对改善乳腺癌预后至关重要[1-3]。超声检查以无辐射、方便、可重复性等优点广泛应用于乳腺病变筛查[4]。然而,乳腺良恶性病变在超声图像特征上存在部分交叉重叠,超声医生读图诊断在很大程度上依赖于自身的主观经验。近年来兴起的深度学习方法模拟识别和人工智能(artificial intelligence, AI)检测影像图像备受关注[5],能够快速精准在短短几秒内锁定病灶,进行自动分析、自动生成诊断报告,辅助超声医师对病灶良恶性进行客观量化判读。部分研究初步表明AI对甲状腺、乳腺、肝脏等结节的良恶性判断具有较高的的实用价值[6-8],可为超声医师提供高准确度、高效率的工作决策支持。
本研究拟利用一种乳腺AI自动检测系统联合常规超声(ultrasonography, US)检查用于综合评价乳腺结节的良恶性,以探讨US与AI联合应用对乳腺良恶性诊断价值。
1 资料与方法
1.1 研究对象

纳入标准: (1) 病灶有清晰可辨的灰阶图像,不带测量标记;(2) AI检测系统能识别乳腺病灶;(3) 同一结节无既往治疗史;(4) 所有病例均经手术切除并确定病理类型。
排除标准: (1) 超声影像资料不全;(2) AI检测系统未能识别乳腺结节。
1.2 仪器及检查方法


1.3 数据分析
采用STATA 15.0软件进行统计分析。分类变量采用χ2检验或Fisher精确检验,连续变量采用独立t检验。BI-RADS分类资料采用Wilcoxon轶和检验。以术后病理结果为金标准,构建受试者工作特征(receiver operating characteristic curve, ROC)曲线,比较AI、US和AI+US等3种检测方法用于诊断乳腺结节良恶性的灵敏度、特异度和准确度。采用卡方检验比较不同诊断方式的ROC曲线下面积(area under the curve, AUC)。P<0.05为差异有统计学意义。
2 结 果
2.1 病理结果和常规超声检查结果
所有253例乳腺结节中,56例(22.1%)经病理分析证实为恶性(浸润性导管癌38例,导管原位癌12例,导管内乳头状癌5例,髓样癌1例)。其余197例(77.9%)为良性(纤维腺瘤105例,乳腺病54例,浆细胞性乳腺炎32例,乳腺炎合并脓肿4例,单纯性囊肿2例)。结节分布位置如下: 位于右乳136例(53.7%),位于左乳117例(46.2%)。其中,恶性结节大多表现为边缘不清和形态不规则,在结节纵横比、内部回声、后方回声、有无钙化、内部血流方面差异具有统计学意义(P<0.05),见表1。

表1 常规超声乳腺病灶特征
2.2 不同检测方法对乳腺BI-RADS分类结果比较


图1 乳腺纤维腺瘤两种检查方法图像

图2 乳腺浸润性导管癌两种检查方法图像
2.3 不同检测方法的ROC曲线及诊断效能分析
根据不同检测方法下的BI-RADS分类特征,以术后病理结果为金标准,绘制ROC曲线(图3),得出AI诊断乳腺肿瘤评分的最佳诊断界点为0.425,最佳分类界点为4a级(即≥4a),比较3种检测方法的诊断价值,发现联合诊断的效能均高于单独使用AI和US的诊断效能(表3),其中联合诊断乳腺结节良恶性的特异度和准确度都高于AI(P<0.01),联合诊断乳腺结节恶性的灵敏度高于US(P<0.01),可得出AI+US的联合诊断效能最高。AI+US与AI、US的AUC值存在显著差异(Z=5.575,P<0.000;Z=2.904,P<0.003)。
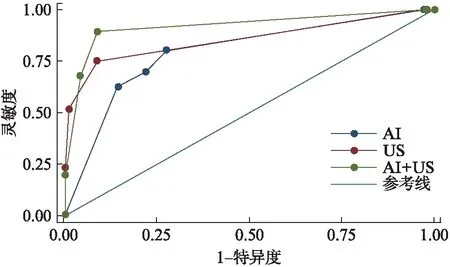
图3 不同检测方法对乳腺结节良恶性诊断的ROC曲线对比
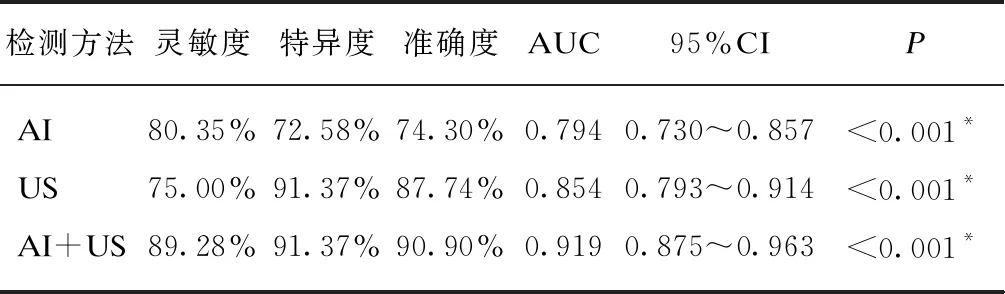
表3 三种不同检测方法对乳腺结节良恶性诊断的效能指标比较
3 讨 论
超声成像技术已被公认为乳腺癌早期诊断的主要方法。超声由于其无辐射性、无创性及其相对较低的成本,就可以获得乳腺病灶图像,被广泛应用于乳腺肿瘤的诊断及治疗[4,10]。然而,在临床实践中,乳腺超声图像的信息量巨大,乳腺癌超声表现又多变,不同年资医师诊断水平差异也较大,这些都是影响乳腺癌诊断准确率的重要原因。因此需要一种可靠、稳定辅助乳腺超声诊断技术[5]。
1956年,美国达特茅斯大学举行首次AI研讨会,John McCarthy等首先提出“人工智能”的概念[11]。近年来,AI在医疗领域的应用引起关注,特别是在辅助乳腺超声诊断技术方面,AI乳腺超声能够对乳腺病灶图像进行自动识别及分类,甚至模拟临床医师对乳腺癌进行诊断和预后评估[12-15]。已有报道AI在乳腺良恶性疾病鉴别诊断中具有较高的有效性和可靠性。Fujioka等[16]基于二维超声成像技术提取乳腺病灶形态特征,自动AI乳腺超声检测,研究结果表明,该类AI乳腺超声对乳腺良、恶性肿瘤辅助诊断的准确率为92.5%,灵敏度为95.8%,特异度为92.5%,而且可在较短时间内完成。高思琦等[17]回顾性分析多中心乳腺病例1 460例,认为AI在鉴别乳腺良恶性病灶中具有较高的特异度,可以为乳腺疾病诊断提供客观依据。但这些报道多是对AI的诊断效能与医师进行对照研究,而没有对AI与US联合诊断进行研究。本研究将两种检查联合发现具有较高的诊断效能,其诊断灵敏度为89.28%,特异度为91.37%,准确度为90.90%,ROC曲线下面积为0.919,显示联合诊断效能均高于单独使用US和AI检测方法,这与杨磊等[18]的研究结果一致。其中联合诊断乳腺恶性结节的灵敏度高于US(P<0.01),考虑AI通过深度学习,能够高效精准地提取乳腺结节的形态特征,如结节细毛刺、微钙化等,较一般超声医师肉眼识别结节更为灵敏和客观,联合AI可提高乳腺恶性结节的检出率[6]。
目前文献报道的研究中乳腺结节多以恶性居多,而本组资料乳腺结节以良性居多(197例),其中乳腺炎病灶有36例。在本研究中,AI检测良性结节呈4类恶性的有54个(27.4%),其中有26例属浆细胞性乳腺炎被误判呈假阳性,大大降低了AI对良性结节检测的特异度。分析浆细胞性乳腺炎影像特征[19],多表现形态不规则的肿块,多无明显包膜,边缘可呈毛刺状,多粘连周围组织及皮肤,极易误诊为乳腺癌。AI根据浆细胞性乳腺炎静态影像图像,容易出现误判。而超声医师可根据动态扫查,多切面综合判断病灶形态特征,浆细胞性乳腺炎多呈现管道状,其内含有炎性分泌物漂浮等影像特征,较容易诊断为炎性病灶,减少了对乳腺炎性病灶的误判,从而提高其特异度。因此本样本联合检测的特异度和准确度都高于单独AI检测(P<0.01)。
此外,本研究还发现常规超声及AI对导管原位癌的诊断能力均较低,可能是由于导管原位癌病灶较小,超声恶性特征不明显,容易导致误诊,这与Xiao等[20]的研究结论一致,但本研究中关于导管原位癌的病理类型仅12例,可能还需要大样本量研究进一步验证。因此,在运用AI检测时,还需结合常规超声影像特点,乳腺结节大小等多方面特点综合判断。不能仅依靠AI检测数据,以免延误乳腺恶性结节早期诊断。
由于本研究属于回顾性研究,尚存在一定的研究局限性。首先,本研究样本量相对较少,尤其是少见病理类型的乳腺结节占比不多;其次,本系统识别仅限于静态图像,没有将动态图像及病史资料等纳入诊断评估中,医生间操作差别也可能降低研究的诊断效能;另外,本研究纳入的恶性结节例数明显少于良性结节,难免造成研究偏倚,未来应加强对多中心、大样本的乳腺结节进行研究。
综上所述,AI自动检测系统可辅助超声诊断乳腺结节,有助于乳腺结节良恶性鉴别;AI自动检测系统与US检查联合应用,能够提高对乳腺结节良恶性的诊断效能。

