基于CT 的机会性筛查评估骨质疏松症的研究进展
陈明月 张雪丽 汤光宇
随着人口老龄化,骨质疏松症(osteoporosis,OP)在全球的患病率逐渐增加,已成为重要的公共卫生问题。OP 是一种代谢性骨骼疾病,其特征为骨量减少和骨微结构的退化,导致骨脆性和骨折易感性增加[1]。骨质疏松性骨折是OP 的严重并发症,可引起急性或慢性疼痛、残疾,极大地降低了病人的生活质量,甚至增加死亡的风险,同时也给医疗卫生和社会保障体系带来沉重负担[2]。
多种影像技术在OP 的诊疗过程中发挥着重要作用。其中,双能X 线吸收法(dual-energy X-ray absorptiometry, DXA)测定的面积骨密度(area bone mineral density, aBMD)能反映骨量信息,是当前诊断OP 的金标准,但其属于二维成像,尚存在以下不足:①脊柱退行性改变、脊柱侧弯及后凸畸形、主动脉钙化和未被识别的轻度骨折都会引起DXA 假性aBMD 增加[3];②DXA 无法区分松质骨与皮质骨,而小梁骨具有比皮质骨更早期的增龄损失[4],这降低了DXA 的敏感性;③体质量或身体厚度影响DXA测量,对肥胖病人的诊断准确性会降低[5];④DXA 对骨骼尺寸存在较大依赖性,在骨骼体积较小的受试者中BMD 值会被错误地低估,因此在儿童骨骼测量中应用受限[6]。同时,越来越多的证据表明仅依赖DXA 进行OP 筛查和骨折风险评估存在一定局限性,如目前英国的临床指南不建议单独使用DXA进行 OP 筛查[7]。
定量CT(quantitative CT,QCT)通过专用软件和校准体模可将CT 值转换为腰椎或髋部体积骨密度(volumetric bone mineral density,vBMD)。QCT 已被普遍认为可以诊断OP。在此基础上,近年有研究者[8]提出了基于CT 技术的OP 机会性筛查,即“机会性CT”,具体是指通过借助因其他临床目的而进行的常规CT 成像来寻找潜在的OP 病人和进一步评估骨折风险。在我国,每年针对各种临床适应证和胸部体检进行了大量的CT 扫描,机会性CT 筛查在辐射剂量、检查时间和成本等方面不会给病人带来额外负担,克服了传统专用QCT(专门为骨骼定量测量获取的CT)的不足。许多定期接受CT 检查的病人可以从这种机会性策略中获益。本文回顾了国内外机会性CT 筛查OP 的最新研究进展,较为全面地阐述了不同筛查方法及相关临床应用,为扩大临床实践提供了理论支持。
1 机会性CT 筛查OP 的方法
基于CT 的BMD 评估方法主要有3 种,分别为传统专用QCT、机会性QCT 和直接使用椎体CT 值,其中机会性QCT 包括异步外部校准QCT 和无体模校准 QCT(phantomless QCT,PL-QCT)(表 1)。QCT的校准体模是由已知浓度的羟基磷灰石或磷酸钾(K2HPO4)制作成的固体模型。传统专用QCT 扫描时,将体模置于受检者下方,与受检者同时接受扫描,采用同步外部校准方式(图1A)。然而,临床常规CT 检查时体模不会与病人一同扫描,因此专用QCT 不适合做机会性筛查。而机会性QCT 和直接使用椎体CT 值为OP 的机会性筛查提供了契机。

表1 基于CT 的BMD 评估方法的特点对照
1.1 机会性QCT 机会性QCT 评估BMD 具有显著的优势,可以从多平面选取兴趣区(ROI),测量结果受脊柱退行性疾病、脊柱畸形、血管钙化、组织重叠以及体质量变化的影响较小(图2)。该方法具有异步外部校准和无体模校准2 种方式,是OP 机会性筛查的主要方法。①异步外部校准QCT 是对体模进行单独质量控制扫描,获得的校准方程式应用于后续的病人扫描,这极大地方便了临床上QCT 的机会性使用(图1B、1C);但病人扫描与体模扫描之间可能存在较大时间差,如果CT 扫描设备不稳定,则不同时间点所获得的vBMD 可能不够准确。在临床实践中,CT 扫描设备的稳定性可以通过间隔较短的定期质量控制扫描来纠正。有研究[9]表明,通过异步校准QCT 可以更加方便地获得脊柱vBMD,且具有与传统QCT 相似的准确度和短期精度。国际临床密度测定学会(International Society for Clinical Densitometry,ISCD)提出,在恒定校准和扫描设备稳定的前提下,可以使用异步校准扫描来代替传统同步体模校准[10]。②PL-QCT 是指将受试者自身内部组织(肌肉、脂肪、血液)和/或空气的CT 值作为校准参考来计算vBMD(图1D)。PL-QCT 避免了异步校准QCT 扫描设备不稳定影响测量结果的问题。然而,PL-QCT 由于手动选择人体内部校准组织的ROI,重复测量精度低于异步校准QCT[11]。此外,由于内部校准组织的成分因受试者而异,PL-QCT 会产生额外的BMD 准确度误差,具体取决于使用的内部校准组织类型[12]。根据受试群体进行具体调整可以最大限度减少此类错误。Liu 等[13]开发了一种自动选择组织ROI 的PL-QCT 新系统,确保了BMD测量的一致性,从而显著提高了精度,同时保持了与基于体模的QCT 相似的OP 诊断性能。这种高精度和高准确度的自动PL-QCT 系统有望作为OP 机会性筛查工具并有较大的临床转化潜力。

图1 基于CT 的BMD 筛查方法。A 图,体模置于病人身下行同步外部校准扫描(传统专用QCT);B、C 图,单独使用体模行质量控制扫描,对后续病人行异步外部校准扫描;D 图,使用腰大肌和皮下脂肪对BMD 行无体模校准;E 图,直接使用L1 椎体CT 值。
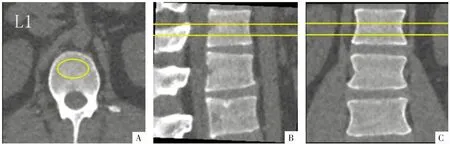
图2 机会性QCT 测量腰椎BMD 方法。以L1 椎体为例,在QCT 工作站上通过调整横断面(A)、矢状面(B)和冠状面(C)影像将ROI(圆圈和横线所示)放置于椎体的中央区域。
1.2 直接使用椎体CT 值 随着CT 扫描设备校准水平的进步,有研究者[8]提出直接使用常规CT 值(以HU 为单位)评估BMD 的可能性。与其他椎体相比,L1椎体作为第1 个不带肋骨的椎体易于识别,它在所有标准的胸部和腹部CT 扫描中均可见,大大提高了机会性CT 的总体筛查率。Perrier-Cornet 等[14]研究表明,在 L1椎体中(避开骨皮质)手动放置椭圆形ROI 是量化椎体CT 值和评估BMD的可靠方法(图1E),测量结果与DXA T 分数密切相关。在纵向评估BMD 变化的机会性筛查中发现,L1椎体CT 值自动测量与手动放置ROI 的数据显示出良好的一致性[15]。不同制造商生产的CT 扫描设备之间存在衰减值测量的系统性偏差[16]。在进行多中心研究时需注意此点。与QCT 相比,直接使用椎体CT 值评估BMD 的准确性相对较低,其诊断OP的价值仍需进一步探讨。
2 机会性CT 筛查OP 的衍生技术
2.1 CT X 线吸收法(CT X-ray absorptiometry,CTXA) CTXA 是利用3D QCT 数据集生成类似DXA 的骨骼投影影像以评估髋部(股骨近端/股骨颈)aBMD 的技术。在使用参考数据计算后,可以通过QCT 衍生的aBMD 得出DXA 等效T 评分。已有研究[17]显示CTXA 与DXA 在股骨近端BMD 测量中具有高度一致性,并在异步校准的机会性QCT 中得到了充分验证。CT 较二维平面投影可获得更多解剖细节,因此CTXA 比DXA 提供更多的研究信息。通过CTXA 在常规骨盆CT 扫描中进行前瞻性或回顾性的股骨颈BMD 的机会性测量,有助于提高OP 整体筛查率。CTXA 的股骨颈aBMD 和等效T 评分的临床接受度比传统QCT 测量值更广泛,现已被引入WHO 骨折风险评估工具(fracture risk assessment tool,FRAXTM)中,该工具整合了多种临床风险因素,可计算40~90 岁人群骨质疏松性骨折的10 年概率[18]。
2.2 有限元分析 骨强度下降是发生骨质疏松性骨折的重要因素之一,但在筛查或分层骨折风险的临床工作中,CT 成像的生物力学相关性仍没有得到充分考虑。有限元分析(finite element analysis,FEA)是一种利用CT 成像数据建立特定模型以评估骨微结构和机械强度的无创性方法。该模型使用CT 衍生的骨几何学、骨皮质厚度和材料特性数据来预测包括脊柱和髋关节在内的骨质疏松性骨折风险。Allaire 等[19]研究表明较低的腰椎强度与新发或恶化的椎体压缩性骨折有关。Rayudu 等[20]使用常规多层CT 成像数据生成FEA 模型以评估椎体骨折风险,结果显示扫描层厚(1 mm 和3 mm)和是否使用静脉对比剂对FEA 预测值无显著影响,基于常规CT 的FEA 机会性应用具有临床可行性。此外,Winsor 等[21]验证了PL-QCT 在FEA 骨强度估计中的有效性。近年来,美国医学协会提出了一种更全面的骨骼评价手段——生物力学CT(biomechanical CT,BCT),其内容包括FEA 的骨强度信息、髋部CTXA 的等效T分数以及脊柱vBMD 测量,OP 机会性筛查被批准作为BCT 检查的主要临床适应证[22]。近年有研究[23]表明,CT 衍生的FEA 骨强度在髋部骨折预测中具有比DXA aBMD 更好的性能,但其用于椎体时并没有显著优于单独使用vBMD,vBMD 和FEA 强度结合只能轻微地改善骨折相关性。
3 机会性CT 筛查在OP 中的临床应用
3.1 筛查OP 病人 通过借助因其他临床目的而进行的CT 成像对OP 进行机会性筛查可以有效降低成本和辐射暴露。此外,机会性CT 允许对既往CT 影像进行回顾性分析,任何胸部、腹部或盆部扫描都适用于椎体BMD 评估。Cheng 等[24]在一项大型多中心研究中报道了机会性使用肺癌筛查的低剂量胸部CT 评估OP 的可行性,结果显示L1-L2vBMD 筛查 50 岁以上中国女性OP 的患病率为29.0%,与DXA 检查的患病率(29.1%)相当,而检出男性 OP 的患病率是 DXA 的 2 倍多(13.5%和6.5%)。尽管胸椎的平均BMD 值高于腰椎,但Therkildsen 等[25]使用心脏CT 扫描评估冠心病病人的胸椎BMD 值的研究表明,基于胸椎BMD 的机会性OP 筛查同样具有临床价值。
2013 年 Pickhardt 等[26]提出根据 DXA 定义的骨量分类,当L1椎体CT 阈值为160 HU 时,其诊断OP的敏感度为90%,阈值为110 HU 的特异度>90%,而L1椎体CT 值<100 HU 可以帮助识别需要进一步评估或治疗的高危人群。随后在此基础上一些研究者[14,27-28]相继在糖尿病、类风湿性关节炎及与骨质流失相关的癌症病人中开展了大量研究。近年,Jang等[29]通过20 000 多例CT 扫描的大样本建立了不同年龄段L1椎体CT 值的参考范围,以便快速进行机会性OP 筛查。在临床应用中,常规椎体CT 值由于诊断价值有限可作为一种初筛工具,帮助识别OP 高风险个体以确定是否需要进一步DXA 或QCT 检查。
3.2 预测骨折风险 椎体骨折(vertebral fracture,VF)是所有骨质疏松性骨折中最常见的,且与后续骨折的发生相关。Leonhardt 等[30]通过前瞻性队列研究报道了使用机会性QCT 在58 例病人3 年随访期内预测新发骨折的可行性,结果显示vBMD 每降低1 mg/cm3,骨折概率增加3%,而DXA T 评分与新发骨折无显著相关性。Johannesdottir 等[31]在更大的队列研究中进一步观察到无论VF 发生位置如何,使用胸椎或腰椎vBMD 及FEA 强度估计都可以很好地进行预测。使用椎体CT 值同样为骨折风险评估提供了客观依据。还有研究者[32]发现中或重度椎体压缩性骨折病人的L1椎体CT 值显著减低,L1椎体CT 值≤90 HU 可能是确定VF 风险的最佳阈值。Lee 等[33]回顾性分析了507 名65 岁以上的成年人胸/腹部CT 影像,其中有114 例病人在随访期内发生骨折,结果表明L1椎体CT 值的降低与未来椎体或其他位点骨质疏松性骨折的发生密切相关。
在过去的5 年中,人工智能技术,尤其是深度学习算法越来越多地应用于OP 骨折风险的预测,对CT 数据集中的椎骨进行全自动分割和标记显著提高了筛查效率。Löffler 等[34]研究发现基于CT 的全自动骨骼测量数据(骨矿含量除外)对VF 的预测能力优于DXA,且自动和手动测量之间无明显差异。近年,一项基于腹部CT 的骨骼、肌肉和脂肪全自动模型提供了与FRAXTM相当的性能,可对无症状成人未来骨质疏松性骨折进行预测[35]。
尽管CT 机会性筛查的各种方法已经展现出良好的性能,但骨质疏松性骨折是多因素共同作用的结果,包括年龄、性别、先前骨折史、使用糖皮质激素或其他高危合并症等[7]。真正改善骨折风险预测的关键可能是将BMD 筛查结果与其他临床风险因素相结合,再整合到骨折风险评估工具中,并提高模型的可重复性。
3.3 纵向评估疗效 OP 治疗旨在改善并维持BMD 以降低骨折风险。皮质骨和松质骨因代谢转换率不同,对药物治疗反应也不同。机会性QCT 不仅可以评估骨的整体vBMD 和骨强度(联合FEA),还能分别评估皮质骨和松质骨,有助于更好地了解OP 治疗对骨骼的具体影响。Brown 等[36]在对绝经后OP 妇女的治疗研究中发现,与阿仑膦酸钠相比,罗莫单抗对腰椎vBMD 和FEA 骨强度参数的改善更显著,其中松质骨的vBMD 百分比变化趋势高于皮质骨(分别为21.4%和17.8%);同时观察到椎体强度的绝对变化与vBMD 变化的相关系数高于DXA。这一发现支持QCT 在评估OP 疗效方面优于DXA。另有研究[37]表明在类风湿性关节炎病人中使用基于CT 的FEA 能够纵向评估疗效;腰椎骨强度预测值在特立帕肽治疗6 个月和12 个月后的百分比增加(10%和14%)均大于aBMD(4.0%和6.6%),更重要的是前者与骨代谢标志物水平的变化显著相关。
3.4 肌肉、脂肪等身体成分信息的获取 机会性CT 筛查可以将BMD 与肌肉、脂肪等身体成分的定量分析结合起来,后者有助于诊断肌少症。肌少症被定义为骨骼肌质量和功能受损,已被证明是髋部骨折的独立预测指标,并且与生活质量下降和死亡率增加相关[38]。肌少症可以根据CT 影像上的肌肉横截面积或肌肉密度来诊断。骨骼和肌肉组织关系密切、交互作用。已有研究[39]显示,椎旁瘦组织对BMD 的变化存在正向作用,而肌间脂肪与之相反。“骨肌减少症”是指同时患有OP 和肌少症的病人,预后通常比仅患有肌少症或OP 的人群要差。机会性CT 在常规CT 扫描的基础上同时获取额外的骨量和身体成分信息,为OP 和肌少症病人的早期诊断、评估和干预提供了客观依据。
4 机会性CT 筛查OP 的注意事项
在机会性CT 的相关研究中,不同扫描设备采集和重建参数的差异较大,对比剂、管电压和管电流以及层厚等因素对BMD 测量的影响尚不明确,应用软件的图像分割技术和分析算法同样影响骨骼评估。将CT 评估所需的技术因素标准化,有助于更广泛地实施OP 机会性筛查。
4.1 CT 扫描参数 较高的辐射剂量一直是限制CT 临床应用的因素,降低管电压和管电流可以降低辐射剂量。Garner 等[40]研究发现,与脂肪或软组织相比,管电压对松质骨CT 值的影响更显著,随着管电压的降低,L1椎体CT 值增加;120 kV 条件下的L1椎体CT 值参考标准不能直接应用于其他电压设置下的单能或双能CT。而当管电流降低至标准值的10%~25%时,CT 影像受噪声干扰较大,导致BMD绝对值的显著改变[41]。采用CT 技术进行机会性筛查时需要严格的质量控制管理,以确保结果的准确性和可重复性。
4.2 对比剂 目前,对比剂对BMD 测量结果的影响意见不一。Ziemlewicz 等[42]研究显示,在盆腔增强CT 中通过CTXA 获得的股骨近端aBMD 几乎与平扫相当。然而有研究[43]表明,在给予对比剂后,脊柱QCT 测量值可能具有较大差异。对比剂注射后渗透到高度多孔且血管化良好的椎体松质骨中,显著增加了其CT 值。因此,如果BMD 测量值没有根据对比增强进行调整,增强CT 可能导致7%~25%的OP病人漏诊。对比剂同样可以导致肌肉密度衰减值增加,在使用椎旁肌肉作参考的PL-QCT 中,增强后的vBMD 测量值平均增加了8.6%[44]。未来还需进一步明确对比剂对BMD 测量的潜在影响,以及是否与对比剂使用量、图像采集时期、心脏射血分数以及骨髓血管化程度有关。
4.3 诊断标准 机会性QCT 的诊断标准较明确,使用国内外专家组制定的腰椎QCT 诊断阈值:BMD(mg/cm3)<80 为 OP,80 ≤BMD ≤120 为 低 骨 量,BMD>120 为骨量正常[45]。而直接使用椎体CT 值的筛查方法目前尚缺乏公认的标准,并且相关阈值根据特定人群的OP 罹患风险高低会有所不同。在糖尿病、类风湿性关节炎等高危人群中,应当使用更高的敏感度阈值,以最大限度地减少假阴性结果。此外,除了较为成熟的椎体筛查,相关研究[46]中也介绍了肱骨近端、桡骨远端、胫骨远端等不同骨骼位点的CT 阈值。在将这些非标准部位的BMD 测量结果纳入临床实践之前,仍需要对各自的诊断阈值进行独立验证。
5 小结
机会性CT 筛查借助临床常规CT 扫描,可以获取骨量、骨强度和身体成分等附加价值,临床应用前景广阔。能够提高临床上OP 病人的检出率,同时减少DXA 检查数量,有望节省大量医疗费用、减少人群辐射剂量。对于存在DXA 假阴性骨折或无法进行DXA 检查的病人,这种机会性策略尤为重要。随着人工智能在OP 研究领域的应用,全自动或半自动机会性CT 可提高骨折高危人群的筛查效率,但其能否真正改善骨折风险评估仍有待长期随访观察,扫描标准化、诊断阈值等问题也需要进一步研究。

