良性与恶性肠梗阻手术预后比较及影响因素分析
杨轼,姜建帅
肠梗阻部分患者(18%~57%)需要手术干预[1],术后并发症发生率为4%~37%,术后病死率为2%~6%[2]。由腹腔内恶性肿瘤引起的肠梗阻为恶性肠梗阻(MBO),晚期原发或转移肿瘤导致的MBO 发生率为5%~43%[3]。研究表明,接受MBO手术干预的患者有较高的并发症发生率(7%~67%)和病死率(6%~32%)[4]。本研究拟比较良性与MBO 手术预后及其影响因素分析,报道如下。
1 资料与方法
1.1 一般资料 收集2018年1月至2021年12月宁波市第一医院收治的肠梗阻患者178例,按引发肠梗阻的原因不同分为良性肠梗阻(良性组)146例,MBO(MBO 组)32例。本研究获得宁波市第一医院医学伦理委员会审核批准。
1.2 方法 收集两组临床数据,包括性别、年龄、美国麻醉学家协会(ASA)评分及合并症,其中合并症包括高血压、呼吸困难、慢性阻塞性肺疾病(COPD)、腹水、肝硬化及糖尿病等;收集两组实验室数据,包括红细胞压积(HCT)及清蛋白水平。
以是否30 d 再住院和发生术后并发症为标准界定预后良好和预后不良,并发症包括心律失常、肾功能异常、肺炎、术后发热、吻合口漏及菌血症,分析预后不良的影响因素。
1.3 统计方法 数据采用SPSS26.0 软件分析,计量资料采用均数±标准差表示,采用t检验;等级资料采用秩和检验;计数资料采用2检验;多因素分析采用Logistic 回归分析。P <0.05 为差异有统计学意义。
2 结果
2.1 基线资料比较 两组ASA 分级、合并腹水、HCT 及清蛋白水平差异均有统计学意义(均P <0.05),见表1。
2.2 预后情况 MBO组术后出现并发症14例,再入院(30d)6例,预后不良20例;良性肠梗阻组术后出现并发症28例,再入院(30d)18例,预后不良46例。178例中预后不良66例,预后良好112例。见表1。

表1 两组基线资料及预后情况比较
2.3 预后不良影响因素分析 癌症、年龄、ASA 分级IV ~V 级、肝硬化、低清蛋白及HCT<30%均是术后并发症独立影响因素(均P<0.05),见表2。癌症、腹水、年龄、ASA分级IV~V级、肝硬化、低清蛋白及HCT <30%均是影响肠梗阻患者30 d 再住院的独立影响因素(均P <0.05),见表3。

表2 影响术后并发症的危险因素分析
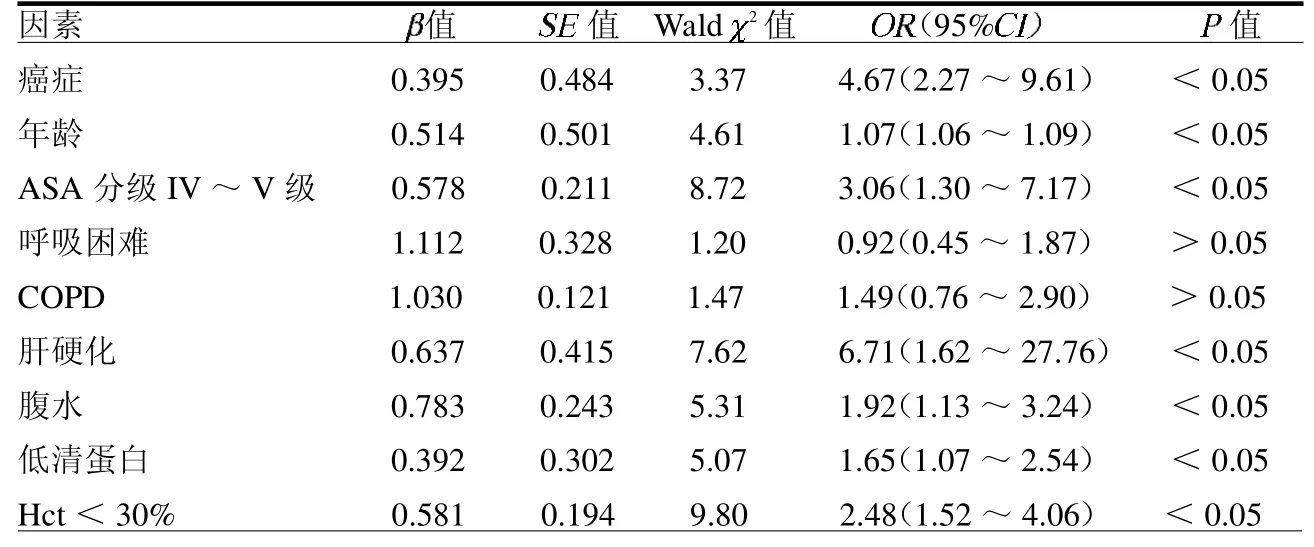
表3 30 d 再入院的危险因素分析
3 讨论
MBO大多发病速度较为缓慢,发生的梗阻类型以不全性肠梗阻较多,其并发症状有腹痛、腹胀、恶心、呕吐及肛门停止排气排便等。发生MBO 时患者往往处于肿瘤晚期,因自身生理机能等问题使其在治疗方法的选择上会处于两难的境地。
本研究比较了良性肠梗阻和MBO患者的手术结果,结果表明MBO 手术的并发症发生率明显高于良性肠梗阻患者,这可能与肿瘤患者应激能力、恢复能力下降有一定关系,但30 d 再住院率这一指标高出部分有限,此结论与Banting等[5]团队研究方向一致。在以解除患者肠梗阻改善生活质量为目的时,适当倾向于手术治疗对患者会造成更有利的局面。
多因素分析结果显示,30 d 再入院和发生术后并发症的独立危险因素包括高龄、高ASA分级、腹水、肝硬化和营养不良。在已知MBO 的背景下,这些结果可以帮助临床医生通过识别容易发生预后不良的患者来评估手术风险,权衡手术治疗与保守治疗的利弊,选择是否使用手术治疗。

