六味地黄丸治疗2 型糖尿病性骨质疏松症的疗效评价
安 娟,匡浩铭,李振宇,张子鸣,沈玲琳,戎 宽,匡建军*
(1.湖南中医药大学,湖南 长沙 410208;2.湖南省中医药研究院附属医院,湖南 长沙 410006;3.湖南省中医药研究院,湖南 长沙 410006)
糖尿病性骨质疏松症(diabetic osteoporosis, DOP)是一种由葡萄糖代谢紊乱引起的全身性代谢性骨病,严重影响骨微结构,导致骨强度降低、骨脆性上升及骨缺损,增加骨折风险和致残率,严重影响患者的生活质量[1-2]。 DOP 这个概念在1948 年首次被定义,证明了糖尿病与骨质疏松症两者之间的关联性[3]。对于2 型DOP 患者,除了要教育患者调整其生活方式、服用常规降糖药外,还应对症治疗骨质疏松症。临床上常用治疗骨质疏松症的药物有维生素D、钙剂、阿仑膦酸钠、骨化三醇等,其中阿仑膦酸钠为治疗骨质疏松症的经典药,但有文献报道其存在全身骨骼肌酸痛、非典型股骨骨折等不良反应[4]。 中医通过“辨证论治、调节脏腑、平衡阴阳”,不仅能减轻DOP 患者的临床症状,还能减少西药的摄入,提升其生活质量[5-6]。 研究发现,2 型DOP 患者往往还存在血清氧化应激水平失衡,加速了疾病发生发展的进程[7]。 本研究通过临床观察经典名方六味地黄丸对2 型DOP 患者疗效、血糖水平、骨密度T 值(腰椎L2~L4)、骨代谢指标、视觉模拟评分(visual analogue scale, VAS)、血清超氧化物歧化酶(superoxide dismutase, SOD)、丙二醛(malondialdehyde, MDA)的影响,具体报道如下。
1 资料与方法
1.1 研究对象
以湖南省中医药研究附属医院门诊2020 年10月至2021 年10 月就诊的60 例2 型DOP 患者作为研究对象,按照随机数字表法将其平均分为治疗组和对照组。 其中,治疗组患者中男性12 例,女性18 例,年龄(55.6±5.4)岁,病程(4.3±2.5)年;对照组患者中男性13 例,女性17 例,年龄(56.0±5.1)岁,病程(5.1±2.9)年。 两组患者上述资料比较,差异均无统计学意义(P>0.05),具有可比性。 该研究已经通过湖南省中医药研究院伦理委员会审查 (批准号:〔202003〕28 号),所有患者均已自愿签署知情同意书。
1.2 诊断标准
1.2.1 中医诊断标准 以《中药新药临床研究指导原则》[8]中治疗骨质疏松症及消渴的临床研究指导
原则为参考标准。 主要症状:多饮多食且多尿,形体日渐消瘦,潮热盗汗,腰酸耳鸣,久站后腰骨疼痛,步履艰难。
1.2.2 西医诊断标准 参照《中国人骨质疏松症诊断标准专家共识(2014 版)》诊断标准[9]、《中国2 型糖尿病防治指南(2020 年版)》诊断标准[10]制定:存在“三多一少”等糖尿病症状,空腹血糖(fasting plasma glucose, FPG)≥7.0 mmol/L,糖化血红蛋白(glycosylated hemoglobin A1C, HbA1c)≥6.5,葡萄糖耐量试验(oral glucose tolerance test, OGTT)0.5 h/1 h血糖≥11.1 mmol/L;发生过脆性骨折,补充钙剂或其他治疗骨质疏松症的药物有效,骨密度T 值<-2.5,影像学检查已确诊。
1.3 纳入标准
(1)符合糖尿病及骨质疏松症的中医、西医诊断标准;(2)年龄为45~65 岁;(3)近2 周内未服用治疗骨质疏松症的药物;(4)患者知情同意,自愿接受并积极配合本研究治疗方案。
1.4 排除标准
(1)患有肝、肾功能严重损伤;(2)患有精神疾病、甲状腺功能亢进、酮症酸中毒、恶性肿瘤伴有骨转移等疾病;(3)近期口服性激素、止痛药等影响骨代谢水平的药物;(4)骨质疏松症严重并发一处或多处骨折者;(5)无法连续3 个月接受治疗的受试者。
1.5 治疗方法
两组患者均给予基础治疗,糖尿病饮食,科普骨质疏松症相关知识,控制体质量,戒不良嗜好(吸烟、饮酒等),适当运动,合理使用降糖药物二甲双胍(湘雅制药公司生产,批号:1912107,0.5 g/次,2 次/d)治疗。
1.5.1 对照组 在上述基础上加用钙尔奇D 片(惠氏制药公司生产,批号:H10950030),1 片/d(600 mg),晚饭后口服;阿仑膦酸钠维D3片(杭州默沙东制药有限公司生产,批号:W000285),1 片/次(70 mg∶5600 U),1 次/周,清晨空腹温开水送服,服药30 min内不宜进食。
1.5.2 治疗组 在对照组的基础上再加服六味地黄丸。 具体药物组成:熟地黄20 g,山药10 g,山茱萸10 g,牡丹皮8 g,茯苓8 g,泽泻8 g。 由湖南省中医药研究院附属医院药剂科煎煮,150 mL/袋,早晚温服,2 袋/d。
1.5.3 疗程 1 个月为1 个疗程,两组患者均治疗3个疗程。 3 个月后检测各项指标,观察疗效。
1.6 观察指标
1.6.1 中医证候积分 治疗前后采用半定量记分法[11]评定。 主症包括气虚、懒言少语、腰酸背痛、腿软无力;次症包括口干舌燥、五心烦热、潮热盗汗、目眩耳鸣。 以病情轻重程度将主症记为0、2、4、6 分,次症记为0、1、2、3 分。
1.6.2 血糖水平检测 治疗前后采集患者空腹静脉血,采用ZY-1200 全自动生化分析仪(上海科华生物技术有限公司)检测FPG、HbA1c 和餐后2 h 血糖(2 hours postprandial blood sugar, 2hPBG)。
1.6.3 骨密度检测 本研究所有患者采用Dexa Pro-I 双能X 线骨密度仪(徐州品源医疗科技有限公司)测定。 在治疗前及治疗3 个月后各测定记录1 次。
1.6.4 VAS 评分 用0~10 代表疼痛程度,疼痛越轻数字越小,依据患者自我主观评价,在标有0~10的游标卡尺上选1 个数字代表目前身体疼痛的程度,研究者实时记录。 在治疗前及治疗3 个月后各测定记录1 次。
1.6.5 骨代谢指标和SOD、MDA 含量的检测 在用药前后收集受试者8 mL 空腹静脉血,常温下静置2 h,3000 r/min(离心半径10 cm)离心15 min 后,用移液器分离出血清,冻存于-80 ℃冰箱中直至使用。 用ELISA 法检测SOD、MDA,试剂盒均购自南京建成有限公司, 批号分别为A005、A003-1;用电化学发光免疫分析法测骨钙素 (bone glaprotein, BGP) 和β-I 型胶原羧基端肽 (β-C-terminal telopeptide of type I collagen, β-CTX)。 在治疗前及治疗3 个月后各测定记录1 次。
1.7 疗效标准
参照《中药新药临床研究指导原则》[8]中骨质疏松症及消渴(糖尿病)疗效判定标准。 显效:患者临床症状消失,无压痛感,骨密度增加,骨代谢指标测定明显好转,FPG 水平正常或下降>40%,HbAlc 水平正常或下降>30%;有效:患者临床症状基本消失,压痛感减轻,骨密度没有下降,骨代谢指标测定稍有好转,血糖下降区间为20%~40%,HbAlc 下降区间为10%~30%;无效:临床症状无明显改变,压痛感明显,骨密度下降,骨代谢指标测定无改变,FPG 和2hPBG血糖指标无改善。 总有效率=(显效例数+有效例数)/总例数×100%。
1.8 安全性观察
分别在治疗前及治疗3 个月后检测血常规、二便常规、肝肾功能及心电图各1 次,并实时记录治疗过程发生的不良反应情况及对症措施。
1.9 统计学方法
采用SPSS 25.0 软件对所有数据进行统计分析。 计量资料以“±s”表示,组内比较用配对t 检验,组间比较用独立样本t 检验;计数资料用“例(%)”表示,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗前后临床疗效及中医证候积分比较
治疗组总有效率为93.3%,对照组为66.7%,故治疗组的临床总有效率高于对照组(P<0.05)。 详见表1。

表1 两组患者临床疗效比较[例(%)]
治疗前,两组患者的中医证候积分比较,差异无统计学意义(P>0.05)。治疗后,两组患者中医证候积分均明显低于治疗前(P<0.01);治疗组中医证候积分低于对照组(P<0.05)。 详见表2。
表2 两组患者治疗前后中医证候总评分比较(±s,分)

表2 两组患者治疗前后中医证候总评分比较(±s,分)
注:与治疗前比较,**P<0.01;与对照组比较,#P<0.05。
组别治疗组对照组n 30 30治疗前13.6±2.0 13.6±1.8治疗后8.5±1.3**#9.5±1.6**
2.2 两组患者治疗前后血糖水平比较
治疗前,两组患者的FBG、2hPBG 含量、HbAlc相比较,差异均无统计学意义(P>0.05)。 治疗后,两组患者FBG、2hPBG 含量、HbAlc 均较治疗前降低,差异有显著统计学意义(P<0.01);治疗组FPG、2hPBG含量、HbAlc 明显低于对照组(P<0.05)。 详见表3。
表3 两组患者治疗前后FBG、2hPBG、HbAlc 的比较(±s)
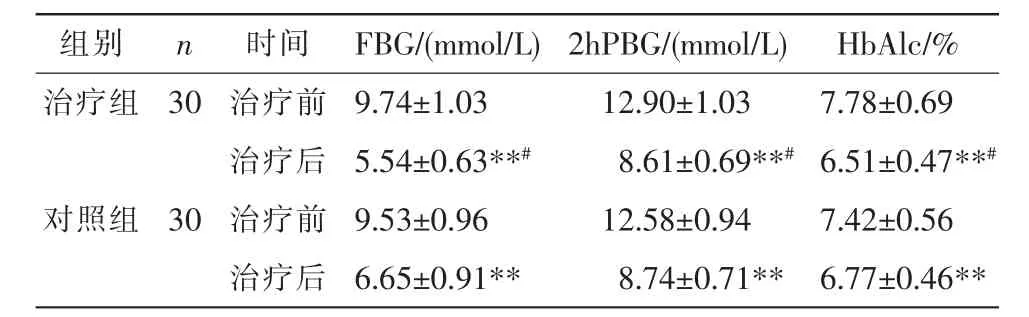
表3 两组患者治疗前后FBG、2hPBG、HbAlc 的比较(±s)
注:与治疗前比较,**P<0.01;与对照组比较,#P<0.05。
组别治疗组n 30对照组30时间治疗前治疗后治疗前治疗后FBG/(mmol/L)9.74±1.03 5.54±0.63**#9.53±0.96 6.65±0.91**2hPBG/(mmol/L)12.90±1.03 8.61±0.69**#12.58±0.94 8.74±0.71**HbAlc/%7.78±0.69 6.51±0.47**#7.42±0.56 6.77±0.46**
2.3 两组患者治疗前后腰椎骨密度T 值及VAS 比较
治疗前,两组患者腰椎骨密度T 值及VAS 评分比较,差异均无统计学意义(P>0.05)。 治疗后,两组患者的腰椎T 值较治疗前明显升高,VAS 评分较治疗前显著降低(P<0.01);治疗组腰椎T 值明显高于对照组,VAS 评分低于对照组(P<0.05)。 详见表4。
表4 两组患者治疗前后腰椎T 值及VAS 比较(±s)
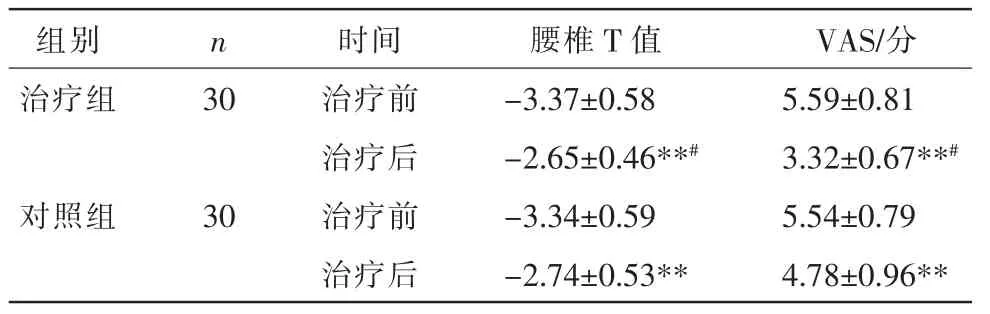
表4 两组患者治疗前后腰椎T 值及VAS 比较(±s)
注:与治疗前比较,**P<0.01;与对照组比较,#P<0.05。
组别治疗组n 30对照组30时间治疗前治疗后治疗前治疗后腰椎T 值-3.37±0.58-2.65±0.46**#-3.34±0.59-2.74±0.53**VAS/分5.59±0.81 3.32±0.67**#5.54±0.79 4.78±0.96**
2.4 两组患者治疗前后骨代谢指标比较
治疗前,两组患者血清BGP、β-CTX 含量比较,差异均无统计学意义(P>0.05)。 治疗后,两组患者BGP 活力较治疗前明显上升,β-CTX 含量较治疗前降低(P<0.05);治疗组BGP 活力明显高于对照组,β-CTX 含量低于对照组(P<0.05)。 详见表5。
表5 两组患者治疗前后骨代谢指标比较(±s,ng/mL)
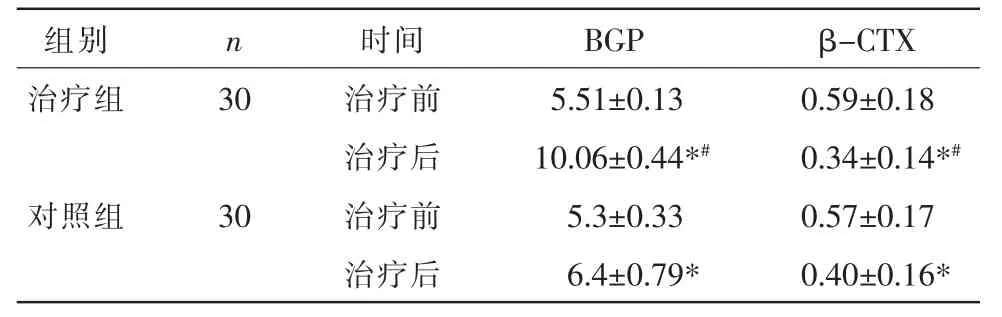
表5 两组患者治疗前后骨代谢指标比较(±s,ng/mL)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
组别治疗组n 30对照组30时间治疗前治疗后治疗前治疗后BGP 5.51±0.13 10.06±0.44*#5.3±0.33 6.4±0.79*β-CTX 0.59±0.18 0.34±0.14*#0.57±0.17 0.40±0.16*
2.5 两组患者治疗前后SOD 活力、MDA 含量比较
治疗前,两组患者血清SOD 活力和MDA 含量比较,差异均无统计学意义(P>0.05)。 治疗后,两组患者SOD 活力明显上升,MDA 含量显著下降(P<0.01);治疗组SOD 值明显高于对照组,MDA 含量低于对照组(P<0.05)。 详见表6。
表6 两组患者治疗前后SOD 及MDA 比较(±s)
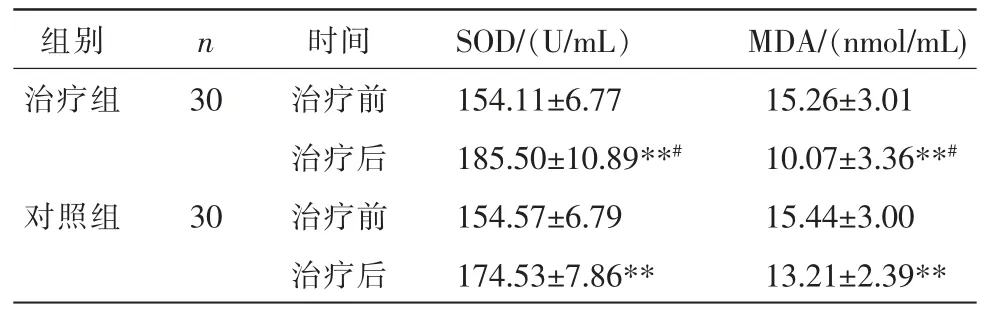
表6 两组患者治疗前后SOD 及MDA 比较(±s)
注:与治疗前比较,**P<0.01;与对照组比较,#P<0.05。
组别治疗组n 30对照组30时间治疗前治疗后治疗前治疗后SOD/(U/mL)154.11±6.77 185.50±10.89**#154.57±6.79 174.53±7.86**MDA/(nmol/mL)15.26±3.01 10.07±3.36**#15.44±3.00 13.21±2.39**
2.6 两组患者不良反应
对照组有1 例受试者出现恶心呕吐等胃肠道反应,但及时对症处理后恢复正常,未发生严重后果,治疗组的受试者均未出现胃肠道反应。 两组受试者未出现药物过敏反应,且治疗后血常规、心电图及肝肾功能等均显示正常。
3 讨论
在中医学中,并没有DOP 的病名,现根据其临床特点和症状体征,将其归属为“骨枯”“骨瘘”的范畴。 《素问·宣明五气》曰“肾主骨”,《素问·阴阳应象大论》曰“肾生骨髓”[12],《灵枢·本神》曰“精伤则骨酸痿厥”。 肾为先天之本,肾脏的精气盛衰决定着骨骼是否强健[13]。 本病的病因病机可归结为消渴阴虚内热,日久不愈,耗气伤津,肾气渐亏,以致肾不主骨,骨失所养,骨质枯槁,骨枯髓减,发为“骨痿”[14]。
《珍珠囊补遗药性赋·卷二》记载熟地黄:“其用有四,活血气,封填骨髓,滋肾水,补益真阴。 ”配味酸,性微温入肝、肾经的山茱萸,补益肝肾;味甘,性平,入脾、肺、肾经的山药补肾益精、健脾养胃;味甘,性平,入心、肺、脾、肾经的茯苓健脾祛湿;味甘,性寒,入肾、膀胱经的泽泻清利下焦湿热;味苦、性寒,入肝、肾、肺经的牡丹皮退虚热[15]。六药合用,既补阴虚又抑阳亢,阴阳渐趋平衡。
现代药理学发现,熟地黄不仅能显著上调小鼠p-AMPK/AMPK 的表达,调控各脏器的能量代谢,从而起到抗炎效应以缓解糖尿病小鼠症状;还能激活碱性磷酸酶活性,调节钙途径,促进钙沉积,拮抗Ca2+从而防止钙超载,从而增加骨强度,提高骨质量,就一定程度而言,可降低骨折发病率[16-17]。 杨丽宁等[18]基于网络药理学得出,山药可以降低血糖、血脂,减少细胞凋亡、抗炎症及氧化,主要和其关键活性成分薯蓣皂苷元相关。 此外,山药通过阻止RANKL 与RANKL 结合,抑制破骨细胞成熟,对去势所引起的骨质疏松症大鼠有显著的治疗效果[19]。徐志猛等[20]通过动物实验发现,山茱萸具有α-糖苷酶抑制剂的功效,能有效改善糖尿病鼠的糖耐量;其还有调节内分泌系统作用, 通过增加雌激素分泌水平, 加速骨代谢, 促进间充质干细胞分化为成骨细胞,从而达到改善骨质量的目的[21]。 相关研究发现,茯苓提取出的活性成分茯苓多糖能激活PPAR-γ通路,减轻对小鼠肾脏损伤,具有降血糖、抗氧化、调节脂代谢紊乱的作用[22-24]。 茯苓配伍山药还能增效减毒,缓解胃肠道症状。 钱增堃等[25]发现,泽泻多糖能显著降低血糖及血脂含量,对糖尿病起着很好的治疗作用。相关研究表明,牡丹皮能调节脂质代谢紊乱,降低糖尿病小鼠MDA 含量,增加SOD 活力[26]。总而言之,六味地黄丸能调节葡萄糖稳态、调控血糖、增加骨密度、改善骨质量,并帮助DOP 患者降低骨折的发病风险。
腰椎(L2~L4)骨密度T 值是目前公认的检查骨质疏松症的金标准,能较为准确地反应糖尿病患者的骨折风险[27]。 BGP 是一种由成熟骨细胞分泌的非胶原蛋白,能反映骨细胞活性,对骨质疏松症的诊断、监测及评估有较高的灵敏性[28]。 β-CTX 为Ⅰ型胶原蛋白降解产物,可反映破骨细胞的活性,且因其稳定易测,对骨吸收有较高的特异性而常被临床采用[29]。 氧化应激水平失衡会抑制成熟骨细胞及骨的形成,从而引发骨质疏松,而SOD 活力及MDA 含量是反映氧化应激的特异性指标[30]。 本临床观察结果显示,六味地黄丸治疗组总有效率高于对照组,且VAS 评分显著下降,说明六味地黄丸能有效缓解患者的疼痛, 临床疗效显著。 两组治疗后的骨密度T值、SOD 活力及BGP 含量均上升,血清MDA、β-CTX水平皆下降,且治疗组明显优于对照组,说明六味地黄丸能有效地增加成熟骨细胞的数量、提高骨密度、改善骨代谢标志物及抗氧化应激。
综上所述,六味地黄丸治疗2 型DOP 的疗效显著,能提高常规西医疗法的治疗效果。 但本研究的样本量相对较小、观察时间较短,六味地黄丸疗效的稳定性还需进一步观察。且2 型DOP 为慢性代谢性疾病,本研究未进行长期随访,很难对本方案的远期疗效进行客观评价,仍需更深入的探讨和研究。

