利妥昔单抗治疗难治性重症系统性红斑狼疮的疗效
杨庆娇 宋美潓
系统性红斑狼疮(SLE)经典治疗方法以非特异性免疫抑制治疗为主,多采用细胞毒药物和糖皮质激素治疗,除不良反应突出外,该治疗方案对部分难治性重症SLE 患者疗效并不理想[1]。近年来,B 细胞清除治疗被广泛应用于自身免疫疾病治疗中。与传统非特异性免疫抑制治疗有一定差别,B 细胞清除治疗主要是通过生物靶向特异性B 细胞的清除作用发挥治疗效果。作为目前备受关注的B 细胞清除治疗药物,利妥昔单抗是一种单克隆抗体,能特异性与B 细胞表面的CD20 抗原结合,通过抗体依赖或补体依赖的细胞毒作用清除B 细胞,继而有效降低机体内炎症介质水平,发挥免疫抑制的治疗效果[2]。本研究就难治性重症SLE 患者给予利妥昔单抗治疗的效果进行分析。现报道如下。
1 资料与方法
1.1 一般资料
选取2018年1月至2020年10月丹东市第一医院收治的82 例难治性重症SLE 患者作为研究对象,按随机数字表法分为对照组与观察组,各41 例。对照组男14 例,女27 例;年龄27~66 岁,平均(41.38±2.57)岁;病程2~142 个月,平均(52.57±9.36)个月。观察组男15 例,女26 例;年龄26~67 岁,平均(41.45±2.63)岁;病程2~141 个月,平均(52.64±9.48)个月。两组患者一般资料比较,差异无统计学意义(P>0.05)。具有可比性。
纳入标准:1)符合难治性重症SLE 相关诊断标准[3];2)经大剂量糖皮质激素治疗后实验室指标、临床指标等未改善甚至病情恶化;3)患者至少一个系统大不列颠群岛狼疮评估组指数(BILAG)达A 级,且重要脏器功能损伤甚至危及生命;4)患者或合法代理人了解研究全部流程并签署了知情同意书。
排除标准:1)精神障碍或认知功能不全;2)合并严重糖尿病、高血压等基础疾病;3)恶性肿瘤;4)对研究药物过敏或严重过敏体质;5)中途退出研究或无法完成治疗。
1.2 治疗方法
对照组实施常规治疗,患者口服甲泼尼龙(Pfizer Italia S.r.l.,意大利,注册证号H20150245),初始剂量4~48 mg/d,4~8 周后根据患者实际病情调整用药剂量;同时配合他克莫司胶囊(国药集团川抗制药有限公司,国药准字H20083943)口服治疗,初始用药剂量为4 mg/d,2 次/d,4~8 周后根据患者实际情况调整用药剂量,逐渐减少至2 mg/d。共治疗6个月。
观察组在对照组基础上加用利妥昔单抗(F.Hoffmann-la Roche Limited,瑞士,注册证号S20080045)治疗,初始用药剂量为180 mg/m2,溶于5%葡萄糖注射液中静脉滴注,控制滴速,1 次/周,连续治疗6 个月,治疗期间根据患者实际情况调整药物用量。
1.3 观察指标
1)疗效判定标准:治疗后全部系统BILAG 均≤C,血尿及间断性发烧等症状消失为显效;与治疗前比较有≥1 个系统BILAG 等级降低1 级,且其他系统BILAG≤B 级为有效;不符合上述标准则提示无效[4]。治疗有效率(%)=(显效例数+有效例数)/总例数×100%。2)统计两组患者血清肌酐(碱性苦味酸终点比色法)、尿红细胞(尿潜血试验)及尿蛋白(蛋白试纸法)水平,用免疫散射比浊法检测免疫球蛋白A(IgA)和C 反应蛋白(CRP)水平,魏氏血沉方法检测红细胞沉降率(ESR)。3)记录两组患者不良反应发生情况,包括肺部感染、肝功能损伤以及胃肠道反应等。
1.4 统计学分析
采用SPSS 23.0 统计软件进行数据分析,计量资料以±s表示,组间比较采用t检验,计数资料以百分率表示,组间比较采用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 治疗效果
观察组治疗有效率高于对照组,差异有统计学意义(P<0.05)。见表1。
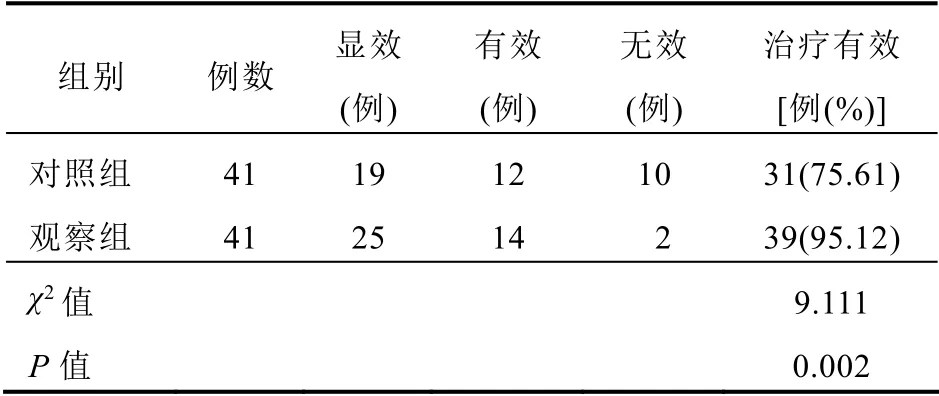
表1 两组患者治疗效果比较
2.2 两组患者血清肌酐、尿红细胞及尿蛋白比较
治疗前,两组血清肌酐、尿红细胞及尿蛋白比较,差异无统计学意义(P>0.05);治疗后,观察组血清肌酐、尿红细胞、尿蛋白低于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者血清肌酐、尿红细胞及尿蛋白比较(±s)
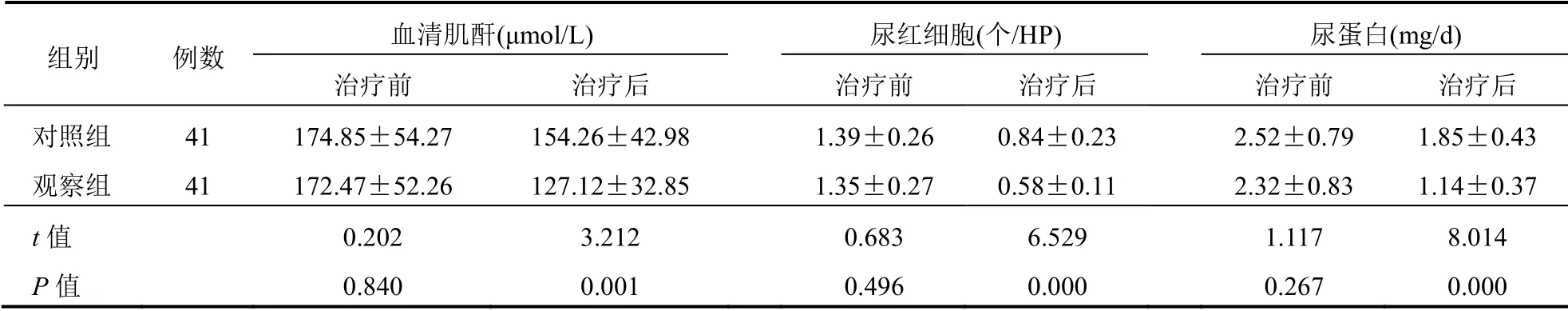
表2 两组患者血清肌酐、尿红细胞及尿蛋白比较(±s)
组别 例数 血清肌酐(μmol/L) 尿红细胞(个/HP) 尿蛋白(mg/d) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 41 174.85±54.27 154.26±42.98 1.39±0.26 0.84±0.23 2.52±0.79 1.85±0.43 观察组 41 172.47±52.26 127.12±32.85 1.35±0.27 0.58±0.11 2.32±0.83 1.14±0.37 t 值 0.202 3.212 0.683 6.529 1.117 8.014 P 值 0.840 0.001 0.496 0.000 0.267 0.000
2.3 两组患者ESR、CRP、IgA 比较
治疗前,两组ESR、CRP、IgA 比较,差异无统计学意义(P>0.05);治疗后,观察组ESR、CRP、IgA 低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组患者ESR、CRP、IgA 比较(±s)
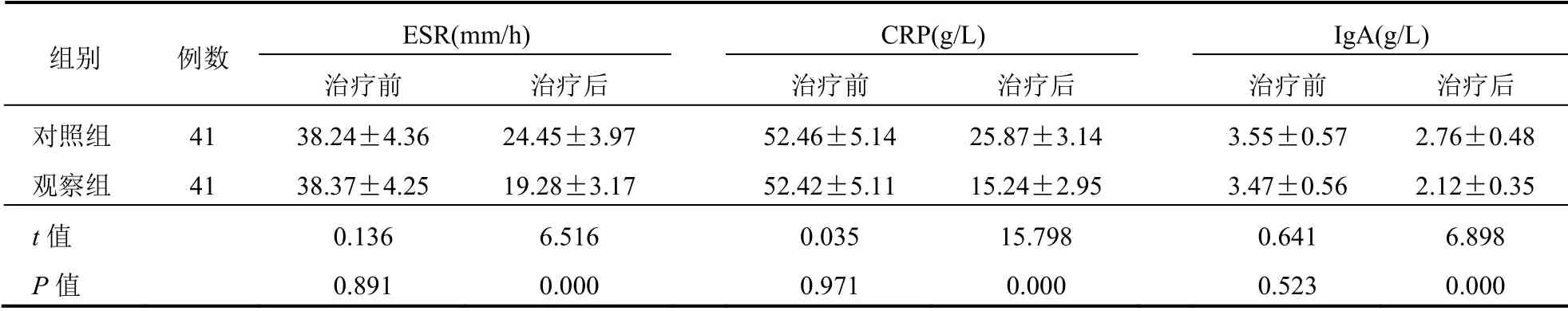
表3 两组患者ESR、CRP、IgA 比较(±s)
组别 例数 ESR(mm/h) CRP(g/L) IgA(g/L) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 41 38.24±4.36 24.45±3.97 52.46±5.14 25.87±3.14 3.55±0.57 2.76±0.48 观察组 41 38.37±4.25 19.28±3.17 52.42±5.11 15.24±2.95 3.47±0.56 2.12±0.35 t 值 0.136 6.516 0.035 15.798 0.641 6.898 P 值 0.891 0.000 0.971 0.000 0.523 0.000
2.4 不良反应
治疗期间,观察组出现1 例肺部感染,2 例胃肠道反应,不良反应发生率为7.32%(3/41);对照组出现1 例肝功能损伤,3 例肺部感染,8 例胃肠道反应,不良反应发生率为29.27%(12/41);两组不良反应发生率比较,差异有统计学意义(χ2=9.225,P=0.002<0.05)。
3 讨论
难治性重症SLE 的发病原因尚不明确,会累及多个器官,包括心、肾、肺、肌肉、关节、黏膜、皮肤等,同时患者循环系统和神经系统也会受到不同程度的损伤[5]。患者患病后血清中会出现多种自身抗体,主要以抗核抗体为主。临床主要采用环磷酰胺、泼尼松、甲波尼龙等药物治疗,能发挥良好的免疫抑制作用,但其会导致患者发生肺部感染、胃肠道反应、肝肾损伤等不良反应。因此临床急需寻找一种更加可靠的治疗方式[6]。利妥昔单抗是生物制剂,在难治性重症SLE 发病机制中B 细胞发挥着重要作用,而其能特异性结合B 细胞表面的抗原,对B细胞发挥杀伤作用。
本研究结果显示,观察组治疗有效率明显高于对照组。说明利妥昔单抗应用于难治性重症SLE 治疗中能显著改善患者临床症状,提高治疗效果。利妥昔单抗治疗难治性重症SLE 的作用机制在于以下几点:1)抗体依赖的细胞毒反应,主要是由于自然杀伤(NK)细胞、巨噬细胞、中性粒细胞等的Fc受体与利妥昔单抗的Fc 片段特异性结合,诱导CD20+B 细胞溶解;2)通过诱导细胞凋亡,进而控制细胞增殖;3)补体介导的细胞毒反应,通过结合Fc 片段和C1q 片段,激活补体级联反应,进而促进B 细胞裂解[7]。利妥昔单抗治疗难治性重症SLE 的主要作用机制在于抗体依赖的细胞毒反应,同时利妥昔单抗能控制T 细胞的分泌,减少T 细胞数量,发挥免疫调节作用。本研究中,治疗后两组血清肌酐、尿红细胞、尿蛋白、ESR、CRP、IgA 均有所下降,且观察组下降幅度更高。与魏建[8]的研究结果相似,利妥昔单抗治疗难治性重症SLE 效果显著,相比他克莫司在调节患者免疫功能、提高临床疗效等方面效果更好。本研究还对两组药物治疗期间不良反应发生情况进行了比较观察,结果显示观察组不良反应发生率明显低于对照组。说明应用利妥昔单抗治疗能进一步减少不良反应发生,用药安全性相对较高。但本研究由于存在样本量少、随访时间短等不足,无法明确利妥昔单抗治疗难治性重症SLE 的远期疗效,不能完全排除免疫指标、血清肌酐、尿红细胞、尿蛋白等结果受样本量小而得出的统计学误差影响等,今后仍需开展多中心、大样本试验得以完善。
综上所述,将利妥昔单抗应用于难治性重症SLE治疗中,相比常规治疗措施效果更好,其有助于改善患者症状,调节免疫功能。

