气道压力释放通气救治急性呼吸窘迫综合征患者疗效观察
滕泽宇,梁映霞,闫早红,张传振,张成明
急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)是呼吸系统常见的危重疾病,可导致多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS)甚至死亡,病死率高达35%~45%[1]。肺保护通气采用低潮气量通气(low tidal volume ventilation, LTV)和呼气末正压(positive end expiratory pressure, PEEP)通气结合的方法,是目前临床治疗ARDS常用的通气模式,低潮气量可预防肺泡过度膨胀导致的气压伤,而PEEP可减少肺不张[2]。气道压力释放通气(airway pressure release ventilation,APRV)是一种持续气道正压通气伴压力周期性短暂释放的通气模式,对自主呼吸无限制。APRV可促进肺泡复张,降低ARDS患者气压伤和低容量肺不张损伤风险及改善通气—灌注匹配[3-4],通过维护肺泡上皮完整性及肺泡表面活性物质来维系肺泡稳定性,从而预防通气诱导肺损伤(VILI)的发生[5-6]。本研究旨在观察应用较新的APRV通气参数设置方案治疗ARDS患者的疗效,并与LTV模式作比较,报道如下。
1 资料与方法
1.1 临床资料 选取2019年11月—2021年9月于潍坊医学院附属医院重症医学科(ICU)接受救治的ARDS患者61例。ARDS患者符合 2012 年欧洲重症医学会重新定制的ARDS“柏林定义”诊断标准[7]。按照随机数字表法分为APRV组31例和LTV组30例。2组患者性别、年龄、预测体质量(PBW)、APACHEⅡ评分、纳入前机械通气时间及ARDS病因比较差异均无统计学意义(P>0.05),具有可比性,见表1。因转院治疗2例,死亡3例,急诊手术2例,最终APRV组有28例患者、LTV组有26例患者纳入结果分析。本研究经医院伦理委员会批准(wyfy-2021-ky-102),患者家属或委托人知情同意并签署知情同意书。
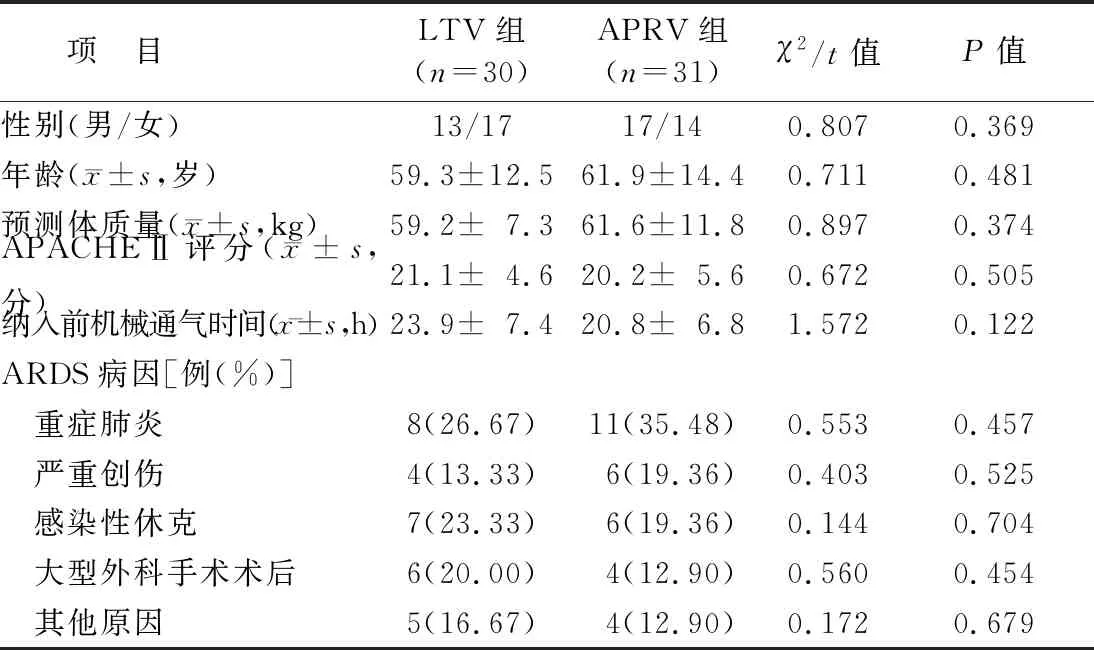
表1 APRV组和LTV组患者一般资料比较
1.2 病例选择标准 (1)纳入标准:①符合“柏林定义”ARDS诊断标准[7];②需要进行气管插管机械通气(MV);③18岁≤年龄≤85岁。(2)排除标准:①纳入前接受MV超过48 h;②妊娠期女性;③严重哮喘和慢性阻塞性肺疾病;④气胸病史或影像学诊断肺大疱;⑤难治性休克;⑥严重心肌缺血、脑供血不足及脑出血;⑦慢性肾衰竭5期需血液滤过治疗;⑧濒死状态,预计在24 h内死亡。(3)剔除标准:①中途死亡;②中途转院治疗;③转急诊手术;④中途发生气胸。
1.3 治疗方法
1.3.1 通气设置:试验所用呼吸机为柯惠PB-840型呼吸机。为评估患者状况,稳定患者病情,消除患者入组前氧合等指标的统计学差异,使2组患者处于同一基线水平,患者入ICU行气管插管后均采用容量控制通气(VCV)模式通气,参数设置:潮气量6~8 ml/kg(PBW),呼吸频率12~18次/min,PEEP 5~10 mmHg。通气目标:PaO2达到55~100 mmHg或动脉氧饱和度(SpO2)达到88%~98%[7]。维持患者呼吸循环稳定0.5~1 h后进行分组试验。APRV组使用APRV模式通气,初始参数设置:气道高压(Phigh)设为VCV下测得的平台压(Pplat),最大不超过30 cmH2O;释放压力(Plow)设为5 cmH2O;高压相持续时间(Thigh)设置范围4.2~4.6 s,释放相持续时间(Tlow)为0.4~0.8 s,调整Tlow使呼气末流速(EEFR)超过呼气峰值流速(PEFR)的50%(EEFR/PEFR≥50%);释放频率12次/min。LTV组使用LTV通气,潮气量4~6 ml/kg(PBW);PEEP与FiO2水平通过PEEP-FiO2表调整,潮气量和呼吸频率根据ARDSnet方案调整[8]。
1.3.2 镇痛镇静方案:2组患者接受相同镇痛及镇静方案,镇痛药物为舒芬太尼,初始静脉注射0.1~0.2 μg/kg背景剂量,然后以0.003~0.01 μg·kg-1·min-1的速度持续泵注;镇静剂使用丙泊酚,初始静脉注射丙泊酚1.5~2.5 mg/kg背景剂量,然后以0.06~0.08 mg·kg-1·min-1的速度持续泵注。运用Ramsay镇静评分评估患者镇静水平,镇静目标为2~4分。若患者出现严重人机异步性、不耐受气管导管及烦躁等现象,加深患者镇静程度最高至深度镇静,允许镇静评分低于镇静目标。每6 h对患者镇静状态进行评估,并调整药物输注速度以维持镇静目标水平。APRV组患者在维持镇静目标的前提下调整剂量以实现良好的自主呼吸。
1.3.3 补充措施:对于氧合指数<100 mmHg持续12 h的严重低氧血症患者,临床医生可以应用神经肌肉阻滞、肺复张操作及俯卧位等支持疗法;若患者发生顽固性低氧血症(PaO2<50 mmHg,FiO2=1.0),授权委托人或家属决定是否接受高频振荡通气及体外膜肺氧合(ECMO)等急救措施。治疗3 d后进行相关指标测定。
1.4 观察指标与方法 (1)循环呼吸指标:包括心率、平均动脉压(MAP)及自主呼吸频率。心率与自主呼吸频率通过多时间点读取监护仪读数后计算平均数获取,MAP通过桡动脉穿刺测压获取。(2)血气分析指标:包括动脉血氧分压(PaO2)、动脉二氧化碳分压(PaCO2)及氧合指数(PaO2/FiO2)等,通过动脉血气分析测得。(3)呼吸力学指标:包括平均气道压(Pmean)、Pplat、吸气峰压(PIP)及呼吸系统顺应性(Crs)等。PIP和Pmean可通过多时间点读取呼吸机读数后计算平均数获取;Pplat通过切换至VCV模式通气,吸气保持后获取;Crs通过公式 Crs=潮气量(VT)/(PIP-PEEP)计算得出。(4)镇静程度指标:治疗前及治疗3 d后采用Ramsay镇静评分测定。Ramsay评分总分6分,分值越高镇静越好。

2 结 果
2.1 2组治疗前后循环呼吸指标比较 治疗第3天APRV组心率较治疗前显著降低且低于LTV组,MAP较治疗前升高且高于LTV组(P均<0.01),2组自主呼吸频率比较差异无统计学意义(P>0.05),见表2。去甲肾上腺素使用量APRV组(72.91±9.6)mg与LTV组(68.73±7.8)mg比较差异无统计学意义(t/P=1.751/0.086)。

表2 LTV组和APRV组ARDS患者治疗前后循环呼吸指标比较
2.2 2组治疗前后动脉血气指标比较 治疗3 d后,2组PaO2/FiO2、PaO2均升高,且APRV组PaO2/FiO2、PaO2均高于LTV组,差异有统计学意义(P均<0.01),2组患者PaCO2治疗前后及组间比较差异无统计学意义(P>0.05),见表3。

表3 LTV组和APRV组ARDS患者治疗前后动脉血气指标比较
2.3 2组治疗前后呼吸力学指标比较 治疗3 d后APRV组Crs、Pmean升高,Pplat、PIP降低,而LTV组仅PIP降低,差异均有统计学意义(P均<0.05);APRV组各指标改善均优于LTV组(P<0.05或0.01)。见表4。

表4 LTV组和APRV组ARDS患者治疗前后呼吸力学指标比较
2.4 2组治疗前后镇静程度指标比较 治疗前Ramsay镇静评分APRV组(4.9±0.5)分与LTV组(5.0±0.4)分比较差异无统计学意义(t/P=0.868/0.389),治疗3 d后APRV组Ramsay镇静评分(4.6±0.6)分,低于LTV组的(5.0±0.2)分(t/P=3.396/0.002),即APRV组患者镇静程度低于LTV组。
3 讨 论
LTV模式治疗ARDS的策略是使用低潮气量并保持低吸气驱动压,同时通过使用高PEEP来维持呼气末肺泡压高于呼吸系统压力—容量曲线下拐点,避免肺泡塌陷从而最大限度减少吸气过程肺组织间的剪切力[9]。但该策略具有明显局限性:首先,损伤肺组织中正常充气与塌陷肺单位分布并不均匀[10-11],PEEP防止肺塌陷的同时可能导致充气肺泡过度膨胀,进而使损伤加重[12];其次,低潮气量可能无法满足危重患者氧合需求,需增加呼吸频率避免严重低氧血症,这会导致“潮汐复张”造成的低容量肺不张损伤风险增加[13]。
APRV模式可在较低PIP水平为患者提供足够的通气支持,从而降低VILI发生风险。VILI与通气过程超越应变阈值相关,且静态应变和动态应变在导致VILI发生过程中发挥作用比重不同,更高比例静态应变造成肺损伤风险小,而APRV模式Phigh使患者大部分时间处于较高水平静态应变,理论上可降低VILI发生风险[14]。而且Phigh可促进肺泡复张,增加用于气体交换的肺泡表面积,肺泡持续充盈还可促进通过科恩侧孔进行侧支通气,使气体从顺应性较好的肺泡重新分配到相邻顺应性较差的肺泡,从而降低肺泡异质性[3,15]。APRV对自主呼吸无限制可减少人机异步性[13],所以APRV比传统通气模式更具优势。
本研究中,治疗第3天APRV组氧合指数高于治疗前,且高于LTV组,与以往研究结果基本一致[4,16]。氧合情况是由Phigh和FiO2决定,Phigh维持肺泡复张,增加参与气体交换的肺泡表面积,从而改善通气—灌注匹配[3]。Tlow和自主呼吸共同决定患者的肺泡通气,Tlow若较长则肺泡在呼气周期有足够时间塌陷,若使肺不张减少及肺泡均匀性改善则需设置Tlow使EEFR/PEFR≥75%[17]。EEFR/PEFR<50%会导致吸气和呼气循环期间的动态肺泡异质性增大,使低容量肺不张损伤风险增加[18]。自主呼吸过程中膈肌活动可促进重力依赖性肺区肺泡开放,减少肺内分流从而改善氧合[13,19]。本研究中,APRV组Pmean高于LTV组,Pplat及PIP低于LTV组,研究证明,控制Pmean不变,当从其他通气模式转换为APRV时PIP会降低[20]。APRV可通过增加Thigh提高Pmean,可在不增加PIP的情况下促进肺不张区域肺泡复张,同时防止正常充气肺泡过度膨胀[21]。
APRV模式中的Phigh与Thigh增加肺内压,继而增加胸腔内压。左心室后负荷由左心室跨壁压决定,而左心室跨壁压为左心室内压与胸腔内压的差值,胸腔内压增加的情况下左心室跨壁压相应降低,从而使左心室后负荷降低,心输出量增加[22]。循环功能与通气改善是密不可分的,肺泡通气显著改善可通过减少缺氧性肺血管收缩(HPV)改善循环,HPV改善程度与肺泡通气改善程度成正比。HPV改善使肺血管扩张,增加肺血管床的有效横截面积,右心室射血阻力降低使射血分数增加,最终改善心输出量及循环功能[16]。同时镇静程度降低也减轻镇静剂扩血管作用导致的血流动力学不稳定[23]。
APRV对自主呼吸无限制,避免重度镇静和肌肉松弛剂的使用[24-25]。但有研究显示,试验初期APRV组与压力控制通气(PCV)组患者相比镇静剂使用减少,而PCV组停止神经肌肉阻滞后2组结果无明显差异[26]。另有研究表明,APRV组和间歇指令通气组镇静剂使用量并无差异[20],原因可能为传统通气模式组为减少人机异步性导致接受神经肌肉阻滞的患者多于APRV组,而接受神经肌肉阻滞患者往往需要更深的镇静。
综上所述,APRV对比LTV模式使ARDS患者氧合、呼吸力学指标及循环功能得到更好改善且镇静需求降低,舒适度相对提高。
利益冲突:所有作者声明无利益冲突
作者贡献声明
滕泽宇、闫早红:设计研究方案,实施研究过程,撰写论文;梁映霞:提出研究方向、研究思路;张传振:资料搜集整理,统计学分析;张成明:论文审核

