两种典型麻类生物炭对水体中镉离子的吸附性能研究
黄薪铭,李丹阳,伍德,张朴心,刘玉玲,铁柏清*
(1.湖南农业大学资源环境学院,湖南 长沙 410128;2.湖南省灌溉水源水质污染净化工程技术研究中心,湖南 长沙 410128;3.农业农村部南方产地污染防控重点实验室,湖南 长沙 410128)
随着经济的快速发展,重金属污染成为危害最大的水污染问题之一[1],重金属具有较强的毒性,在水环境中不能被生物降解,并且容易在生物链中发生富集。镉是一种银白色、有光泽的金属,其毒性较大,被其污染的空气、食物和水等对人体具有严重的危害[2]。因此如何有效解决水体中重金属Cd2+污染问题成为目前环保的热点问题。
生物炭(Biochar)是指由富炭生物质经热解处理,在限氧条件下不完全燃烧生成的一种富含炭的多孔材料[3],主要由碳元素构成,含有的其他元素主要有氮、氢、氧、硫、硅等[4]。生物炭具有高比表面积和微孔型,并且具有高度羧酸酯化、芳香化结构和脂肪族链状结构[5]。这些典型结构特征及生物炭表面丰富的官能团,使生物炭具备了极强的吸附能力。生物炭因其原料廉价易得、操作简便、比表面积和孔容积比较大,对重金属具有较强的吸附性能,成为现今最有优势的吸附剂之一。生物炭的生产和利用是一个减少碳排放的过程。国外在生物炭生产和生物质废弃物热解农业方面做了大量的研究工作[6],但是如何找到一种高效、稳定、易得的生物质材料仍然是生物炭研究的热点问题。
我国拥有丰富的麻类资源,而苎麻和红麻这两种国内最典型的麻类作物,近年来也开始在重金属污染治理领域崭露头角。尹明等[7]对7种红麻在Cd污染耕地中进行植物修复对比试验,发现重度Cd污染下,红麻各部位富集系数为1.11~8.83,转移系数为0.32~4.25,均具较好的生物产量及Cd富集与转移机制;李文略等[8]在两年试验中发现,重金属污染区的红麻Cd富集系数虽未达到1,但具有极高的金属耐性;黄玉敏等[9]选取6种典型红麻品种进行中轻度镉污染农田土壤修复试验,发现其均具有较强的吸收和转运重金属镉的能力。但是目前麻类多应用于土壤中重金属的基础富集,其他方面的研究仍然较少。如徐升[10]利用苎麻麻骨制备生物炭来研究其对水中Cd2+的吸附,理论最大吸附量达到了10.39 mg/g。JIANG等[11]探究了改性苎麻生物炭对水体中铬离子的吸附能力,发现在pH为2.0的条件下,最大吸附量可达197.21 mg/g。
因此,本研究选用苎麻、红麻的茎、叶、皮生物质作为原料,研究其生物炭对水体中Cd2+的吸附性能及机理,以期找到一种清洁、安全、易于获取、价格低廉,能高效去除水体中Cd2+的吸附材料,为去除水体中的Cd2+提供有效材料和理论支撑,同时为麻类作物废弃物的资源化利用提供一种新思路。
1 材料与方法
1.1 供试材料
试验所用苎麻、红麻均采集于湖南省浏阳市焦溪乡常丰村沙德组(113°52.504′E,28°22.983′N)种植调整区,苎麻品种为湘苎一号,红麻品种为湘红麻二号。苎麻镉含量背景值平均为0.030 mg/g,红麻为0.251 mg/g,通过预试验证明,背景值对试验误差影响可忽略。
1.2 试验方法
1.2.1 制备生物炭
植株预处理:将采集回的苎麻、红麻材料用超纯水洗净,使用剪刀将苎麻和红麻的茎、叶、皮分离,分别放入油纸袋中,烘箱烘干,烘干结束后研磨粉末,过80目筛备用。
苎麻和红麻茎、叶、皮生物炭的制备:称取一定量的苎麻、红麻的茎、叶、皮粉末,将粉末放入50 mL瓷坩埚中,使其充满整个坩埚,加盖密封,然后转移至马弗炉中,在500℃[12]下碳化1 h,使粉末受热均匀、充分。完全碳化结束后,冷却,用去离子水清洗至滤出液为中性,烘干,研磨后过100目孔径筛,备用,并将苎麻茎生物炭命名为ZJ,苎麻叶生物炭命名为ZY,苎麻皮生物炭命名为ZP,红麻茎生物炭命名为RJ,红麻叶生物炭命名为RY,红麻皮生物炭命名为RP。
1.2.2 生物炭表征试验
采用M+C型全自动比表面积、微孔孔隙仪分析生物炭孔隙结构。采用Thermo ESCALAB 250XI型X射线光电子能谱进行材料晶体结构分析。采用FEI-QUANTA250热场发射扫描电镜显微镜来观察样品的样貌。
1.2.3 投加量试验
准确称量 0.025、0.050、0.100、0.200、0.300、0.400 g的生物炭材料(表1),放入 50 mL锥形瓶中,同时加入初始浓度为50 mg/L Cd2+溶液30 mL。用0.1 mol/L的NaOH和HCl调节溶液的pH为7,放入恒温振荡箱在25℃、120 r/min条件下振荡8 h,振荡结束后在4000 r/min的条件下离心15 min,用定量滤纸过滤。使用电感耦合等离子体发射光谱(ICP Optima 8300,美国PE公司)测定结果。

表1 投加量试验Table 1 Different material additions processing settings
1.2.4 pH对吸附效果的影响
称取6组0.050 g(投加量试验中最适重量)、均过100目筛的苎麻、红麻生物炭材料,分别放入50 mL锥形瓶中,加入30 mL浓度为50mg/L的镉离子溶液,pH设置如表2,用0.1 mol/L的NaOH和HCl调节溶液的pH值。在25℃、120 r/min振荡8 h,振荡结束后在4000 r/min的条件下离心15 min。用定量滤纸过滤,测定方法同1.2.3。

表2 不同pH处理设置Table 2 Different pH processing settings
1.2.5 反应时间对吸附的影响
称取9组0.050 g(投加量试验中最适重量)、均过100目筛的苎麻、红麻生物炭材料,分别放入50 mL锥形瓶中,分别加入30 mL浓度为50 mg/L的镉离子溶液,用0.1 mol/L的NaOH和HCl调节溶液的 pH为7,在25℃、120 r/min进行震荡吸附。吸附时间分别为 5、15、30、60、120、240、480、960、1440 min(表3)。振荡结束后在4000 r/min的条件下离心15 min。用定量滤纸过滤,测定方法同1.2.3。
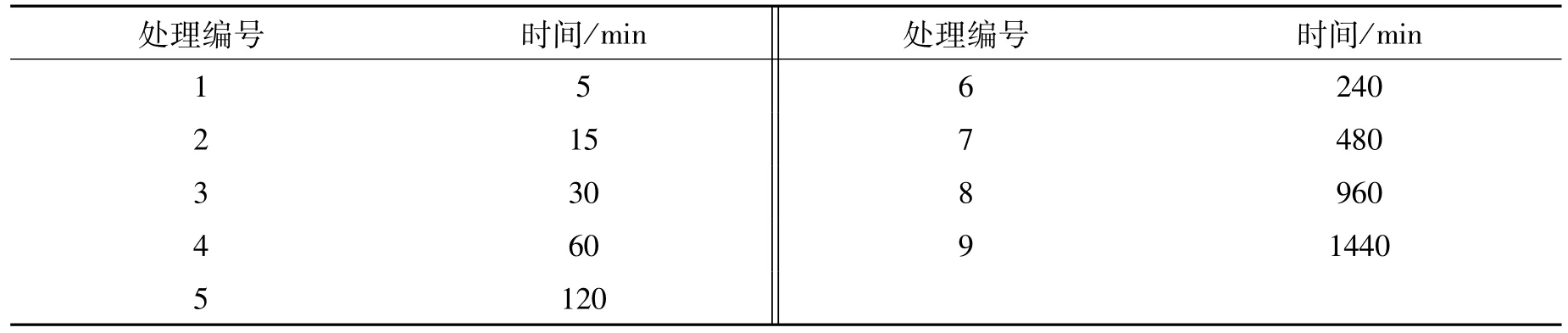
表3 不同反应时间设置Table 3 Different reaction times setting
1.2.6 吸附等温模型
称量10组0.050 g(投加量试验中最适重量)、均过100目筛的苎麻、红麻生物炭材料,放入50 mL锥形瓶中,分别加入30 mL不同初始浓度的镉离子溶液,放入恒温振荡箱中,在25℃、120 r/min条件下振荡8 h,具体浓度见表4。
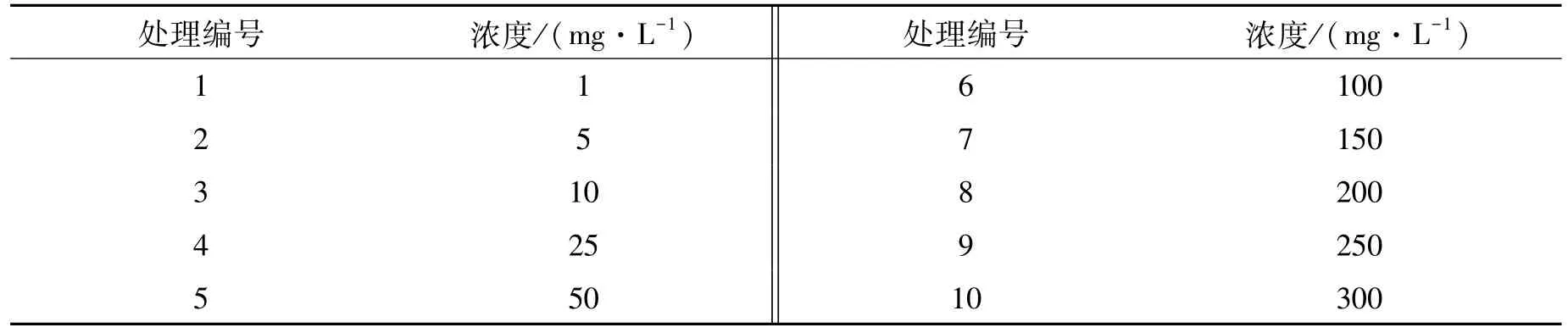
表4 吸附等温处理设置Table 4 Adsorption isotherm processing settings
1.2.7 生物炭再生试验
选取已经达到吸附饱和的苎麻、红麻生物炭材料,放入200 mL锥形瓶中,同时加入2 mol/L的HCL溶液,并在恒温摇床中振荡解析4 h,去离子水洗至中性并烘干。再称取0.050 g解析后生物炭,加入初始浓度为50 mg/L Cd2+溶液30 mL进行二次吸附。三次吸附方法同上。测定方法同1.2.3。
1.3 数据处理
利用Microsoft Excel 2019、Origin 8.5进行数据统计分析及图表绘制。使用一级动力学方程和二级动力学方程模型对苎麻、红麻茎、叶、皮生物炭的吸附动力学进行拟合。并使用Langmuir模型和Freundlich模型对生物炭等温吸附试验数据进行分析。
2 结果与讨论
2.1 材料的表征
2.1.1 生物炭基本性质
表5为6种材料的有机组成元素含量及pH值。生物质在高温碳化过程中,有机组分发生裂解产生稳定的生物炭骨架和易挥发的小分子物质,随着不稳定小分子物质的挥发,生物质中的Na、K、Ca、Mg等碱性组分大量析出[13-14],Ca、Mg、PO3-4形成稳定、难溶的 Ca3(PO4)2和 Mg3(PO4)2等矿物晶体附着在骨架表面[15],Na、K等元素则直接促进生物炭pH值的升高。而叶材料C、H、O、N总含量较低,说明其在相同热解温度下,析出的碱性组分含量相对高于其他材料生物炭,这也是其具有较高pH值的原因。
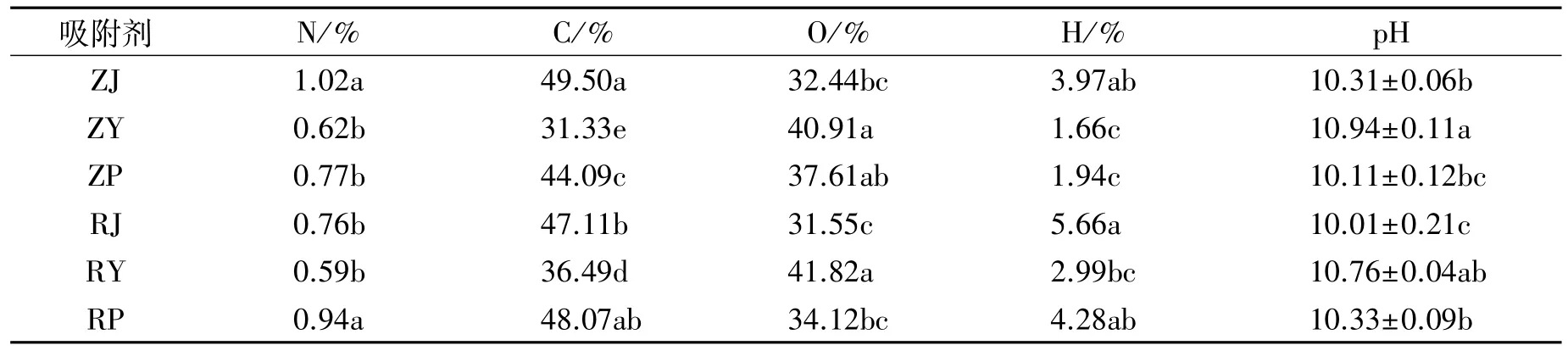
表5 生物炭材料的元素分析及pH值Table 5 Elemental analysis and pH of different biochar materials
表6为6种吸附材料的比表面积、总孔容积、平均孔径。由表6可以看出,叶生物炭的比表面积、总孔容、平均孔径都要大于皮生物炭和茎生物炭,因此3种不同部位的材料相比,叶材料生物炭可能会提供更多的吸附位点,具有更大的吸附潜力。而苎麻叶生物炭的比表面积大于红麻叶生物炭,总孔容积和平均孔径却小于红麻叶生物炭,说明苎麻叶生物炭材料的表面具有更多的孔结构。
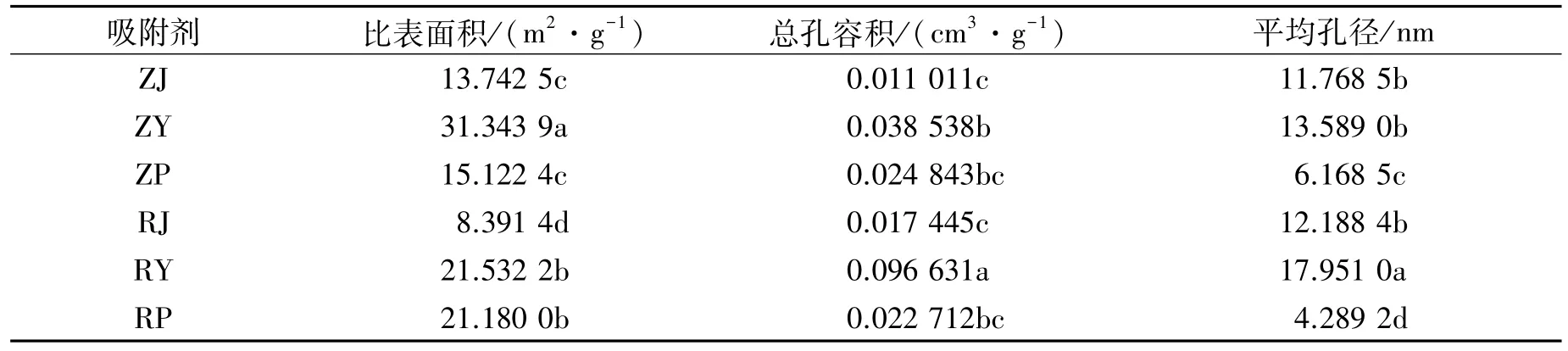
表6 生物炭的比表面积及孔结构参数Table 6 Specific surface area and porosity parameters of biochar
2.1.2 SEM
图1是6种生物炭材料的扫描电镜图。用SEM分析了6种生物炭的表面形态特征,通过选取不同标尺下的电镜照片观察生物炭表面结构。可以看出,茎、叶、皮3种材料所制备的生物炭中,茎生物炭的表面都较为光滑,孔结构分布较为稀疏且孔径较大;叶生物炭与茎生物炭相比,呈类似海绵的疏松多孔结构,表面较为粗糙且呈扭曲状;皮生物炭同为与叶生物炭类似的海绵结构,但不同的是,皮生物炭的表面出现了部分坍塌和堆积,同时出现了细小的条形纹理,主要是因为炭化过程中麻类韧皮纤维会逐渐断裂和损伤[16],纤维长度下降但仍保持原有的条形。

图1 6种材料的电镜图片Fig.1 Electron microscopy pictures of six materials
2.1.3 XPS
X-射线光电子能谱(XPS)拥有比较高的表面灵敏度,通过比较生物炭表面元素结合能的情况,进一步研究生物炭对Cd2+的吸附机理。由图2可知,与茎、皮两种材料的生物炭相比,叶生物炭的氧峰比例最高,苎麻、红麻的叶生物炭氧峰比例分别为37.67%和24.44%,说明叶生物炭与茎、皮部位生物炭相比,表面具有更多的含氧官能团,具有更好的吸附性能。同时苎麻叶表面相较于红麻叶生物炭表面具有更多含氧官能团。
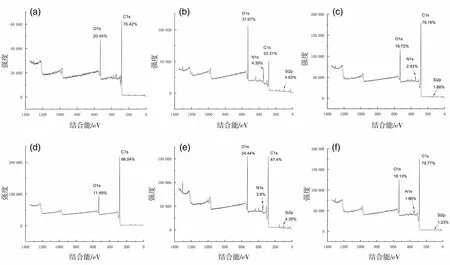
图2 6种材料的XPS总谱图Fig.2 XPS spectra of sixkindsof biochar
通过分峰处理,C峰位置在284.4、285、286.3、288、289.6 eV处出现的峰分别代表的是 C=C[17]、C-C/C-H、C-N/C-O[18]、C=O/O-C=O[19]和碳酸盐[20]。图3为 6种生物炭材料的 C1s谱图,可以看出相较于茎、皮生物炭,叶生物炭的表面具有更高的C=O/O-C=O和C-O/C-N峰面积比例。图4(a)和图4(b)为苎麻生物炭材料对Cd2+吸附前后的C1s谱图,利用XPS peak软件对照RWA值及峰面积进行分析,发现吸附前后C-C/C-H和碳酸盐的峰未发生显著变化,而C=O/O-C=O和C-O/C-N的峰面积发生明显变化,C=O/O-C=O的峰面积从16.36%下降到了12.14%,而C-O/C-N的峰面积从16.69%上升到了18.55%,说明C-C/C-H和碳酸盐形式的碳原子没有直接参与Cd2+的吸附,而-C=O/O-C=O类型的碳在一定程度上参与了生物炭对Cd2+的吸附,并转化成了C-O。图4(c)和图4(d)分别是红麻叶吸附前后的C1s谱图,通过分峰处理后,得到与苎麻叶生物炭同样的结论。
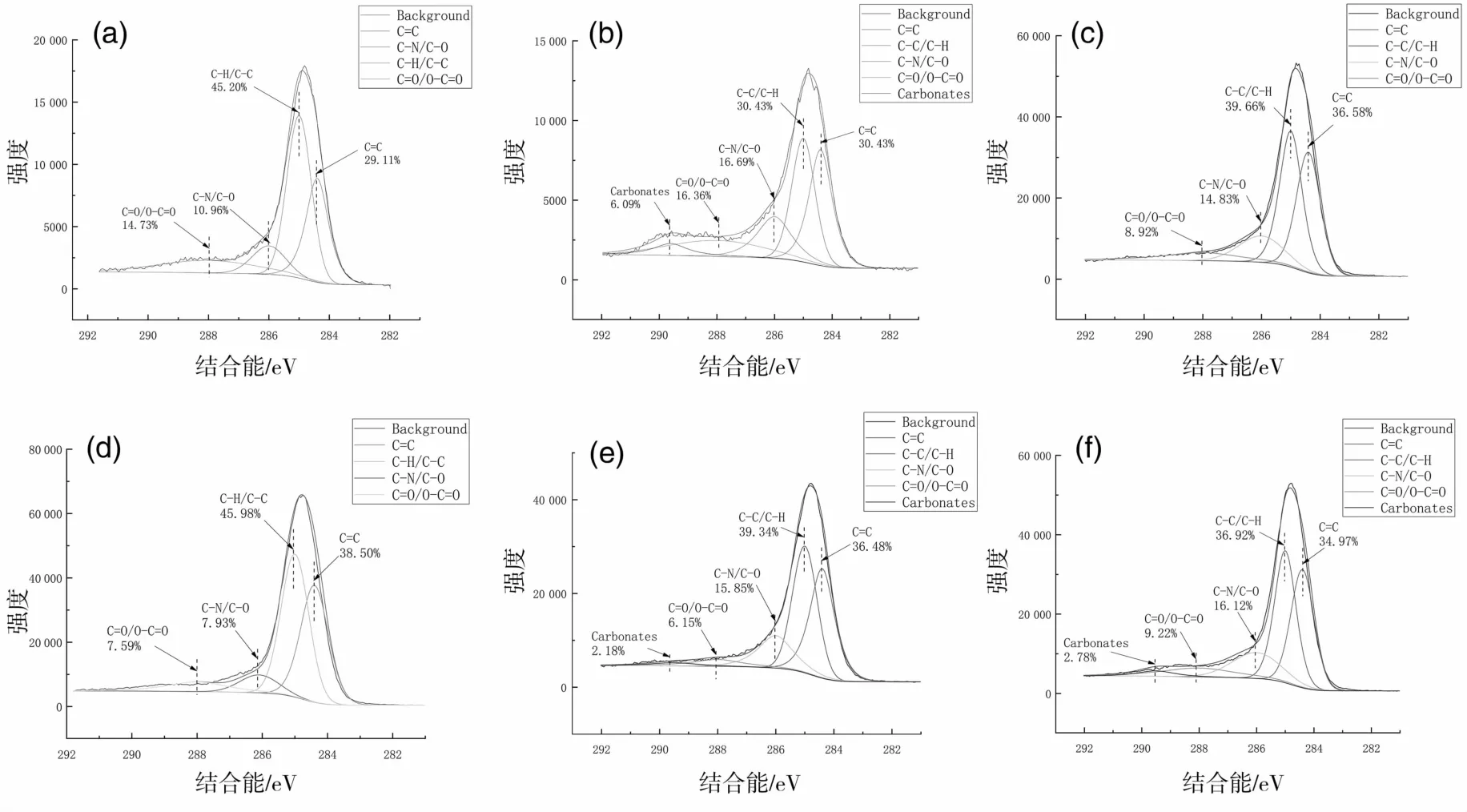
图3 碳元素核心轨道XPS图像Fig.3 Carbonelement core orbit XPS image
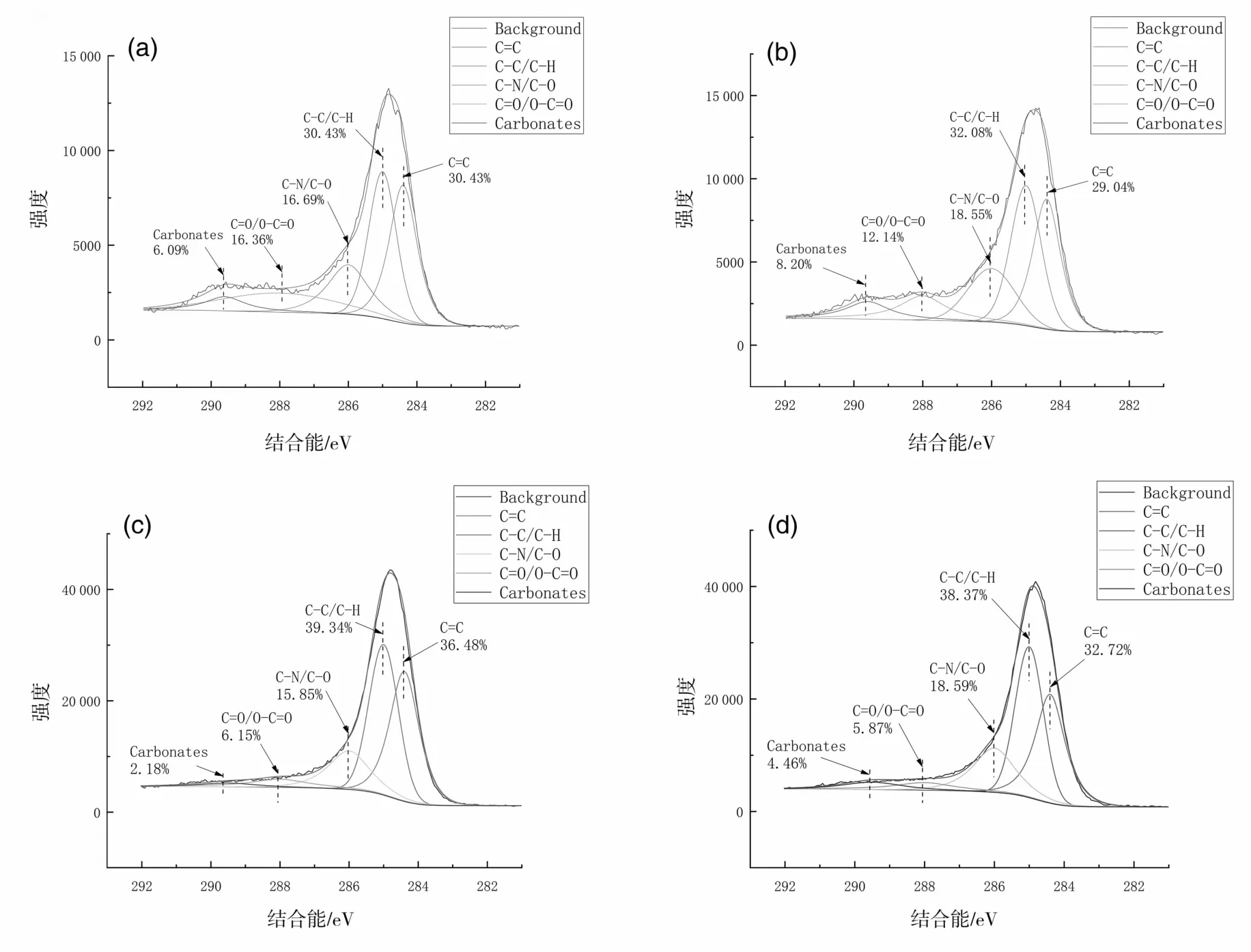
图4 碳元素核心轨道XPS图像Fig.4 Carbonelement core orbit XPS image
结合能的变化可能是因为Cd2+在吸附过程中与氧元素结合,导致氧元素的电子密度降低[21]。结合峰面积的变化,可以推断出C=O/O-C=O上的氧原子是Cd2+的主要吸附点位,官能团上的氧原子可通过阳离子-π作用、络合作用和Cd2+形成配位键。图5(b)和图5(d)分别为苎麻叶生物炭和红麻叶生物炭吸附后Cd3d谱图,经过XPS分析,发现Cd3d的峰出现在405.5 eV的位置,为Cd的氧化物以及-OCdOH。结合C1s谱图分析,表明生物炭对Cd的吸附机理主要为Cd与生物炭表面的羟基化表面(-OH)或其去质子化(-O-)络合[22]。
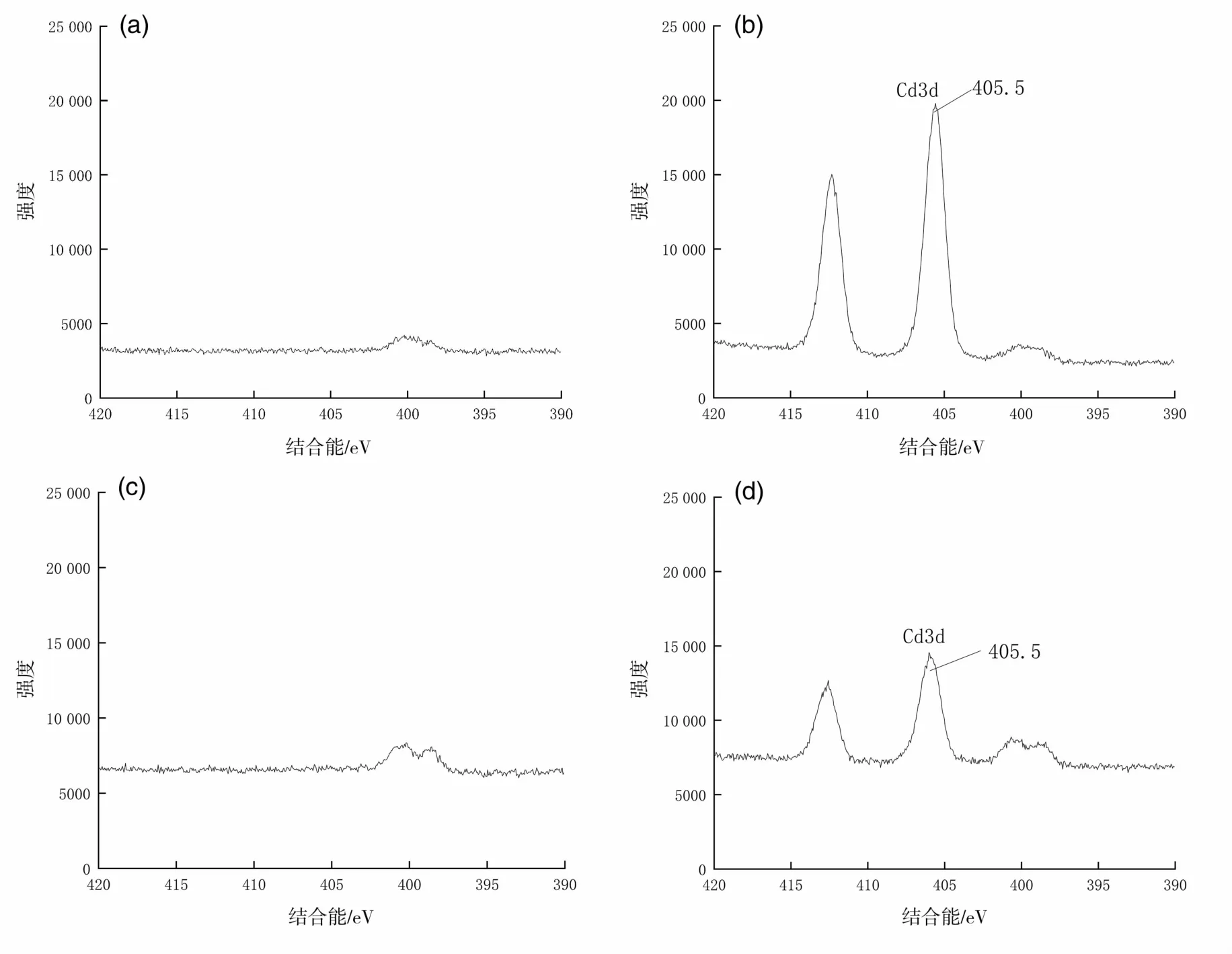
图5 镉元素核心轨道XPS图像Fig.5 Cadmiumelement core orbit XPS image
2.2 静态吸附试验
2.2.1 投加量试验
从图6可知,当水体中Cd2+初始浓度为50 mg/L时,6种生物炭对于水体中的Cd2+都有良好的吸附效果,总体来看,6种吸附材料对水中Cd2+的吸附效果均随投加量的不断增多而增强,并且在投加量大于0.2 g后,对Cd2+的去除率均达到90%以上并趋于稳定。其中,苎麻茎生物炭对Cd2+的去除率范围为1.10%~98.69%,去除率变化范围最大。苎麻皮生物炭对Cd2+的去除率范围为43.42%~98.00%,去除率变化范围最小。因为生物炭材料具有有限的结合位点,低投加量时结合位点较少,去除率较低,随着投加量的增加,材料结合位点增多,去除率上升。综合考虑吸附量及经济因素,后续pH控制及吸附动力学试验等控制材料投加量的试验,投加量均选为0.05 g。
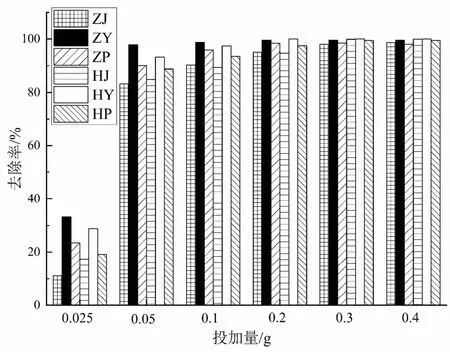
图6 投加量试验Fig.6 Effect of adsorbent dosage on adsorption
2.2.2 溶液pH对吸附效果的影响
由图7可知,当Cd2+溶液初始浓度为50 mg/L时,生物炭对溶液中Cd2+的去除率随着溶液pH的增加而升高并趋于稳定。在pH=2时,除了苎麻叶生物炭对Cd2+的去除率维持在60%以上,其他5种生物炭对Cd2+的去除率均较低。当pH=3时,苎麻叶生物炭和红麻皮生物炭对溶液中Cd2+的去除率迅速上升至95%以上的水平,并且在pH为3~7的情况下对溶液中Cd2+的去除率基本保持稳定。红麻茎、叶生物炭则是在pH为4~7时去除率基本保持稳定。分析上述现象的原因,可能是在强酸性条件下,溶液中大量的H+会占据有限的结合位点,并且与Cd2+产生竞争吸附,降低Cd2+去除率[23];同时,这些H+会改变材料表面的电荷分布,导致一部分有利于Cd2+吸附的表面官能团发生解离,从而使材料对Cd2+的吸附性能下降[24]。随着pH的升高,H+量减少,使大量材料表面结合位点暴露,吸附容量也随之增加[25]。而苎麻皮生物炭对溶液中Cd2+的去除率受pH影响最大,在pH为2~7的情况下对溶液中Cd2+的去除率不断上升。
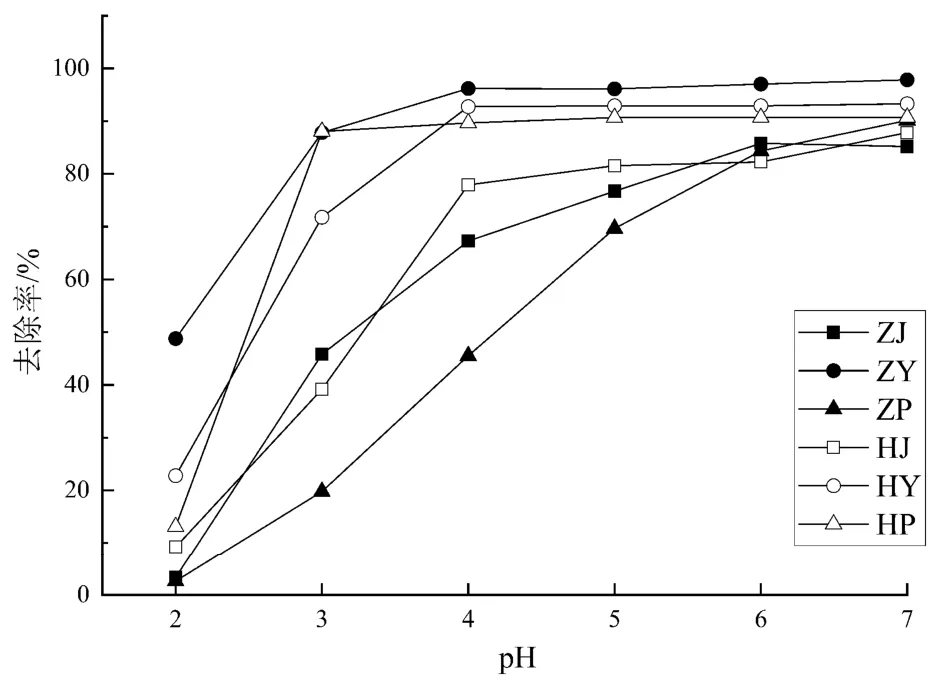
图7 溶液pH对吸附效果的影响Fig.7 Effect of solution pH on adsorption
2.2.3 吸附动力学试验
图8为吸附动力学试验结果,可以看出6种生物炭对Cd2+的吸附量最初均随着时间的增加而增加,并最终达到稳定。苎麻茎、皮生物炭在480 min处达到平衡,苎麻叶生物炭在15 min处达到吸附平衡,红麻叶、皮生物炭在5 min处达到吸附平衡,红麻茎生物炭在960 min时达到平衡。
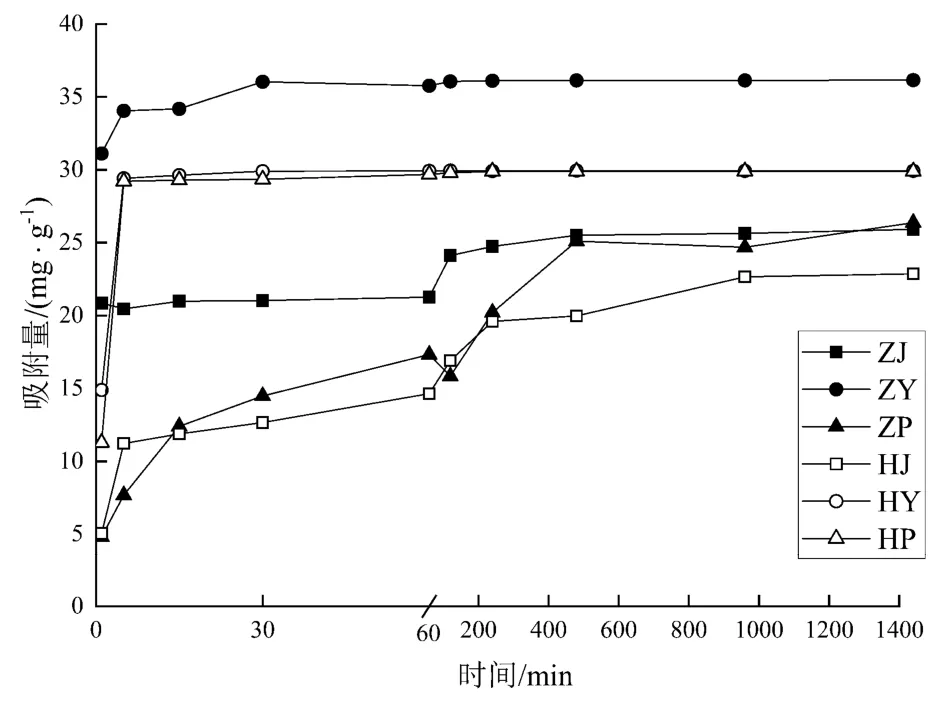
图8 吸附动力学试验Fig.8 Adsorption kinetics experimental results
拟合ln(qe-qt)-t和t/qt-t的线性关系如图9所示。动力学拟合参数如表7所示。由拟合参数可得,当初始Cd2+浓度为50mg/L时,准二级动力学方程能更好地描述这6种生物炭材料的吸附过程。这也表明6种生物炭对Cd2+的吸附主要是受化学吸附作用的控制。
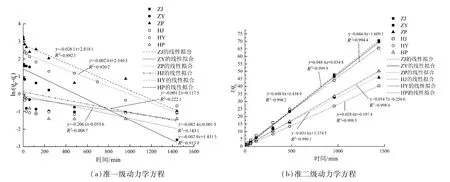
图9 动力学拟合曲线Fig.9 Adsorption kinetics fitting curve
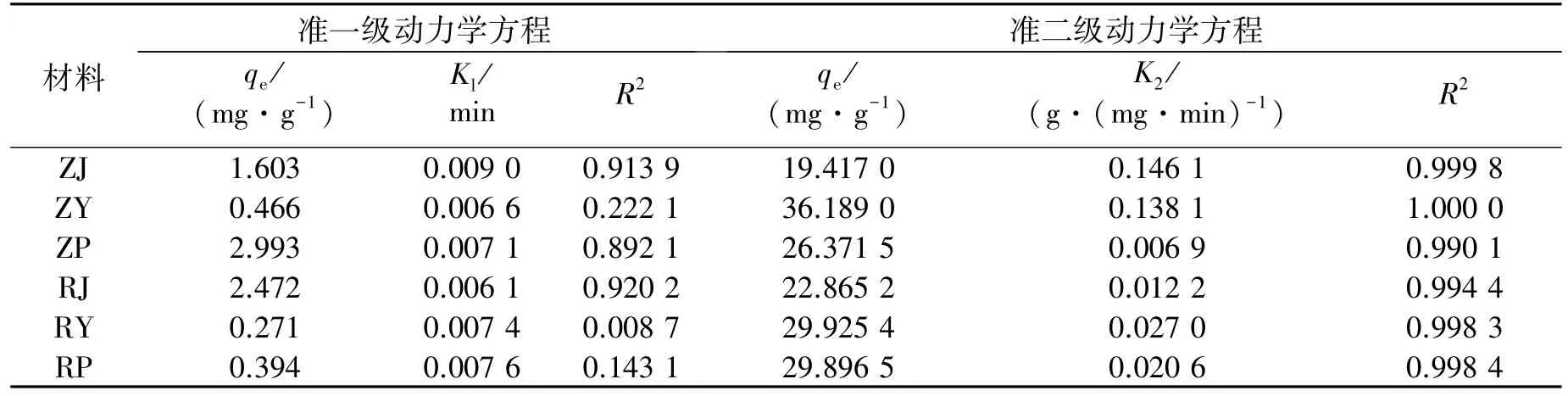
表7 动力学拟合参数Table 7 Kinetic fitting results
2.2.4 等温吸附试验
表8为等温吸附模型拟合参数。从表中6种吸附线性拟合度R2能看出,6种生物炭均更适合Langmuir理论模型。
在Langmuir理论模型中,KL值代表Langmuir理论模型中的平衡常数,其值越大代表此种吸附剂的吸附能力越强。6种吸附材料中,苎麻茎、叶、皮生物炭KL值分别为0.31、2.25、0.69,红麻茎、叶、皮生物炭KL值分别为0.44、1.66、1.33。因而6种材料对水中镉的吸附能力大小为苎麻叶生物炭>红麻叶生物炭>红麻皮生物炭>苎麻皮生物炭>红麻茎生物炭>苎麻茎生物炭。qmax代表的是6种吸附材料的最大吸附量,其中苎麻叶生物炭对水中镉的最大吸附量最大,达到了133.05mg/g,红麻叶生物炭次之,为104.42 mg/g,红麻茎生物炭对水中镉的最大吸附量最小,为45.39 mg/g。
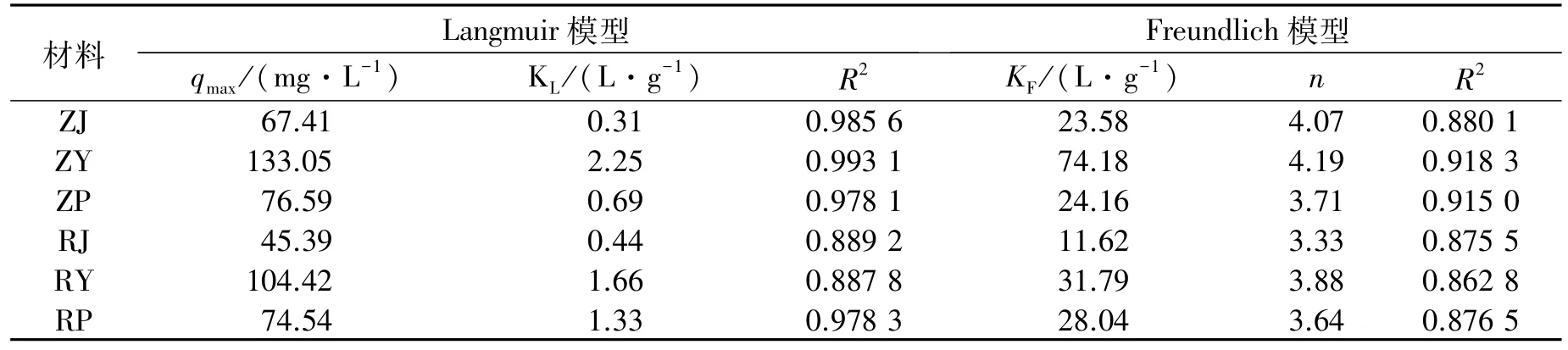
表8 等温吸附模型拟合参数Table 8 Fitness of isotherm models and corresponding parameters
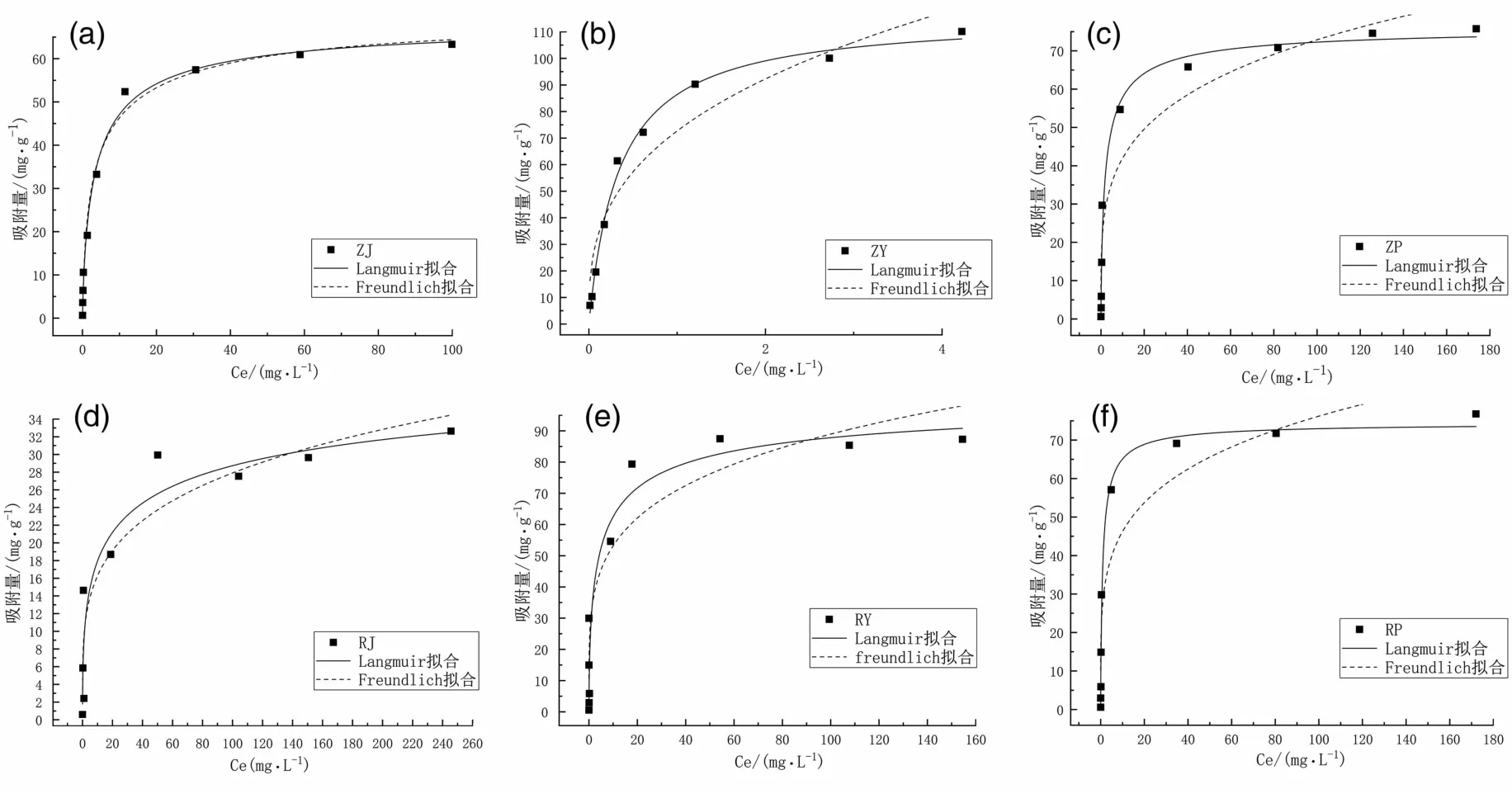
图10 Langmuir和Freundlich吸附等温线Fig.10 Langmir isotherm and freundlich isotherm plot of Cd2+adsorption
2.2.5 生物炭再生试验
从图11可以看出,当溶液初始浓度Cd2+为50mg/L时,苎麻叶、红麻叶生物炭两种材料首次吸附的去除率均在96%以上,经过一次吸附—脱附试验后,6种材料对溶液中Cd2+的去除率均有所降低。经过连续两次吸附—脱附试验后,只有苎麻叶、红麻叶生物炭表现较好,分别降低为43.69%和38.64%,较原材料对Cd2+的去除率分别减少了53.16%和60.67%。其他材料的去除率都下降到了20%左右,说明苎麻叶、红麻叶两种材料均有较好再生性。
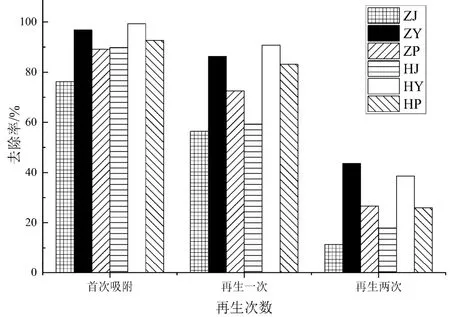
图11 脱附再生试验结果Fig.11 Desorption and regeneration results
3 结论
(1)试验表明,苎麻叶生物炭表面具有6种生物炭材料中最高的含氧官能团比例,同时在对试验溶液中Cd2+的静态吸附试验中表现出最好的吸附效果。
(2)试验发现,6种吸附材料都能较好地拟合Langmuir理论模型和Freundlich理论模型,6种材料均更适合Langmuir理论模型,其中苎麻叶生物炭对水中镉的最大吸附量达到了133.05 mg/g,是6种材料中最高的。
(3)通过动力学试验分析,准二级动力学方程能更好描述6种材料的吸附过程,相关系数R2均大于0.99,苎麻茎、皮生物炭在480min处达到平衡,苎麻叶生物炭在15min处达到吸附平衡,红麻叶、皮生物炭在5 min处达到吸附平衡,红麻茎生物炭在960 min时达到平衡。
(4)试验表明,参与吸附的主要官能团为含氧双键,在吸附反应的过程中转化成碳氧单键。生物炭对Cd的吸附机理主要为Cd与生物炭表面的羟基化表面(-OH)或其去质子化(-O-)络合,以及静电作用。

