铅在土壤中的吸附特性及形态分布研究
李兵,李聪,赵曼青,唐娜,吴双,高焕方
(1.重庆理工大学 化学化工学院,重庆 400054;2.重庆汇亚环保科技有限公司,重庆 400041;3.重庆市固体废物管理中心,重庆 400015)
土壤是农业发展的重要基础[1-2],也是一个多组分的复杂系统,对Pb具有较好的吸附作用[3-4]。铅在土壤中的吸附过程主要受土壤各个组分的影响[5],不同组分吸持的Pb具有不同程度的迁移性[6]和生物可利用性。主要分为弱酸可提取态、可还原态、氧化态和残渣态[7-8],其中铅弱酸可提取态迁移性最强,对环境造成的威胁也最大。
铅在土壤中的吸附特性一般主要通过动力学[9]、等温吸附、热力学等方面进行研究,但对铅吸附在土壤后的形态分布规律研究较少。因此,本文研究了铅吸附在土壤后的形态分布,这对探究铅在土壤中的迁移性和生物可利用性十分有必要。
1 实验部分
1.1 材料与仪器
土壤,均来自重庆未被开发利用地块,采样深度为10~20 cm,性状为黄褐色黏土(经自然风干,研磨后,过100目金属筛,于PE塑料袋中保存备用);硝酸铅、浓硫酸、浓硝酸、浓盐酸、氢氟酸、高氯酸均为分析纯。
PHS-3E pH计;CDH15-ProD48土壤石墨消化炉;SHA-CA恒温水浴振荡器;TGL-400低速离心机;AA-800石墨炉原子吸收光谱仪;Spectrum65傅里叶变换红外光谱仪;QM-3SP4行星式球磨机。
1.2 实验方法
称取3.196 g Pb(NO3)2,定容至2 L的容量瓶中,得到Pb2+浓度为 1 000 mg/L的母液。后续实验中所用不同浓度Pb(NO3)2溶液均由母液稀释所得。将母液稀释配制成100,200,300 mg/L的 Pb(NO3)2溶液,土水比10 g/L,将离心管置于水浴恒温振荡器中,在温度25 ℃,振荡频率180 r/min,振荡时间 10 h。振荡之后的溶液经低速离心机以强度 3 000 r/min 离心20 min。上清液定容50 mL容量瓶中,用石墨炉原子吸收光谱仪测试Pb2+浓度。
计算Pb2+的吸附量(qe)和去除率(R)。
(1)
(2)
式中C0,Ci——Pb2+初始浓度和某一吸附时段的浓度,mg/L;
m——土壤质量(0.000 1 mg);
V0,V1——离心过滤后取样体积和试样定容体积,mL。
2 结果与讨论
2.1 土水比对铅吸附量的影响
土水比对铅吸附量的影响见图1。
由图1a可知,增加土水比,土壤颗粒含量增加,颗粒之间的相互作用引起土壤发生凝聚现象,总吸附表面积降低,导致吸附量降低。由图1b可知,随着土水比的增加,土壤颗粒含量增加,吸附活性位点增多[10],土壤颗粒对Pb2+吸附能力增强,当土水比为10 g/L时,去除率最高,达到90%以上。实验表明,土壤对重金属铅有特定的吸附作用,且吸附性能较好。这可能是因为土壤包含了多种有机质[11]、金属氧化物和矿物质等,各个组分之间相互作用,导致对重金属铅有较好的吸附作用。
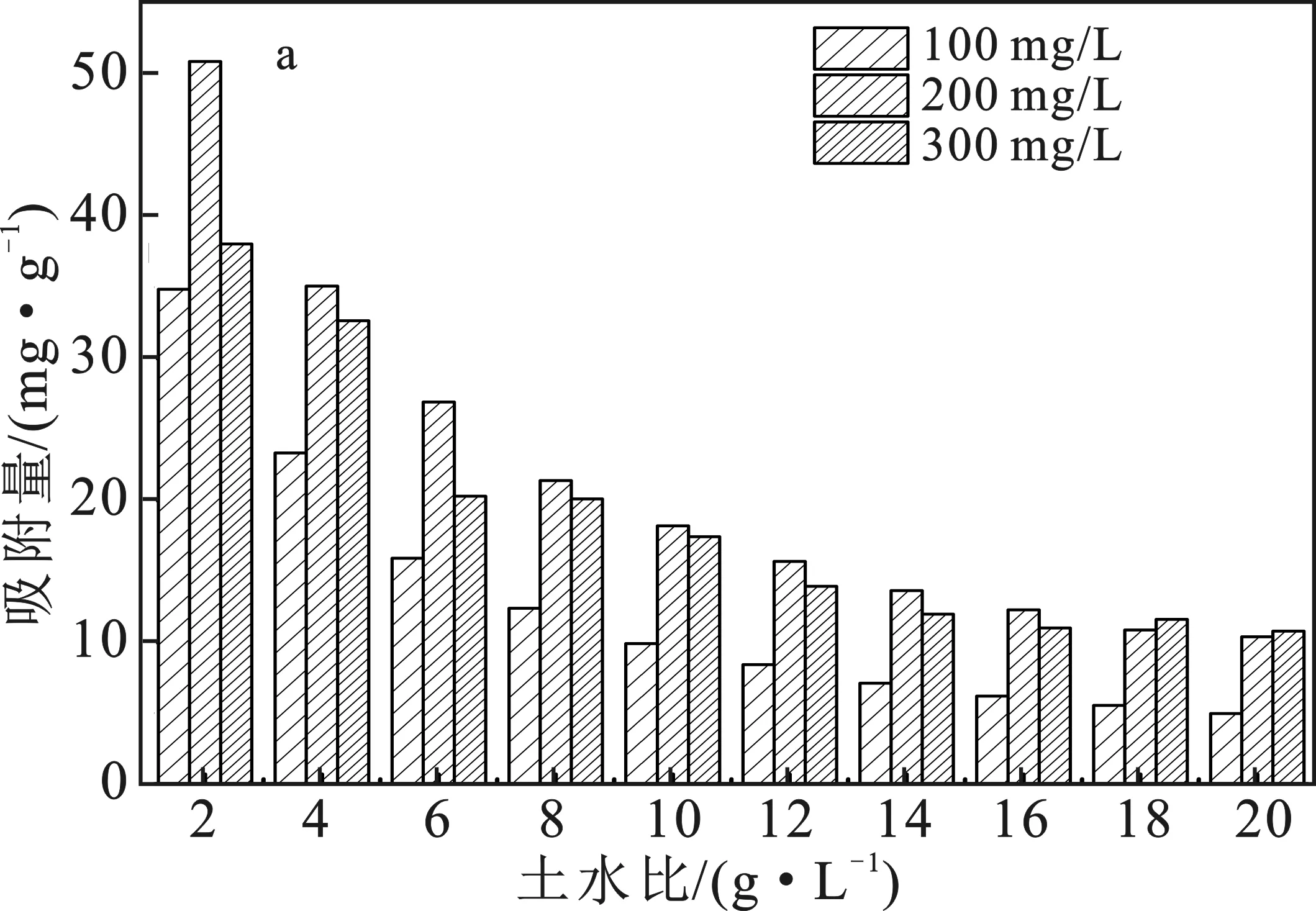

图1 土水比对吸附量和去除率影响Fig.1 Effect of soil-water ratio on adsorption capacity and removal ratea.吸附量;b.去除率
2.2 铅在土壤中的吸附动力学
将母液分别配制成100,200,300,400 mg/L的硝酸铅溶液,控制土水比10 g/L,温度25 ℃,振荡频率(180±20)r/min,振荡之后溶液在 3 000 r/min的条件下离心20 min,上清液定容50 mL容量瓶中,用原子吸收光谱仪测试Pb2+浓度,实验结果见图2。

图2 反应时间对土壤吸附Pb2+的影响Fig.2 Effect of reaction time on adsorption of Pb2+ in soil
由图2可知,铅在土壤中的吸附过程迅速,在10 min内,吸附量快速增加,10 min后,吸附增长开始逐步减缓,重金属铅的去除率趋于平衡。这是因为吸附在土壤中的铅发生了解析反应[12],导致吸附量出现一定波动,且随着时间延长,吸附量可能会出现降低的情况。说明铅在土壤中的吸附是一个快速过程,且能在较短时间内吸附在颗粒表面[13];随着时间增加,表面吸附逐步达到平衡[14],吸附速率降低,吸附过程开始变得缓慢。这是可能因为土壤是一个较为复杂的体系,铅吸附在土壤表面后,再逐步通过内扩散进入土壤,与其中的金属氧化物、有机质和硅酸盐类等物质发生吸附作用[15],从而将铅吸附在土壤中。
对4种吸附曲线分别用准一级动力学方程和准二级动力学方程进行拟合,结果见表1。
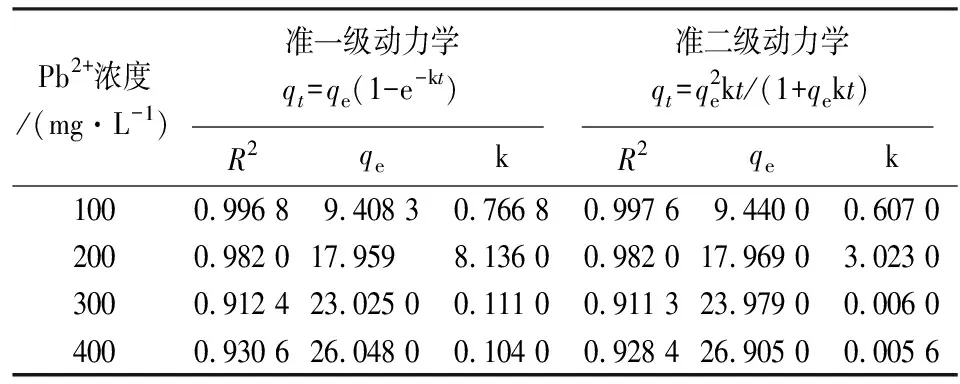
表1 动力学方程拟合参数Table 1 Dynamics equation fitting parameters
由表1可知,准二级动力学拟合效果最好,R2能达到0.99以上,计算的饱和吸附量(qe)分别为9.440 0,17.969 0,23.979 0,26.905 0 g/kg,与实际测试值9.563 2,18.755,24.860 0,26.520 0 g/kg更为接近。表明铅在土壤中的吸附过程主要以化学吸附为主,同时有含铅元素的新化学键形成。
2.3 等温吸附线
在温度25,30,40 ℃,土水比10 g/L,振荡频率(180±20)r/min,振荡时间为(10±2)h,振荡之后溶液在3 000 r/min离心20 min。以原子吸收光谱仪测试上清液的Pb2+浓度。采用Langmuir、Freundlich和Redlich-Peterson模型对实验数据进行拟合,结果见表2和图3。
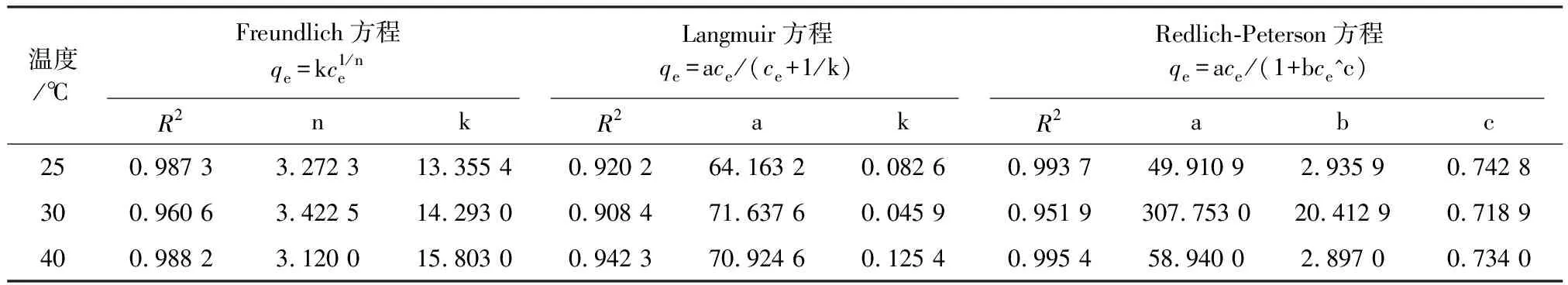
表2 Pb2+在土壤上等温吸附参数Table 2 Isothermal adsorption parameters of Pb2+ on soil
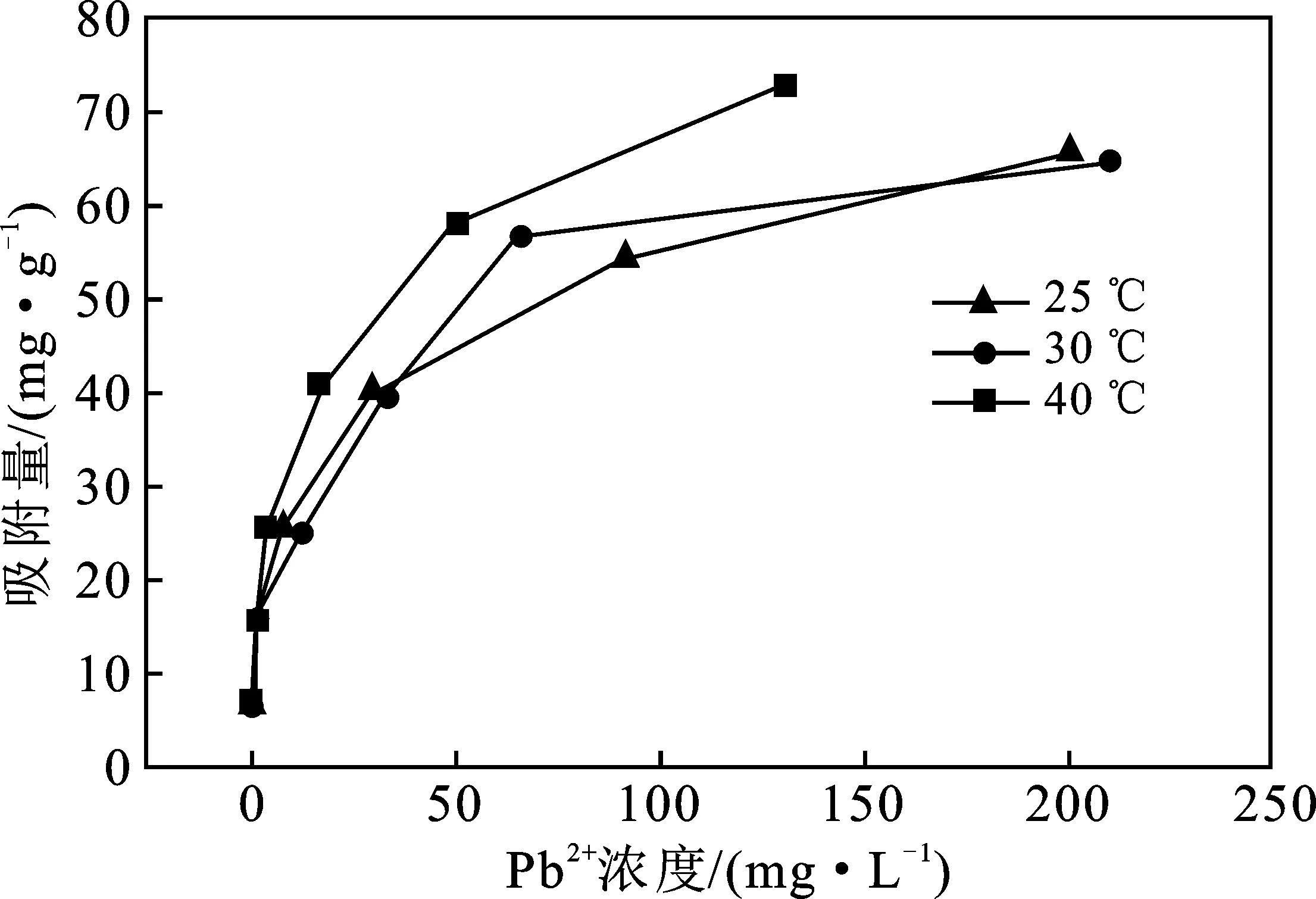
图3 不同温度Pb2+在土壤上的等温吸附线Fig.3 Isothermal adsorption curves of Pb2+ on soil at different temperatures
由表2可知,Freundlich吸附模型拟合效果较好,R2最高能达到0.988 2,且1/n<0.5,这表明土壤对重金属铅的吸附性能较好,计算的最大饱和吸附量分别为67.23,68.23,75.41 mg/g,与实际最大饱和吸附量65.68,66.67,72.68 mg/g较为吻合。表明重金属铅在土壤中的吸附过程不是单一物理吸附,而且重金属铅与土壤组分之间发生电子交换或偏移[16],形成新的化学吸附键。这与动力学实验结果一致,表明土壤对铅的吸附是静电吸附和重金属铅与土壤组分之间离子交换共同作用的结果。
2.4 铅离子吸附在土壤颗粒表面红外光谱分析
在温度为25 ℃,土水比为10 g/L,溶液Pb2+初始浓度为100 mg/L,转速180 r/min的条件下,振荡(24±2)h,在 3 000 r/min的条件下,离心20 min,倒出上清液。将剩余固体物在自然条件下风干,研磨后,于PE塑料袋中保存陈化15 d。然后进行红外光谱分析,结果见图4。
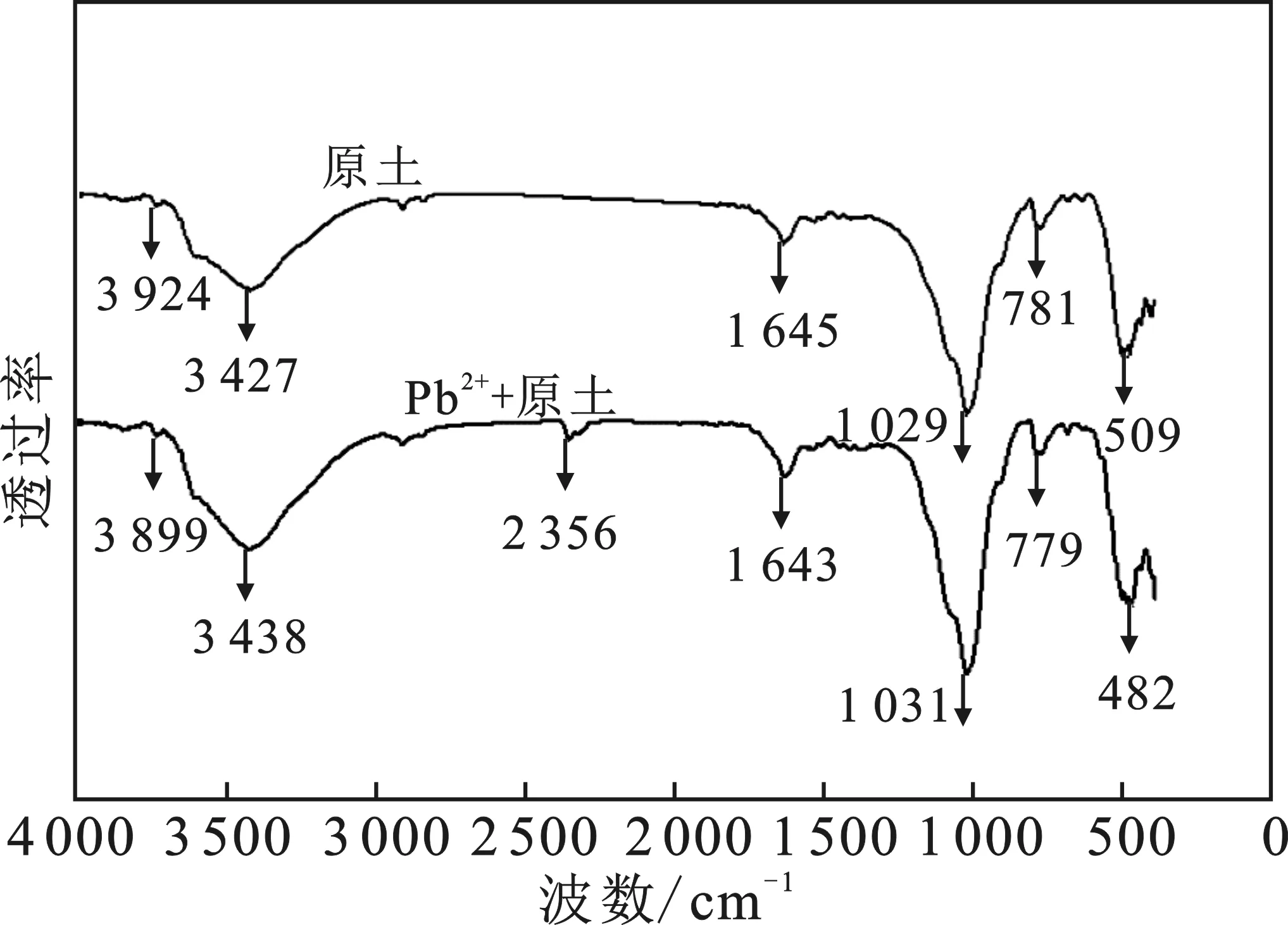
图4 土壤中有机质对吸附Pb2+的影响

2.5 铅在土壤中的形态分布
实验共设9个处理组,在温度为25 ℃,土水比为10 g/L,转速180 r/min的条件下振荡,研究不同浓度(44,400,800 mg/L)和不同时间(10,60,600 min)处理条件下,Pb2+在土壤中的形态分布情况。经过滤后得到的滤饼自然风干后,于PE塑料袋中保存陈化15 d后备用。
2.5.1 溶液中Pb2+变化情况 不同吸附时间和不同初始浓度条件下,溶液中Pb2+去除率见图5。
由图5可知,随着溶液初始浓度的增加,Pb2+在溶液中的去除率由99.93%降至43.2%。这可能是因为土壤颗粒对Pb2+存在吸附平衡,当达到饱和吸附量时,土壤对Pb2+的吸附能力降低,同时吸附在土壤上的Pb2+可能会发生解析,从而引起溶液中Pb2+的去除率降低。在同一浓度处理条件下,Pb2+的去除率随时间的变化较小。这是因为Pb2+在土壤中的吸附过程是快速的,能在较短时间内到达吸附平衡。这与动力学实验结论一致。
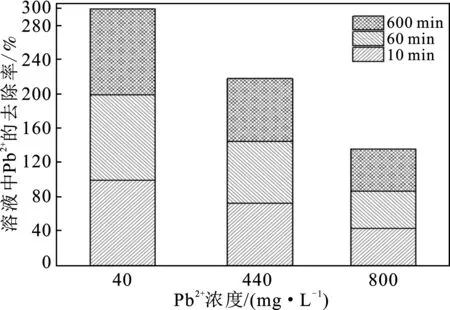
图5 溶液初始浓度及时间对Pb2+去除率的影响
2.5.2 Pb在土壤中的形态分布 根据BCR连续形态提取法(见表3),对陈化后的土壤中铅各个形态含量进行测定,结果见图6。

表3 铅离子各形态提取方式
由图6可知,在较短吸附时间内,有95%的铅转换为弱酸可提取态和可还原态的形式存在于土壤中,剩余的铅转换为氧化态和残渣态的形式存在。这是因为土壤对重金属铅的吸附过程包含了物理吸附与化学吸附,其中化学吸附是主要的吸附过程。土壤中的氧化铁和氧化锰类物质表面有较多的OH-、OH+等基团存在,能使土壤表面拥有大量可与无机和有机离子交换和配位的基团,与重金属铅反应,形成新的化合物。实验表明,重金属铅在土壤中能快速转换为弱酸可提取态、可还原态、氧化态和残渣态四种形式,其中可还原态含量占最高,为85.27%。
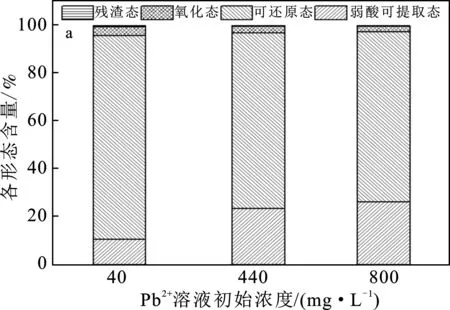


图6 Pb2+在土壤中各形态含量分布Fig.6 Morphological changes of Pb2+ under different treatment conditionsa.10 min;b.60 min;c.600 min
由图6可知,溶液初始浓度由40 mg/L升至800 mg/L时,由于土壤颗粒的静电作用,重金属铅被快速吸附在土壤颗粒表面,导致弱酸可提取态含量逐步增加,但可还原态出现缓慢降低。这可能是因为重金属铅在土壤中的吸附过程分为两个阶段,第一阶段是快速吸附阶段,此时溶液中的铅离子迅速聚集在土壤颗粒表面,通过离子交换或静电引力吸附在土壤颗粒上;第二阶段,此时土壤颗粒表面的活性吸附位点基本被占据,铅离子通过内扩散的作用进入土壤颗粒内部,被其他组分所吸附;第三阶段,此时吸附已经达到平衡状态,并出现解吸现象,从而溶液初始浓度越高,可还原态含量出现下降。
3 结论
(1)土壤颗粒对重金属铅有较好的吸附作用,溶液初始浓度对铅的吸附量和去除率都有较大影响,溶液初始浓度越高,重金属铅在土壤中的吸附量越大,溶液中铅离子的去除率越低。
(2)土壤吸附重金属铅的平衡时间约为 60 min,吸附过程符合准二级动力学模型(R2=0.996 8)和Freundlich吸附模型(R2=0.988 2),整个过程主要以化学吸附为主,并有新的化学键形成。
(3)重金属铅吸附在土壤中后,分别以弱酸可提取态、可还原态、氧化态和残渣态四种形态存在,95%的重金属铅主要是以弱酸可提取态和可还原态的形式存在。表明土壤中的铁、锰氧化物能作为良好的稳定化药剂运用于修复铅污染土壤之中。

