LncRNA TTN-AS1调控miR-139-5p/PDK1/AKT/Caspase-3信号通路促进鼻咽癌的生长和转移
刘春江,司峰志
(新疆医科大学第二附属医院耳鼻喉科,新疆 乌鲁木齐 830092)
鼻咽癌是常见的头颈部恶性肿瘤,起源于鼻黏膜上皮组织[1],虽然鼻咽癌细胞对放疗敏感,但由于鼻咽癌的发生部位隐匿,在早期不容易被发现及诊断,患者往往在确诊时已处于中晚期,为肿瘤的治疗带来一定的困难;中晚期鼻咽癌患者5年生存率不足50%、严重威胁患者生命健康[2-3]。因此,深入研究鼻咽癌的发病机制,寻找新的诊断和治疗靶点意义重大。长链非编码RNA(long non-coding RNA,lncRNA)是近年来被发现可调控肿瘤病理过程且具有成为肿瘤诊断和治疗靶点潜力的非编码RNA[4],可在表观遗传水平、转录水平和转录后水平调控肿瘤的生长、转移、耐药、免疫逃逸等,从而影响肿瘤的发生发展[5]。在鼻咽癌中,lncRNA FAM225A可通过调控miR-590-3p/miR-1275促进鼻咽癌细胞的生长和转移[6],lncRNA SNHG7可调控上皮间充质转化从而促进鼻咽癌的生长[7]。LncRNA TTN-AS1(TTN-AS1)可调控多种肿瘤,如TTN-AS1结合miR-376a-3p可促进子宫内膜癌的发展[8],TTN-AS1可通过激活DGCR8促进乳腺癌的转移[9],但是TTN-AS1在鼻咽癌中的作用目前尚不明确。因此,本文探究TTN-AS1对鼻咽癌细胞增殖、凋亡和转移的影响及其机制,以期为鼻咽癌的诊治提供参考。
1 材料与方法
1.1 材料
鼻咽癌细胞系TW03、C666-2、CNE2,鼻咽上皮细胞系NP69,人胚胎肾细胞HEK 293T购自中科院上海细胞库;PrimeScript RT reagent Kit、Power SYBR Green试剂盒购自日本TAKARA公司;Lipofectamine 2000试剂盒购自美国Invitrogen公司;CCK-8试剂盒、细胞凋亡检测试剂盒购自沈阳万类生物技术有限公司;双荧光素酶报告基因检测试剂盒购自上海翊圣生物科技有限公司;PDK1抗体、Caspase-3抗体、AKT抗体、p-AKT抗体、GAPDH抗体购自美国Cell signaling Technlongy公司。
1.2 细胞培养
TW03、C666-2、CNE2、NP69细胞均培养于含10% FBS的DMEM培养基中,HEK 293T细胞培养于10% FBS的RPMI 1640培养基中,细胞复苏后置于37 ℃、5%CO2恒温恒湿的细胞培养箱中,培养至细胞密度达80%时进行细胞传代,取对数生长期的细胞进行细胞转染。
1.3 细胞转染与分组
将CNE2细胞分为si-NC组、si-TTN-AS1组、si-TTN-AS1+miR-139-5p inhibitor组、si-TTN-AS1+PDK1组,使用Lipofectamine 2000试剂盒,si-NC组和si-TTN-AS1组分别转染TTN-AS1 siRNA Negative Control和TTN-AS1 siRNA,si-TTN-AS1+miR-139-5p inhibitor组共转染TTN-AS1 siRNA和miR-139-5p inhibitor,si-TTN-AS1+PDK1组共转染TTN-AS1 siRNA和PDK1质粒,转染完成后继续培养24 h,进行后续研究。
1.4 qRT-PCR
根据TRIzol试剂盒提取细胞总RNA,取1 μg的总RNA使用PrimeScript RT reagent Kit将其逆转录为cDNA,所得cDNA使用Power SYBR Green试剂盒进行qRT-PCR反应,反应条件:50 ℃尿嘧啶DNA糖基化酶激活2 min;95 ℃热启动DNA聚合酶2 min;95 ℃变性15 s,60 ℃退火/延伸1 min,共40次循环。循环结束后设置95 ℃ 15 s、60 ℃ 1 min、95 ℃ 15 s进行PCR产物曲线溶解。记录各孔Ct值,使用2-ΔΔCt法以GAPDH为内参计算TTN-AS1的表达量,以U6为内参计算miR-139-5p的表达量。

表1 引物序列
1.5 双荧光素酶报告基因实验
使用StarBase数据库预测TTN-AS1与miR-139-5p的结合位点,TargetScan数据库预测miR-139-5p与PDK1的结合位点。采用Lipofectamine 2000试剂盒将TTN-AS1过表达质粒(TTN-AS1 WT)、突变质粒(TTN-AS1 MUT),PDK1过表达质粒(PDK1 WT)和PDK1突变质粒(PDK1 MUT)转染至HEK 293T细胞,然后将miR-NC和miR-139-5p mimic转染至上述细胞,转染24 h后,使用双荧光素酶报告基因检测试剂盒检测各组细胞荧光酶活性。
1.6 CCK-8检测细胞增殖情况
各组细胞按照每孔接种2×103/100 μL的密度平行接种于4块96孔板,置于细胞培养箱中,在接种0 h、24 h、48 h、72 h时,每孔加入10 μL的CCK-8溶液,细胞培养箱中孵育4 h后,在酶标仪 450 nm波长处检测各孔吸光度值(OD值)。
1.7 Transwell小室检测细胞迁移与侵袭能力
各组细胞用不含血清的培养基重悬后,接种至Transwell小室或铺有Matrigel胶的小室中,稀释CNE2细胞至1×105/mL,每个小室中接种100 μL,小室置于24孔板中,每孔加入含10%FBS的DMEM培养基,培养箱中孵育48 h后取出小室,底部用无水甲醛固定后用结晶紫染色10 min,清洗,晾干后于显微镜下观察并拍照,统计各组细胞迁移和侵袭数。
1.8 流式细胞术检测细胞凋亡情况
各组细胞用预冷的PBS洗涤2次,收集1×105个细胞并用100 μL 1×结合缓冲液重悬。每管加入5 μL FITC-Annexin V和5 μL PI工作液。另准备两支新的流式管,每管加入5 μL FITC-Annexin V或PI,用于流式单染的补偿调节,室温避光孵育15 min,每管加入400 μL PBS,通过流式细胞仪检测细胞凋亡情况。
1.9 Western blot检测相关蛋白表达
使用RIPA蛋白裂解液试剂盒提取各组细胞总蛋白,使用BCA蛋白定量试剂盒定量后,将Loading buffer与蛋白样品1∶1混合,沸水浴5 min后,取10 μg蛋白样品进行SDS聚丙烯酰胺凝胶电泳,80 V 30 min,120 V恒压分离60 min,随后250 mA恒流转膜90 min,将蛋白转移至PVDF膜,经过封闭后与PDK1、p-AKT、AKT、Caspase-3、GAPDH一抗4 ℃共孵育过夜,清洗后与山羊抗兔二抗共孵育90 min,清洗后使用ECL试剂盒进行曝光并拍照,使用Image J软件进行定量分析。
1.10 统计学分析
2 结果
2.1 TTN-AS1在鼻咽癌细胞中高表达
qRT-PCR检测结果显示,鼻咽癌细胞系TW03、C666-2、CNE2中TTN-AS1表达显著高于鼻咽上皮细胞系NP69(P<0.05),CNE2细胞中TTN-AS1表达最高(图1a),因此选择CNE2细胞转染si-RNA进行后续研究。相比于si-NC组,si-CCN-AS1组CNE2细胞中TTN-AS1表达显著下调(P<0.05),见图1b。
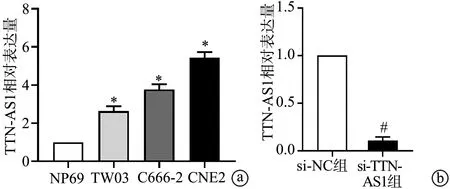
a:qRT-PCR检测TTN-AS1在TW03、C666-2、CNE2、NP69细胞中的表达;b:qRT-PCR检测si-NC组和si-TTN-AS1组CNE2细胞中TTN-AS1的表达 *:与NP69比较,P<0.05;#:与si-NC组比较,P<0.05图1 qRT-PCR检测TTN-AS1在各鼻咽癌细胞以及转染后CNE2细胞中的表达
2.2 TTN-AS1靶向调控miR-139-5p
StarBase数据库预测TTN-AS1与miR-139-5p的结合位点如图2a所示;双荧光素酶报告基因检测结果显示,HEK 293T细胞转染TTN-AS1 WT和miR-139-5p mimic后其相对荧光强度显著低于转染TTN-AS1 WT和miR-NC的细胞(P<0.001),而共转染TTN-AS1 MUT和miR-139-5p mimic的HEK 293T细胞与共转染TTN-AS1 MUT和miR-NC的HEK 293T细胞比较,细胞的相对荧光强度无显著变化(P>0.05),见图2b;qRT-PCR检测结果显示,si-TTN-AS1组CNE2细胞中miR-139-5p mRNA表达显著高于si-NC组(P<0.001),见图2c;说明TTN-AS1可调控miR-139-5p的表达。
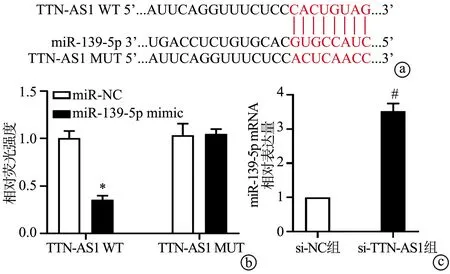
a:StarBase数据库预测TTN-AS1和miR-139-5p的结合位点;b:双荧光素酶报告基因实验验证TTN-AS1和miR-139-5p的靶向关系;c:qRT-PCR检测各组细胞miR-139-5p mRNA表达 *:与转染miR-NC比较,P<0.001;#:与si-NC组比较,P<0.001图2 TTN-AS1靶向调控miR-139-5p
2.3 miR-139-5p靶向调控PDK1
TargetScan数据库预测miR-139-5p与PDK1结合位点如图3a所示;双荧光素酶报告基因检测结果显示,CNE2细胞转染PDK1 WT和miR-139-5p mimic后其相对荧光强度显著低于转染PDK1 WT和miR-NC的细胞(P<0.001),而CNE2细胞共转染PDK1 MUT和miR-139-5p mimic与共转染PDK1 MUT和miR-NC比较,细胞的相对荧光强度无显著变化(P>0.05),见图3b;Western blot检测结果显示,miR-139-5p mimic组CNE2细胞中PDK1蛋白表达显著低于miR-NC组(P<0.001),见图3c,说明miR-139-5p可调控PDK1蛋白的表达。
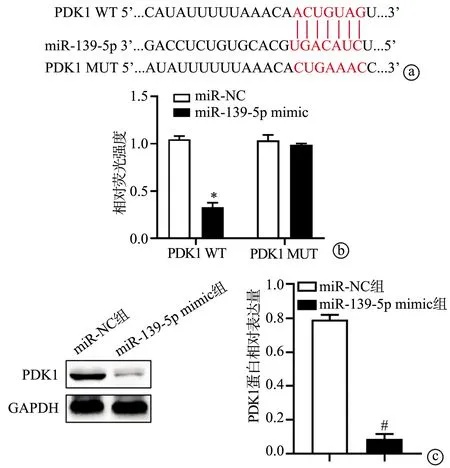
a:TargetScan数据库预测miR-139-5p和PDK1的结合位点;b:双荧光素酶报告基因实验验证miR-139-5p和PDK1的靶向关系;c:Western blot检测细胞PDK1蛋白表达 *:与转染miR-NC比较,P<0.001;#:与miR-NC组比较,P<0.001图3 miR-139-5p靶向调控PDK1
2.4 TTN-AS1调控miR-139-5p/PDK1影响鼻咽癌细胞的增殖、凋亡和迁移能力
CCK-8检测结果显示,相比于si-NC组,si-TTN-AS1组CNE2细胞增殖能力显著降低(P<0.05),si-TTN-AS1+miR-139-5p inhibitor组和si-TTN-AS1+PDK1组CNE2细胞增殖能力均显著高于si-TTN-AS1组(P<0.05),见图4。细胞迁移和侵袭检测结果显示,si-TTN-AS1组CNE2细胞迁移和侵袭数显著少于si-NC组(P<0.05),si-TTN-AS1+miR-139-5p inhibitor组和si-TTN-AS1+PDK1组细胞迁移和侵袭数均显著多于si-TTN-AS1组(P<0.05),见图5。流式细胞术检测结果显示,si-TTN-AS1组CNE2细胞凋亡水平显著高于si-NC组(P<0.05),si-TTN-AS1+miR-139-5p inhibitor组和si-TTN-AS1+PDK1组细胞凋亡水平均显著低于si-TTN-AS1组(P<0.05),见图6。
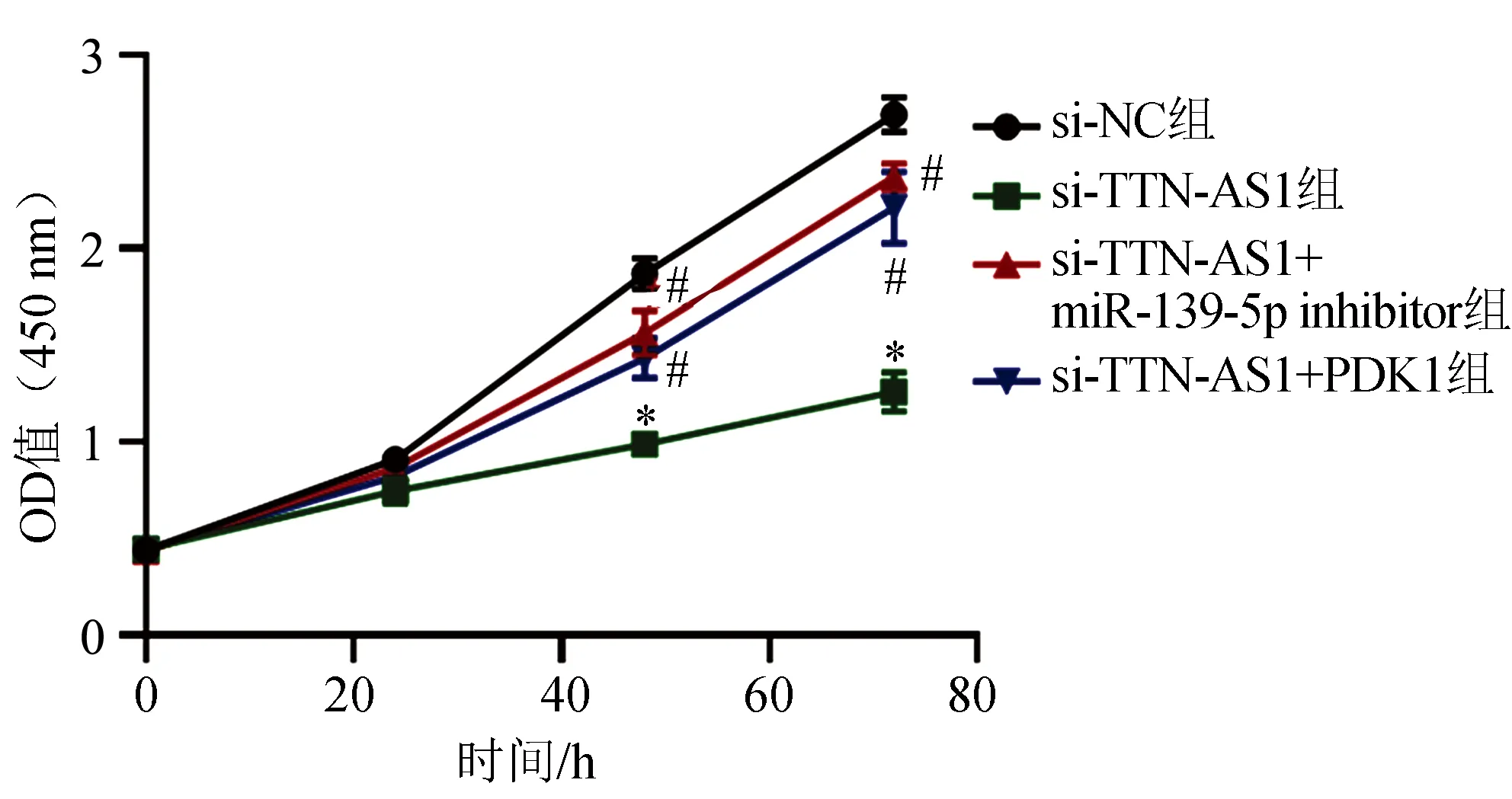
*:与si-NC组比较,P<0.05;#:与si-TTN-AS1组比较,P<0.05图4 CCK-8检测各组细胞增殖能力
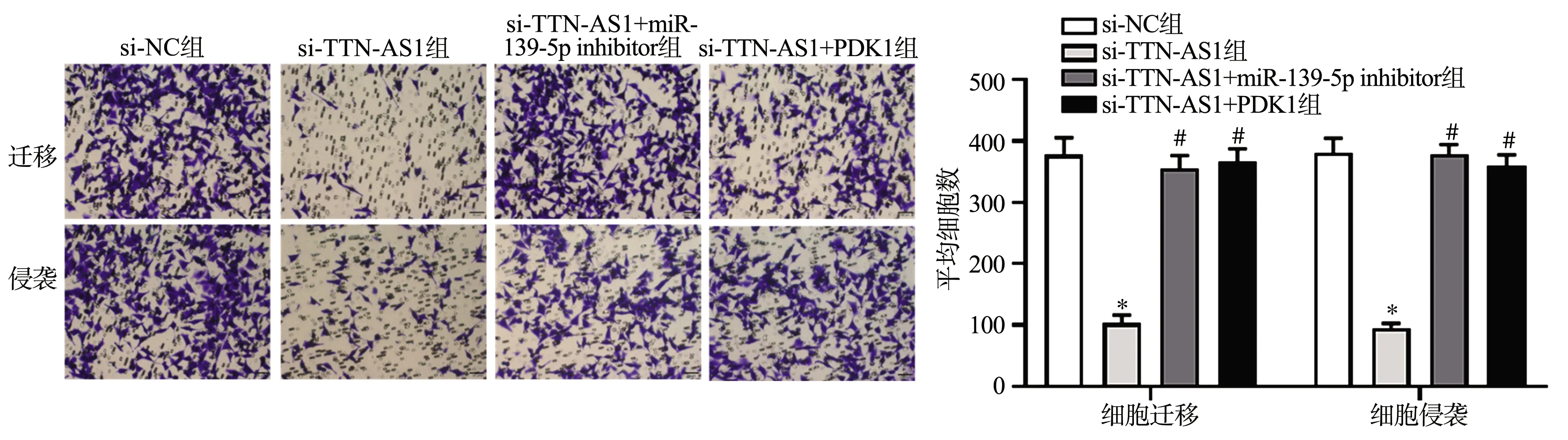
*:与si-NC组比较,P<0.05;#:与si-TTN-AS1组比较,P<0.05图5 Transwell小室检测各组细胞迁移和侵袭能力
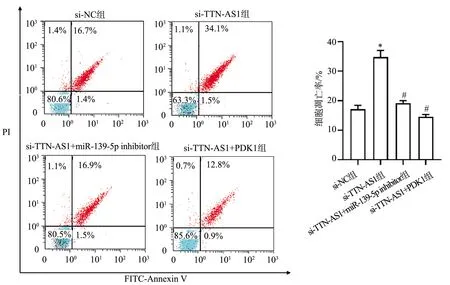
*:与si-NC组比较,P<0.05;#:与si-TTN-AS1组比较,P<0.05图6 流式细胞术检测各组凋亡细胞
2.5 TTN-AS1调控miR-139-5p/PDK1/AKT/Caspase-3信号通路
Western blot检测结果显示,相比于si-NC组,si-TTN-AS1组CNE2细胞中PDK1蛋白表达显著下调(P<0.001),Caspase-3蛋白表达显著上调(P<0.001),p-AKT水平显著下调(P<0.001);相比于si-TTN-AS1组,si-TTN-AS1+miR-139-5p inhibitor组和si-TTN-AS1+PDK1组CNE2细胞中PDK1蛋白表达显著上调(P<0.001),Caspase-3蛋白表达显著下调(P<0.001),p-AKT水平显著上调(P<0.001),说明TTN-AS1调控miR-139-5p/PDK1/AKT/Caspase-3信号通路(图7)。
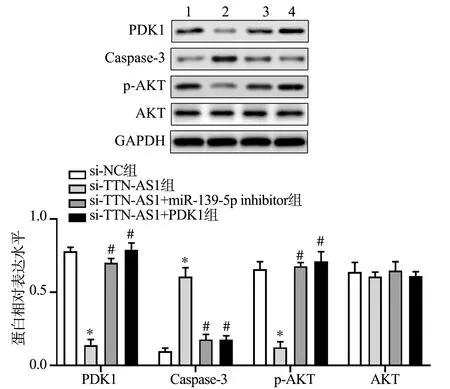
1:si-NC组;2:si-TTN-AS1组;3:si-TTN-AS1+miR-139-5p inhibitor组;4:si-TTN-AS1+PDK1组 *:与si-NC组比较,P<0.001;#:与si-TTN-AS1组比较,P<0.001图7 TTN-AS1调控miR-139-5p/PDK1/AKT/Caspase-3信号通路
3 讨论
鼻咽癌是一种常见的耳鼻喉恶性肿瘤,发病部位多为鼻咽腔顶部和侧壁,目前鼻咽癌的治疗方式主要为放疗和化疗,但是治疗效果并不理想,仍存在肿瘤转移、复发及预后较差等问题,因此需要探究更多鼻咽癌诊断和治疗的新靶点[10-11]。LncRNA是一类长度超过200 nt的非编码RNA,可在转录前、转录后以及蛋白翻译等过程中调控病理生理进程[12]。有研究发现,多种lncRNA的异常表达可促进肿瘤生长、转移及血管新生、免疫逃逸、化疗耐药等[13];亦有研究指出,lncRNA具有肿瘤临床诊断和治疗的潜力[14]。鼻咽癌的发生发展受多种lncRNA的调控,如lncRNA PVT1可通过激活KAT2A乙酰转移酶和稳定HIF-1α促进鼻咽癌细胞的增殖[15];Liu等[16]研究表明,lncRNA SNHG5通过调控miR-1179/HMGB3信号通路促进鼻咽癌的发展;Wang等[17]研究表明,下调lncRNA SNHG7可抑制ROCK1的表达,进而抑制鼻咽癌细胞的增殖和侵袭能力;而Hu等[18]的研究表明,lncRNA SNHG7通过调控miR-514a-5p/ELAVL1轴促进鼻咽癌细胞的增殖。
TTN-AS1是一种促癌基因,位于2号染色体,长度1 077 bp,可通过海绵吸附的方式调控多种miRNA[19],从而影响肿瘤的发生发展,如TTN-AS1可以作用于miR-376a-3p促进大肠癌的进展[20];TTN-AS1可通过作为miR-376b-3p的竞争性内源RNA促进胃癌进展[21];TTN-AS1调控miR-134-5p/PAK3信号通路影响P21信号通路和AKT/GSK-3β/β-catenin信号通路,进而调控人大肠癌细胞的放疗敏感性[22]。本研究结果显示,TTN-AS1在鼻咽癌细胞系中的表达显著高于其在鼻咽上皮细胞系中的表达,鼻咽癌细胞CNE2中转染TTN-AS1 siRNA抑制TTN-AS1表达后,CNE2细胞的增殖、迁移和侵袭能力均显著降低,细胞凋亡能力显著增加,说明抑制TTN-AS1表达可抑制鼻咽癌的进展。
LncRNA发挥调控作用的重要机制是作为内源性RNA与miRNA结合,降低组织及细胞中靶miRNA丰度,减弱miRNA对mRNA结合作用及抑制mRNA翻译,从而提高miRNA靶蛋白表达水平[23],如TTN-AS1靶向抑制乳腺癌细胞中miR-140-5p表达[24];TTN-AS1也可抑制miR-1271表达从而影响前列腺癌细胞的增殖和转移[25]。本研究通过数据库预测以及双荧光素酶报告基因实验验证发现,TTN-AS1可靶向miR-139-5p,miR-139-5p可靶向结合于PDK1 mRNA的3’UTR区,TTN-AS1可调控miR-139-5p/PDK1信号通路,且si-TTN-AS1+miR-139-5p inhibitor组和si-TTN-AS1+PDK1组细胞的增殖、迁移及侵袭能力均显著高于si-TTN-AS1组,细胞凋亡水平显著低于si-TTN-AS1组,说明TTN-AS1可调控miR-139-5p/PDK1信号通路从而影响鼻咽癌细胞的生长和转移。
AKT信号通路是调控肿瘤生长和转移的经典信号通路,该通路的激活可抑制肿瘤细胞的凋亡,促进肿瘤细胞的增殖;PDK1是AKT上游的激活剂,可促进AKT的苏氨酸308位点的磷酸化,进而激活AKT[26]。有研究表明,microRNA-503可通过靶向PDK1/AKT信号通路抑制非小细胞肺癌进展[27],提高PDK1表达可激活PI3K/AKT/mTOR信号传导,进而促进肝细胞癌的抗辐射和去分化表型[28]。本研究结果显示,TTN-AS1可通过抑制miR-139-5p促进PDK1表达进而激活AKT信号通路。Caspase-3是肿瘤中的促凋亡基因,AKT/Caspase-3信号通路可调控多种细胞凋亡,如抑制PI3K/AKT/Caspase-3信号通路可抑制高糖诱导的人髓核细胞凋亡[29]。本研究结果显示,抑制TTN-AS1后Caspase-3表达上调,抑制TTN-AS1并同时抑制miR-139-5p或上调PDK1表达均可使Caspase-3表达下调,说明TTN-AS1可通过miR-139-5p/PDK1信号通路调控鼻咽癌细胞的凋亡。
综上所述,本课题组认为抑制TTN-AS1可通过调控miR-139-5p/PDK1/AKT/Caspase-3信号通路抑制鼻咽癌细胞的生长和转移。