原发性帕金森病患者非运动症状的临床特点
钟真真 申 佩 高云春
常德市第一人民医院,湖南 常德 415000
帕金森病(Parkinson’s disease,PD)是继阿尔茨海默病之后第二常见的神经退行性疾病,主要表现为静止性震颤、运动迟缓、姿势步态异常和肌强直等,运动症状在PD 最为常见,贯穿疾病的早期至晚期[1]。近年来,PD 患者的非运动症状(non-motor symptoms,NMS),如情绪改变、认知障碍、失眠、自主神经功能障碍和疼痛等也备受关注[2],其中一些症状,如嗅觉减退、抑郁、快速眼动睡眠障碍(rapid eye movement sleep disorder,RBD)和便秘,可能比运动症状早几年发生[3-4]。NMS不仅出现在疾病的早、晚期,甚至比运动症状发生更早,增加了帕金森病早期诊断的困难,常易导致漏诊和误诊。因此,须加强对PD 患者非运动症状的分析研究。本研究对常德市第一人民医院收治的71 例PD 患者非运动症状进行分析,总结其临床特点。
1 资料和方法
1.1 研究对象连续纳入2020-01—2021-12 在常德市第一人民医院神经内科门诊和病房住院的PD患者71例。纳入标准:根据《中国帕金森病的诊断标准(2016 版)》诊断标准,①缓慢起病,具有静止性震颤、肌强直和运动迟缓3 项症状中至少2 项;②左旋多巴治疗有效。排除标准:①脑血管病、脑外伤和脑炎等原因所致的帕金森病综合征或帕金森病叠加综合征;②伴有严重痴呆、言语表达障碍影响情感表达和其他精神疾病;③特发性震颤;④患严重恶性肿瘤或其他系统疾病。
1.2 Hoehn-Yahr分期根据PD统一评定量表第五部分Hoehn-Yahr(H-Y)[5]分期:1 期:单侧病变;1.5期:单侧和躯干受累;2 期:双侧病变,无平衡功能障碍;2.5期:轻微双侧病变,后拉实验可恢复;3期:轻-中度双侧病变,某种姿势不稳,可独立生活;4 期:严重残疾,但可独立行走和站立;5期:无帮助时只能坐轮椅或卧床。本研究中PD组1期10例,1.5期14例,2期16例,2.5期15例,3期12例,4期4例。
1.3 非运动症状评价量表(NMSS)根据患者最近1 个月以来对自身情况的严重程度和发作频率进行评估,包含9个方面:心血管系统、睡眠与疲劳、情绪与认知、知觉与幻觉、注意力与记忆力、胃肠道系统、泌尿系统、性功能及混合症状。
1.4 统一帕金森病评定量表(UPDRS)由4个部分组成:精神行为和情绪、日常活动、运动检查、治疗的并发症。精神行为和情绪4项,0~16分;日常活动13项,0~52 分;运动检查27 项,0~108 分;治疗的并发症11项,0~23分。量表测评均在清晨服药后“开”期进行。
1.5 统计学分析数据采用SPSS 21.0 软件进行统计学分析。正态分布的计量资料用均数±标准差(±s)表示,2 组间比较采用t 检验,符合正态分布的2 组数据相关性行Pearson 相关和逐步线性回归分析,非正态分布的2 组数据相关性行Spearman 相关分析。以P<0.05为差异有统计学意义。
2 结果
2.1 原发性帕金森病患者的一般资料共71 例PD患者,年龄(64.53±10.72)岁,其中女34 例,频繁暴露于杀虫剂11 例,职业性溶剂暴露1 例,体重指数(BMI)(23.64±3.10)kg/m2,UPDRS评分(41.37±22.62)分,NMSS总分(30.24±26.30)分,糖尿病7例,高脂血症13例,心脏疾病9例,吸烟(至少1包/d)13例,饮酒16例,喝咖啡(≥3杯/周)2例,喝茶(≥6杯/周)13例;文盲2例,小学及小学以下40例,中学/中专13例,大专及大专以上2例。
2.2 不同H-Y 分期非运动性症状的情况根据患者H-Y 分期,分为1~2 期组(n=40)和2.5~4 期组(n=31),2 组非运动症状临床特点比较,2.5~4 期组NMSS 总分、心血管系统、睡眠与疲劳、胃肠道系统、泌尿系统均高于1~2期组,差异有统计学意义(P<0.01)。见表1。
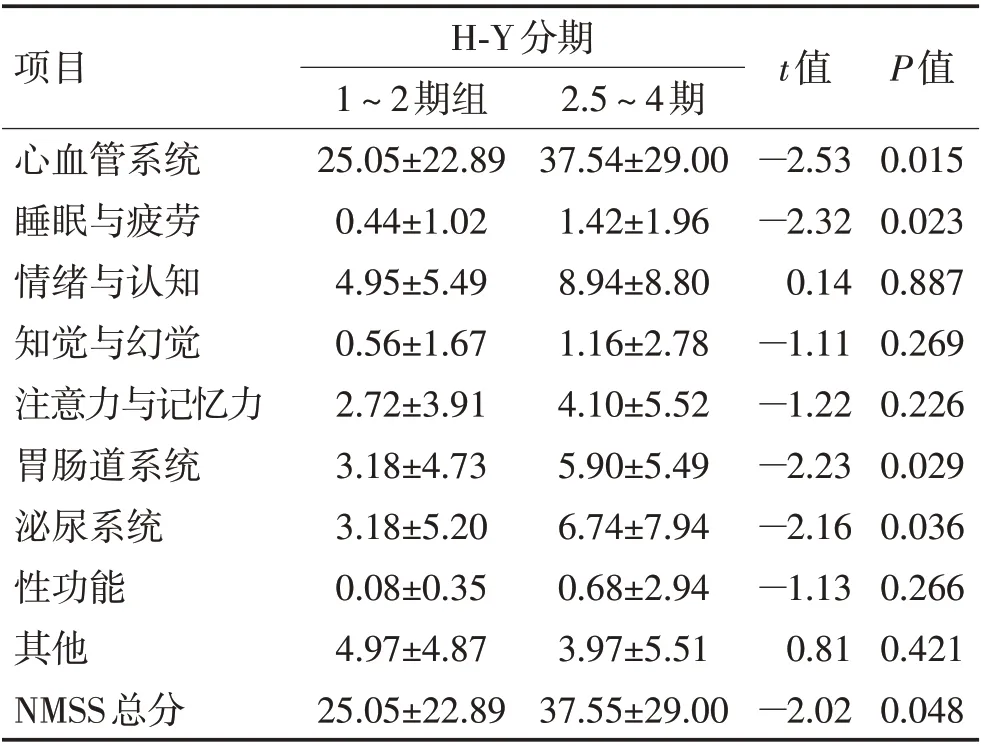
表1 不同H-Y分期非运动性症状情况比较Table 1 Condition non-motor symptoms by Hoehn-Yahr stage
2.3 UPDRS 评分和NMSS 总分的相关性分析Spearman 相关分析显示,UPDRS 评分和NMSS 总分呈正相关(r=0.6,P<0.01)。见图1。
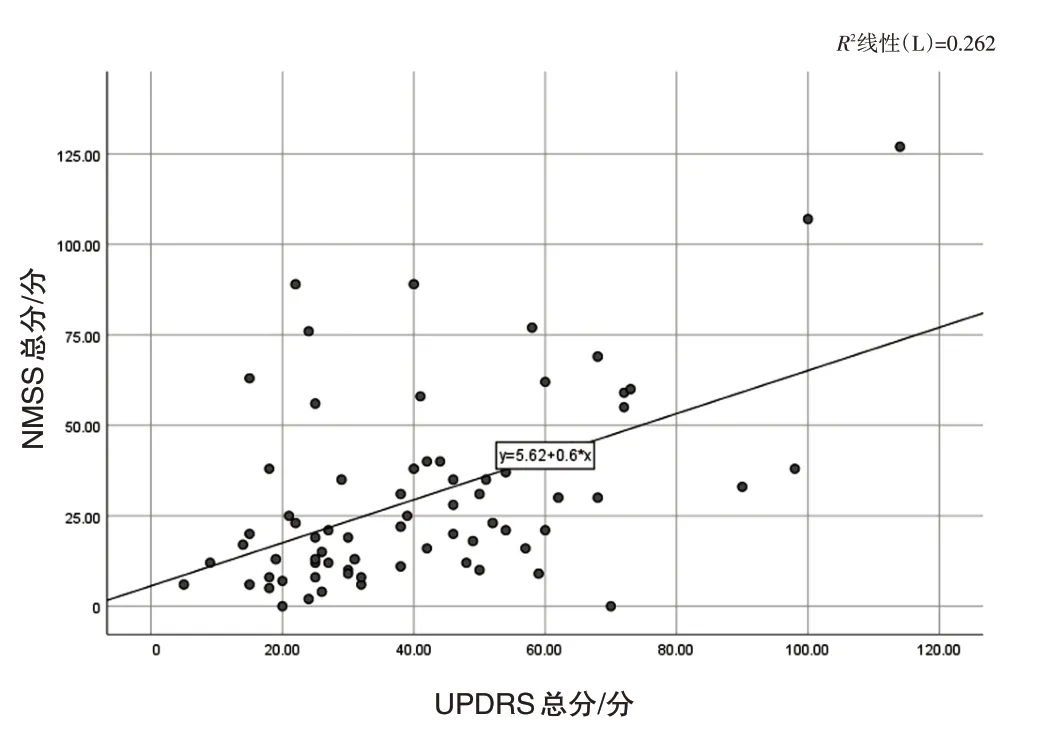
图1 UPDRS评分和NMSS总分的相关性Figure 1 Correlation between UPDRS score and NMSS total score
2.4 影响NMSS 总分多元线性回归分析以NMSS总分作为因变量,UPDRS 评分、性别、高血压、糖尿病、高脂血症、心脏疾病、吸烟(至少1包/d)、饮酒、喝咖啡(≥3杯/周)、频繁暴露于杀虫剂、职业性溶剂暴露、BMI、受教育程度、年龄为自变量,进行多元线性回归分析,结果显示,UPDRS评分是影响NMSS总分的相关因素。见表2。

表2 NMSS相关因素的多元线性回归分析Table 2 Multiple linear regression analysis of factors associated with NMSS
3 讨论
临床上诊断PD 主要通过运动性症状及对左旋多巴的治疗效果来判断。既往一直关注于PD 的运动症状及并发症。近年来,NMS的重要性及对PD患者生活的影响逐渐受到重视,因其可导致严重的残疾和降低与健康相关的生活质量。NMS可能是由于神经元性变性导致神经系统的改变或药物的治疗所致,主要涉及的神经系统为去甲肾上腺素核、嗅觉系统、非运动纹状体区、中缝血清素核[6]。
NMSS是一项综合评估,涵盖了与帕金森病相关的许多非运动症状,共30种非运动症状,分为9个领域[7]。本研究中71例PD患者,分期越高,NMSS总分越高,即非运动症状临床症状越重,尤其在心血管系统、睡眠与疲劳、胃肠道系统、泌尿系统尤为突出。UPDRS 量表作为帕金森病监测疾病进展、评估治疗效果的综合评估工具。OU 等[8]通过调整性别、入组年龄、发病年龄、疾病持续时间后发现,NMS 的数量随着UPDRS 评分的增加而增加。本研究表明,UPDRS 评分与NMSS 总分呈正相关,并且是影响NMSS总分的相关因素,帕金森疾病的进展和疗效直接影响患者的非运动症状。
睡眠障碍包括夜间睡眠中断和白天过度嗜睡、不宁腿综合征、快速眼动睡眠行为障碍、睡眠呼吸暂停、梦游和梦话、噩梦、睡惊和惊恐发作[9]。PD 患者常报告失眠,无论疾病的严重程度如何,患病率为37%~83%[10]。多种因素导致PD患者睡眠障碍。下丘脑多巴胺是调节睡眠-觉醒周期的关键区域,该区域功能障碍可能是其中一个因素。PD 早期外周时钟基因表达的改变可能导致血清褪黑激素和皮质醇等激素水平的变化,从而导致患者的睡眠节律紊乱和睡眠效率降低[11]。多巴胺通过增加睡眠时间和缓解夜间运动障碍来改善睡眠障碍。本研究中PD 患者睡眠障碍表现突出,与既往研究结论相似。
PD患者胃肠功能症状主要表现为便秘、吞咽障碍和流涎。大部分患者在疾病确诊前会有便秘,但通常被患者及家属甚至是医生忽视,且该症状持续时间长。便秘在PD 人群中的发生率为27.10%~70.39%[12]。排便次数减少和大便性状改变成为患者就诊的主要原因[13]。外周、中枢神经系统障碍引起的结肠蠕动缓慢和肛门括约肌障碍所致的肌紧张是导致便秘的主要原因[14]。PD 患者胆碱能神经的亢进可引起唾液分泌的增加,口角活动迟缓,进食时吞咽缓慢导致口腔中唾液聚积外溢,同时部分患者嘴唇闭合不严,加重流涎[15]。
泌尿系统功能障碍是PD患者另一非运动症状,主要表现为患者尿频尿急、夜尿增多以及尿失禁等,多在PD晚期出现。关于PD患者泌尿系统病理生理机制尚不清楚,但可能与多巴胺机制有关。45%~93%的PD患者中膀胱容量减少和逼尿肌过度活动是由于纹状体和皮质下及皮质区退行性变有关[16],与较高的H-Y 分期相关[17],左旋多巴药物或深部脑刺激可缓解上述症状[18]。
心血管调节障碍主要包括体位性低血压(orthostatic hypotension,OH)和心律失常。OH 在PD中很常见,患病率9.6%~64.9%。OH 可能会导致无法解释的跌倒、晕厥、头晕、认知障碍、呼吸困难、疲劳、视力模糊、肩部、颈部或站立时的腰痛[19-26]。心脏交感神经去神经支配和去甲肾上腺素能通路激活的减少是导致PD 患者OH 的主要病理机制[27-35],但另一项研究认为OH 与多巴胺神经的缺失有关。对于需要升压药来控制OH症状的患者,盐酸米多君可改善上述症状[36]。
UPDRS 量表是目前国际上普遍作为PD 患者的评定量表[37-43],以患者的临床症状与体征为依据,用于评估PD 病情严重程度。本研究中UPDRS 评分是影响NMSS总分的相关因素,即证明运动症状和非运动症状是相互影响的,患者的运动症状越重时,非运动症状也越重。
本研究样本量偏小,结果需要在一定范围内进行解释,并存在一些局限性。PD患者非运动症状普遍存在,提示临床医生重视非运动症状,及早发现,恰当治疗,有效延缓疾病进展,提高患者生存质量,为制定相应的治疗方案提供有效的指导依据。

