心房颤动冷冻球囊和射频消融术后肺静脉传导恢复的电生理特点
黄俊 李宜富 丁立刚,2 王靖,2 廖志勇 李腾 阮焕钧 李华龙 姚焰,2
肺静脉及前庭对心房颤动(简称房颤)的触发与维持都起着十分重要的作用,肺静脉电隔离(PVI)是房颤导管消融术的基石[1]。射频导管消融和冷冻球囊导管消融是目前最常用于PVI的两种技术,但无论采用哪种技术进行肺静脉的电隔离,随访期间均可能出现一定比例的复发,而肺静脉传导恢复是房颤复发的主要原因[2-3]。既往有部分研究报道了房颤射频消融术后,肺静脉恢复的特点[4],近几年来也有研究发现房颤冷冻球囊导管消融术后存在一些易恢复传导的部位[5],但比较这两种技术在肺静脉传导恢复的各自特点方面的研究较少。笔者通过比较射频消融与冷冻球囊消融术后复发患者二次手术中肺静脉电位传导恢复的特点不同,来指导导管消融的优化,为房颤导管消融复发再次消融提供指导依据。
1 资料与方法
1.1 一般资料 研究对象为2017 年9 月至2019年9月间在本院行导管消融的房颤患者共478例,其中射频导管消融300例,冷冻球囊导管消融178例,所有患者经食管超声排除左房血栓,并排除左房直径大于55 mm、严重心功能不全(NYHA 心功能分级Ⅲ级以上)、严重慢性阻塞性肺疾病的患者。术后随访过程中复发并接受二次手术的患者,按初次消融时的情况分为冷冻球囊消融组(冷冻组),射频消融组(射频组)。
1.2 术前准备 复发患者二次手术前均行食管超声排除左房血栓,若服用华法林,术前急查国际标准化比率(INR),如INR 在2~3 之间,围手术期不间断口服抗凝药。如INR 小于2,术前停用改为低分子肝素抗凝;如服用新型口服抗凝剂,围手术期不间断口服抗凝药。术前停用抗心律失常药物治疗。所有患者术前均行左房肺静脉CT 明确解剖形态。
1.3 标测与导管消融 术中穿刺股静脉,置入10极电极至冠状窦,经股静脉置入两个8.5F LA 鞘(惠泰医疗公司)并穿刺房间隔至左房,穿刺房间隔成功后,追加肝素100 u/Kg,维持活化凝血时间在300~350 s之间,术中采用CARTO 系统(美国强生公司)或EnSite系统(美国雅培公司)辅助下,Lasso或Pentaray标测导管进行左心房三维电解剖标测建模。消融导管采用Smart TouchTM或Tacti-CathTMQuartz导管,消融参数:预设温度43℃,功率45 W,盐水灌注20~25 ml/min,消融指数(AI)值左房后壁350~400,前壁400~450,损伤指数(LSI)值:左房后壁4.0~4.5,前壁4.5~5.0。
为方便分析左房-肺静脉传导恢复位置,将肺静脉口及前庭区域分为6个对等的节段(顶部、前上部、前下部、底部、后下部、后上部)。对于肺静脉口部消融的反应分为:①肺静脉电位隔离;②标测导管激动顺序变化;③无反应。如在某一阶段消融时出现前两种反应可认为该节段包含漏点。
消融终点:双肺静脉电位完全消失,肺静脉传导双向阻滞,并在30 min的观察期内未恢复。
1.4 术后处理及随访 术后常规给予3个月的口服抗凝药治疗,3个月的抗心律失常药物,术后1、3、6、12个月随访复查常规心电图及24 h 动态心电图,如有症状发作,立即复查心电图。房颤复发定义为消融3个月后,心电图或监护记录到的超过30 s的房性快速心律失常[房颤、心房扑动(简称房扑)、房性心动过速]。
1.5 统计学方法
采用SPSS19.0 软件,连续变量采用均数±标准差或中位数表示,计数资料采用例数(百分数)表示。组间比较采用独立样本的t检验,各肺静脉节段间漏点部分情况比较采用χ2检验。以P<0.05为差异有显著性。
2 结果
2.1 两组临床资料比较 术后随访过程中复发并接受二次手术的患者44例。其中冷冻组19例,射频组25例。射频组左室射血分数(LVEF)低于冷冻组、左房前后径(LAD)大于冷冻组,其他临床特征无差异,见表1。
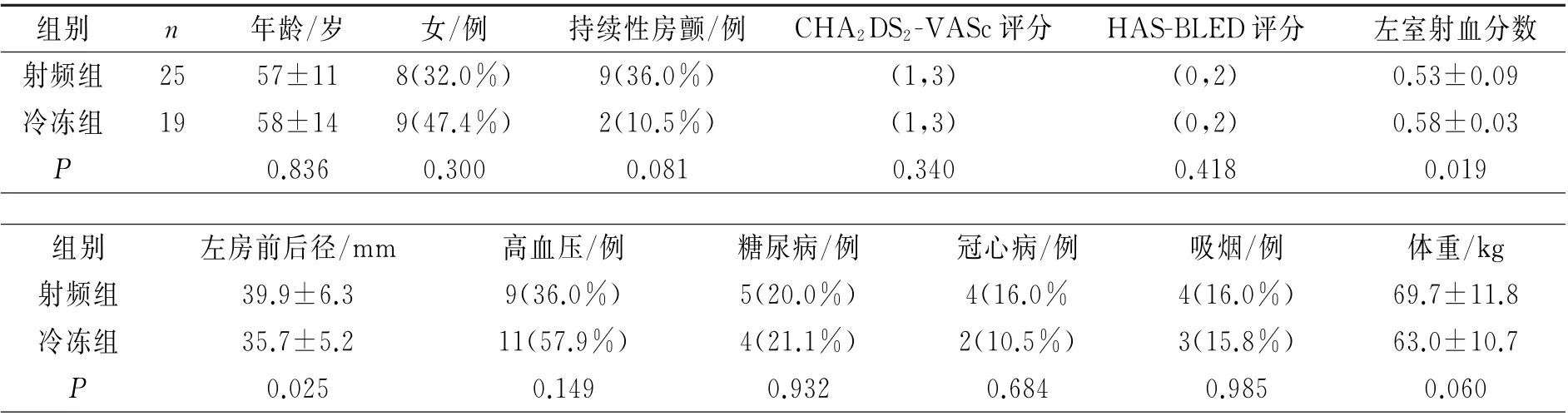
表1 两组临床资料比较
2.2 两组第二次手术时肺静脉恢复传导情况 第二次手术中射频组肺静脉电位恢复数量与冷冻组相比无明显差异,冷冻组与射频组相比左上肺静脉及右上肺静脉电位恢复要低于射频组,而右下肺静脉电位恢复的比例较高,左下肺静脉电位恢复也略高于射频组,但无统计学差异,详见表2。
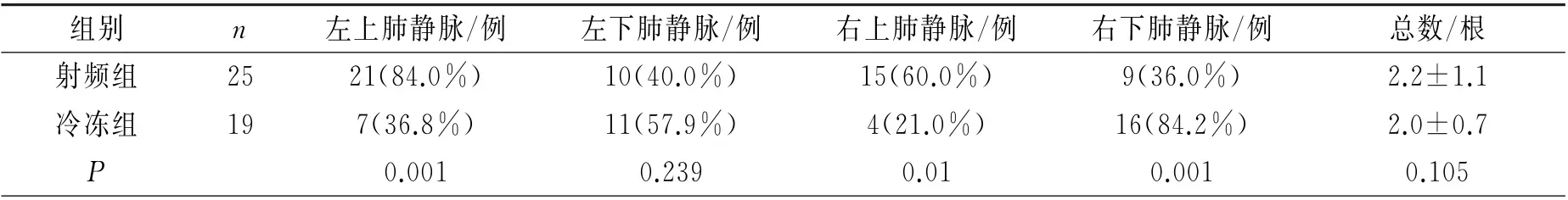
表2 第二次手术时肺静脉传导恢复情况
2.3 两组第二次手术补点消融位置 第二次消融手术中补点消融位置共159处,其中射频组95处,冷冻组64处。射频组在左上肺顶部、左上肺前壁、右上肺顶部、右上肺后壁等位置补点率明显高于冷冻组,在右下肺底部、右下肺前壁等位置补点率低于冷冻组,详见表3。以上肺静脉均于二次手术中成功补点隔离。
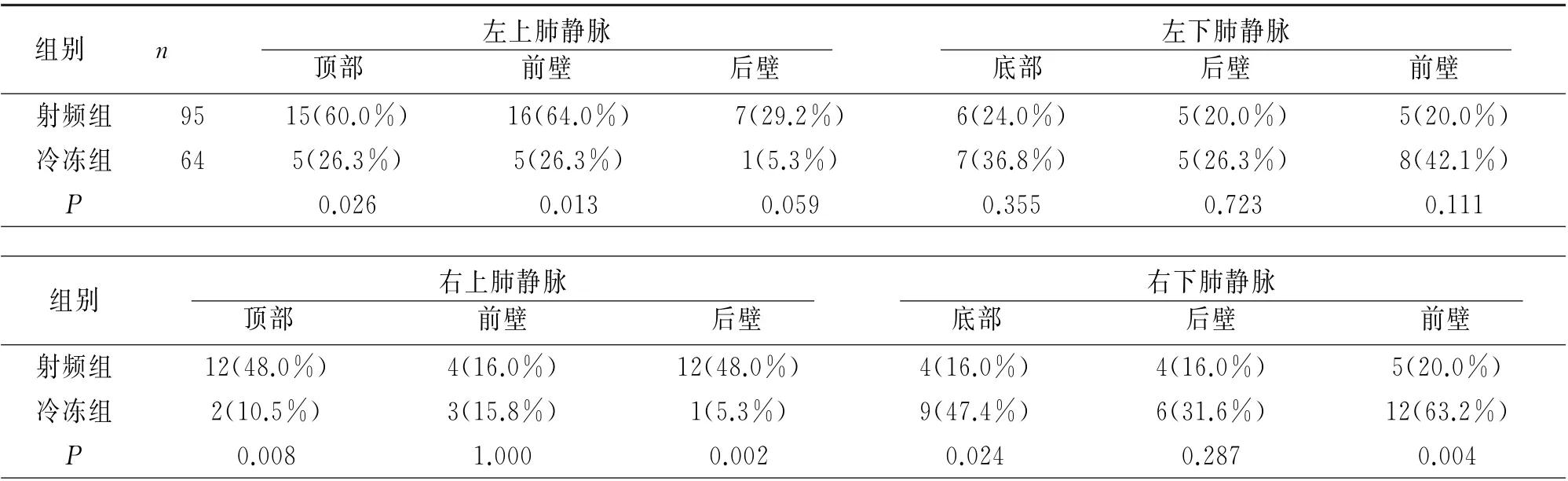
表3 两组第二次手术补点消融位置
2.4 第二次手术后随访结果 第二次消融术后随访(13.2±7.7)个月,仍有5例患者复发,其中有1例复发房扑。二次消融手术后再次复发率射频组与冷冻组无差异[12%(3/25)vs 10.5%(2/19),P>0.05]。二次手术后复发组与未复发组的LVEF、LAD相比较无差异[0.57±0.05 vs 0.56±0.05,(36.2±2.7)mm vs(37.0±4.8)mm,P均>0.05]。回顾二次手术情况5例复发患者共补点19处,其中左下肺8处、左上肺4处及右上肺2处,右下肺5处;其中复发房扑的患者行第三次手术,术中验证四根肺静脉内均无电位,激动标测证实三尖瓣环逆钟向折返的房扑,行三尖瓣峡部线消融后心动过速终止,术后随访6个月未见房颤及房扑复发。
3 讨论
房颤导管消融术后复发的主要原因可能是首次消融未能实现持久的完全肺静脉隔离,消融未能完全透壁损伤或损伤不连续导致传导恢复。射频导管主要以点对点的方式消融结合三维标测可将点连成消融线,其优点在于导管操作比较灵活多变,适应各种开口不同的肺静脉,且可以扩大消融的范围;其缺点是点对点的消融较难保证损伤的连续性及有效性。冷冻球囊导管是球形构造,主要是为更合适贴靠肺静脉开口及前庭,一次消融就可完成目标肺静脉的隔离,而且消融相对更连续,其缺点是肺静脉开口的形态及方向会存在变异,使得部分患者的肺静脉开口不能完全封堵,造成漏点。姜伟峰等[4]对232例再次行房颤射频消融的患者采用Lasso环状电极标测,明确心房-肺静脉恢复部位,提示恢复区域集中于左肺静脉前上部、前下部,右肺静脉后上部及后下部,经过多次手术可完全隔离。周公哺等[5]对冷冻消融术后复发的10例患者进行二次手术,发现其传导恢复存在一定的规律性,主要集中在双侧下肺静脉,补点消融重新隔离肺静脉是安全有效的。
本研究对比射频消融及冷冻球囊消融术后复发患者二次消融手术情况,发现在肺静脉传导恢复方面与射频组相比,冷冻组的左上肺静脉及右上肺静脉恢复显著减少,右下肺静脉恢复显著增加;在补点消融区域来说射频组在左上肺顶部、左上肺前壁、右上肺顶部、右上肺后壁等位置补点率明显高于冷冻组,射频组在右下肺底部、右下肺前壁等位置补点率低于冷冻组,提示射频消融和冷冻球囊消融术后肺静脉传导恢复部位各有不同,这与近年来的一些研究结果相似[6-7],其原因可能与心房解剖结构特点及射频导管与冷冻球囊导管构造特点不同、操作方法不同等有关。首先,射频导管消融主要以点对点方式消融,对稳定贴靠要求较高,而心房解剖特点是不规则的,射频导管有其较难稳定贴靠的区域比如左上肺与心耳交界的嵴部、上下肺静脉交界、右上肺静脉后顶部等,因此这些部位较容易恢复传导。其次,冷冻球囊消融导管主要是球形设计,操作上肺静脉较容易封堵,但处理下肺静脉需要打弯、塑形、下拉才能贴靠,特别是处理右下肺静脉有时难以达到球囊导管与肺静脉同轴,推送球囊时无法将力量传至球囊与肺静脉前庭的接触面,无法保证良好的贴靠,因此双下肺的传导恢复较常见,其肺静脉恢复特点不同于射频导管消融。从第二次手术中补点消融的区域来看,也提示射频组重点需要在上肺及顶部补点,而冷冻组主要需要在底部及下口补点,压力导管、消融指数以及冷冻球囊的设计改进能减少某些特殊位置的传导恢复[8-9],针对不同的器械的特点,提高操作技巧,在可能存在传导恢复的区域巩固消融,或采用两种技术进行杂交,相互弥补缺点保留各自的优点也能增加PVI隔离的成功率,减少复发率[10]。二次消融手术后随访中仍有5例患者复发,再次复发率射频组与冷冻组无差异,复发组与未复发组的LVEF、LAD 相比较无差异,回顾二次手术情况5例复发患者补点位置主要位于左下肺及右下肺,其中1例复发房扑,在第三次手术中验证肺静脉无电位,证实房扑发作与肺静脉触发灶无关。其余4例患者因未能进行第三次手术,其复发原因不明确,可能存在非肺静脉外触发灶的机制。

