富锂锰基正极材料研究进展
李俊潇,李天乐,孟绍良,赵久成,吴军,王文举
(1.南京理工大学能源与动力工程学院,南京 210094;2.南京瑞华新能源电池科技有限公司,南京 210037)
如今,工业持续高速发展,伴随其中的能源危机和环境污染问题已经无法再容忽视。传统燃油为动力源的汽车不但会使能源危机进一步加重,而且其排放的尾气中有大量的有害气体,这无疑会加重环境的污染,而新能源汽车的出现能够有效缓解能源危机和环境污染这两大问题。新能源汽车的核心是电池,随着锂离子电池的发展和近年来国家政策的扶持,动力锂离子电池已经成为了新能源汽车的不二之选。作为一种电能储能器件,锂离子电池无论是在新能源汽车还是非并网的新能源发电侧,都可以很好地实现电能的转移[1]。同时,锂离子电池还对移动电子器件等新兴领域的发展至关重要。
最早的商业化锂离子电池是由索尼公司在1991年推出的,当时是使用金属氧化物基正极和软碳负极。经过30多年的发展,锂离子电池的正极和负极材料已有多种选择,目前投入商业化使用的正极材料主要有锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)、钴酸锂(LiCoO2)、镍钴锰酸锂(LiNixCoyMn1-x-yO2)及镍钴铝酸锂(LiNixCoyAl1-x-yO2)。当前大规模投入使用的正极材料在实际应用中比容量都在110~200 mA·h/g之间,但已实现商业化的负极材料的比容量却很高,约是正极材料比容量的3~20倍不等,石墨负极比容量为372 mA·h/g,硅基负极比容量更是高达2 000 mA·h/g。正极材料正在成为锂离子电池性能进一步提升的瓶颈。在已知正极材料中,富锂锰基层状氧化物(xLi2MnO3·(1-x)LiMnO2)的比容量高达250 mA·h/g,被认为将是提升锂离子电池能量密度的理想选择。但富锂锰基材料也有很多缺陷,如首次不可逆容量高、循环和倍率性能差、电压衰减明显和安全性能差等,因此相关学者做了很多富锂锰基材料改性方法的研究。几种典型正极材料的电化学特征见表1。
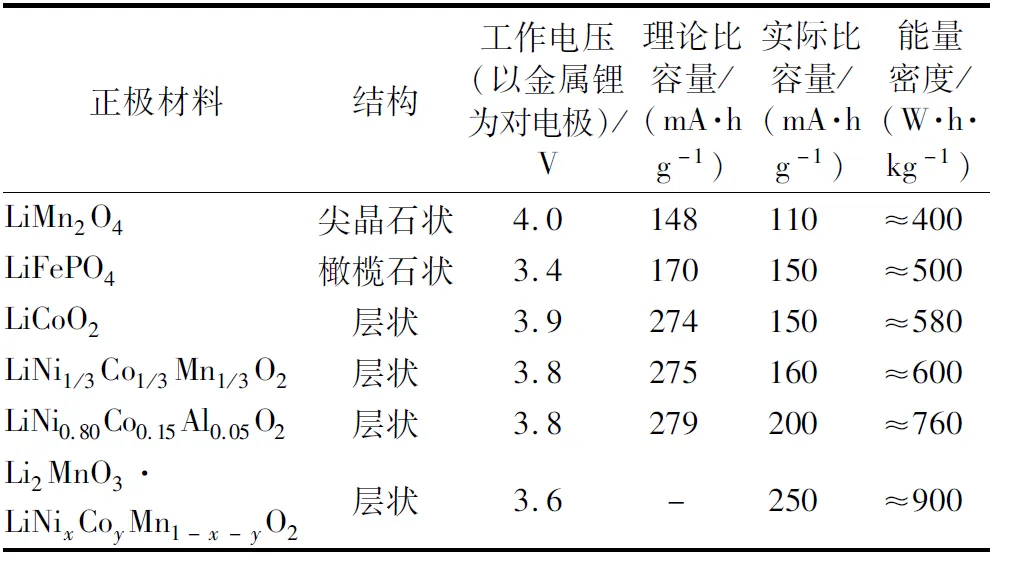
表1 几种典型正极材料的电化学特征
1 锂离子电池充放电机理
锂离子电池主要由正极材料、负极材料、电解质和隔膜这四个部分组成。其中正负极为能量的载体,这是锂离子能够在其中进行可重复的游离和结合的保障;电解质是锂离子可以在电解液中自由迁徙并降低自放电率的保障;而隔膜则是为了把电池正负极分隔开,只允许锂离子通过。锂离子电池的工作依赖于锂离子在正负极浓度的不同带来的锂离子的转移。充电时,锂离子从负极转移到正极,正极变为富锂态。充放电过程中,随着锂离子的转移,相同数量的电子同时在外电路中移动,使正负极发生氧化还原反应。可充电锂离子电池的工作原理图(以LiCoO2电池为例)[2]如图1所示。

图1 可充电锂离子电池的工作原理图
2 富锂锰基正极材料
多年来研究人员一直致力于追求更高性能的电池体系,通过当前达成的成果可以看出,电池里非活性物质的占比已经非常低了,以往我们通过降低非活性物质的量来提高电池能量密度的方法已经没有太多发挥空间了。想要提高锂离子电池的能量密度,最直接的方法就是提高正负极材料的能量密度,即使用更高能量密度的电极材料。正负极的容量适配是设计锂离子电池的首要准则。而目前商用的锂离子电池正极材料的比容量普遍偏低,因此需要更重的正极材料才能匹配相应比容量的负极(至少2 g的正极材料才能匹配1 g的石墨负极材料),碳硅负极材料需要的正极材料往往更多。所以我们要积极寻找新一代高容量正极材料来取代传统正极材料。
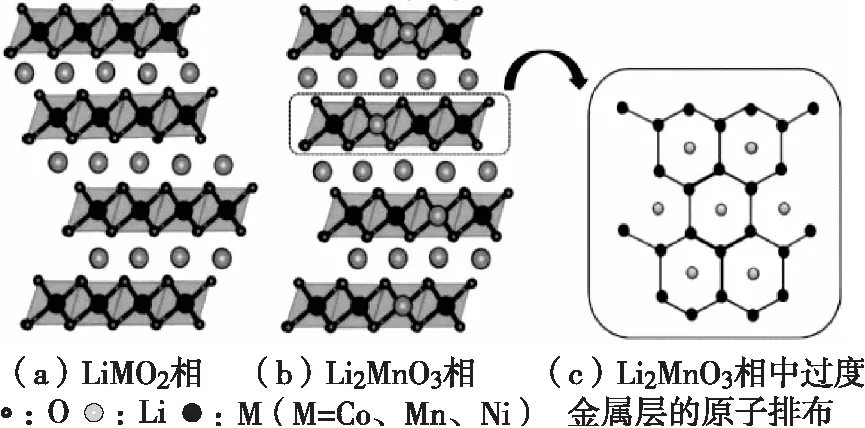
图2 富锂锰基正极材料结构示意图
富锂锰基正极材料放电比容量达250 mA·h/g以上,几乎是目前大规模投入量产使用的正极材料可用容量的两倍左右;富锂锰基以锰元素为主,贵重金属含量少,锰元素价格低,因此富锂锰基整体价格较低,富锂锰基的结构示意图如图2所示[3]。同时,相比于常见的三元钴酸锂和镍钴锰材料,这种材料兼具成本跟安全性的优势。所以,在实现下一代锂电池突破400 W·h/kg,甚至500 W·h/kg的目标途中,富锂锰基正极材料是理想的选择也是技术的关键。富锂锰基正极材料虽然有很多优点,但其也有实际应用中不容忽视的缺陷。尽管近年来国内外在其研究方面取得了重要进展,但若想实现富锂锰基正极材料的商业化,还要面临几个挑战:(1)首次充放电的可逆容量损失大和库仑效率低;(2)容量及电压衰减严重;(3)倍率性能差;(4)安全性能差。
2.1 富锂锰基正极材料的缺陷
2.1.1 首次充放电的可逆容量损失大和库仑效率低
由于富锂正极材料xLi2MnO3·(1-x)LiMO2晶体构造的特殊性,致使其充放电过程中,存在首次不可逆容量损失较大,首圈库伦效率较低的问题,图3为不同组分富锂锰基电池首次充放电曲线[4-5],和后续循环过程的充放电曲线有明显差异。在电化学反应中,富锂锰基正极材料中Li2MnO3容易被激活,晶格氧也会发生流失,从而导致其表面构造和组分的变化,进而出现一些问题。图3中呈现出两个明显的充电平台,在4.5 V前的平台出现来源于其中的Li-MO2发生锂离子脱嵌现象,Ni2+和Co3+被氧化;第二次平台出现在4.5 V附近,但该平台只在首次充电时存在。研究认为,当第一次充电电压高于4.5 V后,不活跃的Li2MnO3组分被活化并参加进反应中,晶格中的O2-通过“Li2O”的形式从Li2MnO3组分中溢出,剩下的部分则成了新组分MnO2。首次充电活化Li2MnO3相会产生含锂化合物且此过程只能单向进行,导致第一次充电损耗容量非常大,进而导致首次库伦效率过低[6]。另外,充电时正极材料也会跟电解液中的Li+相互反应,反应会形成SEI膜,特别是当电压高于4.5 V时会提高该反应的不可逆性,导致Li+损耗增多,这也是引起材料第一次充放电库伦效率降低的因素之一。
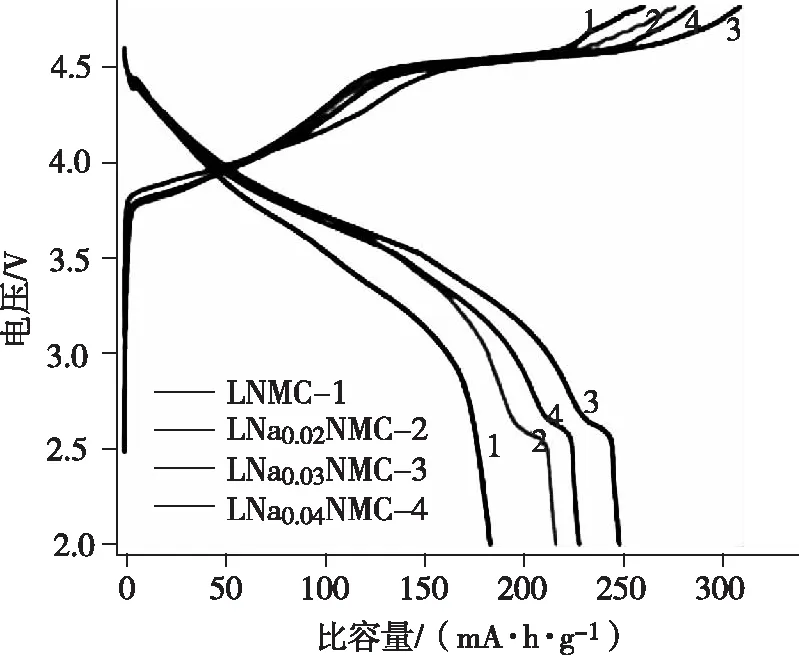
图3 不同组分富锂锰基电池首次充放电曲线
2.1.2 容量及电压衰减严重
富锂锰基正极材料最大的问题就是电压及容量衰减。电压衰减的定义是材料在经过多次充放电后活动电压有明显下降的迹象,活动电压的降低还会很大程度的缩减材料能量密度。图4是不同富锂锰基材料的比容量随循环圈数的变化情况。富锂锰基材料的电压衰减是因为其体相结构发生了变化,充电时材料会失去表面的晶格氧,材料中的过渡金属离子由于氧的配位数减少而发生迁移,晶体由层状结构变为尖晶石结构,最终又变成无序岩盐结构。晶格氧的失去导致了内部的Ni和Mn过渡金属元素向表面移动,因此材料表层呈现出缺Li、多Mn和Ni的尖晶石相重构层。另外,逃逸的氧会和电解液发生反应,随着反应次数的不断增多,晶格氧与电解液的反应越来越剧烈,从而导致尖晶石相陆续由材料表面向中部延申,由此加剧了材料电压和容量衰减问题[7]。大量实验表明以下两点是引起电压衰减的主要因素:(1)材料的自身结构的转变,
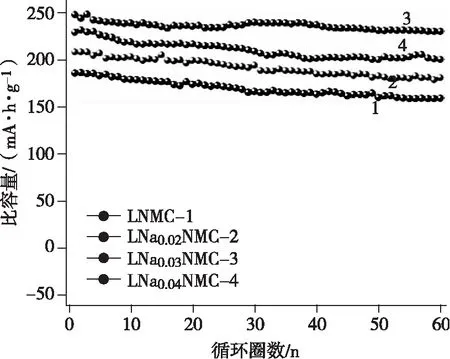
图4 富锂锰基正极材料的循环性能
由层状变为尖晶石相。(2)电极材料与电解液接触的地方发生恶化以及发生副反应,使电极表面形成SEI膜致使电极极化的增大。除此之外还存在其他的次要原因。刘彦辰等[8]还介绍了几种影响电压衰减的因素,分别是过渡金属元素对电压衰减的影响、氧气的不可逆释放对电压衰减的影响和测试条件对电压衰减的影响。
2.1.3 倍率性能差
图5是不同倍率下富锂锰基正极材料的倍率性能,从图5中可以发现倍率越高,材料的比容量越低。分析富锂锰基材料的循环过程发现,首次循环后,其中的一些材料以LiMnO2结构加入到氧化还原反应中,因此稳定性能不佳。同时材料的离子扩散能力多数偏低,因此导致倍率性能也相对较差[9]。另外,电极材料和电解液的共存,让材料表面的晶格氧更加活跃,氧的脱出一方面会使材料比容量减小,另一方面氧还会作用于电解液减少其中的可逆Li+,反应生成不可逆的化合物累积在电极表面,妨碍 Li+从电极材料表面向内部的迁移,直接导致富锂锰基正极材料的倍率性能较差。
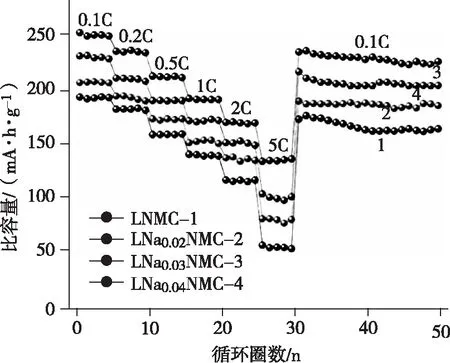
图5 不同倍率下富锂锰基正极材料的倍率性能
2.1.4安全性能差
富锂锰基材料在安全方面也存在一定的隐患,具体表现为首次充电时会有氧气的析出,氧气析出后材料会进一步与电解液发生反应,最终导致产气问题[9]。
2.2 富锂锰基正极材料的制备方法
采用不同方法合成的富锂锰基材料在微观构造、微粒直径、聚团水平以及比表面积等方面都会有所不同,材料的电化学性能也会受到影响。材料制作的工业操作难度、投资成本也会影响到富锂锰基材料的实际生产应用。因此,我们需要不断改良以寻求最佳的合成方法,目前比较主流的制备的方法有溶胶凝胶法、高温固相法和共沉淀法。
2.2.1 溶胶凝胶法
溶胶凝胶法是在溶液中将过渡金属离子充分混合,再加入络合剂使其形成溶胶,然后蒸发溶剂后得到凝胶,对凝胶进行干燥和煅烧即得到成品。溶胶凝胶法的优点是制得的材料元素充分混合、粒径分布窄、颗粒粒径小,缺点是操作流程复杂,大批量生产难度较高,难以实现工业化[10]。
2.2.2 高温固相法
高温固相法是含有不同金属元素的化合物机械混合后,在700~1 000 ℃下煅烧,最终得到产物。该方法的优点是操作简单,便于工业化生产,缺点是得到的产物围观分布不均匀,电化学性质不稳定。邱家欣[11]对传统高温固相制备工艺加以改良,分别以有机物聚乙烯吡咯烷酮(PVP)作为分散剂,以有机物乙二醇(EG)作为粒度调节剂来进行沉淀反应,同时利用水热反应辅助制出MnO2中间体,将其作为锰源制备微米或者纳米结构的富锂锰基正极材料。改良后的方法不仅与传统的高温固相法一样操作简单,而且还改善了制备材料的晶粒团聚问题,对材料形貌的控制也更为精确。
2.2.3 共沉淀法
共沉淀法是采用某种络合剂,使溶液中的过渡金属离子先与络合剂络合,再与沉淀剂反应形成沉淀。该方法需要严格的调控PH值,制得的样品具有优异的形貌结构,多为均匀大小的规则球体二次颗粒。目前工业生产中多采用此方法。李文明等[12]使用草酸盐共沉淀方法,配合后续混锂焙烧制备了锂离子电池0.5Li2MnO3·0.5LiCo0.5Mn0.5O2富锂锰基正极材料。研究材料的化学性能,可以看出在低搅拌转速条件下制作的球状颗粒样品相比于其他样品有更高的振实密度和更优异的电化学性能。
2.3 富锂锰基正极材料的改性方法
2.3.1 组分研究
富锂锰基材料的首次发现是KIM等[13]以不具有电化学活性的层状材料Li2MnO3稳定拥有活泼电化学活性的材料LiMnO2,从而构成富锂层状正极材料xLi2MnO3·(1-x)LiMnO2。将这种正极材料充电到4.5 V后,材料将被活化,其比容量将高达280 mAh/g[14]。富锂锰基正极材料的结构相当复杂,主要是由于x值的不同,为了获得满足不同需求的各种性能,通常采取改变x从而改变材料结构进而改变材料性能的办法。PECHEN等[15]利用共沉淀法合成了xLi2MnO3·(1-x)LiMn1/3Ni1/3Co1/3O2(x=0.2,0.35,0.5)材料,并比对了不同x值对材料的相结构、微观形貌、粒径分布、密度和电化学性能的影响,对电化学测试结果进行分析,当x=0.35时两相的组合能使材料呈现出最优异的电化学性能,经过110次充放电循环容量保持率高达85%。
2.3.2 掺杂
为了提升材料的首次库仑效率,我们通常对富锂锰基材料进行离子掺杂,这样做可以提高材料的循环稳定性,从而削弱循环过程中可能会出现的由于金属阳离子混排导致的材料结构问题[9]。目前主要的离子掺杂形式有:阳离子掺杂、阴离子掺杂、聚阴离子掺杂、共掺杂。忽小宇等[16]通过在前驱体和锂源的高温固相反应阶段加入五氧化二钒作为掺杂剂制备了钒掺杂的富锂锰基正极材料(LNCM)。对这两种正极材料进行表征和电化学测试,结果表明,钒掺杂后,材料的电荷转移阻抗明显降低,倍率性能也得到有效的改善。
2.3.3 表面修饰
体相掺杂虽然可以降低电荷转移阻抗和提高锂离子扩散能力,但是并不能避免材料与电解液的接触。对材料表面进行包裹可以把材料保护起来,使材料免于与电解液直接接触,从而减小材料被电解液腐蚀的风险,达到改善材料的电化学性能的效果。目前常用的包裹材料为惰性氧化物、磷酸盐、氟化物、含锂化合物及导电聚合物等。合肥国轩高科动力能源有限公司发明了一种钼掺杂氧化锌包覆富锂锰基正极材料的制备方法[17],有效的隔绝电极与电解液的接触,改善了电极材料与电解液间的导电能力及离子传输速率,从而提高了富锂锰基正极材料的容量保持率及循环性能。
3 结语
富锂锰基正极材料具有高比容量,低成本等优势,放电比容量达250 mA·h/g以上,将是未来锂电池达到400 W·h/kg,甚至500 W·h/kg的技术关键,具有非常高的应用前景。但如果不解决以下几个技术方面的关键问题,富锂锰基材料将无法在锂离子电池上实际运用:一是降低首次不可逆容量损失;二是改善倍率性能和提高循环寿命;三是削弱循环过程的电压衰减;四是提高安全性能。
目前已有多种手段来解决这些问题:改变组分结构、包覆、酸处理、掺杂、预循环、热处理等。(1)通过合理的改变富锂锰基正极材料的组分和结构可以提高电池的性能,但该研究技术目前还没有完备的理论支撑,目前我们所作的相关研究较少,得到的结果具有一定的局限性;(2)通过对富锂锰基材料进行掺杂可以显著提高锂离子电池的倍率性能,目前已有很多研究者做了用不同离子掺杂富锂锰基材料的实验;(3)通过对富锂锰基材料进行表面包覆可以在材料表面形成保护层,能改善锂离子电池的容量保持率及循环性能,目前已发现多种材料都可用于富锂锰基材料的表面修饰。但是上面这些方法都只针对单个方面提升材料的性能,还没有万全之策。期望未来我们能把多种改性办法结合起来,找到综合提升富锂锰基性能的最佳改性方案。

