纳米通道适配体传感器对马拉硫磷的检测
董晓娅,王旭锐,黄华杰,王雪安
(江苏大学农业农村部植保工程重点实验室, 江苏 镇江 212013)
农业生产活动中,农药过度使用不仅污染农业水土环境,严重影响粮食安全,而且可能造成环境污染,影响人类健康.因此,快速检测环境中农药的残留一直是全球密切关注的热点[1].作为一种高效广谱杀虫杀螨剂,有机磷农药马拉硫磷(Mal)被广泛用于水稻、小麦、棉花等作物害虫的防治.但由于Mal具有抑制神经递质的毒性,可通过皮肤或黏膜接触、吸入或误食而引起人体中毒[2],所以需要开发快速灵敏的检测方法,以更好地保障人民群众身体健康.
目前对马拉硫磷检测的方法主要有色谱法[3]、液相色谱-串联质谱法[4]、荧光方法[5]等.这些方法需要大型的专用仪器、熟练的技术人员,检测成本较高.电化学检测方法具有灵敏度高、速度快、仪器价格低廉、操作简单等特点,被广泛应用于环境、医药、食品等领域[6].目前电化学方法检测Mal的报道中,多使用制备过程复杂的纳米复合物对传感界面进行修饰[7],不便于Mal的快速检测.因此,纳米通道从快速简便、低成本进行检测的角度考虑,需要开发一种新的检测方法.
纳米通道由于其结构的尺寸效应、比表面积效应和纳米管内外的特殊物理化学性质,以及尺寸可控、易制备等特点,被广泛应用于纳米电化学[8]和生物传感[9]等领域.整流现象是纳米通道的一个重要特征,其表现为在对称的输入电势作用下,输出不对称的电流,即在工作电极、参比电极/对电极所施加的外加电场的作用下,缓冲液中的K+和Cl-等离子产生定向运动.当工作电极施加负电压,正离子(K+)通过纳米通道向工作电极移动时,受到纳米通道内静电场的吸引而快速通过,形成较大的离子电流;当工作电极施加正电压,负离子(Cl-)通过纳米通道向工作电极移动时,受到静电场的排斥而缓慢通过,形成较小的离子电流.当溶液中的带电离子通过纳米通道时,与纳米通道表面所修饰的基团发生相互作用,引起纳米通道中的电信号显著变化,从而产生离子电流整流现象(ionic current rectification, ICR)[10].基于纳米通道的整流现象,SA等[11]使用硅烷将二氢咪唑修饰到石英纳米管的纳米通道中检测环境中的Co2+离子.
文中通过在纳米通道中引入可以特异性结合目标物Mal的适配体,利用适配体与Mal结合后引起的纳米通道离子电流整理现象,构建可用于检测Mal的纳米通道适配体传感器,以实现对Mal的检测.
1 试验设计
利用纳米管的整流现象和适配体特异结合目标物的特点,设计了纳米管适配体传感器,如图1所示.首先将适配体1(Apt-1)修饰到镀有金膜的纳米管上,当适配体2(Apt-2)与Apt-1通过碱基互补配对相结合后,玻璃管纳米通道表面由于碱基数量增加而携带有更多的负电荷,从而场强发生改变.由于Mal的存在,2条Mal适配体片段与Mal形成稳定的Apt-1/Mal/Apt-2复合物结构,这使场强变化后的静电场稳定存在[12],并且Apt-1/Mal/Apt-2稳定结构中负电荷增多,增强了适配体传感器纳米通道中的静电场,从而影响检测缓冲液中的K+和Cl-等离子的定向移动,发生整流现象;进一步根据整流现象的离子电流,定量检测Mal.

图1 纳米通道适配体传感器工作示意图
2 试验部分
2.1 化学药品和材料
Mal(1.0×10-4g/mL)购自安谱科技(中国上海).寡核苷酸链适配体(Apt-1,Apt-2)(ULTRA-PAGE级)由生工生物科技有限公司(中国上海)合成和纯化,其碱基序列见表1.三(2-羧乙基)膦盐酸盐(TCEP)、三羟甲基氨基甲烷盐酸盐(Tris/HCl)、6-巯基-1-己醇(MCH)购自安谱科技(中国上海).硼硅酸盐玻璃毛细管(外径1.0 mm,内径0.58 mm;长10.0 cm)购自SUTTER有限公司.

表1 适配体序列
适配体Apt-1和适配体Apt-2分别用1.0×10-2mol/L磷酸盐缓冲溶液(PBS)配制成浓度为1.0×10-4mol/L的溶液,在-20 ℃环境中储存备用.所使用的化学试剂均为分析纯.试验使用的超纯水从MILLI-Q净水系统获取(25 ℃时电阻率大于18.2 MΩ/cm).
2.2 纳米管的制备
将硼硅酸盐玻璃毛细管放入微电极拉制仪(P-97,SUTTER公司)的拉杆中并夹紧,设置拉制参数:HEAT=309,PULL=0,VELOCITY=40,TIME=200,将硼硅酸盐玻璃毛细管的一端拉制成空心圆锥形,使其形成纳米通道.
2.3 纳米通道内镀膜
将拉制好的纳米管固定在真空镀膜仪(LEICA EM ACE600)的工作台平面上,使其空心圆锥形纳米通道正对熔融金属的喷射方向,在工作参数为100 W的RF模式下镀金120 s,使纳米通道内镀上金膜,从而为固定适配体提供条件.
2.4 Ag/AgCl电极的制作
剪取2根长15 cm的Ag丝(Φ0.3 mm),将Ag丝的一端浸入次氯酸HClO溶液中6 cm,室温下静置30 min,使银丝表面被HClO充分氧化产生AgCl,从而制成Ag/AgCl电极.
2.5 纳米管适配体传感器的构建
将-20 ℃环境下储存的适配体Apt-1解冻,用pH为7.4的PBS(1.0×10-2mol/L)将其稀释至1.0×10-6mol/L,之后与1.0×10-2mol/L TCEP溶液混合,Apt-1与TCEP的体积比为10∶1.在室温下避光反应1 h,以断开适配体Apt-1溶液中的二硫键.
使用微量移液器将镀金纳米管中注入去除二硫键后的Apt-1溶液,并确保溶液填充至纳米管尖端部分.在4 ℃条件下放置16 h,使Apt-1 5′端修饰的巯基与纳米通道内的金膜通过金硫键结合,将Apt-1固定在纳米通道内.洗去纳米通道中的残余溶液,向纳米通道内加入1.0×10-2mol/L的MCH溶液,室温下静置10 min,从而封闭纳米通道上的活性位点,最后清洗残余溶液.
2.6 离子电流信号的获取
使用缓冲液(含有5.0×10-2mol/L NaCl,1.0×10-2mol/L KCl,1.0×10-2mol/L MgCl2,5.0×10-2mol/L Tris/HCl,pH为8.0)将Mal稀释至不同浓度,分别将不同浓度的Mal溶液和浓度为1.0×10-6mol/L的 Apt-2溶液混合后,加入修饰有Apt-1的纳米通道中,在室温下孵育40 min,使Mal与适配体Apt-1及Apt-2结合.最后将纳米管中的残余溶液吸出,并用缓冲液冲洗纳米管的纳米通道.
取1根Ag/AgCl电极,将表面为AgCl的一端插入修饰有适配体Apt-1的纳米通道中,并将此纳米通道浸入检测缓冲溶液中,检测缓冲溶液为含有2.0×10-2mol/L的KCl和2.0×10-2mol/L的Tris/HCl(pH为8.0)的混合液.将Ag/AgCl电极的Ag端连接CHI电化学工作站(CHI440C,上海辰华仪器有限公司)的工作电极.取另1根Ag/AgCl电极,将表面为AgCl的一端浸入检测缓冲液中,另一端连接CHI电化学工作站的参比电极和对电极的接线上,构成检测回路.使用CHI440C电化学工作站对检测缓冲液中的离子电流信号进行检测.检测方法为线性扫描伏安法(linear sweep voltammetry),设置运行参数:扫描电势从-1.0 V到+1.0 V,扫描速率为100 mV/s,采样频率为60 kHz.使用CHI-440C软件记录电流-电压曲线(I-E曲线),并使用Origin软件进行数据处理.
2.7 实际样品的准备
取0.9 mL自来水,向其中分别加入0.1 mL浓度为1.0×10-6,2.0×10-6和5.0×10-6mol/L的Mal溶液,配制成Mal浓度分别为1.0×10-7,2.0×10-7和5.0×10-7mol/L的1 mL自来水样.采用标准加入法对样品进行检测.
2.8 实际样品的检测
分别使用本传感器和气相色谱仪对水样进行检测.使用本传感器检测步骤参照上文第2.6节.使用气相色谱仪(Shimadzu 7AG,日本)定量测定自来水样中的Mal时,设置柱头压力为103.4 kPa,进样器温度为250 ℃,进样器在不分流模式下运行 2 min(采样时间),使用氦气作为流动相.
3 结果与讨论
3.1 材料表征
纳米管纳米通道的几何尺寸影响离子电流的大小.采用扫描电子显微镜(scanning electron microscopy,SEM)表征拉制好的纳米管尖端纳米孔的几何尺寸,表征图如图2所示.从图中可以看出,所拉制好的纳米管尖端内径为230 nm,这表明所拉制的纳米管是纳米通道.
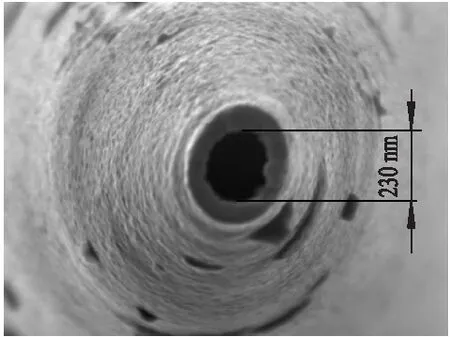
图2 纳米管的SEM图
图3为材料的圆二色光谱(circular dichroism,CD)图,用于表征适配体Apt-1,Apt-2和目标物Mal孵育前后的结构变化.图中θ,λ分别为摩尔椭圆度、波长;曲线②是只有Apt-1和Apt-2片段的情况下的CD谱,曲线②在247 nm处出现波谷,在278 nm处出现波峰;曲线①为加入目标Mal后的CD谱,从图中可以看出,当适配体溶液体系中加入目标物Mal后,CD谱曲线中波谷发生了红移,波谷强度增强,而波峰发生了蓝移,波峰强度增强,这表明Mal与适配体结合,适配体寡核苷酸链的双螺旋体发生了结构变化.
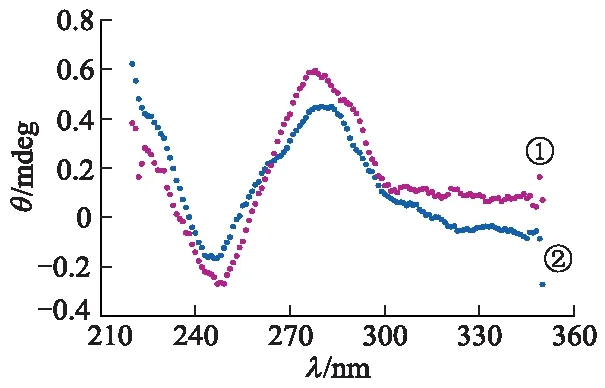
图3 材料CD谱
3.2 可行性验证
为考察传感器对Mal检测的可行性,研究了传感器在不同情况下的离子电流响应.图4为不同结合体系下的离子电流曲线,图中i,E分别为电流、电势;曲线①为镀金膜后的纳米通道的离子电流曲线,可见相对于0 V时,-1.0和+1.0 V处的电流分别增加了4.2×10-8和3.3×10-8A,这一电流不对称性表现出了微弱的整流现象,这是由于纳米通道内壁静电场强比较弱.曲线②,③和④分别为在纳米通道的金膜上修饰Apt-1后、修饰Apt-1和Mal以及修饰Apt-1和Apt-2后的离子电流曲线,可以发现-1.0和+1.0 V处相比在0 V处的电流差值增大,即产生电流整流现象比较明显.产生这一现象是由于纳米通道内修饰适配体后,适配体所带的电荷可以形成有效的静电场,当施加对称电压时,在外加电场下,溶液中K+和Cl-离子产生定向运动.当施加负电压时,K+定向向工作电极移动,由于修饰在纳米通道上的适配体带负电荷,有助于K+通过纳米通道,形成较大的电流;当施加正电压时,Cl-定向向工作电极移动,由于修饰在纳米通道上的适配体带负电荷,阻碍Cl-的定向通过,产生较低的电流,从而产生了比较明显的整流现象.曲线②,③和④在-1.0 V处的电流值相差不大,这是由于修饰Apt-1后,即使加入Mal,由于只有Apt-1时,Apt-1不能与Mal结合形成稳定的结构;当在金膜上修饰Apt-1后,加入Apt-2,没有目标物Mal的存在,Apt-1与Apt-2同样不能形成稳定结构,因此三者的整流现象比较接近.
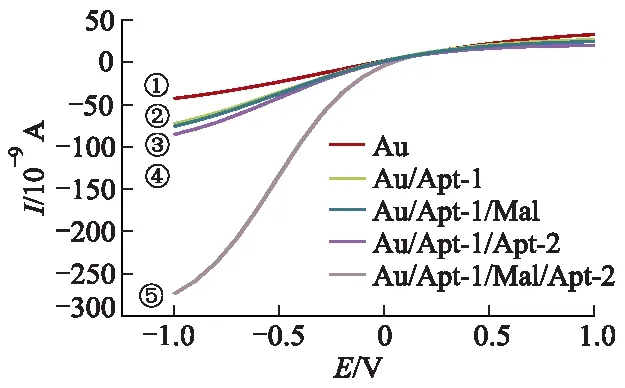
图4 不同结合体系下的离子电流曲线
当在修饰有Apt-1的纳米通道中加入目标物Mal和 Apt-2后,Apt-1与Mal和 Apt-2结合,形成Apt-1/Mal/Apt-2稳定结构,负电荷增多,增强了纳米管传感器内壁的静电场,进而产生更强的整流现象,如图4中曲线⑤所示.
3.3 传感器工作条件的优化
Apt-1的使用浓度影响其在纳米管通道内的修饰量,当Apt-1在纳米通道内的固定量不足,则不能提供足够与目标结合的位点,从而影响传感器的性能.图5为纳米通道内修饰不同浓度Apt-1(1.0×10-7,2.0×10-7,5.0×10-7,1.0×10-6,2.0×10-6,5.0×10-6mol/L)后,在浓度为1.0×10-6mol/L的Mal和1.0×10-6mol/L的Apt-2的混合溶液中孵育后,根据获得的-1.0 V处的离子电流值所绘制的曲线,图中i-1.0 V,CA-1分别为-1.0 V处的电流值、Apt-1溶液浓度.从图中可以看出,随着Apt-1的浓度增加,离子电流不断增大,当Apt-1浓度增到1.0×10-6mol/L时,曲线趋于稳定,电流不再有明显增加.这是因为Apt-1的浓度达到1.0×10-6mol/L时,可以提供足够的位点与目标结合.
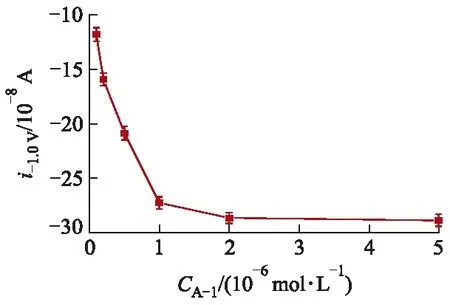
图5 不同浓度Apt-1对应的-1.0 V处的电流值
Apt-2的浓度影响Apt-1和Apt-2对目标Mal的识别.使用浓度为1.0×10-6mol/L的Apt-1修饰纳米通道,考察Apt-2的浓度对传感器离子电流的影响.试验获得-1.0 V处的离子电流值后绘制曲线如图6所示,图中CA-2为Apt-2溶液浓度.从图中可以看出,随着Apt-2浓度增大,离子电流增大,当Apt-2的浓度为1.0×10-6mol/L时,离子电流几乎没有增加.因此,在检测Mal时,Apt-2的浓度采用1.0×10-6mol/L.
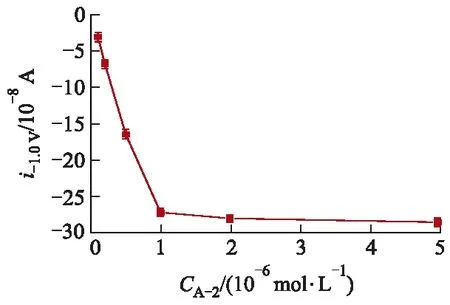
图6 不同浓度Apt-2对应的-1.0 V处的电流值
孵育溶液的pH影响适配体与Mal之间氢键的形成,进而影响Apt-1/Mal/Apt-2复合物的形成.因此需要对孵育溶液的pH值进行考察.图7为不同孵育条件下的离子电流曲线i-1.0 V,图中t为孵育时间.
图7a为采用不同pH的孵育溶液所对应的离子电流.从图中可以看到,孵育溶液的pH为8.0时,获得了最大的离子电流i-1.0 V.因此,使用pH为8.0的孵育溶液.

图7 不同孵育条件下的离子电流曲线的i-1.0 V值
孵育时间影响Apt-1/Mal/Apt-2复合物的形成,因此对孵育时间进行试验.如图7b所示,随着孵育时间增大,i-1.0 V增大,但在孵育时间超过40 min后,获得的i-1.0 V并没有明显的变化.因此,设置传感器的孵育时间为40 min.
3.4 线性范围和检测限
为了考察传感器对Mal定量检测的能力,对不同浓度Mal进行检测,如图8所示.
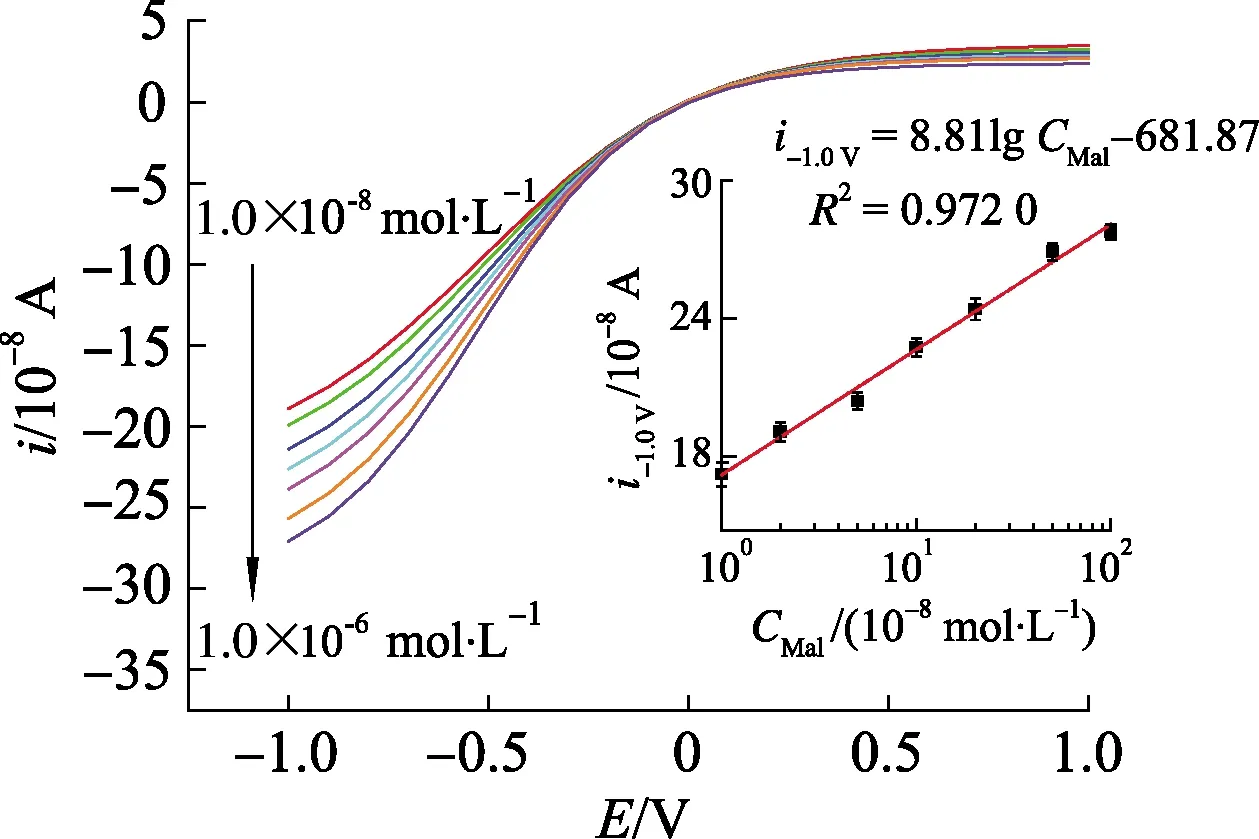
图8 检测不同浓度Mal的i-E曲线(插图:i-1.0 V-lg CMal拟合曲线)
在马拉硫磷溶液浓度CMal为1.0×10-8~1.0×10-6mol/L时,可获得Mal浓度对数和i-1.0 V之间的函数关系为
i-1.0 V=8.81lgCMal-681.87,R2=0.972 0.
(1)
传感器对Mal的检测限LOD为3.33×10-9mol/L.
表2为不同电化学适配体传感器对Mal检测方法的对比,表中LDR为线性检测范围.研究中的纳米通道适配体传感器的检测限低于基于Au纳米颗粒[13]、修饰精胺的Ag纳米颗粒[14]和液晶材料[15]的适配体传感器,同时具有更宽的线性检测范围.与基于由带负电荷的上转换荧光纳米粒子和阳离子聚合物封装的金纳米粒子制作的复合材料的传感器[5]相比,文中传感器的基体材料的制备过程更加简单.

表2 检测Mal的方法比较
3.5 传感器的选择性和稳定性
图9为传感器的选择性和稳定性,图中|i-i0|和n分别为电流差值、试验组别.
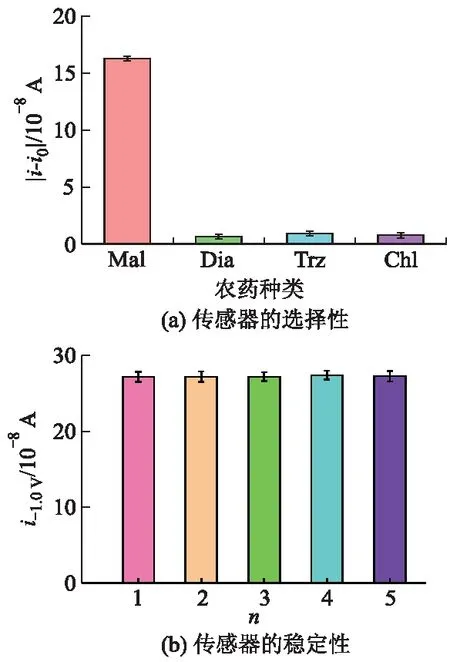
图9 传感器的选择性和稳定性
传感器的选择性是考察传感器性能的重要指标.使用该传感器分别检测二嗪磷(Dia)、三唑磷(Trz)、氯吡硫磷(Chl)和Mal,所有农药浓度均为1.0×10-6mol/L.检测结果如图9a所示,传感器检测Mal时获得的-1.0 V处电流差值|i-i0|远远大于其他3种农药,其中i0表示检测体系中只有Apt-1和Apt-2而没有农药时-1.0 V处的电流值.这表示所设计的纳米管适配体传感器对于检测Mal具有较高的选择性.
稳定性是传感器性能的重要指标.设置5组重复试验,每组试验测定3次.试验结果如图9b所示,组内最大变异系数为2.05%,组间变异系数为0.33%.这表明所设计的纳米通道适配体传感器用于检测Mal时具有较高的稳定性.
3.6 实样检测
为了考察纳米管适配体传感器在实际样品检测中的可用性,采用标准加入法对实际样品进行测定.表3为自来水中的Mal分析(试验次数n=3),表中C+为添加Mal的浓度,GC为使用气相色谱法对水样中Mal浓度的检测结果,Ct为该传感器对Mal浓度检测结果,r为回收率,RSD为相对标准偏差.如表所示,水样中加入Mal的回收率为96.60%~101.00%,相对标准偏差为1.39%~6.02%.使用气相色谱法检测制备的水样,所得结果与使用纳米管适配体传感器所得检测结果相比较,两者基本一致,这表明所构建的传感器可应用于检测实际样品中的Mal.

表3 自来水中的Mal分析(n=3)
4 结 论
1)根据纳米通道信号转导所产生的离子电流整流现象,使用玻璃管作为基体,通过在玻璃管的纳米通道表面修饰适配体,成功地构建了可用于检测Mal的纳米通道适配体传感器.
2)该传感器检测Mal的线性范围为1.0×10-8~1.0×10-6mol/L,灵敏度高,选择性好,并成功用于水样中Mal的检测,有望替代检测成本高昂、需要使用大型专用仪器的传统检测方法,为灵敏检测有机磷农药的发展开辟了新的途径.

