两个基于2,3,5,6-四氟-二(1,2,4-三氮唑-1-甲基)苯和1,4-萘二甲酸混合配体的配位聚合物的合成、结构及其荧光性能
谢京燕
(中山大学 材料学院,广东 深圳 518000)
作为一种近年来被广泛研究的有机-无机晶体材料,易功能化的特点使配位聚合物广泛应用于如气体吸附、磁性、光化学和催化等领域,因而成为近年来的研究热点[1-4]。在构筑配位聚合物时,有机配体是自组装形成特定结构配位聚合物的关键因素之一,影响到配位聚合物的功能化[5-7]。混合配体策略,如酸-酸、碱-碱和酸-碱混合配体策略,由于引入了多种类型的官能团而易于在反应后得到复杂而丰富的拓扑结构,同时利于配位聚合物的功能化,被视为一种行之有效的配位聚合物合成策略。
混合配体中,选择中性氮杂环配体和芳香羧酸配体的酸-碱混合配体策略由于同时结合了酸/碱配体的优点,受到了较多的关注[8-9]。例如,不同间隔基团和构象模式(顺势/反式)的双吡啶[10]、咪唑[11]和三氮唑[12]类配体常被选择与芳香羧酸进行自组装反应,得到了大量结构新颖的配位聚合物。此外,保持氮杂环配体不变,通过调控芳香族多羧酸盐的种类和取代基以设计和构筑特定结构和功能化的配位聚合物也得到了较多关注。例如,3种芳族二羧酸(邻苯二甲酸、间苯二甲酸和对苯二甲酸)作为最具代表性的羧酸配体,被广泛用于研究了取代基的位置异构对混合配体自组装系统的影响[13-14]。此外,还发现芳香羧酸取代基的种类对混合配配位聚合物的结构起着决定性作用[15-16]。
在设计和构筑配位聚合物时,1,4-双(1,2,4-三唑-1-基甲基)苯(btx),作为一种经典的双三氮唑类衍生物柔性配体,由于可以采取多种空间构型且配位能力强,在混合配体的构建中显示出巨大的潜力[17-23]。作为btx体积更大的衍生物,2,3,5,6-四甲基-1,4-双(1,2,4-三唑-1-基甲基)苯也被用于与二羧酸配体自组装构筑配位聚合物[24-26]。利用2,3,4,5,6-四氯邻苯二甲酸和氟化btx的配体 2,3,5,6-四氟的混合配体-1,4-双(1,2,4-三唑-1-基甲基)苯(Fbtx),本课题组此前报道了一种3D互穿钴基配位聚合物,在温和的反应条件下对苯并恶唑的胺化表现出优异的催化活性[27]。此外,还基于Fbtx和邻苯二甲酸的混合配体策略合成了一个3D铜基配位聚合物,并被证明可有效非均相催化醇有氧氧化。
作为混合配体策略研究的后续工作,如Scheme 1 所示,本文选择Fbtx和1,4-萘二甲酸(H2NDC)作为配体,水热条件下分别与钴盐和铜盐反应得到了两个新的过渡金属配位聚合物{[Co(NDC)(Fbtx)(H2O)2]·0.5H2NDC}n(1)和{[Cu(NDC)(Fbtx)(H2O)]·1.5H2O}n(2),通过X-射线单晶衍射和红外光谱等对其进行结构表征,探讨酸-碱混合配体体系下金属离子差异对配位聚合物结构的影响,同时研究了其热稳定性和荧光性能。
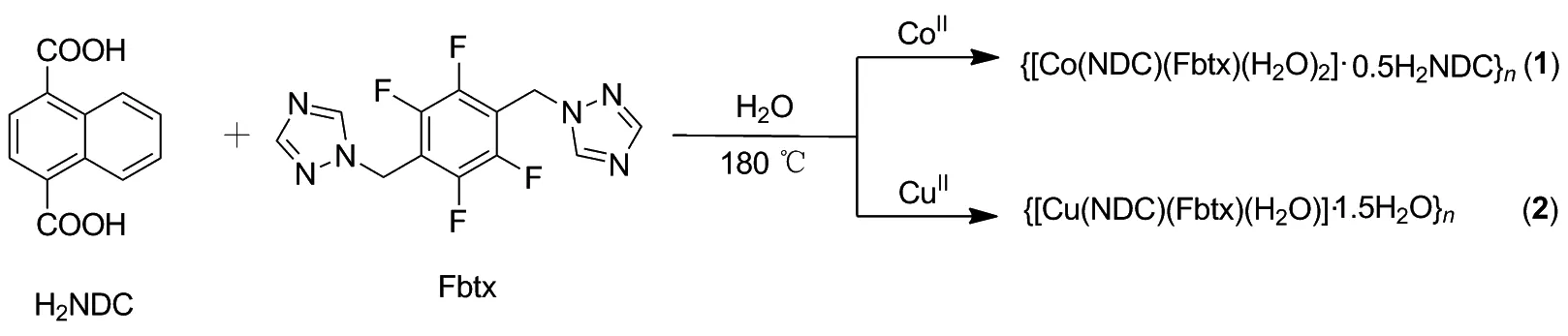
Scheme 1
1 实验部分
1.1 仪器与试剂
Nicolet IS 50型(美国)红外光谱仪(IR)(KBr压片);SDT Q600型(美国)热重-差热分析仪(TG)(氮气氛围下,以10 ℃/min的速率从室温升温至800 ℃收集);Bruker Smart Apex II CCD型(德国)X-射线单晶衍射仪(SC-XRD);Rigaku D/max-2500型(日本)X-射线粉末衍射仪(PXRD)[Cu靶(λ=1.5406 Å),扫描速率0.2°/min,收集5~50°内数据,模拟PXRD谱图通过PLATON[29]软件计算单晶数据得到];Varian Cary Eclipse型荧光仪。
2,3,5,6-四氟-二(1,2,4-三氮唑-1-甲基)苯根据文献[28]方法合成;其余试剂均购自阿拉丁试剂有限公司,纯度为分析纯。
1.2 配位聚合物的合成(以1为例)
将4H2O·Co(OAc)2(24.9 mg, 0.1 mmol)、Fbtx(31.1mg, 0.1 mmol)、H2NDC(24.0 mg, 0.1 mmol)、NaOH(4.0 mg, 0.2 mmol)及6 mL去离子水的混合物加入至10 mL带有聚四氟乙烯内衬的不锈钢反应釜中,于180 ℃恒温反应3 d。冷却至室温后得到适合X-射线单晶衍射的粉色块状晶体,产率45%(23.3 mg,基于H2NDC);IRν: 3446 br, 3156 s, 3010 s, 1710 m, 1613 s, 1591 s, 1536 m, 1494 w, 1455 m, 1412 w, 1364 w, 1282 w, 1202 m, 1175 s, 1132 m, 1031 w, 1002 m, 956 s, 886 m, 883 m, 794 w, 702 m, 652 m, 581 m, 508 m cm-1。
用类似的方法合成蓝色片状晶体2,产率53%(68.6 mg,基于Fbtx); IRν:3440 br, 3152 s, 3012 s, 1615 s, 1591 s, 1534 m, 1495 w, 1458 m, 1412 w, 1364 w, 1282 w, 1202 m, 1174 s, 1131 m, 1029 w, 1001 m, 958 s, 885 m, 881 m,795 w, 702 m, 651 m, 581 m, 507 m cm-1。
1.3 晶体结构测试方法
在273 K温度下,用石墨单色器单色化的Mo-Kα射线(λ=0.71073 Å)以ω的扫描方式在单晶衍射仪上收集衍射数据,用SADABS进行半经验吸收校正,并用SAINT程序进行衍射曲线的积分[30]。使用SHELXS程序通过直接方法求解结构[31],并通过全矩阵最小二乘方法对所有非氢原子进行各向异性修正,而氢原子用各向同性参数进行修正。化合物1和2(CCDC: 2103022和2103023)的晶体学参数见表1,主要键长和键角数据见表2。
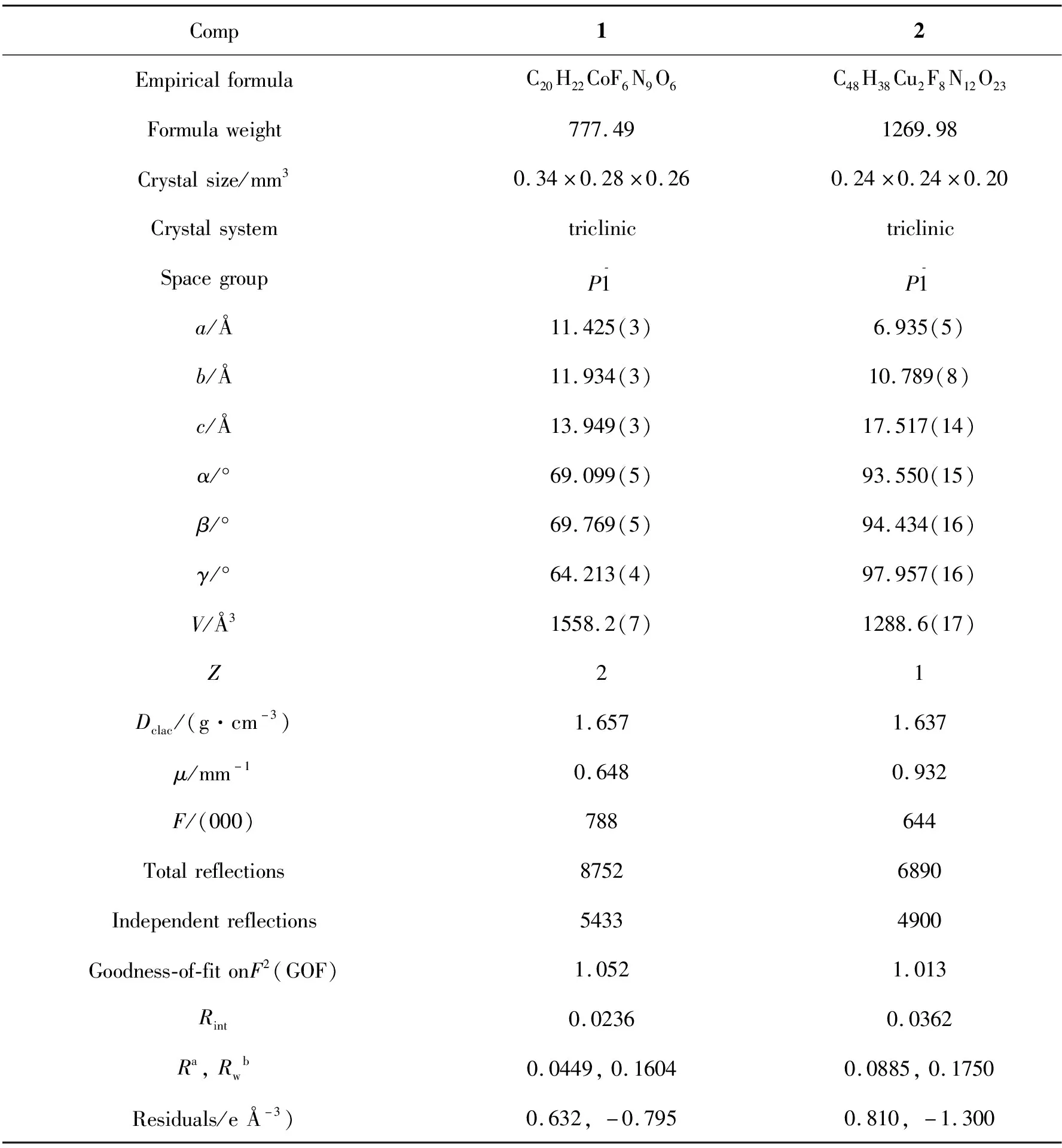
表1 化合物1和2的主要晶体学数据
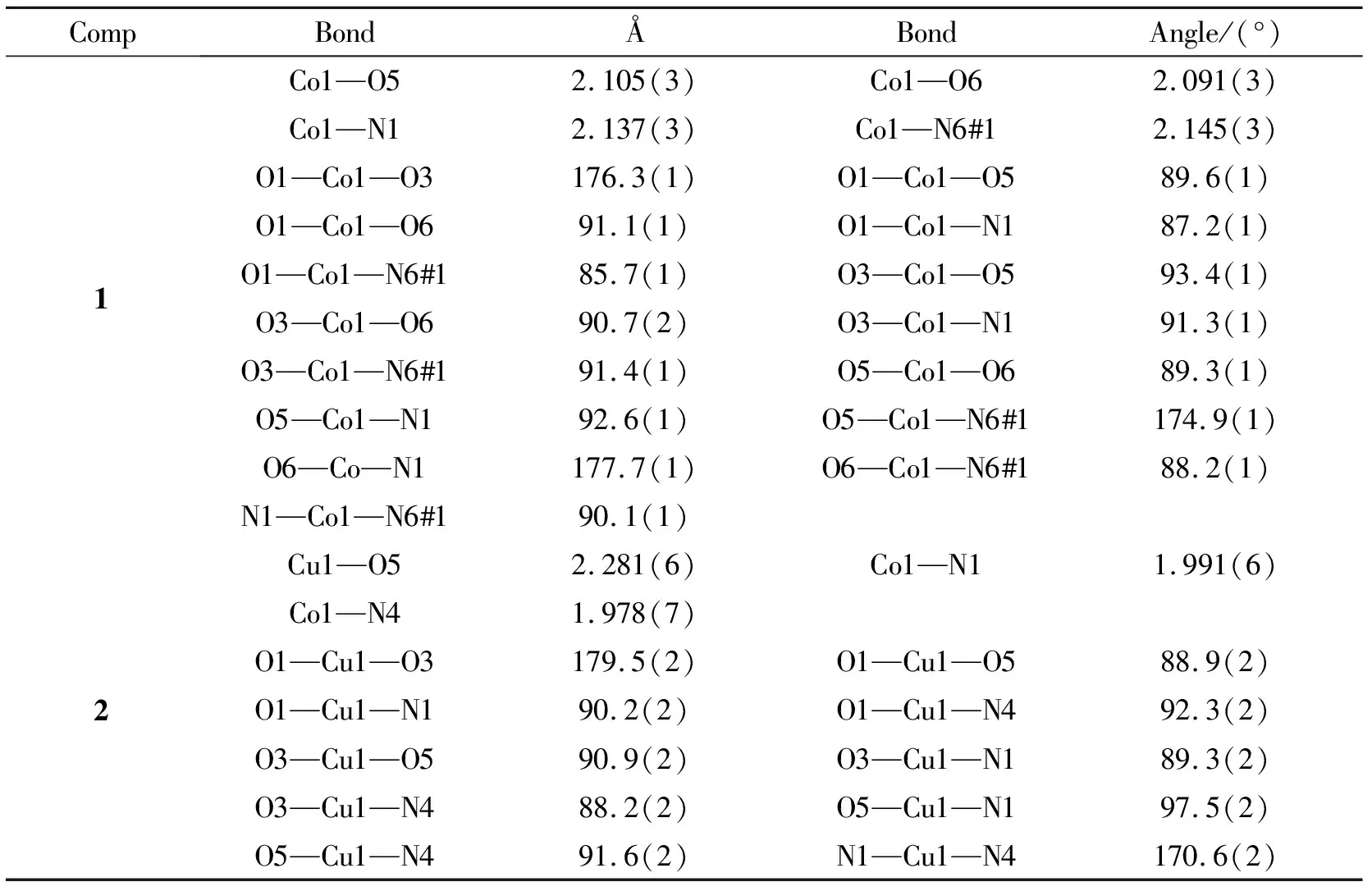
表2 1和2的主要键长(Å)和键角(°)
2 结果与讨论
2.1 合成
混合配体是构筑配位聚合物的一种有效策略,配体的选择对配位聚合物的结构影响显著。芳香羧酸具有丰富的配位模式,易于形成不同配位模式的无机中心,氮杂环配体具有较强的配位能力,是一种优良的桥联配体。本文以刚性的H2NDC和柔性的Fbtx配体结合,构筑了基于CoII和CuII的两个过渡金属配位聚合物,其中心金属离子的差异最终导致了1和2结构的细微差异。
分析化合物1和2的红外谱图(图略)可知,在3446/3444 cm-1处的宽峰对应其结构中配位水O—H的伸缩振动。1中1710 cm-1处特征峰为游离客体H2NDC中的羰基的吸收峰,说明客体没有去质子化,1615~1613和1366~1364 cm-1的特征峰为化合物1和2有机配体去质子化后羰基的对称和非对称伸缩振动吸收峰。如图1所示,1和2单晶数据模拟与实验测得的PXRD的特征峰吻合较好,说明它们均有较高的相纯度。
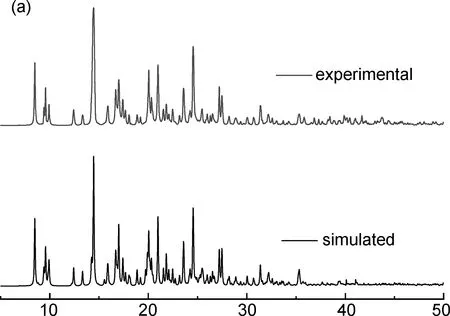
2θ/(°)
2.2 晶体结构分析
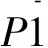
图2 (a)化合物1中CoII的配位环境;(b)化合物1的二维层状结构;(c)化合物1的二维sql拓扑
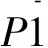
图3 (a)化合物2中CuII的配位环境;(b)化合物2的二维层状结构;(c)化合物2的二维sql拓扑

Temperature/℃
1.4 化合物的热重分析
研究了化合物1和2的热稳定性,测试条件为25~800 ℃,氮气氛围下以10 ℃/min的升温速率进行测试。化合物1和2是在相同的条件下合成的,区别仅仅是反应体系加入的金属盐不同,如图4所示,化合物1和2的骨架具有相近的热稳定性,在75~125 °C区间开始第一段失重,分别失重4.8%和3.7%,可归结于化合物1和2中的配位水(理论值4.6%/3.5%)。化合物1和2的配位骨架可以稳定至305 ℃,随后发生了连续的失重,直到800 ℃仍没有停止。
1.5 荧光性质
图5为配体Fbtx、H2NDC以及配位聚合物1和2在室温下的固态荧光谱图。由图5可知,配体Fbtx和H2NDC在激发波长为336 nm时,在450~540 nm内出现宽的荧光发射峰。在相同激发波长下,具有二维层状结构的配位聚合物1和2的发射波长都较为相似,分别在476 nm(1)和475 nm(2)处呈现最大的发射峰,同时在492 nm(1)和490 nm(2)以及510 nm(1)和511 nm(2)处也出现较弱的肩峰,发光机理可以归结为配体内部芳香环上π→π*和/或n→π*的电子跃迁。在荧光强度方面,配位聚合物1和2的荧光强度都明显弱于有机配体,这可能是由于配体与金属离子配位后,配位聚合物中高能震荡的O—H…O和C—H…F作用导致的荧光淬灭,增加了配体内(π→π*)激发态的无辐射衰变[32]。配位聚合物1和2的荧光衰减寿命分别为1.42和1.37 ns,而它们的荧光量子产率也较低,分别只有2.27%和2.43%。
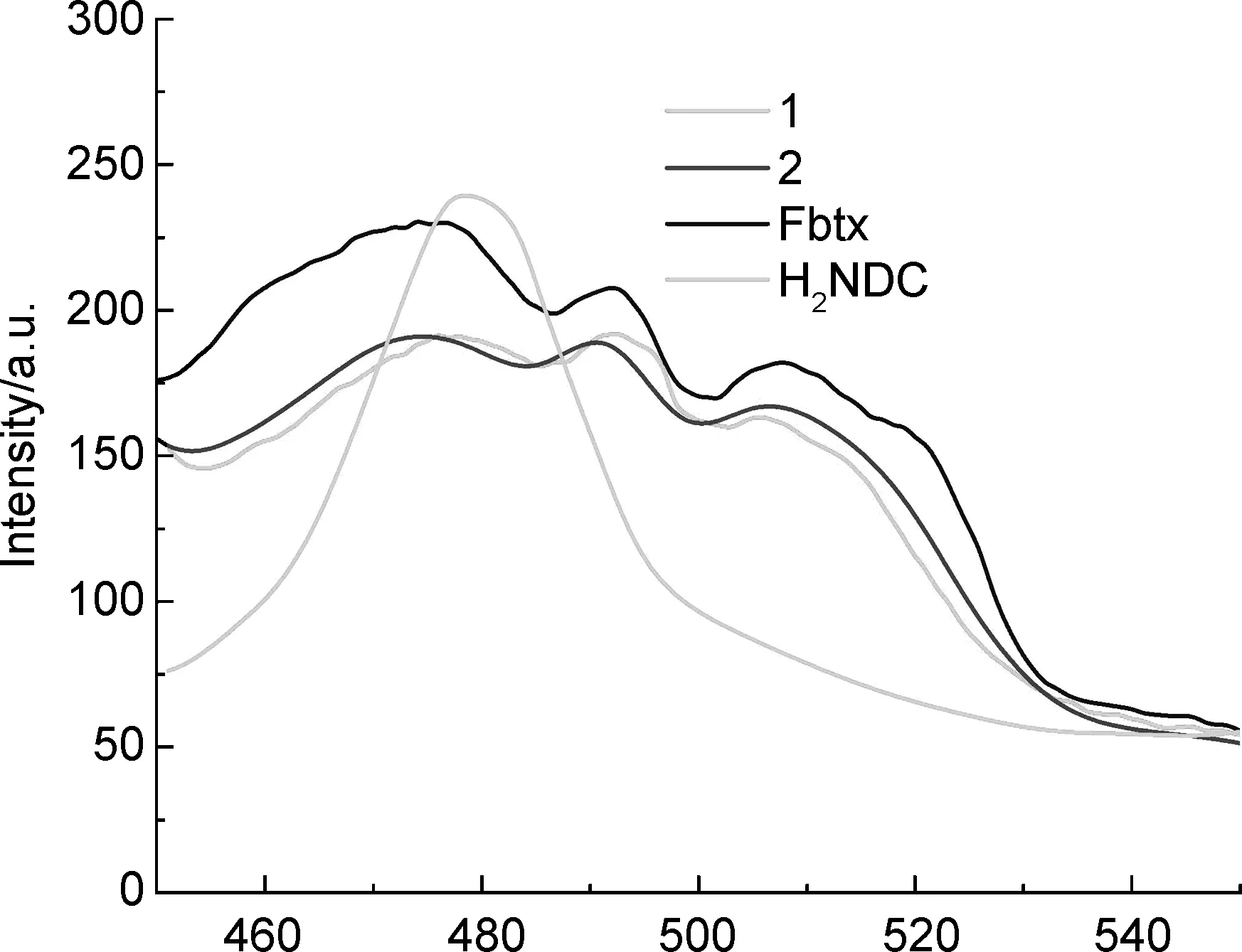
λ/nm
通过调控金属离子,水热合成了两个新的基于2,3,5,6-四氟-二(1,2,4-三氮唑-1-甲基)苯及1,4-萘二甲酸的酸-碱混合配体配位聚合物。配位聚合物1和2中的金属分别为六配位的CoII和五配位的CuII,二者均为二维层状的结构,中心金属离子的差异导致了它们sql拓扑上细微差异。固态荧光测试显示1和2的荧光光谱与Fbtx配体相似,强度略有降低,这可能是配体与金属离子配位后的淬灭效应导致的。

