血清IL-17A、IL-6与妊娠期亚临床甲状腺功能减退症及妊娠结局的关系
曹凯凤,明亚琼,龚丽,高亚丽,孙吉荣,冉峥嵘,莫远娟,张昌容
亚临床甲状腺功能减退症(subclinical hypothyroidism,SCH)是临床常见的全身代谢性疾病,以促甲状腺激素(thyroid stimulating hormone,TSH)浓度升高,血清游离甲状腺素(free thyroxine,T4)水平正常为特征,妊娠期间发生SCH可导致流产、早产、妊娠糖尿病、妊娠高血压、先兆子痫、胎盘早剥、胎膜早破、宫内生长受限、低出生体质量、小于胎龄儿、新生儿出生Apgar评分偏低和死亡等不良妊娠结局[1]。现有研究发现,SCH的发生与自身免疫反应引起的甲状腺炎有关[2]。甲状腺自身免疫疾病患者妊娠早期辅助性T细胞(T helper cell,Th)17相关细胞因子水平与正常妊娠孕妇存在显著差异,表现为血清白介素(interleukin,IL)-17水平明显增高[3]。IL-17A是IL-17家族中研究最多和最具代表性的细胞因子,可促使T细胞活化,在甲状腺自身免疫疾病发病机制中发挥关键促进作用[4]。IL-6是一种促炎细胞因子,可激活初始CD4+T淋巴细胞并控制调节性T细胞(T regulatory cells,Treg)和Th17分化,启动免疫反应[5]。IL-17A与妊娠期间SCH的关系报道十分少见,其关系尚不清楚,鉴于此,本研究拟检测血清IL-17A、IL-6水平,分析其与妊娠期间SCH发生的关系,以期为临床诊治提供参考,报道如下。
1 资料与方法
1.1 临床资料 选择2020年1月—2021年12月贵州中医药大学第二附属医院产科收治妊娠期SCH孕妇107例(SCH组),再根据妊娠结局分为妊娠结局不良亚组和妊娠结局正常亚组。另选择同期于医院妇产科产检的正常妊娠孕妇109例为对照组。SCH组年龄、既往产次≥3次、既往流产史、SCH家族史、妊娠期碘摄入偏低比例高于对照组(P<0.01),其他资料比较差异无统计学意义(P>0.05),见表1。本研究经医院伦理委员会批准(191052),入选孕产妇及家属均知情同意并签署知情同意书。
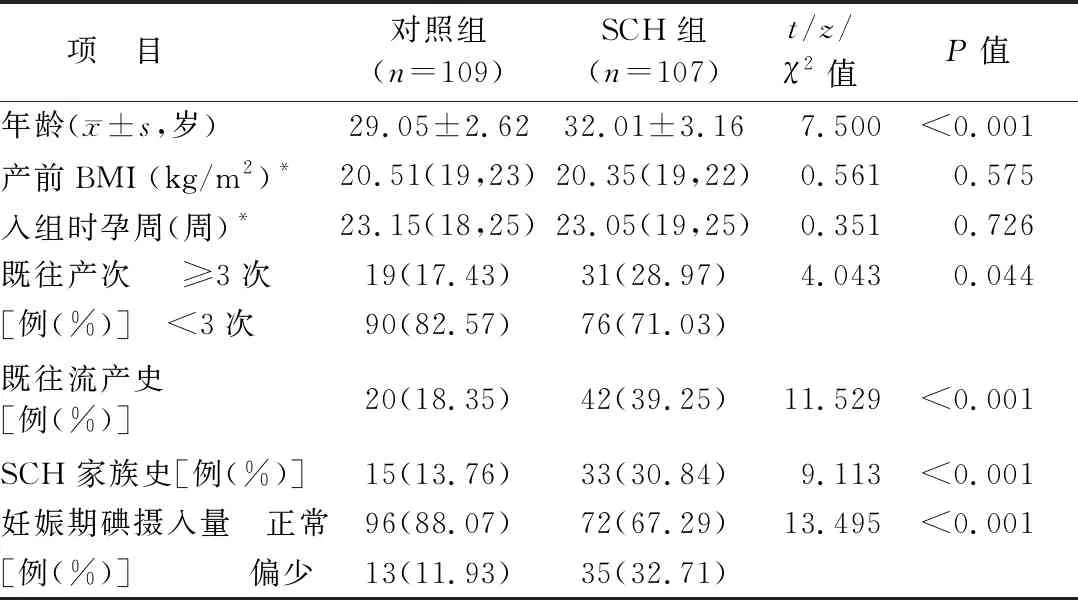
表1 SCH组和对照组基线资料比较
1.2 病例选择标准 (1)纳入标准:①年龄在18~40岁;②单胎妊娠;③TSH升高(>4.0 mIU/L),FT4正常(12~22 pmol/L),符合“2017 年美国甲状腺协会妊娠和产后甲状腺疾病诊断和管理指南”中SCH诊断标准[6]。(2)排除标准:①妊娠前甲状腺疾病史、居住在碘缺乏地区或服用可能影响甲状腺功能的药物或接受甲状腺激素替代治疗;②既往慢性传染病、慢性自身免疫性疾病;③妊娠糖尿病;④妊娠期间合并甲状腺功能亢进症。
1.3 观测指标与方法
1.3.1 血清IL-17A、IL-6检测:对照组孕产妇入组时、SCH组在给药前采集空腹8 h以上静脉血3 ml,离心获得血清在-80℃保存待检。采用Varioskan LUX酶标仪(美国赛默飞公司)以夹心酶联免疫吸附试验测定血清IL-17A、IL-6水平,试剂盒购自美国 Bio Legend公司,根据试剂盒说明书操作。
1.3.2 血清TSH、FT4水平检测:上述血清采用日立h7060全自动化学免疫分析仪检测血清TSH、FT4水平。
1.3.3 妊娠结局追踪:追踪SCH组孕妇妊娠结局,包括流产、胎儿宫内死亡、早产、妊娠期高血压、先兆子痫、胎盘早剥、宫内生长受限和新生儿呼吸窘迫或死亡。SCH组妊娠结局不良21例,妊娠结局正常86例。

2 结 果
2.1 2组血清IL-17A、IL-6水平比较 SCH组血清IL-17A、IL-6水平高于对照组(P<0.01),见表2。

表2 SCH组和对照组血清IL-17A、IL-6水平比较
2.2 SCH组不同妊娠结局孕妇血清IL-17A、IL-6水平比较 妊娠结局不良亚组血清IL-17A、IL-6水平高于妊娠结局正常亚组(P<0.01),见表3。

表3 SCH组不同妊娠结局患者血清IL-17A、IL-6水平比较
2.3 2组血清TSH、FT4水平比较 SCH组血清TSH水平高于对照组(P<0.01),而FT4水平比较差异无统计学意义(P>0.05),见表4。

表4 SCH组和对照组血清 TSH、FT4水平比较
2.4 SCH组血清IL-17A、IL-6与TSH的相关性分析 血清IL-17A、IL-6与TSH均呈正相关(r=0.493、0.369,P均<0.001),IL-17A与IL-6之间亦呈正相关(r=0.556,P均<0.001)。
2.5 妊娠期发生SCH的多因素Logistic回归分析 以妊娠期是否发生SCH为因变量(0=否,1=是),以年龄、既往产次、既往流产史(0=否,1=是)、SCH家族史(0=否,1=是)、妊娠期碘摄入(0=正常,1=偏少)、IL-17A、IL-6为自变量,结果显示,妊娠期碘摄入偏少及血清IL-17A、IL-6高是妊娠期发生SCH的危险因素(P<0.01),见表5。

表5 影响妊娠期发生SCH的多因素Logistic回归分析
2.6 血清IL-17A、IL-6诊断妊娠期SCH的价值分析 血清IL-17A联合IL-6诊断妊娠期SCH的曲线下面积高于单独IL-17A、IL-6检测(Z=5.683、3.912,P<0.05),见表6、图1。
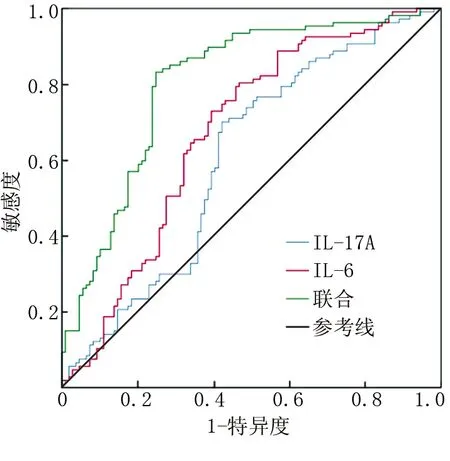
图1 血清IL-17A、IL-6诊断妊娠期SCH的ROC图

表6 血清IL-17A、IL-6诊断妊娠期SCH的效能
3 讨 论
妊娠期间维持充足的甲状腺激素水平对胎儿生长发育有重要作用,甲状腺激素可促使甲状腺素结合球蛋白(thyroxine binding globulin,TBG)、甲状腺素运载蛋白和白蛋白转运,正常妊娠期间,TBG浓度会增加2~3倍,引起T4、T3水平升高,降低TSH水平,TBG和白蛋白还可与 α-I-抗胰蛋白酶、β-I-酸性糖蛋白一起参与母体和胎儿循环,局部调节母胎激素转运改变甲状腺激素的再摄取和脱碘作用,促使胎儿甲状腺发育,刺激下丘脑—垂体—甲状腺系统形成及中枢神经系统发育[7]。甲状腺功能障碍在孕妇中普遍存在,多由慢性自身免疫性甲状腺炎引起,SCH是最常见的甲状腺功能障碍类型之一,其发生与自然流产、胎盘早剥、早产、胎儿窘迫和先兆子痫等妊娠不良结局有关[8]。由于SCH缺乏显著的临床特征,其早期诊断困难,因此探讨与妊娠期间SCH发病相关的生物学标志物十分重要。已知自身免疫性甲状腺疾病是导致甲状腺功能减退的最常见原因,T淋巴细胞及其分泌的细胞因子在调节免疫反应中发挥着不可或缺的作用,T淋巴细胞功能障碍或其分泌的细胞因子异常表达会导致免疫耐受破坏,导致异常的免疫反应,参与自身免疫性甲状腺疾病过程[9]。
Th17 细胞及其标志性细胞因子IL-17是甲状腺自身免疫发病的关键因素,IL-17A是IL-17家族代表性细胞因子,广泛表达于上皮细胞、成纤维细胞和巨噬细胞等,诱导IL-1β、IL-6和IL-8等促炎介质释放,并与其结合表现出强烈的协同作用[4]。现有研究显示,自身免疫性甲状腺疾病大鼠模型甲状腺组织中IL-17A水平明显升高,当阻断与TBG合成和Th17活化有关的转录因子——激活蛋白1的激活时,IL-17A 水平则降低[10]。本研究发现,血清IL-17A增高与妊娠期间甲状腺功能减退有关。可能的原因为在甲状腺免疫性炎性损伤临床进展过程中,Treg/Th17向Th17偏倚,导致Th17 细胞过度活化并释放大量IL-17A[11],IL-17A进入外周循环后引起血清IL-17A水平增高。本研究通过追踪妊娠结局发现,妊娠结局不良亚组血清IL-17A水平高于妊娠结局正常亚组,表明IL-17A与妊娠SCH患者妊娠结局有关。IL-17A在胎盘绒毛组织中也有表达,主要由胎盘巨噬细胞合成,有助于调节胎盘发育和功能,在维持正常妊娠过程中发挥关键作用[12]。现有研究显示,妊娠合并先兆子痫引起的胎盘缺血反应可引起IL-17A表达上调,IL-17A可活化溶细胞性自然杀伤细胞,进而导致高血压、炎性反应和胎儿生长受限[13]。推测原因:首先,IL-17A水平过高可能诱导和加剧胎盘炎性反应,导致胎盘和胎儿宫内发育异常,引起不良妊娠结局,Crosby等[14]报道也指出血清IL-17水平升高与不孕症女性辅助生殖治疗失败有关。其次,本研究相关性分析结果显示,IL-17A与TSH水平呈正相关,表明IL-17A水平增高可能引起TSH水平增高,而高TSH与妊娠不良结局也有密切关系,Lee等[15]研究显示,妊娠期母体血清TSH浓度> 4 mIU/L可使早产、新生儿呼吸窘迫综合征风险增加2倍。
IL-6是启动 Th17 细胞发育的必要细胞因子,可由巨噬细胞和单核细胞、间充质细胞和成纤维细胞等先天免疫细胞产生,急慢性炎性反应可驱动 IL-6 的产生,IL-6激活后主要通过受体相关的 Janus 激酶启动信号转导,调节次级淋巴器官中 T 细胞和 B 细胞反应,并促使局部间充质细胞中趋化因子和炎性细胞因子的产生,过量或持续IL-6产生可增强Th17细胞的分化,扩大炎性反应,导致组织损伤[16-17]。现有研究显示,IL-6在自身免疫性甲状腺疾病大鼠甲状腺组织中水平明显升高,通过靶向抑制IL-6有望成为自身免疫性甲状腺疾病的新疗法[18]。本研究结果显示,IL-6水平增高与妊娠期发生SCH密切相关,提示IL-6有望成为妊娠SCH的生物学标志物。Gupta等[19]报道也指出,SCH患者血清IL-6水平明显高于甲状腺功能正常者,IL-6水平与TSH 呈显著正相关(r=0.66),与本研究相关性分析结果相同,提示IL-6浓度增高的原因可能一方面是受TSH刺激导致,另一方面推测在SCH炎性环境刺激下导致IL-6生成增加,IL-6浓度增高后进一步促使促炎性Th17细胞反应,引起IL-17A水平增高,进而形成恶性循环,最终导致甲状腺功能减退,本研究相关性分析中IL-6与IL-17A呈正相关也可佐证这一观点。进一步分析发现IL-6水平增高与妊娠SCH患者妊娠结局不良有关,Leanos-Miranda等[20]指出IL-6浓度增加与羊膜腔内炎性反应及早产有关,增加不良妊娠结局的风险。
综上,妊娠期SCH患者血清IL-17A、IL-6水平均增高,高水平血清IL-17A、IL-6与妊娠期间SCH的发生及妊娠结局不良均有关,可作为妊娠SCH诊断的辅助指标。IL-17A、IL-6与TSH呈正相关,IL-17A与IL-6亦呈正相关,提示IL-17A、IL-6可能相互作用促使了妊娠期间甲状腺功能减退的发生。本研究ROC分析结果显示,血清IL-17A、IL-6在诊断妊娠期SCH方面具有一定价值,联合2项指标可弥补单项指标诊断效能不足的弊端,提高诊断效能,提示血清IL-17A、IL-6有望成为妊娠期SCH辅助诊断的生物学指标,对临床病情判断和治疗有一定价值。
利益冲突:所有作者声明无利益冲突
作者贡献声明
曹凯凤:设计研究方案,实施研究过程,论文撰写;明亚琼:提出研究思路;龚丽:分析试验数据;高亚丽:论文审核;孙吉荣:资料搜集整理;冉峥嵘:论文修改;莫远娟:进行统计学分析;张昌容:课题设计与指导

