用硫酸从镍钴渣料中两段浸出镍钴
班 政,肖 莉,唐新村
(1.中南大学 化学化工学院,湖南 长沙 410083;2.中南大学 化学电源湖南省重点实验室,湖南 长沙 410083)
废锂离子电池正极材料中含有大量镍、钴,通过分选、硫酸浸出、除杂净化等工序,可以回收钴、镍、锰,并进一步制备棒状草酸钴粉末、LiCoO2及电池正极材料LiNi1/3Co1/3Mn1/3O2[1-5]。酸洗废液中的镍钴锰,可采用纯碱-氨水混合液沉淀回收[6-7],镍红土矿浸出液中的镍和钴可用螯合树脂和预还原工艺加以回收[8-9]。
现有的镍钴回收工艺通常是将镍、钴单独回收,而后镍、钴又被重新混合生产高性能、高附加值产品。如新疆某冶炼厂,通过深度除杂、调节酸碱度、萃取和电解等工序,得到电解镍和电解钴产品[10-11],但之后又将二者混合生产LiNi1/3Co1/3Mn1/3O2正极材料,这显然造成了很大浪费,流程优化空间很大。对此,提出了以两段浸出法处理镍钴渣料,无须进行镍、钴分离,所得产物简单处理后即可直接用于制备LiNi1/3Co1/3Mn1/3O2正极材料。
1 试验部分
1.1 试验原料、试剂与仪器
试验原料:取自新疆阜康冶炼厂,为电解镍工艺中用黑镍(NiOOH)氧化沉钴所得的镍钴渣料,黑色,含水量30%~35%,堆密度2.01~2.24 g/cm3,化学组成见表1。

表1 镍钴渣料的主要化学组成 %
主要试剂:浓硫酸,分析纯;过氧化氢,分析纯,质量分数30%;去离子水。
主要仪器:循环水式多用真空泵,集热式恒温加热磁力搅拌器,电热恒温鼓风干燥箱,pH计,电子天平等。
1.2 试验原理
二价镍、钴和大部分二价杂质离子易溶于低浓度硫酸中,而三价镍、钴较难直接溶出,需添加还原剂才能完全浸出,因此,通过两段浸出从镍钴渣料中分段浸出镍、钴。一段浸出用低浓度硫酸对镍钴渣料进行浸出,通过控制浸出终点pH调节浸出液中镍、钴质量浓度,实现镍、钴及杂质的初步分离;二段浸出用硫酸/过氧化氢溶液对一段浸出渣进行还原酸浸,以过氧化氢作为还原剂,实现镍、钴完全浸出。浸出过程中的主要化学反应如下:



4H2O+O2↑;

4H2O+O2↑。
1.3 试验方法
一段浸出:常温下,镍钴渣料置于烧杯中,按液固体积质量比10 mL/1 g加入一定浓度硫酸溶液,搅拌,反应充分后测定pH,然后继续添加硫酸直至浆料pH达设定要求且维持稳定。浸出结束后抽滤,滤渣水洗2次,高温干燥后与浸出液一起进行元素分析。
二段浸出:对一段浸出渣,按一定液固体积质量比加入一定浓度硫酸溶液和过氧化氢溶液,反应在设定温度下进行。浸出结束后,对浸出液分析中钴、镍离子质量浓度。
2 试验结果与讨论
2.1 一段浸出
按试验方法,控制浸出终点pH,常温下用低浓度硫酸浸出镍钴渣料,终点pH对一段浸出效果的影响试验结果见表2。

表2 一段浸出终点pH对浸出液中镍、钴质量浓度及浸出率的影响
由表2看出:随终点pH降低,一段浸出液中镍质量浓度升高,镍浸出率提高;钴质量浓度在终点pH≥2.5时较低,浸出率低于1.09%,但终点pH<2.5后,随终点pH降低,溶液中钴质量浓度明显升高,浸出率增大至25.84%。溶液酸度较大时,渣料中三价钴离子溶解率明显提高。综合考虑,确定一段酸浸终点pH为2.5,此条件下酸浸液和酸浸渣的化学成分分别见表3、4。

表3 一段浸出液的主要化学成分 g/L
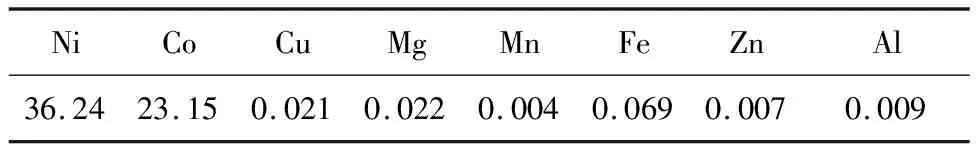
表4 一段浸出渣的主要化学组成 %
由表3、4看出:一段浸出液中,镍质量浓度较高而钴质量浓度较低,同时杂质离子(如Cu2+、Mg2+等)质量浓度较高。说明一段浸出过程中,大量镍和杂质溶解而钴溶解率较低,大部分留在浸出渣中。
2.2 二段浸出
2.2.1 反应温度对镍、钴浸出率的影响
镍钴渣料一段浸出渣质量10 g,反应时间3 h,硫酸浓度1.5 mol/L,过氧化氢溶液用量(过氧化氢溶液体积/渣料质量)1.5 mL/g,液固体积质量比10 mL/1 g,反应温度对镍、钴浸出率的影响试验结果如图1所示。
由图1看出:随温度从30 ℃升高,镍、钴浸出率均大幅提高。随温度升高,化学反应速率加快,且H2O2反应活性增强;温度达70 ℃时,镍、钴浸出率达最大;继续升温,镍、钴浸出率基本稳定,且温度过高易导致H2O2分解。综合考虑,确定二段浸出温度以70 ℃为宜。
2.2.2 反应时间对镍、钴浸出率的影响
镍钴渣料一段浸出渣质量10 g,反应温度70 ℃,硫酸浓度1.5 mol/L,过氧化氢溶液用量1.5 mL/g,液固体积质量比10 mL/1 g,反应时间对镍、钴浸出率的影响试验结果如图2所示。
由图2看出:随反应时间延长,镍、钴浸出率大幅提高;浸出2 h后,镍、钴浸出率达最大,反应趋于完全。综合考虑,确定二段浸出时间以2 h为宜。
2.2.3 硫酸浓度对镍、钴浸出率的影响
镍钴渣料一段浸出渣质量10 g,反应温度70 ℃,反应时间2 h,过氧化氢溶液用量1.5 mL/g,液固体积质量比10 mL/1 g,硫酸浓度对镍、钴浸出率的影响试验结果如图3所示。

图3 硫酸浓度对镍、钴浸出率的影响
由图3看出:随硫酸浓度增大,镍、钴浸出率提高;硫酸浓度为1.5 mol/L后,镍、钴浸出率达最大且趋于稳定。随硫酸浓度增大,反应环境中H+的量增加,有利于浸出反应进行;但硫酸浓度过大,设备腐蚀性加大,也会造成硫酸浪费,综合考虑,确定硫酸浓度以1.5 mol/L为宜。
2.2.4 过氧化氢用量对镍、钴浸出率的影响
镍钴渣料一段浸出渣质量10 g,反应温度70 ℃,反应时间2 h,硫酸浓度1.5 mol/L,液固体积质量比10 mL/1 g,过氧化氢溶液用量对镍、钴浸出率的影响试验结果如图4所示。

图4 过氧化氢用量对镍、钴浸出率的影响
由图4看出:过氧化氢溶液用量较少时,镍、钴浸出率很低;随过氧化氢用量增大,镍、钴浸出率显著提高;过氧化氢用量为2.0 mL/g时,镍、钴浸出率达最大,之后趋于稳定。三价镍、钴一般难以直接溶于低浓度硫酸中,但被还原为二价后则溶解度显著提高。综合考虑,还原剂过氧化氢溶液用量以2.0 mL/g为宜。
2.2.5 液固体积质量比对镍、钴浸出率的影响
镍钴渣料一段浸出渣质量10 g,反应温度70 ℃,反应时间2 h,硫酸浓度1.5 mol/L,过氧化氢溶液用量2.0 mL/g,液固体积质量比对镍、钴浸出率的影响试验结果如图5所示。

图5 液固体积质量比对镍、钴浸出率的影响
由图5看出:随液固体积质量增大,镍、钴浸出率显著提高;液固体积质量比增大至10 mL/1 g时,镍、钴浸出率达最大,之后趋于稳定。在硫酸浓度一定条件下,液固体积质量较小时,溶液黏度及离子浓度较大,液固相传质不充分,影响浸出反应进行;液固体积质量比增大到一定后,溶液黏度适宜,离子浓度适宜,液固相之间的传质较为充分,镍、钴浸出率达最大。综合考虑,确定液固体积质量比以10 mL/1 g为宜。
2.2.6 综合试验
根据上述条件试验结果,在最优条件下进行综合试验:取一段浸出渣,按10 mL/1 g液固体积质量比加入1.5 mol/L硫酸溶液和2.0 mL/g过氧化氢溶液进行二段浸出,在70 ℃下反应2 h。二段浸出液的主要化学成分见表5。

表5 二段浸出液的主要化学成分 g/L
由表5看出:在优化条件下,一段浸出渣中的镍、钴浸出率分别达99.56%、99.40%,浸出效果较好,且杂质浸出率非常低。
3 结论
对镍钴渣料进行两段浸出:一段用低浓度硫酸对镍钴渣料进行浸出,大部分镍进入酸浸液中而钴留在酸浸渣中;二段用硫酸/过氧化氢溶液对一段浸出渣进行还原浸出,镍、钴浸出率分别为99.56%、99.40%,浸出液中杂质含量很低。
一段浸出液中,镍和杂质离子质量浓度相对较高,钴质量浓度较低,可直接返回镍电解系统除杂,无须额外设置除杂流程;二段浸出液中杂质含量相对较低,且镍、钴质量比由渣料中的6/1降为1.5/1,只须添加少量钴盐、锰盐,即可达到镍、钴配比平衡,简单处理后即可用于制备LiNi1/3Co1/3Mn1/3O2正极材料。该工艺流程大大简化,镍、钴得到有效回收。

