氟哌噻吨美利曲辛联合认知行为疗法治疗癔球症91例分析
崔征,侯鹏飞,刘伟
癔球症属常见功能性食管病,又称咽异感症,表现为咽部非疼痛性异物感或团块感,常伴胀满、阻塞等不适感,绝经期女性多发,大多数病人存在精神因素影响,因情绪变化诱发或加重,症状持续时间长,呈反复发作特征[1]。目前尚未明确其病因病机,缺乏特异性治疗手段。已明确食管运动功能异常、胃食管反流、食管高敏状态等均与癔球症发病有关[2-3]。但较多癔球症病人进行常规抑酸、促动力学治疗后仍获益不明显[4]。近年来越来越多报道提出,精神心理因素在癔球症发病中有关键作用,可通过影响中枢神经系统、肠神经性神经反射导致咽部异物感[5-6]。故必须重视癔球症精神心理因素的干预。最新报道认为,认知行为疗法、抗抑郁药物可改善癔球症心理状态及睡眠质量[7]。氟哌噻吨美利曲辛主要成分为盐酸氟哌噻吨和盐酸美利曲辛,属典型抗抑郁药物,已被证实对轻中度抑郁及焦虑症病人抑郁、焦虑症状均有明显的改善作用[8]。但对癔球症的干预价值尚少见报道。本研究从精神心理调节的角度将氟哌噻吨美利曲辛及认知行为疗法联合用于癔球症治疗中,并与常规抑酸、促动力学治疗进行对照,探讨氟哌噻吨美利曲辛联合认知行为疗法对癔球症症状及心理状态的改善作用,以期为癔球症临床治疗提供依据。
1 资料与方法
1.1一般资料前瞻性选取2017年9月至2019年8月濮阳市油田总医院收治的182例癔球症病人。入组标准:满足癔球症罗马Ⅳ诊断标准[9];主诉持续或间歇发作咽喉非疼痛性团块或异物感;症状持续超过6个月;无胃食管反流确切症状;无吞咽困难;入组近4周内未服用抑酸剂或促胃肠动力学药物;病人及近亲属均履行告知义务;知情且自愿签署研究同意书。排除标准:咽喉、食管器质性病变;结缔组织病或甲状腺功能异常;无法配合食管测压或有食管动力学检查禁忌证,包括食管肿瘤、食管溃疡、鼻咽或食管梗阻者;食管静脉曲张;合并心肝肾肺功能器质性障碍或消化系统疾病;合并凝血功能障碍;严重脑血管疾病;对研究用药过敏者;依从性差,不能配合治疗者。按随机数字表法分为对照组与观察组每组91例。研究经濮阳市油田总医院伦理委员会审核批准(2017045)。
1.2方法两组均给予认知行为疗法。由同一心理咨询团队予认知行为干预,①与病人共同探讨不良情绪、负面心理与癔球症症状的关系,对其癔球症不适感受予肯定,理解各项症状为真实存在,取得病人信任;②告知病人个人态度、观念对情绪的调节作用及对行为的驱动作用,向病人解释认知对行为的影响作用;③纠正病人对癔球症错误认知,减少错误信念对认知的干扰,告知癔球症症状的可控性,减少病人对疾病的过度夸大反应,避免其出现灾祸性认知,减少对癔球症症状的关注;④使病人认识正性观点对心理调节的作用,纠正不良行为习惯;⑤鼓励病人改变错误思维模式及行为,建立癔球症科学、正确认知模式,引导病人认识癔球症病因及病因与配合治疗的关系,引导病人尽情宣泄,并给予安慰及鼓励,促使病人加强自我锻炼,科学、理智、积极主动克服自身性格缺陷。认知行为干预每2周1次,每次45 min,持续6周,分3阶段进行,第1~2周了解病人对于癔球症具体想法、观点,明确病人认知误区,建立针对性认知干预手段,进行解释性心理治疗,使病人及近亲属明确癔球症属功能性疾病,完全可治愈,消除病人及近亲属对疾病的疑虑,稳定其情绪,加深其对癔球症的认知程度,促使其积极配合医生治疗。第3~4周进行癔球症认知培训,使病人掌握疾病知识及心理因素对疾病的影响,指导其进行放松训练、社交锻炼、自我认知重建,转移注意力,减少对癔球症症状的关注,保持积极乐观的态度;给予暗示治疗,在安静环境下进行,详细询问病史,建立良好护患关系,在言语暗示的同时依据症状采取针对性措施,包括针刺、吸氧、注射维生素C,推注钙剂等,消除症状,使病人在心理上发生转变;配合催眠疗法,通过言语暗示,消除癔球症症状。第5~6周要求病人将认知理念转移至是实践中,合理安排饮食,戒烟戒酒,忌食刺激性食物,保持心情愉悦,积极遵医嘱,配合治疗。在此基础上对照组采用埃索美拉唑、莫沙必利等抑酸、促肠动力学治疗。埃索美拉唑(阿斯利康制药有限公司生产,批次1603127,批号J20080032,规格:20 mg×7片)口服,40毫克/次,1次/天;莫沙必利(上海新黄河制药有限公司生产,批次100806,批号H20173152,规格:5 mg×24片)口服,5毫克/次,早中晚3次餐前服用。观察组在对照组基础上加用氟哌噻吨美利曲辛(丹麦灵北制药有限公司生产,批次110649,批号H20171104,规格:0.5 mg∶10 mg×20片)治疗,口服,1片/次,早餐、午餐饭后服用。两组均持续治疗12周。
1.3观察指标以下各指标评定及检测均于治疗前、治疗12周后评估。①癔球症症状观察。采用癔球症症状评分量表(glasgow edinburgh throat scale,GETS)[10]评估,量表主要评估癔球症症状积分的变化,评分范围为0~70分,分数越高,代表癔球症症状越严重。②心理状态。采用焦虑自评量表(SAS)[11]与抑郁自评量表(SDS)[12]评估。SAS表总分超过50分视为存在焦虑,分数越高,焦虑程度越高;SDS表超过53分视为存在抑郁,评分越高,抑郁状态越严重。③睡眠质量。采用匹兹堡睡眠质量指数(PSQI)[13]评估病人近期睡眠质量,总分超过7分表示存在睡眠障碍,分数越高,表示睡眠质量越差。④食管上括约肌运动功能指标。采用胃肠道动力学测定仪(迈达公司,MedSample 360 V2.0型24通道水灌注高分辨胃肠动力监测系统)检测食管上括约肌静息压、残余压及松弛时间、松弛时程。⑤脑肠肽指标。采集外周空腹静脉血,采用酶联免疫吸附测定检测神经肽Y、P物质、降钙素基因相关肽(CGRP)等脑肠肽指标的变化。⑥安全性。记录两组治疗过程中不良反应发生情况。
1.4统计学方法采用SPSS24.0统计。计量数据行正态性及方差齐性检验满足正态性及方差齐性要求,采用±s描述,组间独立样本t检验,组内配对t检验;计数资料以率表示,χ2检验或Fisher确切概率法;Pearson相关性分析检验GETS评分与食管上括约肌运动功能指标的关系。检验水准α=0.05。
2 结果
2.1两组研究对象基本资料对比两组性别、年龄等基本资料差异无统计学意义(P>0.05),见表1。
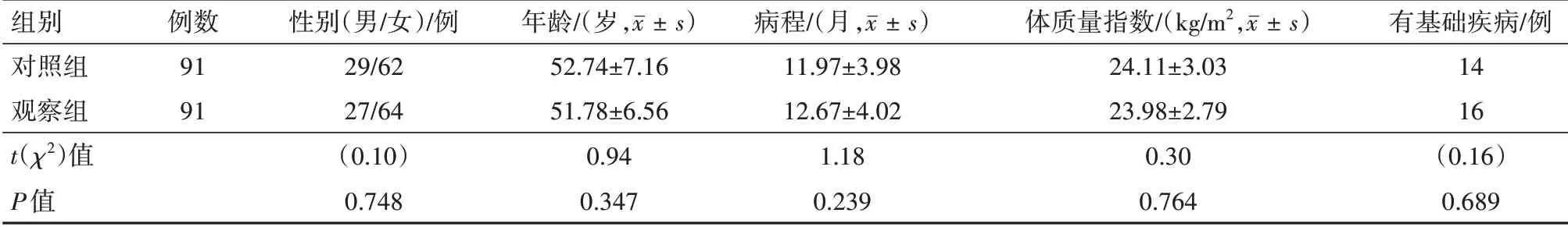
表1 两组癔球症基本资料对比
2.2两组治疗前后癔球症症状及心理状态评分的变化治疗前,两组GETS评分、SAS表及SDS表评分比较差异无统计学意义(P>0.05),治疗12周,两组以上量表评分均降低(P<0.05),观察组各评分低于对照组(P<0.05),见表2。
表2 两组癔球症治疗前后癔球症症状及心理状态评分的变化/(分,±s)
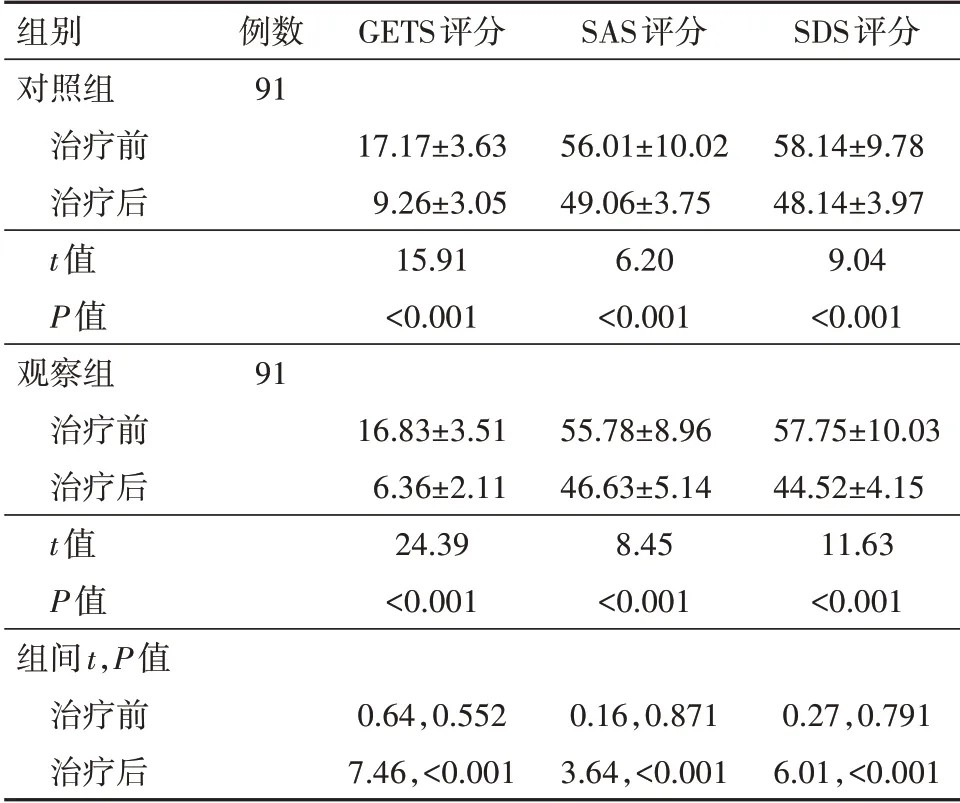
表2 两组癔球症治疗前后癔球症症状及心理状态评分的变化/(分,±s)
注:GETS为癔球症症状评分量表,SAS为焦虑自评量表,SDS为抑郁自评量表。
组别对照组治疗前治疗后t值P值观察组治疗前治疗后t值P值组间t,P值治疗前治疗后例数91 91 GETS评分17.17±3.63 9.26±3.05 15.91<0.001 16.83±3.51 6.36±2.11 24.39<0.001 0.64,0.552 7.46,<0.001 SAS评分56.01±10.02 49.06±3.75 6.20<0.001 55.78±8.96 46.63±5.14 8.45<0.001 0.16,0.871 3.64,<0.001 SDS评分58.14±9.78 48.14±3.97 9.04<0.001 57.75±10.03 44.52±4.15 11.63<0.001 0.27,0.791 6.01,<0.001
2.3两组治疗前后PSQI量表评分对比治疗前,对照组[(9.83±3.06)分]与观察组[(9.78±3.12)分]PSQI表评分比较差异无统计学意义(t=0.11,P=0.913);治疗12周,对照组[(5.23±0.78)分]与观察组[(4.71±0.65)分]PSQI表评分均较治疗前降低(t=13.90,P<0.001;t=15.18,P<0.001),观察组PSQI量表评分低于对照组(t=4.89,P<0.001)。
2.4两组治疗前后上括约肌运动功能指标对比治疗前,两组上括约肌静息压、残余压、松弛时间及松弛时程对比差异无统计学意义(P>0.05),治疗12周,两组静息压降低(P<0.05),观察组静息压低于对照组(P<0.05),见表3。
表3 两组癔球症治疗前后上括约肌运动功能指标对比/±s
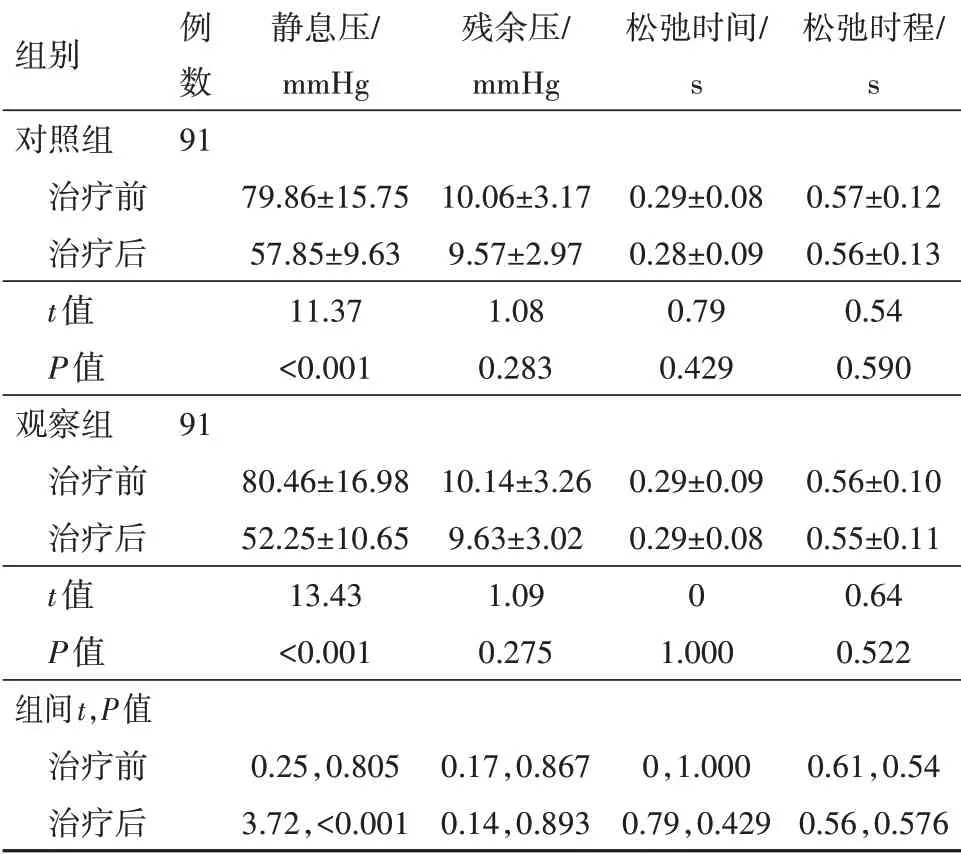
表3 两组癔球症治疗前后上括约肌运动功能指标对比/±s
组别对照组治疗前治疗后t值P值观察组治疗前治疗后t值P值组间t,P值治疗前治疗后例数91 91静息压/mmHg 79.86±15.75 57.85±9.63 11.37<0.001 80.46±16.98 52.25±10.65 13.43<0.001 0.25,0.805 3.72,<0.001残余压/mmHg 10.06±3.17 9.57±2.97 1.08 0.283 10.14±3.26 9.63±3.02 1.09 0.275 0.17,0.867 0.14,0.893松弛时间/s 0.29±0.08 0.28±0.09 0.79 0.429 0.29±0.09 0.29±0.08 0 1.000 0,1.000 0.79,0.429松弛时程/s 0.57±0.12 0.56±0.13 0.54 0.590 0.56±0.10 0.55±0.11 0.64 0.522 0.61,0.54 0.56,0.576
2.5两组治疗前后脑肠肽指标对比两组治疗前神经肽Y、P物质、CGRP等指标对比差异无统计学意义(P>0.05),治疗12周,两组神经肽Y上升,P物质及CGRP均降低(P<0.05),观察组P物质及CGRP低于对照组(P<0.05),神经肽Y高于对照组(P<0.05),见表4。
表4 两组癔球症治疗前后脑肠肽指标对比/(ng/L,±s)

表4 两组癔球症治疗前后脑肠肽指标对比/(ng/L,±s)
注:CGRP为降钙素基因相关肽。
组别对照组治疗前治疗后t值P值观察组治疗前治疗后t值P值组间t,P值治疗前治疗后例数91 91神经肽Y 640.89±55.76 706.25±50.14 8.31<0.001 635.85±50.98 780.25±30.06 23.28<0.001 0.64,0.525 12.08,<0.001 P物质887.14±98.96 750.63±49.87 11.75<0.001 890.25±102.56 665.14±98.52 15.10<0.001 0.21,0.835 7.39,<0.001 CGRP 238.96±51.79 210.89±16.25 4.93<0.001 240.05±56.56 181.15±23.63 9.17<0.001 0.14,0.892 9.89,<0.001
2.6两组治疗不良反应发生情况比较观察组出现头晕2例,嗜睡3例,胃肠道反应3例,总不良反应发生率为8.79%(8/91),对照组头晕3例,嗜睡1例,胃肠道反应2例,皮疹1例,总不良反应发生率为7.69%(7/91),两组治疗不良反应发生率比较差异无统计学意义(χ2=0.07,P=0.788)。
2.7癔球症病人GETS评分与食管上括约肌运动功能指标的相关性分析癔球症GETS评分与残余压(r=0.11,P=0.539)、松弛时间(r=0.16,P=0.386)及松弛时程(r=0.18,P=0.305)无明显相关性,与食管上括约肌静息压呈正相关(r=0.46,P<0.001)。
3 讨论
癔球症属食管运动性疾病,以持续或间歇性咽喉非疼痛异物感、哽咽感为特征,被认为属病因复杂心身疾病[14]。本研究报道,癔球症症状表现与之相似,且癔球症病人以女性居多,考虑可能与男女性格差异有关,女性内向性人格成分居多,更易产生癔球症心理问题。近年来较多报道发现,精神心理因素在食管运动功能异常及胃肠道功能紊乱中发挥重要作用[15-16]。李慧等[17]发现,癔球症病例大多数性格呈现神经敏感、内向性等特征,常伴不同程度紧张、焦虑、过度悲伤等精神异常现象。李浩、魏良洲[18]进一步研究发现,负面心理、不良情绪均可通过影响脑-肠肽轴双向连接通路,支配胃肠感觉及运动功能,产生消化系统症状。但前期针对癔球症治疗对围绕抑酸、改善胃肠道动力障碍展开,收效甚微[19]。氟哌噻吨美利曲辛系新型三环类抗焦虑、抑郁合剂,主要成分为盐酸氟哌噻吨和盐酸美利曲辛,前者可作用于突触前膜多巴胺调节受体,促进多巴胺合成及释放,增加神经突触多巴胺水平,发挥抗抑郁及焦虑效应[20];后者则可降低突触前膜5-羟色胺及肾上腺素摄取率,提高突触间隙5-羟色胺及肾上腺素含量,发挥抗抑郁作用[21]。而氟哌噻吨美利曲辛为两者复合制剂,协同作用较单药更强,已被证实可减轻功能性消化不良病人抑郁及焦虑情绪,促使其积极配合治疗[22]。但对其用于癔球症治疗中的作用鲜少见报道。
临床实践中发现,大多数癔球症病人对疾病本身知之甚少,常因身心不适症状出现焦虑、烦躁、抑郁、恐惧、担忧等情绪,不利于其治疗及康复[23]。本研究调查发现,癔球症普遍存在焦虑、抑郁情绪,获得较高的SAS表、SDS表评分,支撑上述结论;且研究发现癔球症病人睡眠质量较差,这与黄丽华、梁列新[24]调查结论相似,考虑癔球症长期焦虑、抑郁等不良情绪对其睡眠质量产生干扰。故必须重视对癔球症精神、心理因素的干预。认知行为疗法则为通过改变思维及行为方式纠正不良认知,进而达到改善负面情绪,建立正确行为的心理治疗手段[25]。前期已被证实对提高癔球症病人对疾病的认知,纠正癔球症不良心理情绪有积极的作用[26]。本研究所有病人均采用认知行为疗法,在此基础上对照组采用常规抑酸、促胃肠动力药物治疗,观察组在对照组基础上加用氟哌噻吨美利曲辛治疗,结果发现,12周后观察组焦虑、抑郁评分改善情况均优于对照组,PSQI评分改善优于对照组,癔球症症状积分降低幅度高于对照组,经过认知行为疗法、对症干预及氟哌噻吨美利曲辛治疗后,观察组病人心理状态产生正性改变,睡眠质量得到明显改善,癔球症症状发生频率降低,提示认知行为疗法基础上加用抗抑郁、焦虑药物用氟哌噻吨美利曲辛治疗对癔球症病人负面情绪有积极的调节作用,可通过纠正精神心理因素改善癔球症症状,提高病人睡眠质量。考虑通过认知行为疗法可重建病人对癔球症认知,明确精神心理因素对癔球症的影响,进而产生行为改变,促使病人形成建立乐观的态度,积极的信念,配合治疗,提高依从性,优化治疗效果;在此基础上应用氟哌噻吨美利曲辛较单受体选择性5-羟色胺再摄取抑制剂相比,对焦虑、抑郁症状改善效果更好,可改善大脑皮质功能状态,降低中枢神经系统对肠道神经系统的干扰,降低食管敏感性,提高疼痛阈值,促进紊乱食管功能恢复及睡眠质量改善,并通过纠正精神因素改善癔球症症状。
也有学者表示,食管上括约肌静息压上升与癔球症发生有关[27]。国外有报道认为,上括约肌压力恢复正常可降低癔球症症状出现频率[28]。也有观点认为,食管上括约肌运动功能状况无癔球症无明显关联[29]。本研究发现,治疗前,两组癔球症病人食管上括约肌静息压处于较高水平,高于刘杰等[30]报道的正常人,同时相关性分析证实,癔球症食管上括约肌静息压与病人GETS评分呈正相关,推测癔球症咽喉异物感症状可能与食管上括约肌静息压上升有关。但与残余压、松弛情况无明显关联,考虑可能与食管上括约肌静息压上升,造成上括约肌运动功能紊乱,可引起环咽肌痉挛,导致迷走神经兴奋性提升,反射性使咽部产生异物感、团块感。而治疗后,观察组食管上括约肌压力降低幅度高于对照组,提示加用抗抑郁、焦虑合剂氟哌噻吨美利曲辛可促进食管功能恢复,调节胃肠道运动功能,降低上括约肌静息压,有助于改善癔球症症状。脑-肠轴系统同样与癔球症精神心理因素所致胃肠道功能紊乱及食管运动异常有紧密关联。社会心理压力上升、经历生活负性事件等应激刺激均可能引起脑-肠肽分泌异常,导致中枢神经系统、肠神经性神经反射改变及脑-肠肽体内互动变化,引起脑-肠轴系统紊乱,影响胃肠感觉支配,导致食管运动异常,增加胃肠道对应激反应敏感度,导致内脏敏感性提升,诱发癔球症。本研究还发现,治疗前,两组脑肠肽指标P物质、CGRP均异常上升,神经肽Y降低,提示癔球症患病时病人脑-肠肽分泌明显紊乱,食管敏感性较高,引起皮质感觉中枢系统兴奋性提升,增加胃肠道对应激反应敏感度,造成食管上括约肌压力上升,反射性产生咽喉异物团块感。而治疗12周后,观察组P物质及CGRP低于对照组,神经肽Y高于对照组,整体脑肠肽指标改善情况优于对照组,推测加用氟哌噻吨美利曲辛可减轻精神心理因素对肠神经系统干扰,抑制5-羟色胺释放及再摄取,消除其对胃肠道及中枢神经系统刺激,促进脑-肠轴功能恢复,平衡脑-肠肽调节,纠正内脏感知高敏感状态,减轻其对食管上括约肌压力的影响,降低食管对应激刺激的敏感度,有助于改善癔球症症状。另外,两组不良反应发生率接近,提示加用氟哌噻吨美利曲辛安全性肯定,病人耐受性较高。
因此本研究建议必须重视精神心理因素在癔球症发病中的作用,以精神心理因素为导向,采用氟哌噻吨美利曲辛联合认知行为疗法较常规抑酸、促胃肠道功能等对症疗法更能改善病人癔球症症状,减轻病人焦虑、抑郁程度,促进睡眠质量恢复,减低食管上括约肌静息压,平衡脑-肠肽轴调节。

