超声引导下隐神经阻滞联合帕瑞昔布用于胫骨高位截骨术后精准镇痛的临床应用研究
李宗原 石波 唐诗添 李月 王陶 汪世坤 谢明锐 谢珂琪
胫骨高位截骨术首次由Jackson 应用于治疗膝关节骨性关节炎[1]之后,截骨保膝就被逐渐开展起来。近年来胫骨高位截骨手术发展迅速,在国内外的手术量逐年增长,与全膝关节置换手术相比,具有切口小、疼痛轻、术后恢复快等优点,但是术后早期仍存在疼痛明显的问题。目前国内外对胫骨高位截骨术式的研究很多[2-3],但对术后镇痛方面的研究甚少,若不能及时有效止痛,对病人术后心理及膝关节功能的恢复可能都会产生不良影响。术后常规镇痛存在治疗不充分、用药过多、重复、不良反应较多等问题。因此为了提高胫骨高位截骨术后的镇痛效果,且降低药物不良反应,我们设计了超声引导下隐神经阻滞联合帕瑞昔布用于胫骨高位截骨术后镇痛的临床研究,以寻找一种更好的精确镇痛方案,更合理地指导临床工作。
资料与方法
一、纳入标准与排除标准
纳入标准:①膝关节内侧间室中度骨关节炎,外侧间室无关节炎或轻度骨关节炎;②胫骨内侧平台塌陷畸形愈合,外侧关节面较平整;③接受行胫骨内侧高位截骨术的病人;④无手术禁忌;⑤病人依从性较好;⑥年龄<70岁。
排除标准:①对所用药物过敏者;②有明确的精神异常症状及长期服用精神类药物史,或曾诊断有焦虑症或抑郁症;③明显肝、肾功能不全(血转氨酶及肌酐水平超过正常上限2倍);④既往有消化道出血病史病人。
剔除标准:①不遵医嘱用药;②术后随访资料不完善者;③中途要求退出研究者。
二、一般资料
选取2020年1月至2021年3月于我院行胫骨高位截骨手术的病人,按照时间顺序进行分组研究,将病人分为三组:2020 年1 月至2020 年5 月超声引导隐神经阻滞(罗哌卡因)联合术后静脉注射帕瑞昔布者纳入A组;2020年6月至2020年10月超声引导隐神经阻滞(罗哌卡因)联合术后静脉镇痛泵(舒芬太尼)者纳入B 组,2020 年11 月至2021 年3 月术后静脉镇痛泵(舒芬太尼)者纳入C组。本研究通过我院科研项目伦理审查和学术委员会审查。
A 组 病 人60 例,男27 例,女33 例,年 龄 为(51.88±7.80)岁(48~69岁);B组病人61例,男29例,女32例,年龄为(50.30±13.46)岁(37~68岁);C组病人56 例,男30 例,女26 例,年龄为(52.63±9.10)岁(46~67岁)。三组病人的性别、年龄、左右侧别等一般资料比较,差异无统计学意义(P>0.05),具有可比性。数据分析详见表1。
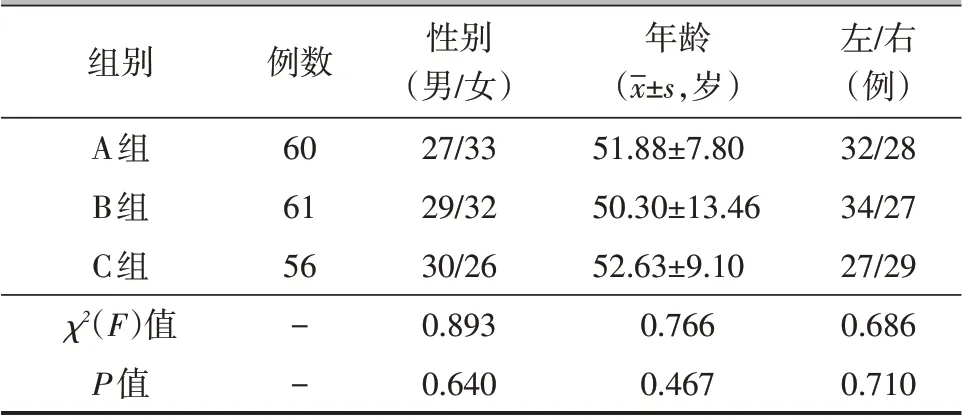
表1 3组病人基本资料对比
三、镇痛及手术治疗
(一)镇痛方法
三组病人均采用全身麻醉。A组病人于麻醉前行超声引导隐神经阻滞(1%罗哌卡因等比例稀释成0.5%罗哌卡因10 mL),穿刺点体表定位:大腿内侧中、下1/3 收肌管处[4],确定股内侧肌与缝匠肌的间隙,于此处用指端深压可出现向小腿放射的异感,即为穿刺点。术后静脉注射帕瑞昔布(40 mg/12 h)镇痛2 d。B 组病人于麻醉前行超声引导隐神经阻滞(罗哌卡因),术后安置静脉自控镇痛泵(舒芬太尼2支,共100 μg,稀释至150 mL)镇痛2 d。C组病人术后安置静脉自控镇痛泵(舒芬太尼2支,共100 μg,稀释至150 mL)镇痛2 d。
(二)手术方法
手术由同一组医师完成,病人取平卧位,全身麻醉满意后,先于关节镜下作关节清理,修整或缝合损伤的半月板,行微骨折处理软骨下骨外露。以胫骨结节内侧3~4 cm为中心,切开、显露,按照标准流程行截骨、植骨、使用TomoFix胫骨近端内侧锁定接骨板固定。术中注意顺着隐神经走行作切口,以减轻术后切口疼痛及周围麻木;使用带槽专用拉钩保护其后方的神经血管结构;在鹅足肌腱上缘(关节面下约3~4 cm)作截骨,避免损失鹅足肌腱,以减轻术后活动时的疼痛;置半管形引流条1 枚,皮内缝合切口,棉垫及弹力绷带包扎。
(三)术后处理及康复
术后患肢抬高,麻醉失效后即开始行踝泵、下肢肌肉等长收缩及床上直腿抬高训练。术后第1天开始在连续被动运动装置(CPM)辅助下练习膝关节活动度,术后第1天下床扶助行器部分负重活动,术后3~5 d 开始扶助行器完全负重活动,术后5 d 膝关节屈曲活动度达到90°以上,术后3周弃拐活动。
四、观察指标
记录病人术前、术后4 h、12 h、24 h、48 h、6 d、1 个月、3 个月、6 个月时静息及膝关节屈曲活动45°时的疼痛视觉模拟量表(visual analogue scale,VAS)评分;术前、术后24 h、48 h、6 d、1 个月、3 个月、6 个月时膝关节功能Lysholm评分;镇痛满意度评分(0~10分,0分为镇痛无效,完全不满意;10分为无痛,对镇痛完全满意);术后不良反应(恶心呕吐、消化道出血)发生情况;术后6 d 内下肢深静脉血栓发生情况。术后1、3、6个月通过门诊随访病人的膝关节疼痛情况及功能恢复情况。
五、统计学处理
采用SPSS 22.0(IBM 公司,美国)进行数据分析,计数资料组间比较采用交叉表卡方检验,计量资料按均数±标准差(±s)表示,三组间对比使用单因素方差分析(ANOVA)进行处理,采用独立样本t检验进行两两比较。P<0.05为差异有统计学意义。
结 果
所有病人均随访至术后6 个月,无失访病例。静息状态下,术后4 h、12 h,A组VAS 评分均明显低于B组和C组;术后4 h、12 h、24 h,A组、B组VAS评分均明显低于C 组;术后48 h、6 d,A 组明显低于C组,差异有统计学意义(P<0.05)。屈曲45°活动状态下,术后4 h、12 h、24 h、48 h时,A组和B组VAS评分均明显低于C组;术后6 d,A组明显低于B组和C组,差异有统计学意义(P<0.05)。术后1、3、6个月三组病人在静息状态和活动状态下,VAS 评分的差异均无统计学意义(P>0.05),见表2、3。
表2 3组病人不同时间点静息状态VAS评分对比(±s,分)
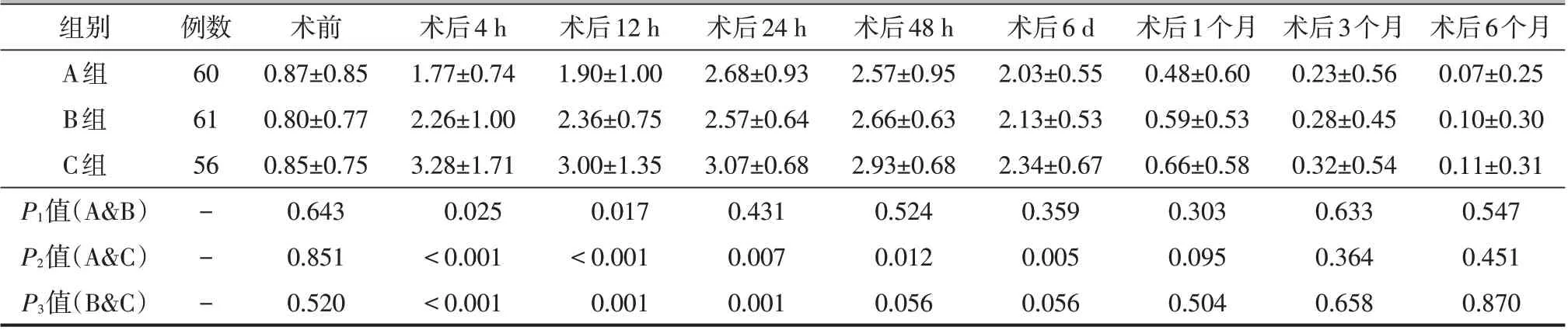
表2 3组病人不同时间点静息状态VAS评分对比(±s,分)
组别A组B组C组P1值(A&B)P2值(A&C)P3值(B&C)例数60 61 56---术前0.87±0.85 0.80±0.77 0.85±0.75 0.643 0.851 0.520术后4 h 1.77±0.74 2.26±1.00 3.28±1.71 0.025<0.001<0.001术后12 h 1.90±1.00 2.36±0.75 3.00±1.35 0.017<0.001 0.001术后24 h 2.68±0.93 2.57±0.64 3.07±0.68 0.431 0.007 0.001术后48 h 2.57±0.95 2.66±0.63 2.93±0.68 0.524 0.012 0.056术后6 d 2.03±0.55 2.13±0.53 2.34±0.67 0.359 0.005 0.056术后1个月0.48±0.60 0.59±0.53 0.66±0.58 0.303 0.095 0.504术后3个月0.23±0.56 0.28±0.45 0.32±0.54 0.633 0.364 0.658术后6个月0.07±0.25 0.10±0.30 0.11±0.31 0.547 0.451 0.870
表3 3组病人不同时间点活动状态VAS评分对比(±s,分)
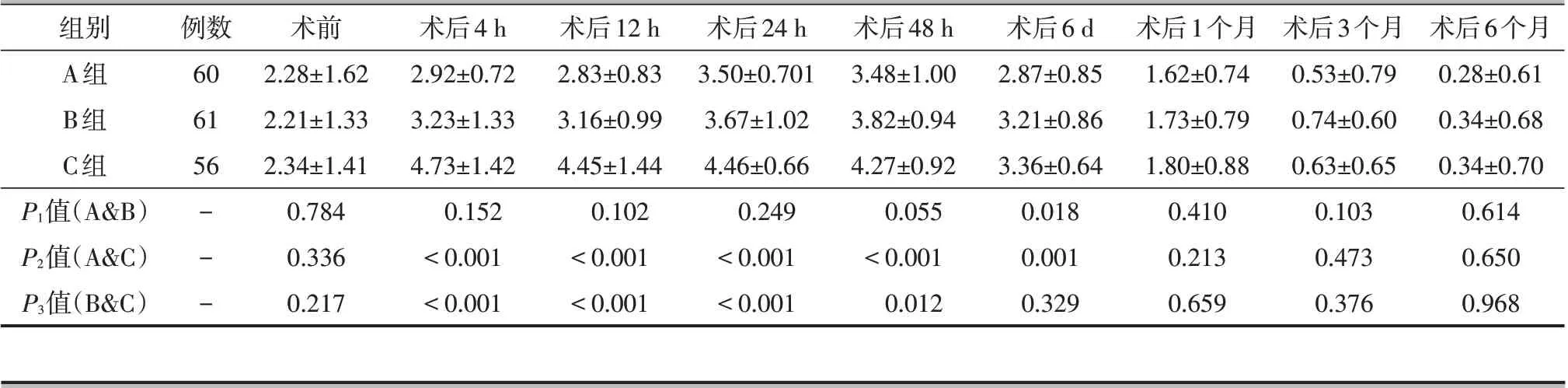
表3 3组病人不同时间点活动状态VAS评分对比(±s,分)
组别A组B组C组P1值(A&B)P2值(A&C)P3值(B&C)例数60 61 56---术前2.28±1.62 2.21±1.33 2.34±1.41 0.784 0.336 0.217术后4 h 2.92±0.72 3.23±1.33 4.73±1.42 0.152<0.001<0.001术后12 h 2.83±0.83 3.16±0.99 4.45±1.44 0.102<0.001<0.001术后24 h 3.50±0.701 3.67±1.02 4.46±0.66 0.249<0.001<0.001术后48 h 3.48±1.00 3.82±0.94 4.27±0.92 0.055<0.001 0.012术后6 d 2.87±0.85 3.21±0.86 3.36±0.64 0.018 0.001 0.329术后1个月1.62±0.74 1.73±0.79 1.80±0.88 0.410 0.213 0.659术后3个月0.53±0.79 0.74±0.60 0.63±0.65 0.103 0.473 0.376术后6个月0.28±0.61 0.34±0.68 0.34±0.70 0.614 0.650 0.968
术后24 h、48 h,A组膝关节功能Lysholm评分优于B 组和C 组;术后6 d,A 组优于C 组;术后24 h,B组优于C 组,差异有统计学意义(P<0.05),但是术后48 h,B 组与C 组的差异无统计学意义(P>0.05)。术后1、3、6 个月,三组病人膝关节功能评分的差异无统计学意义(P>0.05),见表4。
表4 3组病人不同时间点膝关节Lysholm评分对比(±s,分)
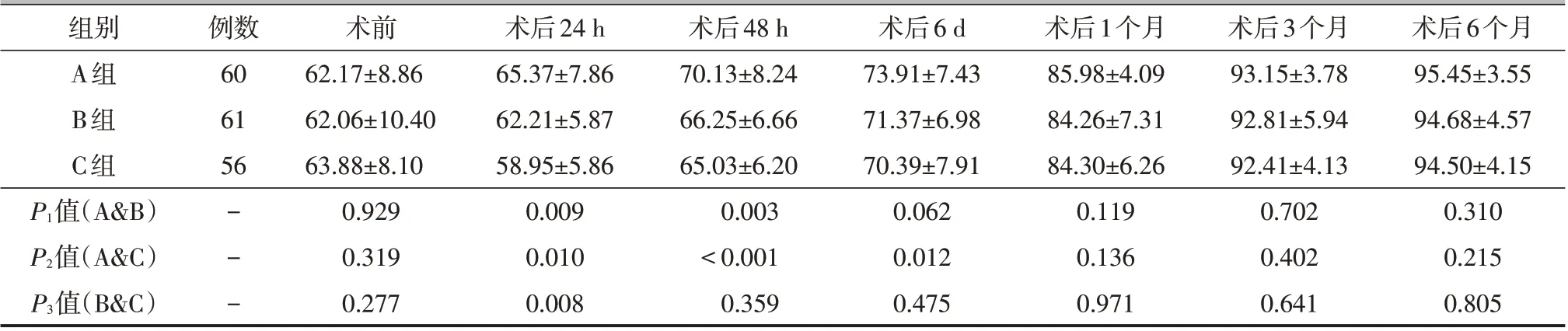
表4 3组病人不同时间点膝关节Lysholm评分对比(±s,分)
组别A组B组C组P1值(A&B)P2值(A&C)P3值(B&C)例数60 61 56---术前62.17±8.86 62.06±10.40 63.88±8.10 0.929 0.319 0.277术后24 h 65.37±7.86 62.21±5.87 58.95±5.86 0.009 0.010 0.008术后48 h 70.13±8.24 66.25±6.66 65.03±6.20 0.003<0.001 0.359术后6 d 73.91±7.43 71.37±6.98 70.39±7.91 0.062 0.012 0.475术后1个月85.98±4.09 84.26±7.31 84.30±6.26 0.119 0.136 0.971术后3个月93.15±3.78 92.81±5.94 92.41±4.13 0.702 0.402 0.641术后6个月95.45±3.55 94.68±4.57 94.50±4.15 0.310 0.215 0.805
术后3 d,A组镇痛满意度优于B组和C组,B组优于C组,差异有统计学意义(P<0.05);术后6 d,A组和B 组镇痛满意度优于C 组,差异有统计学意义(P<0.05),A 组和B 组之间的差异无统计学意义(P>0.05),见表5。A 组术后住院时间[(6.27±0.76)d]短于C组[(6.61±0.87)d],差异有统计学意义(P<0.05);A 组和B 组[(6.46±0.79)d]之间、B 组和C 组之间住院时间的差异无统计学意义(P>0.05)。
表5 3组病人术后镇痛满意度对比(±s,分)
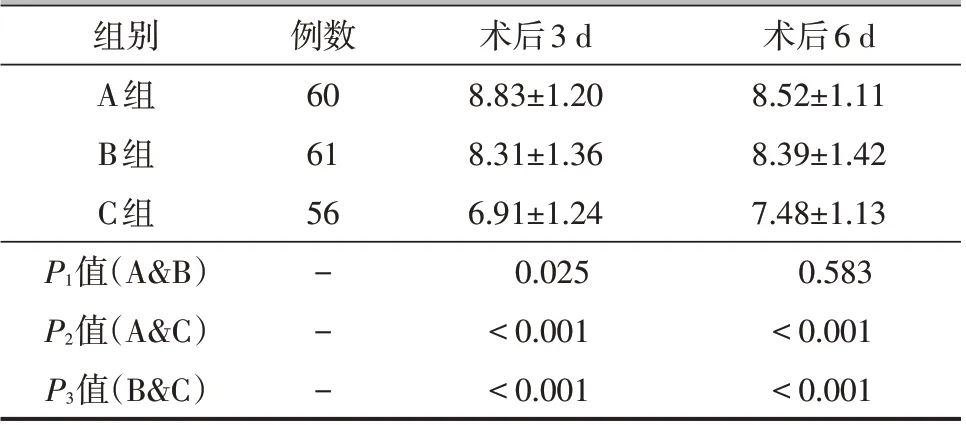
表5 3组病人术后镇痛满意度对比(±s,分)
组别A组B组C组P1值(A&B)P2值(A&C)P3值(B&C)例数60 61 56---术后3 d 8.83±1.20 8.31±1.36 6.91±1.24 0.025<0.001<0.001术后6 d 8.52±1.11 8.39±1.42 7.48±1.13 0.583<0.001<0.001
消化道并发症:A组有3例病人出现胃区不适及呕吐;B组有3例病人出现胃区不适及呕吐;C组有2例病人出现胃区不适及呕吐;三组均未发现消化道出血病例。静脉血栓出现情况:A组有5例病人出现肌间静脉血栓,1 例出现肌间静脉及腓静脉血栓;B组有6例病人出现肌间静脉血栓,1例出现胫后静脉血栓;C组有6例病人出现肌间静脉血栓,3例出现肌间静脉及腓静脉血栓。三组病人在消化道和静脉血栓并发症方面的差异无统计学意义(P>0.05)。
讨 论
近年来,人们对镇痛的需求日益增加,术后有效镇痛成为医生亟待解决的问题。目前外科术后镇痛主要参考世界卫生组织的癌症三阶梯镇痛治疗原则,主要是全身用药,存在治疗不充分,用药非个体化,药物作用部位及用药量不精确等问题。传统的非甾体抗炎药增加术后出血概率,而多数阿片类镇痛药物镇痛时间短,需反复用药,不良反应呈剂量依赖性等,都给术后镇痛治疗提出新的挑战。
一、静脉镇痛泵及椎管内麻醉镇痛的优势与不足
静脉自控镇痛泵虽然可以持续镇痛,且可以根据个体需求调整用药,但是镇痛泵留置时间不能太长,且费用较高。麻醉后早期使用镇痛泵,病人易出现恶心呕吐、头晕头痛、尿潴留、低血压、呼吸抑制等并发症[5-6]。本组研究中接受胫骨高位截骨的病人,年龄普遍较大,各组织器官的老化使机体疼痛敏感性增强,且心血管类疾病病人较多,血流动力学较不稳定,手术的安全性较低。传统上手术常采用腰麻或腰硬联合椎管内麻醉,虽然短期的麻醉镇痛效果较好,但由于下肢交感神经的节前纤维受到阻滞,容量血管和阻力血管被迫扩张,引起其他相应的神经兴奋,干扰了血流动力学的变化,使得病人术后出现头痛、恶心、呕吐、静脉血栓等并发症的可能性增加[7]。
二、超声引导下隐神经阻滞联合帕瑞昔布的精准性
隐神经阻滞在早期主要依靠解剖标志及阻力消失法定位,这些盲探的方式有较高的失败率,神经刺激器辅助的外周神经阻滞虽能通过观察是否会引起所支配肌肉收缩以明确穿刺针与目标神经的关系[8],但隐神经为纯感觉神经,受刺激仅产生麻木感,这种方法不能得到广泛应用。股神经高位阻滞虽然也可满足对下肢前侧手术的镇痛,但对股四头肌肌力影响很大,影响术后功能锻炼。
超声定位技术可为神经阻滞操作者提供清晰的解剖图像,为神经阻滞精确定位,且药物的扩散过程可动态观察[9],提高了神经阻滞的成功率及镇痛效果[10],超声引导的隐神经阻滞多在大腿远端1/3 处采用缝匠肌下入路[4],因为在这个水平收肌管处最容易在超声下找到隐神经[11]。利多卡因镇痛持续时间较短,而使用罗哌卡因行神经阻滞,具有浓度低、容量高、阻滞效果确切、安全性高的特点[12]。
与传统的椎管麻醉镇痛方式相比,神经阻滞可显著降低对病人机体整体的影响与干扰,有利于血流动力学的稳定,减少病人术后并发症的发生[13],其应用价值在臂丛神经及坐骨神经已得到较广泛证实,研究表明神经阻滞可以获得与硬膜外阻滞相似的镇痛效果[14]。
高选择性的隐神经阻滞对股四头肌肌力影响很小[15],便于病人早期活动,可以预见隐神经阻滞在临床上将会得到越来越多的应用普及。本研究中胫骨高位截骨切口正好为隐神经支配区域,但隐神经较细小,无明显且固定的体表定位标志。超声引导下行隐神经阻滞可以提高阻滞的成功率及镇痛效果,降低穿刺相关并发症。
良好的精准镇痛有利于改善病人的就医体验,便于病人功能锻炼,也有利于血流动力学的稳定,减少不良反应发生。
三、帕瑞昔布镇痛的优点
帕瑞昔布钠是强效特异性环氧合酶2(COX-2)抑制剂戊地昔布的前体药物[16],作为一种COX-2选择性的非甾体抗炎镇痛药,具有良好镇痛作用,相对于非选择性非甾体抗炎镇痛药,还可以减少胃肠道、凝血功能及肾功能的不良反应,在胃肠及肝胆外科已有较多的应用[17],在骨科的髋、膝关节置换中也开始有应用报道[18-19],但未查见有应用于胫骨高位截骨的报道。单次静注帕瑞昔布钠40 mg后,约10 min起效,并于2 h内达到最大效果,止痛时间6~12 h,甚至更长[20],常规给药每天2次,术后应用可以明显减轻手术后疼痛和阿片类药物的使用量。
四、隐神经阻滞联合帕瑞昔布镇痛的优点
胫骨高位截骨术后疼痛因素有切口的疼痛,肌腱、韧带、骨组织损伤产生的无菌性炎症,局部血肿、积液引起的不适。单纯应用中枢性或非甾体类消炎药物,效果不佳。
隐神经阻滞联合帕瑞昔布镇痛,符合多模式镇痛原则。联合应用不同作用机制的镇痛药物或多种镇痛方法,由于每种药物的剂量减少,相应的副作用也随之降低,不同药物之间的作用相加或协同,从而使效应/副作用比达到最大。本组研究结果显示,术后6 d内,隐神经阻滞联合帕瑞昔布镇痛,其VAS评分以及膝关节功能Lysholm 评分均明显优于单纯使用镇痛泵组。帕瑞昔布不仅镇痛,还有消除炎症作用。隐神经阻滞联合帕瑞昔布镇痛使得病人术后早期疼痛轻,功能康复快。且总体用药少,不良反应少,镇痛花费相对较低。
五、术中微创操作对术后疼痛的影响
减轻疼痛的措施,当然不能局限于使用镇痛药物。术中微创操作也能起到很大的作用,有时甚至起到关键性的作用。术中注意顺着隐神经走行作切口,减轻对隐神的损伤,这样就可以降低术后切口疼痛及周围麻木;另外在鹅足肌腱上缘(关节面下约3~4 cm)作截骨,避免损失鹅足肌腱,以减轻术后活动时鹅足肌腱牵拉所致的疼痛。
六、长效的神经阻滞药物与长效COX-2选择性非甾体抗炎镇痛药的应用前景
目前常规的镇痛药物代谢半衰期均较短,罗哌卡因神经阻滞有效镇痛时间也就9~17 h[21],若是隐神经阻滞药物有效镇痛时间能达到48 h以上,则完全可以达到和替代镇痛泵的效果,这样可以降低镇痛费用,也能降低镇痛泵带来的不良反应。若是COX-2选择性的非甾体抗炎镇痛药的有效镇痛时间能进一步延长,可以明显降低非甾体抗炎镇痛药用量和给药频次。
七、小结
本研究使用超声定位行隐神经阻滞降低了操作难度,提高阻滞效果,联合帕瑞昔布钠镇痛可显著提高镇痛效果,降低药物不良反应,缩短病人住院时间,实现快速康复,提高整体治疗效果。本研究所采用的方法较简单,所需研究费用较低,便于推广,产生良好的社会效益。当然本研究仍存在不足,病例数较少、随访时间短,故有待进一步积累病例并做长期随访观察。

