儿童类化妆品微生物检查方法学研究
杭 婧,邢海艳
(淮安市食品药品检验所,江苏 淮安 223300)
与成人相比,婴幼儿皮肤有以下特点:更薄更柔弱,皮脂少,低pH值平衡的能力,更易干燥,黑色素含量低,高光敏度[1]。婴幼儿皮肤屏障较脆弱,生活在同样的环境中,在同样的刺激因素作用下,婴幼儿比正常成人皮肤更易出现敏感症状[2];对婴幼儿的皮肤刺激会进一步导致皮肤通透性提高,从而引起微生物的二次入侵[3]。微生物还可能产生毒素,导致皮肤感染, 严重的会诱发败血症[4]。我国现行的2015年版《化妆品安全技术规范》[5](以下简称《规范》)中允许使用的防腐剂有51种,除去三岁以下儿童禁用的3种防腐剂后,仍有48种。防腐剂通过作用于微生物的细胞膜、细胞壁和酶等多个靶点, 破坏细胞分裂,抑制细菌生长和繁殖[6]。微生物检验通过在培养基中加入卵磷脂或聚山梨酯80,中和化妆品中的防腐剂等抑菌物质。但实际生活中化妆品防腐剂多种多样,添加防腐剂的浓度各不相同,因此很难保证防腐剂和其他抑菌成分被有效中和,从而出现化妆品中的微生物检测项目很少超标现象。因此,本文参考USP34版中防腐剂体系对微生物的抑杀效果试验[7]和中国药典2020年版中微生物限度检查方法进行适用性试验[8]。选取目前市场中使用功效上常见的儿童用化妆品:清洁类1种、保湿类2种、爽身类1种、防晒类2种,进行微生物方法学研究,通过进行方法适用性试验,中和或消除化妆品内防腐剂等物质的抑菌作用,旨在真实反映产品微生物污染情况。
1 仪器与材料
1.1 仪器
BCM-1600A洁净工作台(苏州安泰空气技术有限公司);101-3电热恒温鼓风干燥箱(上海跃进有限公司);SPX-350型生化培养箱;MLS-3781L-PC型高压蒸汽灭菌锅(松下);BagMixer 400CC均质器(法国Interscience);HTY-2000B集菌仪(杭州泰林生物技术设备公司);BSC-1304IIA2生物安全柜(苏州安泰空气技术有限公司);PL6001电子天平(梅特勒公司);BHS-6水浴锅(JOANLAB)。Waters 2695/2998高效液相色谱仪(美国Waters公司);戴安U3000高效液相色谱仪(美国赛默飞公司);Waters Symmtery C18(2.1 mm×250 mm,5 μm),资生堂CAPCELL PAK MG ⅡC18色谱柱(4.6 mm×250 mm,5 μm),Millipore超纯水机(美国Millipore公司),0.45 μm有机系针筒式微孔滤膜(上海安谱公司)。
1.2 试验样品
试验样品信息、标识防腐剂类型及含量见表1。
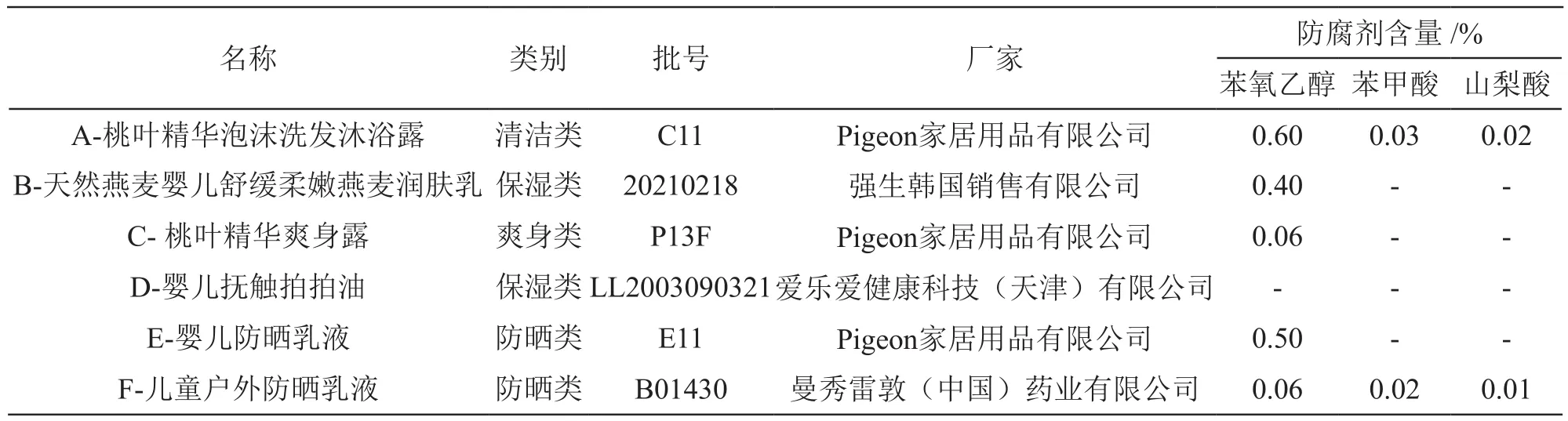
表1 样品信息、标识防腐剂的类型及含量
1.3 菌株
金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]、铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]、枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501]、白色念珠菌(Candida albicans)[CMCC(F)98001]、黑曲霉(Aspergillusniger)[CMCC(F)98003]、大肠埃希菌(Escherichia coli)[CMCC(B)44102],以上菌株来自中国食品药品检定研究院。
1.4 培养基与试剂
卵磷脂-吐温80营养琼脂(批号:1090181),孟加拉红(虎红)琼脂(批号:1096661)、SCDLP液体培养基(批号:1087061),双倍乳糖胆盐(含中和剂)培养基(批号:1080131)、Baird-Parker琼脂基础(批号:1092405)、溴化十六烷基三甲铵琼脂培养基(批号:1081171)、伊红美蓝琼脂培养基(批号:1091601),以上培养基规格均为250 g;卵黄亚碲酸钾增菌液(批号:6108128),以上培养基和试剂均来源于广东环凯微生物科技有限公司。0.9 %无菌氯化钠注射液(250 ml:2.25 g,江苏淮安双鹤药业有限公司,批号:200514 2C),吐温80(CP,国药集团化学试剂有限公司,批号:20190812),液体石蜡(AR,国药集团化学试剂有限公司,批号:20200616)。磷酸(麦克林试剂公司),色谱纯乙腈(德国,默克公司),色谱纯甲醇(德国,默克公司)。苯甲酸、苯氧乙醇、山梨酸(中国食品药品检定研究院,纯度均大于99.0 %)。
2 方法
2.1 菌液制备
选取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的三代新鲜培养物,用0.9 %无菌氯化钠溶液采用十倍稀释法将上述菌种制成每l ml含菌数小于100 cfu的菌悬液。
2.2 供试液制备
按照《规范》进行供试液制备。样品A和样品C:各吸取 10 ml 加至 90 ml灭菌生理盐水中,混匀后,制成1:10的检液。样品D:取样品 10 ml,先加5 ml灭菌液体石蜡混匀,再加10 ml灭菌的吐温80,于40~44 ℃水浴中振荡混匀10 min,加入灭菌的生理盐水 75 ml,于40~44 ℃水浴中乳化,制成 1:10悬液。样品B、E、F称取 10 g,加10 ml灭菌液体石蜡,10 ml吐温 80,70 ml灭菌生理盐水,使用均质器均质3~5 min,充分混合,制成 1:10检液 。
2.3 微生物计数方法适用性试验
2.3.1 常规法:① 试验组 取供试液10 ml加入2.1中制备的5种试验菌液0.1 ml,混匀,使每1 ml供试液中含菌量≤100 cfu,每皿加1 ml含菌供试液,倾注15~20 ml卵磷脂吐温 80 营养琼脂培养基,琼脂冷却凝固后倒置平皿,置36 ℃培养48 h,霉菌和酵母菌浇注15~20 ml虎红培养基,置 28 ℃培养 5 d,同时均设空白对照。② 菌液组 用稀释液代替供试液,按上述①组步骤加入5种试验菌液并进行微生物回收试验。③ 供试品对照组 取制备好的供试液,用稀释液替换5种菌液,其余步骤同①组。参考《中国药典》2020年版四部,回收比值=(试验组菌落数-供试品对照组菌落数)/菌液对照组菌落数。5种试验菌回收比值在0.5~2,符合方法适用性试验要求。若试验组菌落数减去供试品对照组菌落数的值小于菌液对照组菌落数的50 %,可采用培养基体积稀释的方法、加中和法、薄膜过滤法等方法[8]。
2.3.2 中和剂法 用含0.1 mol/L的氯化镁中和剂的无菌氯化钠制成1:10供试液 ,增加中和剂对照组:取含0.1 mol/L氯化镁稀释液10 ml加入2.1项中制备的5种试验菌液0.1 ml,混匀,浇注适宜的卵磷脂吐温80 营养琼脂培养基和虎红培养基,其余组别同常规法。
2.3.3 培养基稀释法 试验组 分别取供试液0.5,0.2 ml/皿加入5种试验菌液,混匀,其余操作同常规法。若回收比值低于50 %,可采用薄膜过滤法等方法。
2.3.4 薄膜过滤法 ① 试验组 取按2.2项制备的1:10供试液1 ml加入50 ml稀释液中,再加入小于100 cfu试验菌菌悬液,进行薄膜过滤。用0.9 %无菌氯化钠溶液分3次进行冲洗,每次冲洗100 ml。抽干并取出滤膜正面朝上贴于相应的培养基并按规定温度进行培养。② 菌液组 取2.1项菌悬液1 ml加入50 ml稀释液中,进行薄膜过滤。用0.9 %无菌氯化钠溶液分3次进行冲洗,每次冲洗100 ml。抽干并取出滤膜正面朝上贴于相应的培养基并按规定温度进行培养。③ 供试品对照组 取1:10供试液1 ml加入50 ml稀释液中,进行薄膜过滤。用0.9 %无菌氯化钠溶液分3次进行冲洗,每次冲洗100 ml。抽干并取出滤膜正面朝上贴于相应的培养基并按规定温度进行培养。
2.4 控制菌方法适用性试验
2.4.1 常规法 ① 耐热大肠菌群(10 ml/管):取1:10样品10 ml,分别接种于2管10 ml双倍乳糖胆盐(含中和剂)培养基,其中一管不加大肠埃希菌作为阴性对照组,另一管加入≤100 cfu的大肠埃希菌作为试验组。② 金黄色葡萄球菌(90 ml/瓶):取1:10样品10 ml,分别接种于两瓶90 ml的SCDLP培养基中,其中一瓶不加金黄色葡萄球菌作为阴性对照组,另一瓶加入≤100 cfu的金黄色葡萄球菌作为试验组。③ 铜绿假单胞菌(90 ml/瓶):取1:10样品10 ml,分别接种于90 ml的SCDLP培养基中,其中一瓶不加铜绿假单胞菌作为阴性对照组,另一管加入≤100 cfu的铜绿假单胞菌作为试验组。
2.4.2 稀释法 铜绿假单胞菌(200 ml/瓶):取1:10样品供试液10 ml,分别接种于两瓶200 ml的SCDLP培养基中,其中一瓶不加铜绿假单胞菌作为阴性对照组,另一瓶加入≤100 cfu的铜绿假单胞菌作为试验组,置36 ℃培养24 h,划线于十六烷三甲基溴化铵琼脂培养基,置36 ℃培养24 h,观察结果。金黄色葡萄球菌(200 ml/瓶):取1:10样品供试液10 ml,分别接种于两瓶200 ml的SCDLP培养基中,其中一瓶不加金黄色葡萄球菌作为阴性对照组,另一瓶加入≤100 cfu的金黄色葡萄球菌作为试验组,置36 ℃培养24 h,划线于Baird Parker培养基,置36 ℃培养24 h,观察结果。
3 结果与分析
3.1 微生物限度回收率
以中国药典2020年版中各试验菌回收比值在0.5~2为参考标准,样品A中金黄色葡萄球菌直到采用薄膜过滤法时,金黄色葡萄球菌以及枯草芽孢杆菌回收率达到要求,可见样品A代表的儿童发用沐浴类抑菌性较强,对5种试验菌均有较强的抑菌作用;采用现行标准的常规法难以检出目标菌,现行儿童化妆品微生物检验标准有待优化。采用培养基稀释法(0.2 ml/皿)对样品B进行需氧菌试验,常规法对霉菌和酵母菌总数进行试验。样品D采用中和剂法时,白色念珠菌的回收率符合要求,故采用常规法对样品D进行需氧菌试验,中和剂法对霉菌和酵母菌总数进行试验。样品E采用培养基稀释法(0.2 ml/皿)时,铜绿假单胞菌回收率达到回收率要求。故采用培养基稀释法(0.2 ml/皿)对样品E进行需氧菌试验,常规法对霉菌和酵母菌总数进行试验。样品C和样品F采用常规法进行实验时,5种试验菌回收率均可达到50 %以上,故样品C和样品F可采用常规法(1 ml/皿)进行需氧菌总数、霉菌和酵母菌总数的计数检查。结果见表2。

表2 计数方法适用性试验回收率/%
3.2 控制菌检查方法适用性
结果见表3。样品B、样品C、样品E、样品F采用常规法进行控制菌(耐热大肠菌群10 ml/管、金黄色葡萄球菌90 ml/瓶、铜绿假单胞菌90 ml/瓶)方法学验证时,试验菌均可检出:双倍乳糖胆盐(含中和剂)发酵管产酸产气,伊红美蓝琼脂培养基(EMB)上呈紫黑色圆形且带金属光泽的菌落,革兰染色为G-短杆菌,靛基质试验呈阳性结果,阴性对照组均无菌生长,可见样品B、C、E、F可采用常规法(10 ml/管)进行耐热大肠菌群试验。样品A采用90 ml/瓶进行金黄色葡萄球菌进行实验时,试验菌未生长,培养基体积增加至200 ml/瓶时,检出金黄色葡萄球菌:SCDLP培养基浑浊生长,Baird Parker平板上呈黑色圆形菌落,周围有浑浊带,其外层有透明带,革兰染色为G+球菌呈葡萄串状排列,甘露醇发酵试验和血浆凝固酶试验均呈阳性反应,阴性对照组均未长菌,可见样品A可采用培养基稀释法(200 ml/瓶)进行金黄色葡萄球菌试验。样品D采用90 ml/瓶进行铜绿假单胞菌实验时,试验菌未生长,直到采用200 ml/瓶时,检出铜绿假单胞菌:SCDLP培养基浑浊生长,十六烷三甲基溴化铵平板上呈灰白色菌落,周围蓝绿色素扩散,革兰染色为G-短杆菌,氧化酶试验和绿脓菌素试验均呈阳性反应,阴性对照组均未长菌,可见样品D可采用培养基稀释法(200 ml/瓶)进行铜绿假单胞菌试验。

表3 控制菌方法学研究结果
4 讨论
样品A对5种试验菌均有不同程度的抑菌作用,其中金黄色葡萄球菌采用前四种验证方法时回收率均为0,表明其对G+球菌有很强的抑菌作用;样品B和E对G-杆菌有抑菌作用;样品D中白色念珠菌采用中和剂法回收率可达到回收标准,表明中和剂可提高样品中真菌类微生物生长,减少假阴性结果出现。此结果与文献[9-10]报道一致,由样品A的结果可见,中和剂法并未明显提高样品霉菌和酵母菌的试验回收率,此处考虑与中和剂对不同的防腐剂中和效果不同有关。结果表明,用目前的化妆品法定方法并不能全部检出样品内的微生物,故需要进行方法优化,抑菌性低的样品采用稀释法、中和剂法,抑菌性高的样品采用薄膜过滤法或几种方法联用,提高阳性检出率,降低儿童使用化妆品感染微生物的风险。
传统的化学防腐剂抑菌效果好,如苯氧乙醇有广谱抑菌性,特别是对于铜绿假单胞菌有较好的灭菌效果[11],这也一定程度解释了样品A、B、E对铜绿假单胞菌有不同程度的抑菌作用。目前市场上,各种儿童护肤产品愈发丰富,同时出现很多“防腐剂零添加”“天然植物成分”的儿童用化妆品来吸引消费者。儿童化妆品中防腐剂的成分和含量,与抑制微生物能力之间的关联有待进一步研究。本研究可对目前儿童化妆品市场的抽样检验及市场监管提供参考。

