合成MRI与传统定量方法对T1、T2弛豫值测定的模体验证对比研究
刘雅文,牛海军,尹红霞,郑作锋,任鹏玲,张婷婷,,赵鹏飞,吕晗,王振常,*
作者单位:1.北京航空航天大学生物与医学工程学院,北京 100191;2.北京航空航天大学生物医学工程高精尖创新中心,北京 100191;3.首都医科大学附属北京友谊医院放射科,北京 100050;4.北京市垂杨柳医院放射科,北京 100022
定量磁共振成像(quantitative magnetic resonance imaging,qMRI)技术是随着精准磁共振成像的发展而出现的一种成像技术,可以提供人体组织物理特性的定量信息,是目前国际MRI应用研究的前沿。狭义上的qMRI 技术指对弛豫时间进行定量,主要包含对纵向弛豫时间(longitudinal relaxation time,T1)和横向弛豫时间(transverse relaxation time,T2)的测量。通过对T1、T2 等人体组织成分固有参数值的测量,可以准确区分不同的组织类型,为临床诊断提供重要依据[1-2]。
目前已有多种技术用于弛豫时间的定量计算,传统的T1 Mapping成像技术使用基于饱和恢复法和反转恢复法对T1 值进行定量,T2 Mapping 主要使用基于单回波的自旋回波序列或多回波的快速自旋回波序列[3-4]。各种定量技术各有优点和局限性,通常情况下,为了获得更准确的定量值,需要进行多次序列扫描或者在同一个序列下改变参数得到更多的信号值以便进行拟合计算,但是这样会使单次扫描的时间大幅增加,不利于在临床中的推广应用。因此,在定量原理和基础序列之上衍生出多种快速定量成像技术。
目前,合成磁共振成像技术和磁共振指纹成像是两种主要的快速同步定量成像技术[5-6]。其中,基于动态多回波(multiple-dynamic, multiple-echo,MDME)序列的合成MRI技术是一种全新的qMRI采集方式,可以通过一次采集获得包含T1 Mapping 和T2 Mapping 在内的多种定量和对比度图像。MDME 序列包含两个重复的数据采集阶段,第一阶段使用片选饱和脉冲进行层面选择,第二阶段通过激励脉冲和多个重聚焦脉冲对另一个层面进行多回波自旋回波采集,最终通过多回波和不同的饱和延迟进行T1 和T2的定量估计。在生成定量图像后,可以通过任意改变回波时间(echo time,TE)和重复时间(repetition time,TR)值以获得不同对比度的图像,便于临床应用[7-8]。针对合成MRI获得的加权图像,目前已有研究表明,其在不同部位和疾病的诊断中与传统扫描序列图像的诊断价值相当,具有较好的应用前景[9-11]。除此之外,合成MRI 的扫描时间较短,使得这一技术有望在常规临床扫描中得到应用[12]。
但是,相较于合成MRI 的应用研究,目前对合成MRI 的定量测定准确性评估及与传统定量技术对比的验证研究较少,而准确性又是qMRI 方法得以发展的前提和关键,将会影响其在定量研究中的应用和推广[13-15]。因此,本研究针对3.0 T MR设备,对灰质、白质、脑脊液模体采用合成MRI 和传统定量技术对T1 和T2 弛豫时间进行重复定量测定,对比研究合成MRI在定量研究中的准确性和可重复性。
1 材料与方法
磁共振模体采用万东公司配制的磁共振人体组织仿真模体:灰质(gray matter,GM)模体(圆柱形,型号WD-TP001,内部填充水1000 g,六水合氯化镍0.25 g,琼 脂 糖9.6 g 和 山 梨 酸 钾0.1 g),白 质(white matter,WM)模体(圆柱形,型号WD-TP002,内部填充水1000 g,六水合氯化镍0.50 g,琼脂糖11 g和山梨酸钾0.1 g),脑脊液(cerebrospinal fluid,CSF)模体(圆柱形,型号WD-TP003,内部填充水1000 g,五水硫酸铜0.02 g)。三个模体内部填充的物质较为均匀。
1.1 MR扫描及序列参数
MRI设备采用GE 3.0 T Pioneer,配备数字环绕技术体线圈和头颈联合线圈,进行合成MRI和传统定量成像。使用GE 设备中的动态多回波序列(magnetic resonance image compilation,MAGiC)进行合成磁共振图像采集,具体扫描参数如下:TE1=18.3 ms,TE2=91.4 ms;TR=4000 ms;扫描野=220 mm×220 mm;矩阵=320×256;回波链长度=16;层厚=5 mm;层间距=1 mm;三个模体可同时扫描,从上至下扫描20层,扫描时间为4 min 30 s。T1 Mapping的扫描序列为快速自旋回波序列,反转时间(inversion time,TI)取6 个不同的值,分别设置为50、100、200、500、1000 和2500。其他扫描参数如下:TR=4000 ms,TE=7.8 ms,层厚=5 mm,矩阵=192×160;依次扫描三个模体,每个模体扫描5层,覆盖模体中间区域,用时共计约10 min。T2 Mapping采用基础自旋回波序列,依次预扫描三个模体,设置TR=5000 ms,层厚=10 mm,层间距=2.5 mm,矩阵=128×128,回波时间分别设置为20、40、60、80、100、120、180、240、300、400、500、1000 ms,用时共计约10 min。
1.2 T1和T2的计算方法
基于MDME 序列的合成MRI 通过设置两个回波时间和4个延迟时间来获取原始图像,并通过最小二乘法拟合计算出T1 和T2 定量图,定量拟合计算公式见式(1)[16-17]:
其中,S 是信号强度,A 为常数,α 是翻转角,θ 是饱和翻转角。
本研究中的传统T1拟合计算方法基于Barral等[18]提出的T1计算方法:
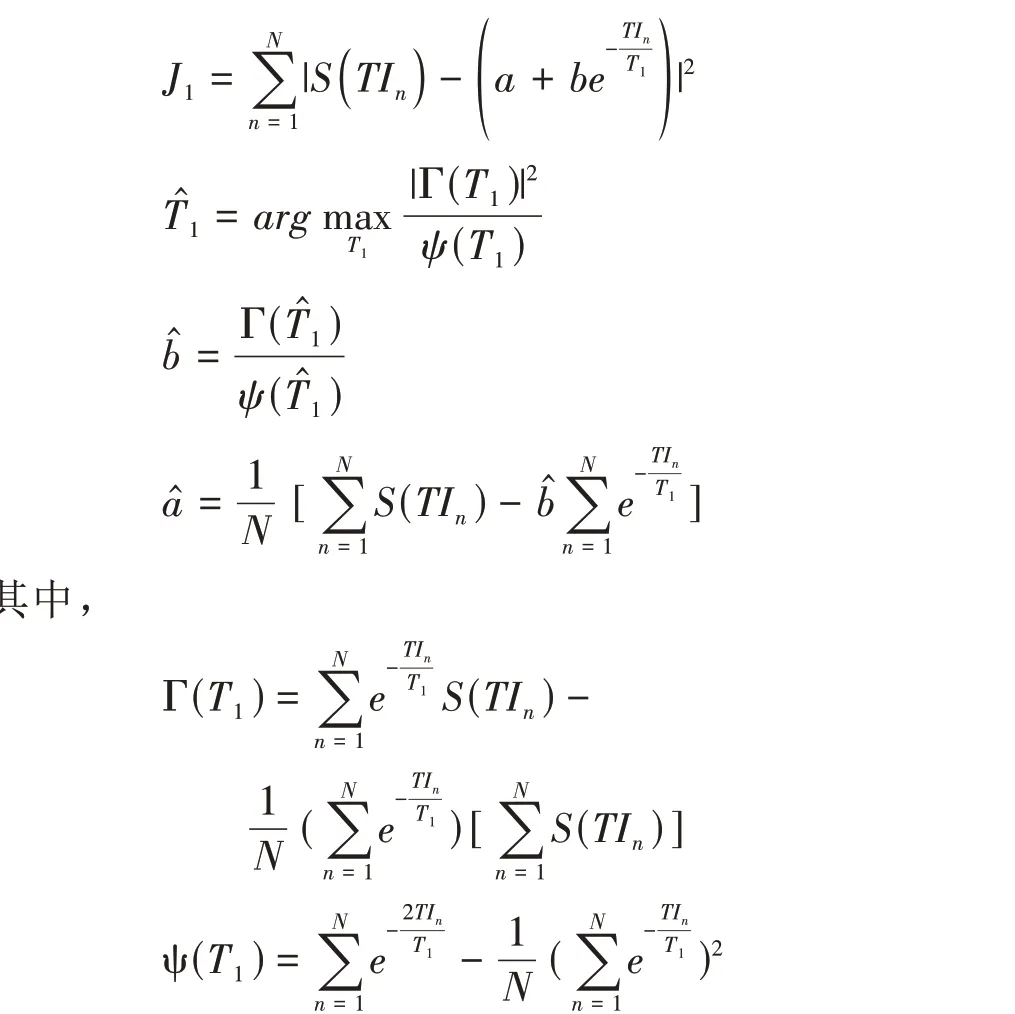
N 是采样点的个数,TIn是不同的反转时间,â、b̂、T̂1分别是复数数据和T1的估计值。
对于传统的T2 曲线拟合,通过最小化Blcoch 方程对不同回波时间的信号强度进行最小二乘拟合:

S = K·[H]·(1 -e-TR T1)·e-TE T2
其中,[H]为组织的质子密度,K 为常数,S 为整体信号强度,当TR >>T1 时,e-TR T1接近于0,即可由最小二乘法拟合计算出T2值。
1.3 模体实验
为了验证合成MRI 技术对T1、T2 弛豫定量测定的准确性,本研究除进行合成MRI 序列扫描外,还基于基础磁共振序列和T1、T2 拟合测定方法对模体进行扫描。共扫描四次,每次至少间隔半天,每次扫描前模体处于静置状态,扫描中环境温度和模体温度基本不变。
合成MRI扫描时将模体进行组合,整体放置在头线圈中进行,采用GE 公司提供的专用MAGiC 后处理软件[19]进行图像重建,在重建过程中无错误记录。在重建后的第十层图像上进行感兴趣区的选取和勾画,感兴趣区形状为方形,大小尽可能覆盖模体的成像区域,软件自动计算得到T1 和T2 值并记录。每例的后处理时间约为2 min。
传统T1 Mapping 扫描时将模体进行组合,整体放置在头线圈中进行,T1 定量图的计算和生成在MATLAB 平台下完成,每例的计算时间约为1 min,计算完成后得到T1定量图及其阈值范围。对计算得到的T1 定量图,选取第三层图像,使用ImageJ 软件(version 2.0.0,http://imagej.net)的ROI 选取和测量功能,测得不同组织模体在相同ROI 下的T1 值并记录。
传统T2 Maping 依次扫描GM、WM、CSF 模体,使用手动预扫描模式对不同回波时间下的信号强度进行测量和记录。根据T2 拟合公式在MATLAB 平台下进行计算,得到T2值及指数拟合曲线图。
1.4 统计学分析
采用GraphPad Prism 9.1.1 软件进行统计学分析,P<0.05 表示差异具有统计学意义。对测得的T1和T2值,以传统定量计算结果为金标准,计算合成MRI与传统定量计算结果的差值。使用Bland-Altman分析对传统定量计算和合成MRI 定量计算的结果进行一致性评估。双因素重复测量方差分析用于测量传统定量计算和合成MRI 定量计算的结果的差异和四次重复实验之间的可重复性。
2 结果
合成MRI 和传统定量计算得到的T1,T2 及二者差值显示除CSF 的T1 值之外,误差基本在20%以内(表1)。

表1 合成MRI和传统定量计算的T1,T2值及误差Tab.1 T1 and T2 value of synthetic MRI and conventional mapping methods
合成MRI 和传统定量计算方法得到的定量值的Bland-Altman 图如图1 所示。所有的数据点均在95%的一致性范围内。图2 为四次重复测量下合成MRI 和传统定量计算方法的折线图,其结果经过Sidak 多重比较检验。统计结果表明,对于T1 值计算,两种定量计算方法差异无统计学意义(F=0.113,P=0.7537),并且四次测量之间差异也无统计学意义(F=0.613,P=0.4968);同样地,两种方法计算的T2 值之间差异无统计学意义(F=0.001,P=0.9737),四次测量之间差异无统计学意义(F=1.162,P=0.3498)。计算方法对T1 和T2 值的影响不会随着时间的变化而变化,二者之间不存在交互作用(分别为F=1.187,P=0.3560;F=0.797,P=0.5190)。
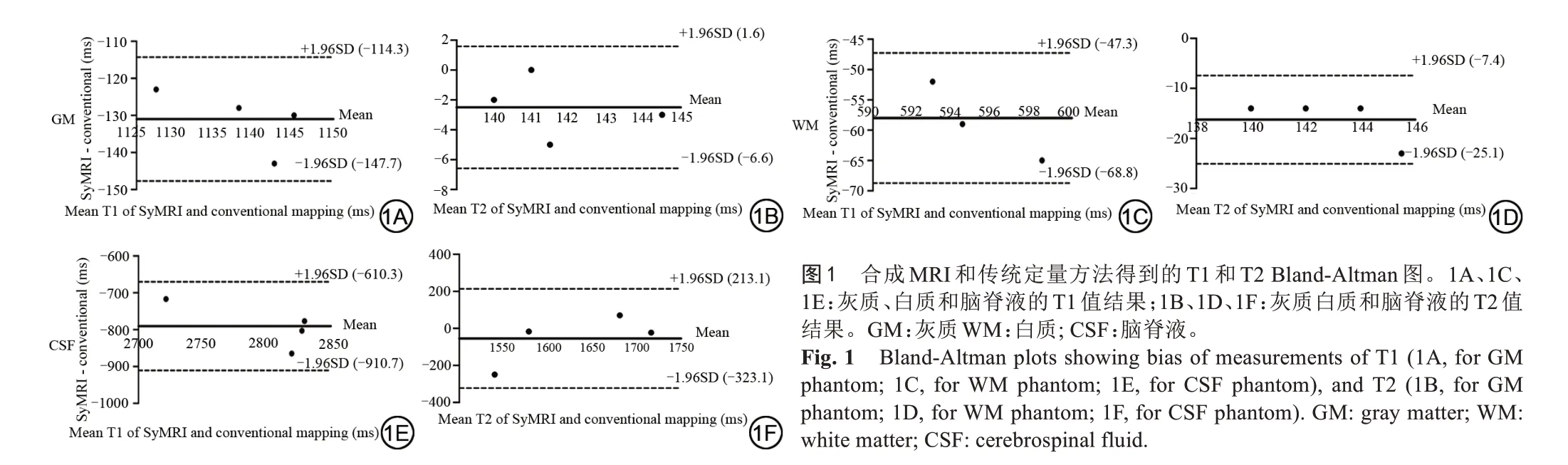

图2 合成MRI和传统定量方法重复测量结果的折线图。2A:T1值的结果;2B:T2值的结果。Fig. 2 Synthetic line charts of MRI and conventional quantitative methods for repeated measurements. 2A: result of T1 value; 2B: result of T2 value.
3 讨论
本研究针对3.0 T MR 设备,采用合成MRI 序列和传统定量成像技术分别对灰质、白质、脑脊液三个模体进行四次重复扫描,并采用MAGiC后处理软件和传统T1、T2拟合计算方法进行定量计算,观察传统拟合方法和合成MRI定量计算的结果的差异及稳定性。研究结果表明,重复测量下的合成MRI和传统拟合的T1 和T2 值差异无统计学意义,合成MRI 下弛豫值定量计算表现出较好的稳定性和可重复性,且操作更为简便,这为合成MRI序列及其定量计算的临床应用和推广提供了初步支撑。
3.1 T1、T2值的测定方法的比较
传统的弛豫定量已在全身多个部位的扫描及鉴别诊断中有了一定的应用。T1 定量在心脏及脑部中的应用较多,如Matthew等[20]比较了两种常用的T1定量方法的细胞外容积测量稳定性,Daniel 等[21]使用T1定量方法获得了正常人从婴儿期到成年的T1弛豫时间,但是,即使采用快速T1 定量方法,单次扫描时间也近3 min。对于T2 定量,Kim 等[22]比较了两种T2 定量方法在膝关节软骨中的应用,David 等[23]将T1和T2定量用于肝脏纤维化的检测和分期。传统的T1 和T2 定量方法类型多样,通常以延长扫描时间为代价获得更精确的参数定量,使其无法在临床中广泛应用。与传统的定量成像技术相比,合成MRI序列参数设置简单,可实现一次扫描多种成像,极大缩短了扫描时间,在得到定量图之后,还可以通过任意改变TE 和TR 值,得到不同的加权图像,为临床提供丰富的影像信息。在本文研究中也体现了合成MRI 弛豫定量的高效性,传统方法需对两个弛豫值分开测定,合成MRI的扫描仅需5 min内即可同时获得T1和T2值。因此,采用合成MRI进行弛豫值测定更便于在临床中应用和推广。
3.2 T1、T2值的测定准确性及可重复性的比较
在应用合成MRI 技术进行定量研究方面,Hagiwara 等[24-25]的相关研究表明,从MDME 序列中得出的定量值总体上是稳定的,且组织的弛豫值和大脑体积会随着年龄的变化而改变,这有助于进行大脑疾病的诊断。Xu 等[1]在同一台机器上进行了两次扫描,初步验证了集成MRI 定量测定的可重复性。Kang等[26]研究了不同参数设置对合成MRI弛豫测定的影响。除了2D的MDME序列,也诞生了基于3D-QALAS序列的三维定量合成磁共振序列,其被用于心脏成像中T1 和T2 的同步定量,并在心脏和具有不同组织特性的模型中显示出高精确度和准确性[27-28]。但是,已有研究多是基于临床验证或单一使用合成MRI 技术的重复性验证。本研究使用模体进行验证,对比传统定量方法和合成MRI 技术弛豫值技术的准确性和可重复性。差值计算的结果显示,两种方法计算得到的T2 值差值较小,CSF 的T1 值的差值较大,超过了20%,这可能是因为实验中所用的CSF 模体基本为纯水,其T1 弛豫时间绝对值非常大(2000~3000),接近弛豫曲线的顶部,合成MRI 和传统T1 扫描在这个区域取点稀疏,拟合误差大。除此之外,实验所用的MDME 序列是为分析真实脑组织而开发的,机器中搭载的MDME序列可能没有针对不同弛豫特性的材料进行充分的优化,从而对计算结果产生一定的影响[24]。但是,Bland-Altman 图和重复测量方差分析表明两种测量方法间差异无统计学意义。综合研究结果表明,合成MRI在定量成像方面具有与传统定量成像方法相当的水平,为下一步合成MRI技术的推广应用和提高打下了坚实的基础。
3.3 局限性
本研究仍存在以下局限性:首先,研究仅使用了单中心的单一磁共振机器,因弛豫定量受环境等因素较大,不同机器在应用时需要再单独进行验证。其次,本研究中仅使用了模体进行验证,虽然排除了个体差异的影响,但同时也缺乏临床验证,需增加研究对象进一步进行验证。此外,研究中的扫描参数相对固定,尚不清楚不同扫描参数对弛豫定量的计算是否有影响,需要进一步设计实验方案,使验证更加全面。
总之,本研究通过在模体上的对比验证表明,在T1 及T2 弛豫值测定中,合成MRI 扫描计算方法与传统定量拟合计算方法具有同等效力,且扫描参数设置简单,有利于临床开展相关定量研究。合成MRI应用能极大提高qMRI的可操作性和应用性。
作者利益冲突声明:全体作者均声明无利益冲突。

