分子靶向药物对中晚期肝细胞癌疗效的系统综述与Meta 分析
朱陈倩,蒋素文,胡爱荣,张露侃
原发性肝癌包括肝细胞癌(HCC)、肝内胆管癌和肝细胞癌肝内胆管癌混合型,位居我国恶性肿瘤致死原因第2 位,其中HCC 占85%~90%[1]。各种原因导致的肝硬化是HCC 发生过程中最重要的环节,85%~95%HCC 具有肝硬化背景[2]。乙型肝炎病毒感染相关肝硬化患者HCC 年发生率为3%~6%,是我国HCC 的首要病因[3]。外科手术是肝癌分期(CNLC)Ia、Ib 及IIa 期首选治疗方法,但因患者大多有肝硬化基础,或者在确诊时大部分已达中晚期,能获得手术切除机会的患者仅20%~30%;且患者术后5 年的复发转移率高达40%~70%[4]。对不符合手术切除适应证的进展期肝癌或肝癌复发,选择分子靶向药物或分子靶向药物联合治疗方案,可延长患者的总体生存时间[5]。本研究旨在通过Meta分析评价分子靶向药物对中晚期HCC的疗效,报道如下。
1 资料与方法
1.1 检索策略 计算机搜索知网数据库(CNKI)、万方数据库、维普数据库(VIP)、中国生物医学文献服务系统(SinoMed)、PubMed、考克兰图书馆(Cochrance Library)、Embase、中国临床注册试验中心(http://www.chictr.org.cn)及美国临床注册试验中心(https://clinicaltrials.gov)相关的数据,根据分子靶向药物使用年限,检索时限为2017 年1 月1 日至2021 年10 月1 日。中文检索词包括:肝癌、原发性肝癌、肝内胆管癌、原发性肝细胞性肝癌、靶向、分子靶向、索拉非尼、仑伐替尼、随机对照、随机及RCT;英文检索词包括:neoplasms hepatic、neoplasms liver、liver neoplasm、neoplasm liver、hepatic neoplasms、hepatic neoplasm、neoplasm hepatic、cancer of liver、liver cancer、hepatocellular cancer、cancers hepatocellular、hepatocellular cancers、hepatic cancer、cancer hepatic、cancers hepatic、hepatic cancers、molecular targeted-drugs、molecular targeted drugs、molecular targeted therapy、molecular targeted therapies、targeted therapy molecular、therapy molecular targeted、targeted molecular therapy、molecular therapy targeted、targeted molecular therapies、therapy targeted molecular、sorafenib、lenvatinib、randomized controlled trial、randomized、placebo。采用Google Scholar、百度文库等搜索引擎。检索的所有文献均使用Noteexpress 格式导出,用Noteexpress(3.2.0)进行查重、去重以及阅读摘要剔除。
1.2 纳入和排除标准 纳入标准:(1)研究类型:单独分子靶向药物或分子靶向药物联合其他治疗方案与非分子靶向药物治疗,包括肝动脉化疗栓塞术(TACE)、常规化疗方案、免疫节点抑制剂(ICIs)、立体放射治疗等,治疗中晚期HCC 的Ⅱ或Ⅲ期随机对照试验(RCT)。(2)研究对象:病理学检查确诊的中晚期肝癌患者,肝功能为Child-Pugh 评分A或B 级,肾功能及造血功能良好。(3)干预措施:实验组和对照组分别为分子靶向药物单独治疗或分子靶向药物联合其他治疗、非分子靶向药物治疗(包括TACE 治疗和ICIs 治疗)。(4)评价指标:根据世界卫生组织制定的改良版实体瘤疗效评价标准(mRECIST)对肿瘤的控制情况进行疗效评价。主要结局指标为半年、1 年、2 年及3 年的生存期(OS),OS 定义为患者自治疗开始至末次随访或死亡的时间。次要结局指标包括客观缓解率(ORR)和无进展生存期(PFS)以及常见不良反应。疗效分为完全缓解(CR)、部分缓解(PR)、进展(PD)及稳定(SD)4 个等级;ORR=(CR +PR)/总例数×100%。PFS 定义为患者自治疗开始至肿瘤进展或随访丢失或死亡的时间。排除标准:(1)非随机临床对照试验如Ⅰ期临床试验、综述等文献;(2)无法提供研究数据或者完整研究方案的文献;(3)其他不符合本研究纳入标准者;(4)动物试验。
1.3 文献筛选与数据提取 由2 名研究者独立完成文献筛选,若遇到意见分歧,需讨论或交由第三方裁定。首先对检索的文献进行剔重,然后通过阅读标题和摘要进行初步筛选,进一步查阅可能符合纳入标准的文献全文,仔细阅读后进行筛选。对最终纳入的文献进行资料提取,包括作者、发表年份、试验方法、纳入数据的年龄、性别、疾病客观缓解例数、不良反应及对照组治疗方案等。
1.4 文献质量评价 采用Newcastle-Ottawa Scale(NOS)量表进行质量评价,评价标准包括研究人群选择、组间可比性及结果测量,满分为9 分,≥6 分为高质量,<6 分为低质量[6]。纳入分析文章均为高质量文章。
1.5 统计学处理 直接Meta 分析运用Revman 5.3 进行数据处理,结局指标为分类资料,故采用优势比(OR)及95%可信区间(95%CI)为效应指标,P <0.05 为差异有统计学意义。通过Q 检验、I2检验确定纳入文献是否存在异质性[7]。若I2<50%且P >0.1,认为纳入文献具有同质性,选用固定效应模型进行Meta 分析;若I2>50%或P<0.1,则认为纳入文献存在异质性,选用随机效应模型进行Meta 分析。
2 结果
2.1 基本特征 共检索相关文献591篇,经查重、剔除不符合标准等筛选,最终纳入22 篇[8-29],17 篇中文文献,5 篇英文文献;累计患者3782 例,对照组为ICIs治疗1228 例,TACE治疗1271 例。所有文献NOS≥7 分。
2.2 OS分析 22 篇文献均比较了OS,各个组别存在异质性(I2=42,P <0.1)。其中半年及2 年OS 组内间均无异质性(OR半年=2.36,95%CI 1.67~3.35,P >0.1;Z=4.85,P <0.05;OR2年=2.49,95%CI 1.89~3.28,P >0.1;Z=6.52,P <0.05),分子靶向药物治疗组半年OS 及2 年OS 有明显升高。1 年及3 年OS 组内间存在异质性,查找异质性来源,发现1 年OS中Sanger等[27]和3 年OS中Hidaka等[29]这2 篇文献存在异质性,为使结果更客观准确,故剔除存在异质性的2篇文章(OR1年=2.14,95% CI 1.78~2.57,P >0.1;Z=8.12,P <0.05;OR3年=2.83,95% CI 1.56~5.13,P >0.1;Z=3.42,P <0.05)。Meta 分析结果显示,对于半年、1 年、2 年及3 年OS,单独分子靶向药物治疗或分子靶向药物联合治疗对中晚期HCC 的改善作用优于对照组(OR=2.29,95% CI 2.00~2.62,P >0.1;Z=11.96,P <0.05)。见图1。
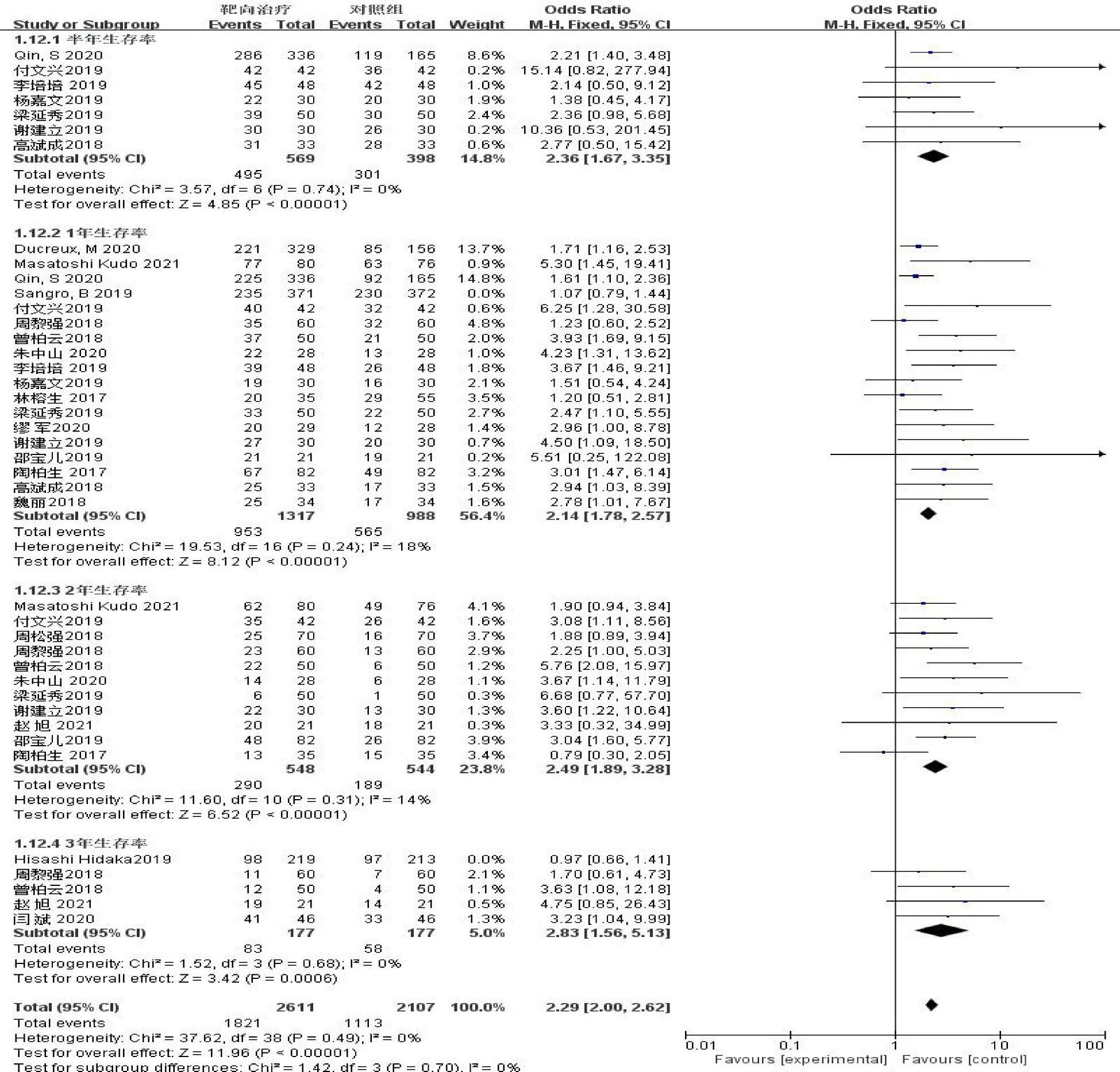
图1 观察组与对照组对OS 影响的森林图
2.3 ORR 分析 15 篇文献[9,12-24,27]进行了ORR的分析,两个组别之间无异质性(I2=0,P>0.1),分子靶向药物的应用大大增加了中晚期HCC 的ORR(OR=2.51,95% CI 2.00~3.17,P >0.1;Z=7.84,P <0.05),见图2。
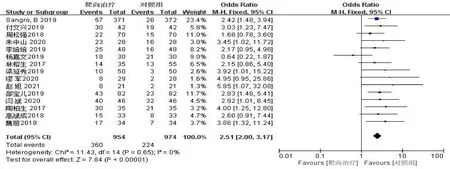
图2 观察组与对照组对ORR 影响的森林图
2.4 PFS分析 4 篇文献[23,25-27]进行PFS的分析,4 篇文献有异质性(I2=76,P <0.1)。异质性较大,使用随机效应模型分析,寻找异质性来源,发现Sanger等[27]这篇文献异质性来源最高,且因为其他3篇文献质量较高,且文献数较少,为保证数据完整性,故只剔除1 篇文献进行分析。分子靶向药物的应用延长了患者的PFS(MD=3.40,95%CI1.91~4.89,P <0.1;Z=4.48,P <0.05),见图3。
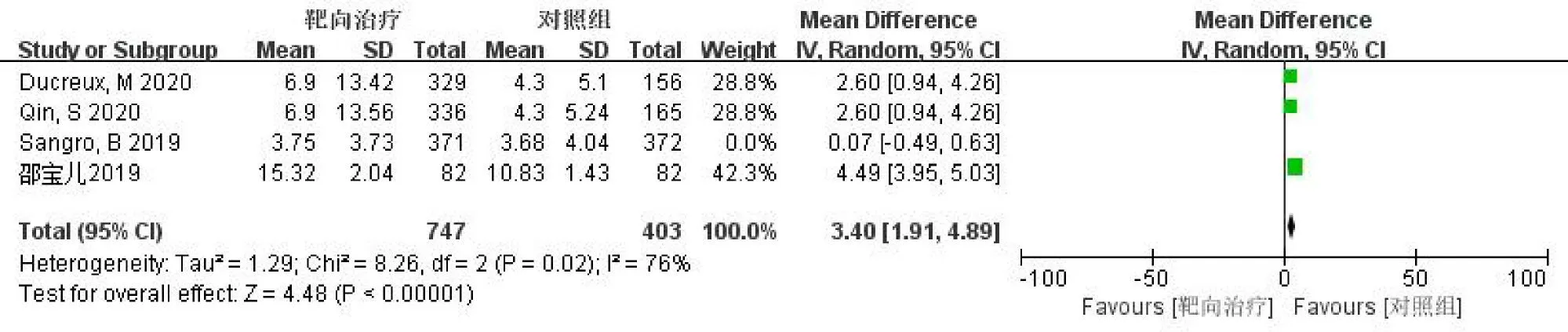
图3 观察组与对照组对PFS 影响的森林图
3 讨论
Meta分析结果显示,单独分子靶向药物治疗或与其他药物(治疗方法)联合使用(如联合TACE)可显著延长中晚期HCC 患者的OS 和PFS,增加ORR。两项著名的全球性试验SHARP 研究[30]和ORIENTAL 研究[31]的结果均显示,一线分子靶向药物索拉非尼在改善不可切除和晚期HCC 患者OS 方面的有效性。分子靶向药物索拉非尼最常见的治疗相关不良反应包括高血压、蛋白尿、手足皮肤反应及出血等[1],以及腹泻、体质量减轻、疲劳和厌食等[30,32]。这些非特异性不良反应可能与疾病本身及患者的全身状态相关,由于这些非特异性不良反应而导致索拉非尼停药的可能性较小[31]。
在纳入分析的22 篇文献中,大部分观察组的靶向药物为索拉菲尼,而缺乏另一个一线药物仑伐替尼作为观察组的随机对照研究,这可能与仑伐替尼上市不久有关。2018 年一项仑伐替尼与索拉菲尼对比的非劣效性临床试验的研究显示[33],仑伐替尼的中位OS 为13.6 个月,而索拉菲尼为12.3个月;仑伐替尼的PFS为7.4 个月,而索拉菲尼为3.7 个月;仑伐替尼的ORR 为24.1%,而索拉菲尼为9.2%。因此,仑伐替尼于2018 年9 月在我国获批用于晚期HCC 的一线治疗。有关仑伐替尼单药或联合其他药物(治疗方法)的研究尚在进行中(NCT03713593、NCT03905967 及NCT04127396 等)[34]。通过文献的阅读与分析,尽管目前对于中晚期HCC 的治疗有了新的进展和成效,但仍有许多领域需要进一步的探索,如现阶段的分子靶向药物联合ICIs、一线分子靶向药物仑伐替尼联合TACE 等其他治疗方式的组合,需要更多的临床研究来证实。

