人工湿地在农业面源污染治理中的应用研究进展
张 琦 周 洲,2 贾 丽 梁振明 郑 玥
(1.中国电力工程顾问集团华北电力设计院有限公司,北京 100120; 2.北京师范大学环境学院,北京 100875)
面源污染又称为非点源污染,它是指污染物在不固定的排放点,通过径流方式汇入水体从而引起水体恶化的污染[1-2]。农业面源污染的污染源主要来自农田、农村生活污水、畜禽养殖废弃物等,其中污染物主要有含氮物质、含磷物质、重金属、农药等。陈文英等人[3]的研究表明农业面源污染已经成为地表水污染主要原因,因此对农业面源污染研究和治理已经成为水处理领域关注的重点。
人工湿地模拟了天然湿地生态系统,利用物理、化学、生物的作用降解污染物,其主要作用机理包括过滤、吸附、沉淀、植物吸收和微生物分解[4]等。目前,人工湿地按照水流方向分为地表流湿地、潜流湿地、垂直流湿地和潮汐流湿地,其中地表流湿地和潜流湿地应用最为广泛[5]。
人工湿地在农业面源污染治理中的应用起源于20世纪70年代,具有投资少、效益好、运行管理方便、抗面源负荷冲击能力强等优点,在农业面源污染治理中应用广泛,如杨扬等人[6]对洱海湖滨地区农业非点源污染控制示范研究中,采用植物碎石床人工湿地系统对农业面源污水进行处理,在高负荷下COD、TN和TP去除率分别能达到83%~97%、50%~87%和78%~84%。虽然人工湿地能够很好的去除污染物,但运行效果受季节影响较大,研究表明夏季污染物去除效果明显高于冬季。
本文从污染物降解途径来研究人工湿地的应用,包括氮循环、磷循环、重金属去除和农药的降解四个方面。通过研究人工湿地中污染物降解机理,可以在农业面源污染治理中更好的设计和管理人工湿地。
1 农业面源污染物的迁移、转化和降解
1.1 氮循环与含氮物质降解
水体中含氮污染物主要来自地表水径流、农业回流、排水沟渠、生物固定和大气的干湿沉降等,其中农业径流是导致下游水体氮污染的主要方式。水体中氮类污染物形态主要包括硝态氮、铵态氮和有机氮(溶解态和颗粒态),具体含量受矿化速率、土壤性质和化肥使用情况的影响[7],相关调查结果表明面源污染水体中氮含量以硝酸盐为主,有机氮和氨氮的含量相对较少,而人工湿地中硝酸盐的降解效率大于有机氮和氨氮的降解效率[8],因此人工湿地是对农业面源污染中硝酸盐进行削减控制的最佳选择。
氮类物质在人工湿地的循环如图 1所示,其主要的去除机制为微生物对硝酸盐的反硝化作用,即在无氧条件下(其氧化还原电位约250 mV),硝酸盐可在微生物作用下向N2O和N2转化[9],这一反应过程主要在氧化还原电位低的厌氧土壤层中进行;此外,人工湿地中氮类物质还会通过沉积、矿化、颗粒物吸附以及植物和微生物的同化进行去除[10]。向地下水浸出也是硝酸盐的一种去向,但是这一过程可能引起地下水硝酸盐含量超标,因此在人工湿地建设过程中做好地下水防渗十分有必要。
在人工湿地中,反硝化过程是去除硝酸盐重要途径,会受溶解氧浓度、硝酸盐浓度、沉积物有机质浓度、温度、植被的覆盖率等因素的影响[12];在表面流湿地中,反硝化速率还受水体和缺氧土壤层的混合程度影响。许多对人工湿地反硝化的研究报道均证实了上述影响,如位于美国伊利诺伊州尚佩恩县的人工湿地反硝化原位测量结果所示[11],4~25℃环境下的反硝化速率范围为2~11.8 mg N/(m2·h),当环境温度上升至11~27 ℃范围时,人工湿地的反硝化速率范围会随之提高至12~63 mg N/(m2·h);位于美国加利福尼亚州河滨县的多功能示范湿地二次改造效果表明,挺水植物生物量的减少和深水区域的增加会将反硝化速率从0.29 mg N/(m2·h)上升至14.92 mg N/(m2·h),总N去除率可增加32%[12]。反硝化速率在人工湿地中差异的原因多样,可根据进水水质情况和环境条件进行最优设计。
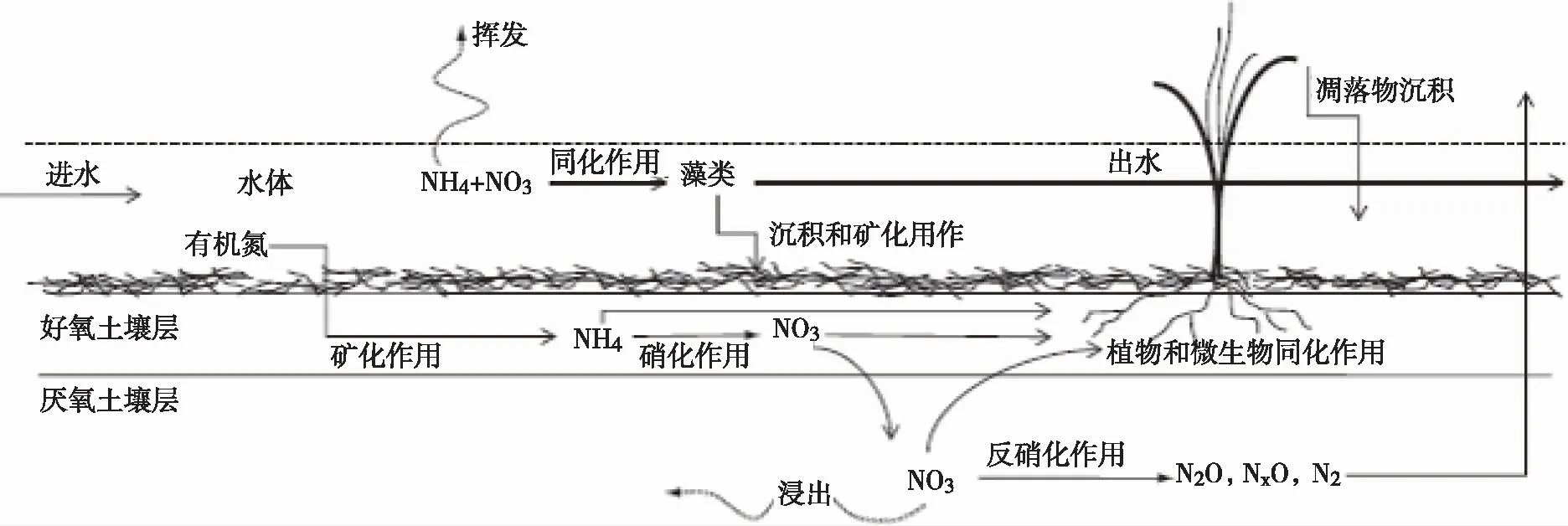
图1 人工湿地中的氮循环[11]
1.2 磷循环与含磷物质降解
氮、磷污染是引起水体富营养化主要原因,其中农业面源磷污染逐渐成为流域水体富营养化的主要磷源之一[1]。人工湿地可通过设置强化净化系统、种植高效除磷水生植物等方式去除含磷物质[13-14]。在农业流域,进入湿地水体中的含磷物质赋存形式通常包括微粒无机磷 (PIP)、微粒有机磷 (POP)、溶解无机磷 (DIP)和溶解有机磷 (DOP),这些含磷物质在人工湿地的循环如图2所示,其主要的去除途径为物理沉积、化学沉淀和吸附以及生物的体内存储,在无防渗人工湿地中,磷与周围水体(如地下水)的交换对磷的去除也起着重要影响[15]。
颗粒磷随悬浮颗粒沉淀是传统湿地磷去除的主要过程,湿地土壤会成为磷的主要去向[16]。磷在人工湿地中的沉积会受到土壤pH和氧化还原电位的影响,当土壤呈中性至酸性并且含有大量Fe和Al氧化物或者碱性钙氧化物时,湿地土壤对磷的吸附能力显著增强;而土壤的氧化还原电位则是会影响土壤的固磷能力[17]。此外,湿地土壤-水交界面天然金属氧化层也会影响土壤向水体释放磷的过程,其中Fe的还原和溶解及其在该氧化层的重结晶都对水中的磷有强吸附的作用[18]。近些年来,含金属基质在人工湿地中的应用可以明显提高湿地去磷效果[19],基质中的金属离子可吸附和沉淀可溶性磷酸盐形成微溶的金属结合-P,如钢渣、建筑垃圾、石灰石、页岩等[20],同时,羟基质子化的农业生物质、热处理或化学处理的农业生物质也表现出不俗的磷吸附能力[21-22],可为农业面源污染控制的人工湿地设计提供新思路。
通过生物作用是将磷从人工湿地系统去除最有效方式,通过植物和微生物的吸收和同化将无机磷合成ATP等储存于生物体内[23],再通过植物收割被带出湿地系统。在农业流域,磷主要以颗粒形式从耕地输送至湿地[24],然后以沉积物和有机颗粒物质形式留存于湿地系统中;颗粒形式的磷需经过转化才能进行生物利用[25],而人工湿地存在的浅水区、悬浮沉积物的短沉降时间、厌氧土壤层和波动的水文周期便可为其转化提供条件,如沉积过程中便可需通过Eh/pH过程(如氧化铁溶解)和动力学过程(如解吸附和有机磷矿化)促进颗粒磷向溶解性磷转变[26]。
湿地中磷循环是一个复杂的过程,研究人工湿地对无机磷的高效去除机理,才能更好利用人工湿地降低农业面源带来的磷污染影响。
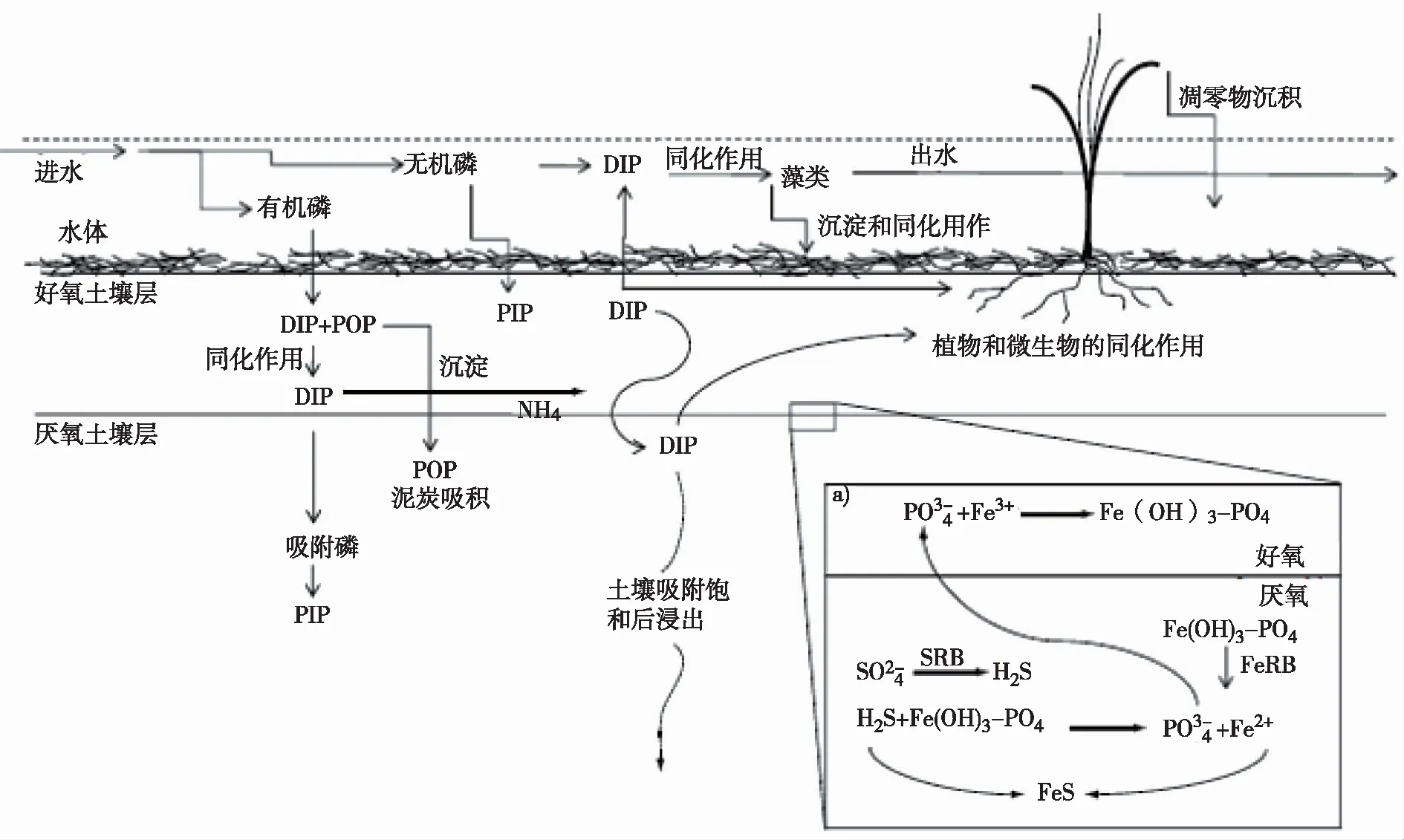
图2 人工湿地中的磷循环[11] 注:图中PIP代表微粒无机磷、POP代表微粒有机磷、DIP代表溶解无机磷和DOP代表溶解有机磷
1.3 重金属的沉淀与迁移
矿业活动、交通和农业生产等人为因素及成土母质自然因素均会导致农田重金属污染[27],其中污水灌溉、长期不当施用化肥和有机肥、污泥和农药的使用是导致农田土壤中重金属浓度上升的主要农业生产活动[28]。在农田土壤中积累的重金属会通过降雨和农业灌溉径流入水体,对流域水生态健康产生威胁[29];已有研究表明人工湿地可以有效的去除水体重金属[30-31],湿地土壤、基质、湿地植物、生物膜和水中污染物之间的相互作用在重金属的去除过程中起着重要作用[32],湿地的相对大小、内含的土壤介质及栽种的植物会通过改变湿地水力条件、物化及生化过程来影响重金属的去除[33]。
人工湿地中痕量重金属的去除过程主要包括物理沉淀、过滤、化学沉淀、吸附、微生物交互作用以及植物吸收,具体去除机制与水体重金属的形态、湿地环境条件紧密相关。人工湿地土壤会随着存在季节性水淹条件在好氧和缺氧之间变化,影响痕量金属的化学形态和迁移[34],改变重金属的去除过程;在好氧条件下,土壤表层有机物、磷酸盐、碳酸盐、铁、铝、锰的氧化物及粘土矿物等可络合沉降、吸附或共沉淀水体中的微量金属,将其沉淀到土壤表层[35],pH、氧化还原电位、金属的溶解度(Ksp)、重金属浓度、离子强度、电解质成分等会影响该吸附和沉淀过程[11, 36];在还原状态下,Cd、Cu、Zn等重金属会与硫化物矿物共沉淀[34],增加重金属在湿地土壤中的沉积量。此外,通过湿地基质种类的调整,诸如引入石灰石、沸石、砾石和钛酸钠纳米纤维等基质[37],可以进一步强化人工湿地对水体重金属的吸附去除。
然而,人工湿地土壤和基质去除水体重金属存在吸附饱和的问题,且无法彻底将水体重金属从湿地系统中去除,湿地重金属的彻底去除需依赖于湿地的生物过程,包括植物对重金属的吸收、转运和积累[38],已有很多研究表明香蒲(Typhaorientalis)、芦苇(Phragmitesaustralis)、凤眼莲(Eichhorniacrassipe)、大薸(Pistiastratiotes)、莎草(Carexaquatilis)、泽泻(Alismaplantagoaquatica)等植物可以富集重金属[38],同时湿地生物膜中微生物会通过对重金属价态的转化、胞外生物吸附和积累等过程协同植物修复[39-40],如Huang等人[41]利用小球藻菌具有挥发硒的能力,在湿地系统中增设藻类处理装置,与香蒲联合处理可以使得60%的硒挥发大气中而去除;Si等人[42]则应用微电场辅助人工湿地,通过减轻植物细胞的氧化损伤增加对Cu、Zn和Cd 的提取,同时改变湿地生物膜中细菌群落结构,显著促进生物膜对Cu、Zn、Cd和Co的富集。
当人工湿地进行汞矿区附近的农业面源污染治理时,值得注意的是含汞进水不适宜进行长期厌氧处理,厌氧微生物容易将无机汞转变成甲基汞[43],甲基汞一种很强的神经毒素,不利用水体中的生物存活,因此需设计合适的湿地的水淹环境,减少湿地系统内甲基汞的产生。
1.4 农药的迁移转化与降解
化学农药在保证农作物保值增产方面发挥着重要作用,但农药的滥用也会导致各种环境问题和人类健康风险,其中田间施用的农药会通过农田排水和降雨等途径进入受纳水体[44],目前,在大多数的河流中都有农药检出,其中主要的农药种类为除草剂、杀虫剂、杀真菌剂和杀线虫剂。人工湿地能够通过物理、化学和生物过程的综合降解水体中的农药[45-46],其中物理过程以沉降和吸附为主[47],化学过程以水解和光解为主[48],生物过程则有植物吸收和代谢,以及微生物降解[49];农药的理化性质、湿地的基质、湿地生物及运行参数等要素会影响非持久性农药的去除效率[49-50]。
农药会在水环境迁移转化过程中发生光解、挥发、水解、吸附和解吸附等行为,不同类型的农药会因其结构特点的不同而产生差异很大的迁移、转化特性,导致在人工湿地中的去除效率不同。张希丽等人[51]统计了32种常见农药在人工湿地中的去除效率,按农药化学结构分类,拟除虫菊酯类>有机磷类>三唑类>酰胺类>三嗪类>脲类。去除率高的农药大多数具有低溶解度和非常高的KOW和KOC系数,但低去除率的农药在此方面无明显关系[49]。
湿地基质在农药的吸附和转移过程中起着重要的作用,对于富含有机颗粒物的农药污染水体而言,与颗粒物共沉降是农药去除的主要途径[52-53],水体中的农药随之转移至湿地基质中。与此同时,湿地基质可以直接吸附农药,如李咏梅和魏海林便发现沸石、砾石和钢渣均可以直接吸附烟嘧磺隆[54],吸附于基质中的农药会进一步根据基质环境发生生物或者非生物降解[55-56]。此外,基质可为湿地中农药的物理化学反应及生物反应提供反应界面。
植物吸收是湿地农药的降解主要途径之一[57],有研究表明人工湿地植被密度与农药去除率之间存在正相关关系,如Stearman等人[58]研究了除草剂在湿地系统去除效果,结果表明在没有植被的情况下,甲草胺和西咪嗪的平均去除率为63%和64%,而在植被存在时,甲草胺和西咪嗪的去除率可以提高到82%和77%;微生物降解在人工湿地去除有机农药的过程中亦扮演着主要角色,微生物的酶促反应可将有机农药分解为小分子,降低进水毒性[59],此外,微生物的矿化、代谢等活动会改变农药的降解环境,进而影响湿地农药的降解效率[60]。
人工湿地的水文和水力是影响农药去除的关键因素,主要通过沉积颗粒物的尺寸、悬浮颗粒物的絮凝过程影响湿地中农药吸附和解吸附,影响出水中的农药浓度。植物的存在能降低湿地水力流动性,增强颗粒物对农药的吸附;此外,水力停留时间的延长明显有助于农药的降解,Stearman等人[58]发现湿地水力停留时间大于10天时,其农药去除率可以达到90%,而水力停留时间小于4天时,农药的去除率小于70%,但研究表明水力时间的延长对COD等常规污染物的去除提升不明显[61],因此需根据进水的水质特点和处理需求来进行成本控制,从而确定湿地的最佳水力停留时间。
2 结论与展望
人工湿地作为面源污染控制研究的常用技术,建设和运行成本低,运行管理方便,目前的研究已证实人工湿地可对水体中的氮、磷、重金属和农药实现可观的去除率,在农业面源污染控制领域应用潜力巨大;但人工湿地对于重金属和农药的去除更偏向于单一污染物的降解研究,实际应用过程中与氮、磷的共同去除效率尚需更多案例验证,且随着湿地基质材料发展和污染物富集植物种类的丰富,未来人工湿地的设计可联合不同工程措施和植物修复方案来应对不同负荷特征的水污染处理;同时,因人工湿地能为动物提供栖息地,某些经济植物的应用还能产生一定的经济效益,与景观设计、生态等学科的结合应用,可以有效的改善农村风貌和提高区域生态功能。

