全中枢多中心放疗中铅门固定与跟随技术的应用研究
苏坤普,黄 霞,周德力,刘岩海,马俊刚,耿明英
1.陆军军医大学特色医学中心肿瘤科(重庆 400042);2.重庆大学附属肿瘤医院 肿瘤科(重庆 400042)
由于全中枢神经系统肿瘤靶区较长,直线加速器最大40 cm×40 cm 的射野限制无法包全整个靶区,所以常把全中枢神经系统肿瘤分为2~3段靶区进行放射治疗,但在射野衔接无法避免剂量冷热点、靶区剂量分布不均匀的问题[1-2]。刘志杰等[3]报道了在全脑全脊髓的放射治疗中,全脑全脊髓多中心调强适形放射治疗(intensity modulated radiation therapy,IMRT)相对与常规二维计划可以获得更优的靶区剂量分布和更低的危及器官受量;鞠孟阳等[4]研究发现全脑全脊髓调强放疗时,射野重叠区大小设置在4~6 cm最佳;廖雄飞等[5]报道多中心容积弧形调强放射治疗(volumetric-modu⁃lated arcRadiotherapy,VMAT)很好的解决了全中枢神经肿瘤靶区衔接处剂量冷热点的现象。另外有研究[6-7]表明IMRT采用铅门跟随和铅门固定两种技术,靶区和危及器官受量均能满足临床治疗要求,而铅门跟随技术能更好地降低正常组织和危及器官的剂量照射。李成等[6]的研究显示在鼻咽癌的计划设计中,铅门跟随技术相较于铅门固定技术可以降低多个危及器官的限值剂量和低剂量区。王艳菊等[8]就髓母细胞瘤调强计划中AAA 算法与PBC 算法的对比研究,结果表明PBC 算法比AAA算法能够更好地满足临床要求。但是对于多中心的IMRT、VMAT计划及铅门固定和跟随技术在临床上的应用鲜有人研究。本文就全脑全脊髓放疗的多中心IMRT、VMAT 计划,分别采用铅门固定或者铅门跟随技术,评估靶区和危及器官受照剂量、机器执行效率进行探索与比较,以期为临床选择不同的治疗技术提供指导与参考。
1 资料与方法
1.1 一般临床资料
随机选择2020年接受全中枢放疗的患者14例,其中男性9 例,女性5 例,年龄4~25 岁,中位年龄9 岁。均首次治疗,且无放疗禁忌症。本研究患者均知情同意,并通过医院伦理委员会审核批准。
1.2 治疗计划
1.2.1 定位图像采集 所有患者均采取仰卧位,用头颈肩一体板和热塑膜做头颈及体部的固定,在Philips Bigbore 16排多层螺旋大孔径CT机上,进行3 mm层厚增强扫描,定位扫描范围自头顶至坐骨结节,CT 图像经过DICOM传输至Elekta Monaco 5.11治疗计划系统。
1.2.2 治疗计划制定 由经验丰富的放疗主治医生确定全中枢神经肿瘤计划靶区:全脑PTV1、颈胸段脊髓PTV2、腹部段脊髓PTV3。各段靶区的处方剂量均为36 Gy/20次,危及器官参考ICRU 83号报告定义分别勾画了晶体、心脏、肺、肾脏等,其限制剂量参考常规照射正常组织耐受剂量[9]。采用Elekta Monaco 5.11治疗计划系统和Axesse 加速器8 MV X 射线模式分别制定多中心铅门固定IMRT 技术(IMRT with multi-ISO centers and static jaw technique,IMRT-MISO-SJT)、多中心铅门跟随IMRT 技术(IMRT with multi-ISO centers and jaw tracking technique,IMRT-MISO-JTT)、多中心铅门固定VMAT 技术(VMAT with multi-ISO centers and Static jaw technique,VMAT-MISO-SJT)、多中心铅门跟随VMAT技术(VMAT with multi-ISO centers and jaw track⁃ing technique,VMAT-MISO-JTT)这4 种治疗计划。4 组计划设置相同的优化目标和约束条件,要求处方剂量至少包绕95%的靶区体积,处方剂量的110%所包绕的体积不得超过靶区体积的1%。PTV1、PTV2、PTV3的计划等中心分别命名为ISO1、ISO2、ISO3,为减少治疗过程中的移床操作可能造成的摆位误差,三个中心的坐标只在头脚方向有差异,左右和腹背方向保持一致;4 组计划靶区衔接处射野重叠4~5 cm。IMRT 计划ISO1 射野角度分别设置为268°、82°、180°,ISO2、ISO3射野角度[10]分别设置为215°、0°、145°;VMAT计划三个中心分别单独设置一个beam两个全弧。计划分别设置field,选择auto与fix field确定是否选择铅门跟随模式。
1.2.3 计划比较评估 比较4组计划的剂量-体积直方图(Dose-Volume Histogram,DVH)和等剂量分布,采用适形度指数(Conformity Index,CI)和均匀性指数(Ho⁃mogeneity Index,HI)评估靶区的剂量分布。评估公式:CI=(VT,ref/VT)×(VT,ref/Vref),其中,VT,ref为参考等剂量所包绕的靶区体积[11],Vref为参考等剂量所包绕的体积,VT为靶区体积,这里参考等剂量取处方剂量。参考Elekta Monaco 5.11治疗计划系统定义HI=D5%/D95%,D5%为5%靶区体积对应高剂量,D95%表示95%的靶区体积受到的照射剂量。CI的值为0~1,越接近1,表明靶区处方剂量线适形度越好;HI值大于1,其值越接近1,靶区均匀性越好,HI为1 是最佳理想情况。评估晶体最大剂量Dmax、左右肺V5%和平均剂量Dmean、心脏Dmean、左右肾脏Dmean、Body 的Dmean、500 cGy 低剂量区域体积、机器跳数的差异。
1.3 统计学分析
采用SPSS 19.0统计学软件进行数据处理,计量资料用均数±标准差(±s)表示,采用配对t检验进行分析,P<0.05 为差异有统计学意义。
2 结果
2.1 靶区剂量分布
对于所选取的14 例病例,4 组计划的靶区剂量分布均能满足临床使用要求,且靶区Dmean、D2%及D98%四组计划差异无统计学意义(P>0.05);VMAT-MISO-SJT靶区处方剂量覆盖率及靶区剂量适形度最好,与IMRT-MISO-SJT、IMRT-MISO-JTT差异均有统计学意义(P<0.05),与VMAT-MISO-JTT差异无统计学意义(P>0.05);VMAT-MISO-JTT靶区剂量均匀性最好,与IMRT-MISO-SJT 差异有统计学意义(P<0.05),但与IMRT-MISO-JTT及VMAT-MISO-SJT差异无统计学意义(P>0.05)。铅门固定与跟随技术对IMRT 及VMAT计划的靶区剂量分布无明显影响,见表1。
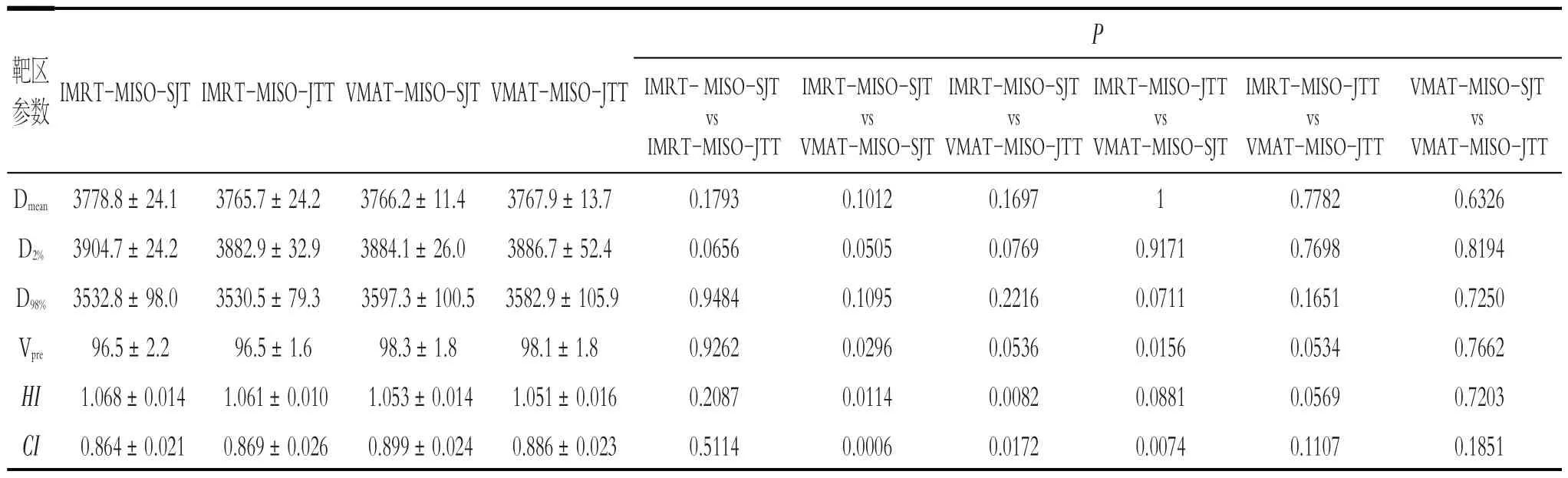
表1 14例全脑全脊髓患者4种计划靶区剂量各评估参数比较Table 1 Comparison of dosimetric parameters of target areas in 4 plans for 14 CSI patients
2.2 危及器官剂量分布
四组计划的危及器官和正常组织剂量分布均达到临床基本要求。在危及器官的保护上,IMRT-MISO-SJT左、右肾脏平均剂量,与VMAT-MISO-SJT、VMATMISO-JTT 差异有统计学意义(P <0.05),但是与IMRT-MISO-JTT 差异无统计学意义(P>0.05)。IMRT左肺Dmean、V5%与VMAT 计划相当,且差异无统计学意义;IMRT 右肺Dmean、V5%与高于VMAT 计划,且Dmean差异有统计学意义;其中左右晶体最大剂量、心脏平均剂量、body 的平均剂量差异无统计学意义(P>0.05)。铅门固定与跟随技术对IMRT 及VMAT 计划的危及器官受照剂量无明显影响,见表2。
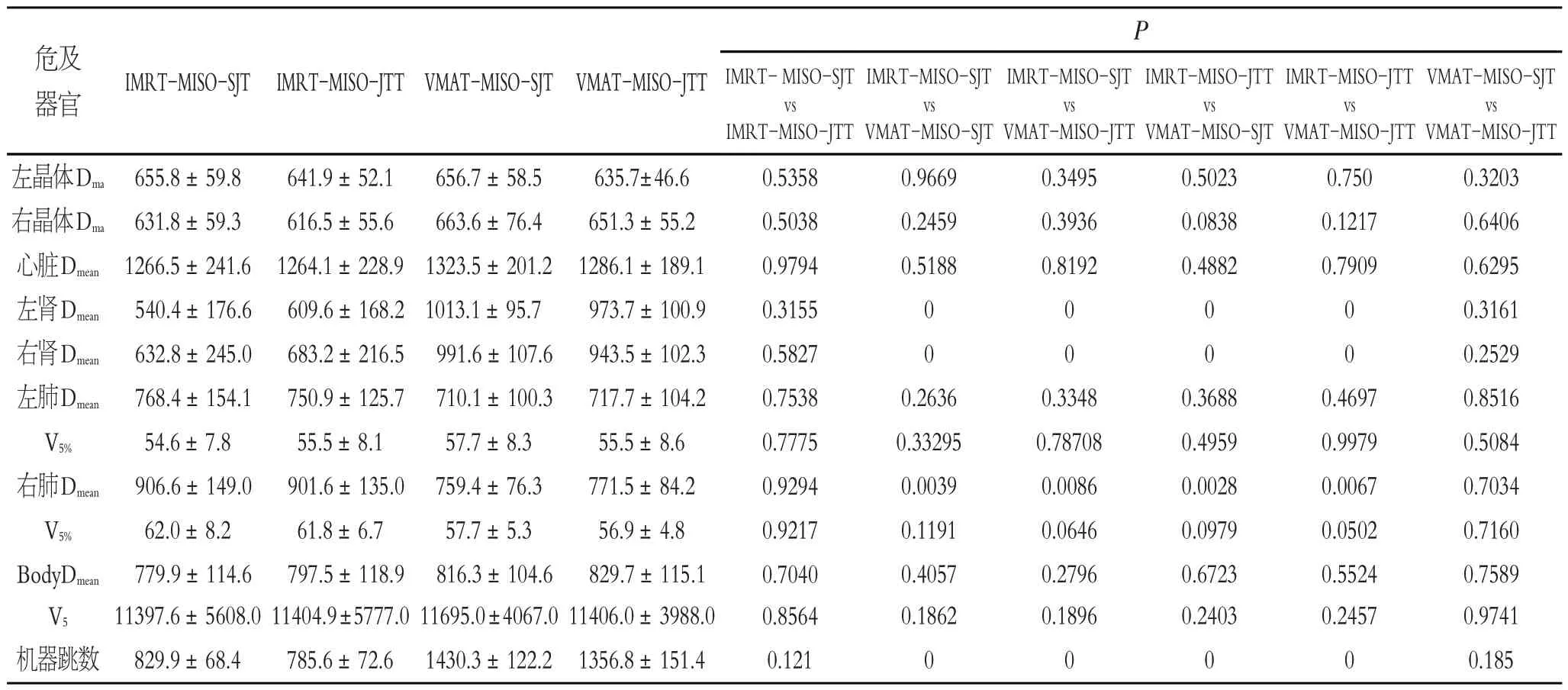
表2 4种计划各危及器官受照剂量(cGy)、低剂量的组织体积(cm3)及机器跳数(MU)比较Table 2 Comparison of dose of organs-at-risk(cGy),low-dose volume(cm3)and monitor units in 4 plans
其中四组计划在500 cGy 低剂量覆盖体积,VMAT计划均高于IMRT 计划,但差异无统计学意义(P>0.05);由机器跳数比较可知,VMAT 计划均高于IMRT计划,且差异具有统计学意义(P<0.05)。铅门固定与跟随技术对IMRT及VMAT计划的500 cGy低剂量覆盖体积及机器跳数无明显影响,结果见表2及图1、图2。
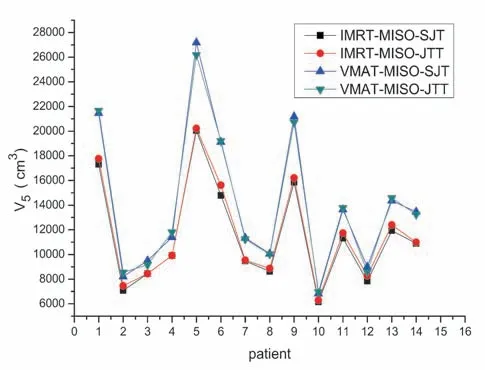
图1 14例全脑全脊髓患者4种计划的500cGy低剂量覆盖的体积比较Figure 1 Volume comparison of low-dose coverage of 500cGy in 4 plans for 14 CSI patients
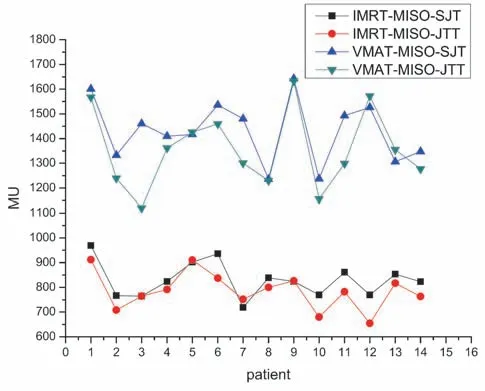
图2 14例全脑全脊髓患者4种治疗计划的机器跳数比较Figure 2 Comparison of monitor units in 4 plans for 14 CSI patients
3 讨论
全中枢神经肿瘤的靶区包括全脑和全部脊髓,其治疗照射范围远远超过加速器最大照射射野。早期的射野相切技术、非共面射野衔接技术、半野照射技术、正向子野添加技术、通过辅助结构限定照射区域等技术,有效的缓解或避免了衔接处剂量冷热点[11-17]。但是放疗实施复杂、临床广泛开展具有一定的难度,比如转床等也可能引入新的治疗误差。本研究主要探讨了多中心的IMRT、VMAT计划结合铅门固定与跟随技术在全中枢神经肿瘤放疗中的应用,研究结果表明四组计划均能满足临床要求,整个靶区无剂量冷热点存在。而且治疗计划设计与治疗实施都比较便捷,与常规的射野拼接技术比较具有明显优势。
本研究中四组计划靶区Dmean、D2%及D98%无显著性差异,VMAT相对于IMRT可以获得更好的靶区适形度和均匀性。这是因为VMAT技术在出束角度更多,靶区剂量更容易满足,因而适形度较好;而IMRT 的射野方向固定,为了最大限度的同时满足靶区和危及器官的剂量分布,在子野的生成上有一定的限制,很容易在靶区内外产生高量、热点区域,从而影响靶区均匀性。在贺先桃等[18]的研究中也表明在乳腺癌术后根治放疗中,VMAT 相比于IMRT 有更好的CI和HI。总体上来说,在危及器官的保护上IMRT 计划优于VMAT 计划,该结论与朱俐颖等[19]研究结果不相同。分析其原因,IMRT固定角度调强射野可以有效的、更多的避开各危及器官,比如晶体、肾脏、心脏等,故而这些危及器官受照剂量低于360°全弧的VMAT 计划。有研究报道To⁃mo、VMAT 计划患者身体受照的整体剂量及低剂量体积较多,这可能增加二次致癌的风险[20-23]。同时SERA⁃VALLI等[24]指出在全脑全脊髓放疗中,总的处方剂量小于等于36 Gy,大多数危及器官耐受剂量比较宽泛,很难推荐一种放疗技术而不使用另外一种放疗技术。
另外,本研究发现对于同种IMRT或者VMAT技术而言,采用铅门跟随或者铅门固定的方式造成靶区和危及器官的差异基本无统计学意义。其原因在于全中枢神经肿瘤靶区,第一段全脑PTV1,靶区较大但靶区形状简单,铅门开放的位置相对较大且比较固定;第二段、第三段靶区PTV2、PTV3,其靶区形状呈长条形,相对比较规则。因而铅门固定与铅门跟随情况下铅门的位置变化差异不大,所以MLC的漏射和透射对靶区和危及器官受照剂量影响较小,进而SJT与JTT在全中枢多中心计划中剂量学差异不明显。刘乐乐等[25]的分析也显示,在靶区相对简单规则的计划中,SJT 和JTT 技术对靶区的CI和HI值的差异无统计学意义。冯仲苏等[26]报道,铅门跟随技术可以更好的降低直肠癌治疗的危及器官和正常组织受照的剂量,其原因在于直肠癌靶区形状不规则且体积大,铅门开放的位置相对较大,MLC的漏射与透射会对靶区和危及器官的剂量产生较大的影响。
4 结论
在全中枢神经肿瘤放射治疗计划设计中,如果重点强调靶区处方剂量的覆盖率、剂量均匀性,处方剂量适形度,优先选择VMAT-MISO-SJT 或VMAT-MISOJTT的计划设计方法;如果重点强调限制晶体、肾脏,心脏受照剂量及500 cGy 低剂量体积区域、机器跳数等,则优先选择IMRT-MISO-SJT 或IMRT-MISO-JTT 的计划设计方法。全脑全脊髓放疗计划中,铅门固定与跟随技术对IMRT 及VMAT 计划的剂量分布及机器跳数无明显影响,在其他病种放疗计划中的影响有待进一步探索。
(利益冲突:无)

