早产儿脐静脉置管术后并发症危险因素分析及护理对策
(郑州大学第一附属医院 河南郑州450000)
世界卫生组织曾于2012年在全球早产儿报告中明确将早产儿进行定义及分类,即胎龄<37周(259 d)的活体新生儿[1]。受胎龄小、器官功能发育不完善、体重轻、病情危重等诸多因素影响,早产儿出生后早期生存情况依赖于完善的抢救药物、复苏及营养支持策略,建立安全可靠、稳定有效的静脉通路直接影响患者生命安全[2]。脐带静脉导管采用原料聚氨酯PUR、丙烯腈-苯乙烯-丁二烯共聚物ABS、聚碳酸酯PC和合成橡胶材质,通过环氧乙烷消毒,一次性使用,经新生儿尚未完全关闭的脐静脉插入,继而在下腔静脉与右心房交界处置入导管,属于一种特殊的中心静脉置管术[3]。脐静脉置管术在早产儿输注药物、预防反复穿刺产生不良影响等方面意义重大,但其在临床上难以避免的存在导管滑脱、医源性皮肤损伤等多种并发症发生风险[4]。目前,脐静脉置管术后早产儿发生并发症的高危因素及护理对策尚未达成一致。基于此,本研究选取161例行脐静脉置管术的早产儿为研究对象,回顾性分析其各项资料,旨在探讨术后并发症发生的主要危险因素,并制订针对性护理对策。现报告如下。
1 资料与方法
1.1 临床资料 回顾性分析2019年12月1日~2020年12月31日本院收治的161例行脐静脉置管术的早产儿各项资料。纳入标准:①胎龄<37周(259 d)的活产新生儿;②患儿脐带未干结且脐部无任何异常;③患儿具备脐静脉置管术适应证且脐静脉血管未闭锁;④患儿监护人自愿签署脐带静脉置管的知情同意书;⑤患儿各项临床资料完整。排除标准:①患儿脐周围、脐带存在异常;②患儿临床资料部分或全部缺失;③患儿存在脐静脉置管禁忌证。
1.2 调查方法 收集161例患儿一般资料调查表、出生记录单、医嘱单、病情记录及各项检查报告,纳入性别、胎龄、出生体重、分娩方式、营养支持方式、先天性疾病情况、医用粘胶、置管位置(标准:横膈上0.5~1 cm与其对应8~10胸椎)、置管深度(方法:1.5×出生体重+5.6 cm+脐带残端)、置管时间等指标,按照置管后并发症发生情况将161例患儿分为发生组、未发生组,分析上述患儿各指标与其并发症之间的相关性。
1.3 并发症判定标准 ①导管异位:根据2016年美国静脉输液护理学会发布的实践指南,脐静脉导管尖端正确位置应为右心房交界处的下腔静脉内。除该位置外的导管尖端位置则称为位点异位(导管尖端位于下腔静脉,但位置过深或过浅,而非最佳位置)和路径异位(导管尖端进入除下腔静脉外的其他分支血管)[5]。②导管滑脱:导管发生脱出且长度超过1 cm(含1 cm)。③脐部渗血:术后患儿活动时脐部可见新鲜渗血。④医源性皮肤损伤:脐静脉周围皮肤因手术操作发生医用粘胶相关性损伤(移除后皮肤出现糜烂、水疱、红斑或撕裂等症状超过30 min),化学性灼伤(因各种化学物质或温度对皮肤造成腐蚀、刺激等继而发生的皮肤黏膜损害)导致患儿皮肤完整性受损[6]。⑤血流感染:即导管相关性血流感染,带有或拔除血管内48 h出现真菌或菌血症,且伴呼吸暂停、低血压、反应差等感染症状,除导管外并无明确感染源[7]。
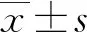
2 结果
2.1 早产儿脐静脉置管术后并发症的单因素分析 161例早产儿中,脐静脉置管术后出现并发症46例,其中导管异位34例、导管滑脱与脐部渗血5例、医源性皮肤损伤5例、导管相关性血流感染2例,总发生率为28.57%。根据是否发生并发症分为发生组和未发生组,单因素分析显示,两组新生儿出生体重、医用粘胶选择、固定方式、先天性疾病、置管位置、置管时间方面比较差异有统计学意义(P<0.05)。术后并发症单因素分析,见表1。

表1 术后并发症单因素分析(例)
2.2 早产儿脐静脉置管术后并发症多因素Logistic回归分析 将差异存在统计学意义的指标赋值进行多因素Logistic回归分析,见表2。多因素Logistic回归分析,低出生体重、医用粘胶选择不当、固定方法不当、置管位置不标准、置管时间过长是早产儿脐静脉置管术后并发症的独立危险因素(P<0.05),见表3。

表2 多因素Logistic回归赋值表
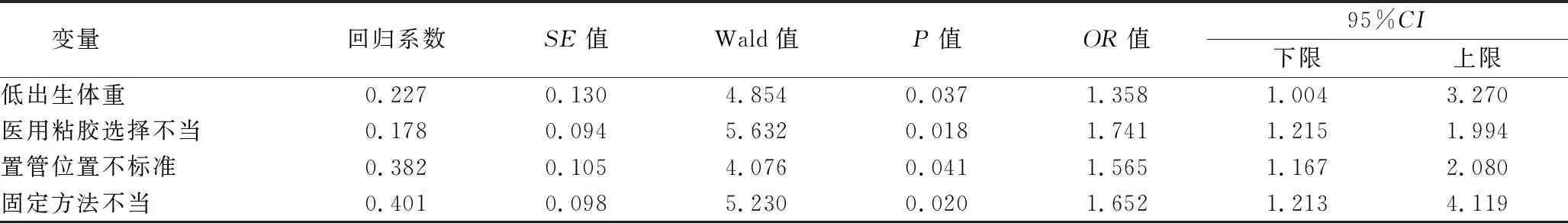
表3 多因素Logistic回归分析
3 讨论
3.1 早产儿脐静脉置管术后并发症的危险因素 脐静脉置管术是有效利用新生儿脐带、脐静脉及动脉发育尚未成熟的特点对其进行中心静脉置管的临床技术,早产儿脐部血管较粗且纹路清晰可见,相较于其他中心置管方式适应性及安全性更高[8]。但脐静脉置管术在救治早产等病情危重患儿的同时,难以避免存在一定并发症发生风险。程莉萍等[9]研究发现,脐静脉置管术后并发症发生率约为20.00%;而黄向红等[10]研究显示其发生率高达64.00%。本研究161例行脐静脉置管术的早产儿术后并发症发生率为28.57%,可见受不同地区、经济等多重因素影响,并发症发生率存在较大波动。本研究经多因素Logistic回归分析可见,低出生体重、医用粘胶选择和固定方法不当、置管位置不标准是早产儿脐静脉置管术后出现并发症的独立危险因素(P<0.05)。分析原因可能为:①低体重早产儿多为胎儿阶段母体营养不良或自身疾病等因素导致的发育迟缓,该类患儿出生体重过轻且脐带扭曲偏细,加之其静脉壁相对健康新生儿更薄,加大了置管难度,反复置管极易引发多种并发症。②新生儿表皮角质层薄,基底膜弹力纤维及结缔组织发育不全,因此疏松、细嫩,若固定方法不当或固定材质不适合,极易引发脐周皮肤张力性损伤、表皮剥脱甚至撕裂伤。③早产儿胃肠道发育尚未成熟,局部免疫力及胃肠动力低下。若脐静脉置管位置不标准,可能导致患儿肝内置管从而增高内部血压,经门静脉流通的胃肠道血液进入下腔静脉,导致腹胀、肠炎等并发症的发生[11-12]。
3.2 早产儿脐静脉置管术后并发症的护理对策
3.2.1 导管异位 由护士长、科室护理IV-team团队、新生儿科医生等成员共同成立脐静脉置管小组,对组内成员及相关管理人员进行长期的规范化培训,主要培训内容及形式如下。①风险管理培训:由1名新生儿医生(主治医师及以上职称)为组员介绍早产儿脐血管特点、解剖位置及差异;1名放射科医生(主治医师及以上职称)为组员解读早产儿腹部、胸部X线片及导管尖端位置;科室护理IV-team团队(专科工作经验≥5年)对护士进行导管置管操作技术及维护能力培训。②理论考核:新生儿医生、放射科医生、科室护理IV-team团队及护士长共同围绕培训内容联合出题并完善、修订,考核全部脐静脉置管术相关医护人员,考核成绩85分及以上者可进入临床置管及维护工作[13]。③制订规范化流程:医院感染管理科、重症医学护理专家、新生儿医生、放射科医生、科室护理IV-team团队及护士长共同以新生儿PICC置管流程为基础制订脐静脉置管及维护的规范化流程。
3.2.2 导管滑脱与脐部出血 蓝国锋等[14]认为,置管操作前需在脐静脉插管处提前套上结扎脐带的气门芯套,置管及缝合完毕后再将该气门芯在患儿脐带根部套住以达到紧固患儿脐带组织及导管的目的。我们研究后认为,置管完成后应用弹力橡胶管固定后,缝线缝合脐血管根部,并将缝线与导管打结,在脐带湿滑的情况下也可保证导管紧密不滑脱。采用“镂空式”法固定,将无菌透明贴膜中心剪出半径为15 mm的圆孔,采用同样方式处理皮肤保护敷料,首先在患儿脐周贴皮肤保护敷料,圆孔露出的脐带残端,其次将导管刻度朝上,然后将其盘在脐周皮肤保护敷料上,最后将无菌透明贴膜圆孔露出的脐带残端后覆盖固定导管。固定后,设计使用导管固定装置,由魔术贴及医用硅胶制成,柔软、透明、中央凸起并有小孔,透气、易观察,在日常维护中,可随时打开消毒脐部,更换纱布,且防止外界摩擦保护脐带根部。
3.2.3 医源性皮肤损伤 结合早产儿特点,选择合适的医用粘胶,并正确使用。因医用粘胶的材质不同,对皮肤的损害程度也存在差异。如水胶体辅料优于聚氨酯薄膜材料;医用粘胶为软聚硅酮,则证明其对皮肤附着力较小,在移除过程中对皮肤的损伤较小,其温和性优于纸质粘胶、水状胶体敷料等。结合早产儿特点,应正确选用皮肤消毒液,采用含有0.45%有效碘的碘伏消毒液替代复合碘消毒液。消毒过程中对用量进行精准控制,以防止消毒棉球含有的消毒液饱和度过高,造成患儿背部、腰臀沾染消毒液。于消毒前将中单垫至患儿腰臀部,消毒完成后及时将中单撤走,防止床单被浸湿,使床单保持干燥平整。若早产儿胎龄更小,则在消毒液干后,选择0.9%氯化钠溶液棉球对消毒部位进行擦拭,减少消毒液与皮肤接触。
3.2.4 导管相关性血流感染 ①严格执行手卫生消毒及管理,手卫生质量导管相关血流感染的重要影响因素,护理人员在脐静脉导管操作开始前,需使用流动水和抗菌洗手液彻底清洁、消毒手部后才可进行置管等操作。②脐静脉相关的各项操作均遵循无菌原则;选择大小合适的消毒棉片或消毒棉球,通过来回旋转的摩擦力对脐静脉导管接口处的螺纹及其横切面彻底消毒,每次擦拭时间不得少于15 s,直至将其表面微生物祛除方可继续执行静脉治疗。③做好导管相关血流感染的监控工作,由科室院感小组成员(病区主任、护士长、院感医生、院感护士)负责对留置脐静脉的维护人员(主管医生、责任护士、静疗护士)进行督导检查,包括每天评估拔管指征、中心相关血流感染防控措施的落实情况。
综上所述,早产儿脐静脉置管术后并发症发生的危险因素主要包括低出生体重、医用粘胶选择、固定方法不当、置管位置不准确等,针对上述因素,建立置管及维护团队、实施风险管理培训、护理相关对策实施,可降低并发症发生风险,值得推广应用。

