5 例GNAO1 基因相关疾病临床及遗传学分析
杨海波 文泳欣 章清萍 包新华
1.北京大学第一医院小儿外科(北京 100034);2.广东省妇幼保健院康复医学科(广东广州 510010);3.北京大学第一医院儿科(北京 100034)
GNAO 1基因变异最初报道与早发性婴儿癫痫性脑病相关,近年来的研究发现,存在GNAO 1基因变异的患者其临床表现具有异质性,除早发癫痫性脑病外,还可以表现为不伴癫痫发作的运动障碍等[1]。该基因变异所导致的疾病目前尚无特效治疗,深部脑刺激(deep brain stimulation,DBS)可缓解部分患儿的运动障碍。本病罕见,北京大学第一医院及广东省妇幼保健院自2017年9月至2021年1月共诊治了5例GNAO1基因变异患儿,并对其中两例在国内率先开展了DBS 治疗。现回顾分析5 例患儿的基因变异特征与临床特点,以及治疗反应,并结合文献探讨本病的治疗方法。
1 临床资料
5例患儿中男3例、女2例,8月龄~5岁7个月,平均3岁。分别来自无血缘关系家庭,所有患儿父母身体健康,均非近亲婚配,均无相关神经系统疾病家族史。所有患儿均为足月儿,出生史及母孕期无特殊。患儿的临床表现、辅助检查及治疗反应见表1。
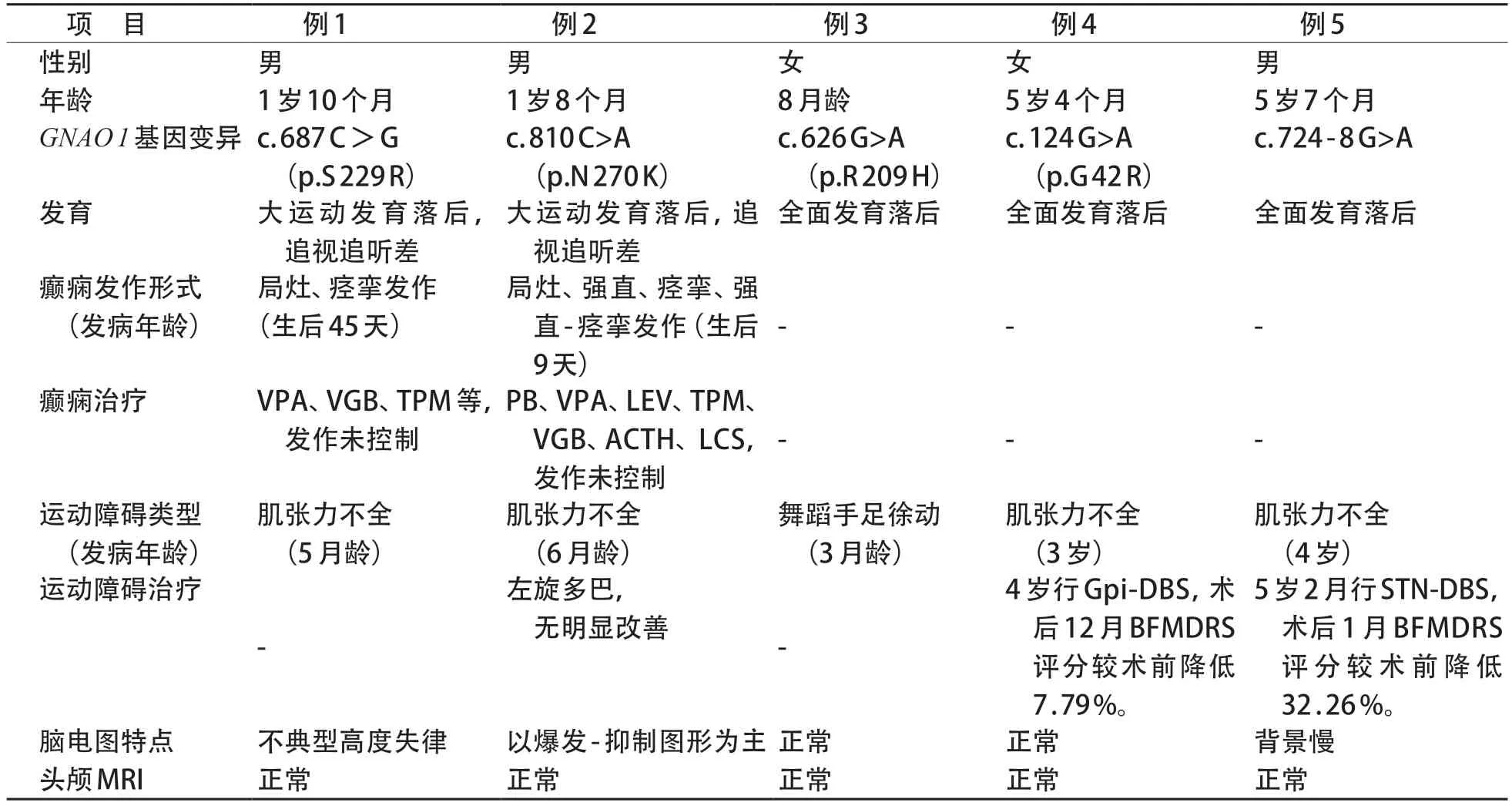
表1 GNAO1基因变异患儿的临床特征
例1、例2 以早发性癫痫脑病为主要表现,分别于生后45天和9天出现癫痫发作,发作形式多样,包括局灶性发作、痉挛发作、强直发作等,发作频繁,每日发作数次至数十次。例3、例4 及例5 暂无癫痫发作。5例患儿均有锥体外系症状,首次出现时间为3个月~4岁,平均8.2个月。除例3主要表现为手足徐动外,其余4例均表现为肌张力不全。5例患儿均有严重的发育落后,例1 与例3 抬头不稳,例2 与例4尚不能独坐,例5为其中运动发育最好的患儿,于18月龄独走,但目前仍站立及行走不稳。例1、2、3均存在追视追听差;例4至今无语言,例5吞咽构音欠佳。
例2于6月龄行小儿神经心理检查提示大运动、精细动作、适应能力、语言、社交行为均发育落后。例4于4岁3月行Gesell发育评估提示适应性、大运动、精细运动、语言、社交均为极重度落后。其余患儿未行发育评估。
5例患儿均行脑电图检查,其中例1、例2脑电严重异常,分别为不典型高度失律和爆发-抑制图形;其余3 例脑电图未见痫样放电。5 例患儿均行头颅MRI检查、血尿代谢筛查,均未见异常。
为进一步明确病因,经家属知情同意,采用家系全外显子组测序的方法筛查患儿的基因变异。结果显示,5例患儿均存在GNAO1基因杂合变异,4例为错义突变,1例为剪切位点变异,分别是c.687C>G(p.S229R)、c.810C>A(p.N270K)、c.626G>A(p.R209H)、c.124G>A(p.G42R)和c.724-8G>A。例1、例2、例3和例5的GNAO1变异为新生变异;例4 母亲未见相应位点的变异,由于缺乏父亲DNA 样本,其变异情况不详。上述所有变异经PolyPhen-2、SIFT和Mutation Taster预测均为有害变异。其中,例3(c.626 G>A,p.R 209 H)与例4(c.124 G>A,p.G 42 R)为既往文献已报道的致病变异;例5 的c.724-8G>A变异在ClinVar数据库中收录为致病性变异,根据ACMG指南定义为疑似致病性变异;例1(c.687C>G,p.S229R)与例2(c.810C>A,p.N270K)的变异既往未见报道,为本研究新发现的变异,经ACMG指南判读定义为疑似致病性变异。
例1与例2以癫痫为主要表现,予多种药物抗癫痫治疗,包括促肾上腺皮质激素、丙戊酸钠、托吡酯、氨己烯酸、苯巴比妥、左乙拉西坦、拉考沙胺等,发作依旧难以控制,每日发作10余次。
例1与例2同时存在肌张力不全表现,例1未用药,例2 予左旋多巴治疗,疗效不明显,暂未行DBS治疗。例3 以舞蹈手足徐动为主要表现,目前在做DBS治疗的准备。例4、例5以肌张力不全为主要表现,曾予左旋多巴、盐酸苯海索治疗,症状无明显缓解,遂予DBS治疗。
例4、例5 分别于4 岁、5 岁2 月行DBS 治疗,选用北京品驰医疗设备有限公司的刺激器,植入电极型号为L 302,植入刺激器型号为G 102 R,治疗前后采用Burke-Fahn-Marsden肌张力障碍评估量表(Burke-Fahn-Marsden Dystonia Rating Scale,BFMDRS)进行评分,DBS 术后缓解率=(术前BFMDRS 运动评分-术后BFMDRS 运动评分)/术前BFMDRS 运动评分×100%。两例患儿术后定期随访评估疗效并调整程控参数(表2)。例4 植入靶点为双侧苍白球内侧核(globus pallidus interna,GPI),术后经影像融合提示植入点与术前计划完全吻合。患儿术前BFMDRS评估为77分,术后12个月BFMDRS评估为71分,改善程度为7.79%。考虑例4 行GPI-DBS 术后改善效果不明显,经科内专家讨论及综合评估,决定例5 的植入靶点为双侧丘脑底核(subthalamic nucleus,STN),术后经影像融合提示植入点与术前计划完全吻合。患儿术前BFMDRS评估为62分,术后1月BFMDRS评估为42分,改善程度为32.26%。
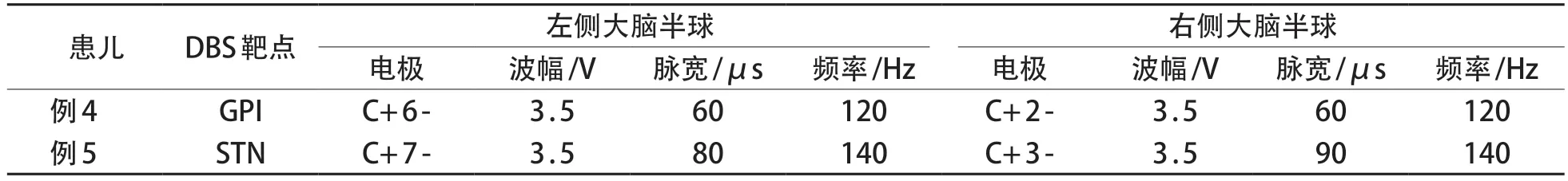
表2 DBS程控参数
2 讨论
GNAO 1基因编码G 蛋白的α 亚基多肽链O(Gαo),是脑内最常见的膜蛋白,占脑组织膜蛋白的1%,在脑组织内分布广泛,在海马、纹状体和小脑中高表达。Gαo亚基可与多种重要的G蛋白偶联受体(G protein coupled receptors,GPCRs)结合,包括γ-氨基丁酸B 型(GABAB)受体、α 2 肾上腺素能受体、腺苷A1受体和多巴胺D2受体等,在调节神经递质释放和神经发育中发挥重要作用。Gαo还参与多种信号通路的调节,如通过抑制腺苷酸环化酶下调环磷酸腺苷(cyclic adenosine monophosphate,cAMP)水平、抑制N型(Cav2.2)和P/Q型(Cav2.1)钙通道、调控神经递质囊泡释放等[2],这或许是GNAO1变异致运动障碍的机制之一。此外,Gαo和Gβγ亚基还可结合内向整流钾(G protein-coupled inward rectifying potassium,GIRK)通道,以刺激通道开放,而GIRK通道异常与癫痫发作相关[3],这可能是GNAO1突变导致癫痫性脑病的机制之一。
早在2013 年Nakamura 等[4]在大田原综合征及早发性婴儿癫痫性脑病17 型(early infantile epileptic encephalopathy,EIEE17,OMIM 615473)的患者中发现GNAO 1基因变异,随后研究发现GNAO 1基因变异还与神经发育异常伴不随意运动(neurodevelopmental disorder with involuntary movements,NEDIM,OMIM 617493)相关[5]。有研究显示肌张力低下和发育迟滞是GNAO 1变异患者最常见的临床表现,分别占已报道病例的68%和78%;此外,癫痫,智力障碍和锥体外系症状如肌张力不全、舞蹈手足徐动也是这类患者较为常见的临床表现。近期有文献指出,GNAO 1的基因型与临床表型有一定的相关性:在体外cAMP 调节实验中,GNAO1基因功能缺失性(loss of function,LOF)变异多与癫痫脑病相关,而正常功能性(normal function,NF)(仅指在HEK-293T细胞中下调环磷酸腺苷的功能,不排除其它功能异常)或功能获得性(gain of function,GOF)GNAO1基因变异则与伴或不伴癫痫发作的运动障碍相关[1]。迄今,已报道的GNAO1基因变异患者约50余例,女性稍多于男性,主要为新发变异[1],但也有同胞携带同样GNAO1变异的病例报道,这可能是由于父母存在生殖细胞嵌合突变所致[6]。在已报道的GNAO1基因变异中,错义变异最为常见,其中p.G203、p.R209、p.E246是GNAO1基因变异致运动障碍表型的热点突变[1]。
本研究的5例患者中,2例患儿以难治性癫痫为主要症状,同时存在肌张力不全表现;2例患儿主要表现为肌张力不全,1例患儿主要表现为舞蹈手足徐动,无癫痫发作。5 例患儿均存在严重的发育落后。例1、例2表现为早发性婴儿癫痫性脑病,有严重的癫痫发作、发育迟滞,同时伴有肌张力不全的临床表现。其中,例1的基因变异c.687C>G(p.S229R)既往未见报道,根据患儿的临床表现,推测该变异以功能缺失性变异的可能性大;例2 的基因变异c.810C>A(p.N270K)虽然尚无文献报道,但其相同的氨基酸位点变异p.N270H已有报道,为功能缺失性变异[7]。例3、例4、例5以锥体外系症状为主要表现,同时伴有发育迟滞,暂无癫痫样发作。其中,例3 的变异c.626 G>A(p.R 209 H)既往已有报道,为正常功能性(下调环磷酸腺苷的功能)变异[7];例4的变异c.124G>A(p.G42R)既往已有报道,为功能获得性变异[7];例5的基因变异c.724-8G>A在ClinVar数据库中已被收录,但尚无体外功能性实验验证的报道,根据患儿的临床表现,推测其为正常功能性变异或功能获得性变异的可能性大。需要注意的是,部分患者癫痫发病时间较晚,特别是早期以运动障碍为主要表现的患者,可到10岁后才出现癫痫发作[8,9],本研究中3例以锥体外系症状为主要表现的患儿,后续仍需密切观察有无癫痫发作。
目前尚无针对GNAO1基因变异的特异性治疗,从机制上来说,Gαo偶联受体拮抗剂可通过抑制功能获得性的GNAO 1基因变异,从而减轻运动障碍患者的症状;相反地,Gαo偶联受体激动剂则可能对GNAO1基因变异引起的癫痫发作有效[1]。在运动障碍患者中,四苯喹嗪是最有效的药物,但其副作用限制了其广泛使用。此外,抗精神病药物(neuroleptics,如利培酮)可能对GNAO 1基因变异患者的舞蹈样动作有缓解作用[10]。既往研究报道托吡酯减轻了1 例患者的舞蹈样动作[11],可乐定改善了2 例患者的运动障碍,而急性加重期患者似乎只对大剂量苯二氮卓类或麻醉类药物有反应[8]。本研究中2 例以癫痫为主要症状的患儿,均为药物难治性癫痫,多种抗癫痫药物无法控制发作;5 例患儿均有锥体外系症状,如肌张力不全、手足徐动,左旋多巴、苯海索等药物对锥体外系症状均无明显疗效。DBS 是治疗药物难治性的遗传性单基因肌张力障碍的安全有效的方法,截止到2021 年1 月,国外共报道了16例GNAO1突变相关疾病患者进行了Gpi-DBS治疗(8 例女性,8 例男性),患者年龄中位数为9.5 岁(5~17岁),术后患者的运动障碍都有不同程度的缓解[6,8-9,12-16]。对GNAO1突变患者DBS治疗长达数年的随访,显示DBS对GNAO1变异患者长期有效,特别是运动障碍方面有显著的疗效,提高了患者的生活质量。本研究中例4行GPI-DBS手术治疗后1年,肌张力障碍症状较术前改善不显著,其疗效与国外文献报道有差异,不排除与基因变异位点不同有关,既往文献报道的DBS有效的GNAO1基因变异多为p.R209、p.E237、p.E246等热点变异,本患儿所携带的p.G 42 R 变异尚未有DBS 术后疗效的相关报道。此外,本研究的随访时间较短,有报道随时间的延长DBS 的疗效会进一步提高。本研究还对例5 率先尝试了STN-DBS 靶点治疗,术后BFMDRS 评分较术前改善了32%,提示STN 也可作为GNAO 1基因变异患者DBS 的植入靶点。从本研究随访数据来看,STN-DBS对GNAO1基因变异患者的改善效果优于GPi-DBS,但需更大样本量的研究来评估两个靶点DBS治疗对GNAO1基因变异患者的疗效。
本研究提示GNAO 1基因变异患儿的临床表现存在差异性,且与基因变异存在一定的相关性。患儿可以癫痫为主要表现,也可以运动障碍为主要表现,但即便是以癫痫为主要表现的患儿,往往也存在锥体外系症状;此外,患儿普遍存在严重的智力运动发育迟滞。DBS 是药物治疗无效的锥体外系疾病的手段之一,对癫痫发作也有一定疗效,而GNAO1基因变异所致的癫痫和锥体外系症状药物治疗均无明显疗效,故可以尝试DBS 治疗。本研究中例5 行STN-DBS治疗,术后1月BFMDRS评分较术前下降约30%,是目前首例选择STN 靶点治疗的GNAO 1基因变异患儿,提示STN也可作为本病DBS治疗的靶点。有关DBS 对GNAO 1基因变异患者的疗效还需更多病例、更长时间的随访研究。

