尿沉渣白细胞计数标准物质的研制
刘瑛颖, 张 玲, 杨乔斯
(1.中国计量科学研究院,北京 100029; 2.迪瑞医疗科技股份有限公司,吉林 长春 130000)
1 引 言
尿沉渣(urine sediment,US)检查是对尿液中的有形成分进行检查,主要包括细胞、管型、结晶、细菌、寄生虫等各种病理成份,是辅助对泌尿系统疾病作出诊断的重要常规试验项目[1]。其中的白细胞(white blood cell,WBC)项目对泌尿系统的检测具有重要意义,提示着泌尿系统存在着细菌感染或肾脏疾病等病理特征[2,3]。全自动尿沉渣分析仪是采用显微图像自动识别技术或流式细胞技术对尿液中的有形成份进行自动定位及捕捉,并且对尿液中的有形成分进行自动识别和分类计数的一种检验设备。由于其快捷性和准确性,全自动尿沉渣分析仪已成为临床尿液检测分析的常规仪器。为了保证该类仪器在日常检测工作中的性能水平和检测结果的真实可靠,国家市场监督管理总局颁布了JJF 1823—2020《全自动尿沉渣分析仪校准规范》,并于2020年4月开始发布实施。该文件主要对红细胞、白细胞两个测量项目的空白值、示值误差、重复性、携带污染率等计量特性进行了规范[4]。为了保证该校准规范的正常实施和良好操作,相关校准项目配套的标准物质是必不可少的。标准物质是具有高度均匀性、良好稳定性和量值准确性,用来校准测量仪器,对测量方法进行评价或为物质定值的物质,在分析测试各行业中得到广泛应用[5,6]。因此,本研究以固定后的人血液白细胞为原料完成了尿沉渣白细胞计数标准物质的制备,并考察了其细胞形态真实性、标准物质均匀性、稳定性和临床样本的互通性,研制的标准物质可配合相关校准规范用于全自动尿沉渣分析仪中白细胞项目的周期校准、质量控制,以及相关检测方法的确认和验证。
2 标准物质的制备
2.1 标准物质细胞原料
对体格检查中满足献血者健康检查有关要求的无偿献血者初筛(乙肝表抗、转氨酶、快速HIV)合格的EDTA-K2静脉抗凝血,取抗凝血液标本,以2 000 r/min离心3 min,分离获得白膜层,取白膜层加入溶血素进行残余红细胞溶解;然后加入磷酸盐缓冲溶液(0.1 mol/L,pH 7.2)稀释,以2 000 r/min离心3 min,洗涤3次得到白细胞悬液,加入磷酸缓冲盐(0.1 mol/L,pH 7.2)溶液和甲醛(终浓度1%,体积分数)混合,混匀器上混合30 min,置4 ℃冰箱过夜。第二天,取出后再用混匀器混合30 min,离心弃去上液得到醛化固定白细胞。
2.2 标准物质的配制和分装
将醛化固定后的白细胞按一定比例加入磷酸盐缓冲溶液(0.1 mol/L,pH 7.2)中配制成目标浓度,充分混匀后分装,透明玻璃圆底长管中每管加入30 mL白细胞悬浮液,旋紧管盖,放置冰箱备用。操作过程在生物安全柜中进行,避免细菌污染。
2.3 标准物质候选物细胞形态确认
为了保证本标准物质候选物能够通用于所有全自动尿沉渣分析仪的检测校准,尤其是基于显微图像自动识别技术的仪器,所用的醛化固定后的白细胞应具有与新鲜细胞非常高的形态相似性。本研究将4 ℃保存了12个月的标准物质候选物白细胞与新鲜血液样本中的白细胞,通过扫描电子显微镜拍摄,并进行了超高分辨率显微图像的比较。每种样本随机选取了20~40个细胞进行图像拍摄和比较。与新鲜血液白细胞相比,长期保存的醛化固定白细胞发生明显的破裂、皱缩等形态变化。这说明从细胞形态特征方面,本研究制备的尿沉渣白细胞计数标准物质候选物是可以代表新鲜白细胞的。

图1 不同样本中白细胞的扫描电子显微镜图像
3 标准物质的定值
3.1 定值方法的选择
本研究中采用了2种方法进行了定值:高通量显微成像法和流式细胞术测定。显微镜测量方法是上世纪90年代前血细胞计数的传统参考方法,也是目前美国临床检验标准委员会和中国临床检验标准委员会建议的尿沉渣白细胞计数的参考方法[7,8]。该方法的优点是直接绝对,弊端是检测通量小导致测量结果标准偏差大,主观性过强。因此,本标准物质的研制中采用了高通量显微成像法作为了定值方法之一。该方法通过基于时间延迟积分技术的电荷耦合器件(time delay integration charge coupled devices, TDICCD)可对鞘液流中高速流过的单个细胞进行快速显微拍摄,包括明场和多个荧光通道的暗场图像[9,10]。通过该技术我们得到了待定值制备物中的白细胞明场光学显微图像;同时通过核酸特异性荧光染料DRAQ5进行白细胞细胞核染色,还可得到细胞核荧光显微图像(见图2)。因此,该技术不仅实现了对研究对象的直接绝对的确认,同时可高通量(5 000 cells/s)分析测量待检测细胞,显著改善显微镜检测量的不确定度水平。

图2 人新鲜血液样本白细胞的高通量显微成像多通道图像
本研究的另一定值方法是流式细胞术测量法。流式细胞术与人工显微镜测量法有着根本的不同,前者是基于细胞表面免疫标志即从免疫学特征对白细胞进行分类计数,且可以计数大量细胞[11]。同显微镜法相比,流式细胞术分类计数白细胞的优势在于计数的细胞数量更多(>10 000个细胞),因此灵敏度、特异性更高,重复性更好。
3.2 标准物质定值数据与处理
本研究共制备了300瓶标准物质候选物,依据JJF 1006—1994《一级标准物质技术规范》随机抽取了15瓶进行了定值[12]。从每瓶中随机分别抽取3个样本进行测定,共45个样本数据,定值数据及统计处理见表1。

表1 标准物质的定值测量数据统计分析
用夏皮罗-威尔克(Shapiro-Wilk)法对两组测量数据进行正态分布检验,用格拉布斯(Grubbs)法检验有无异常值,结果表明测量数据为正态分布、无异常值[13]。用F-检验检查确认高通量显微成像法与流式细胞术的测量精度是一致的。通过计算得到本标准物质定值的算术平均值为516.0 cells/μL。
3.3 标准物质的均匀性检验
为了保证检验结果能够充分代表整体特征,本研究按照JJF 1006—1994《一级标准物质技术规范》随机选取15瓶[12],每瓶通过流式细胞术进行白细胞浓度测定3次,利用方差分析法对瓶内和瓶间的均匀性进行分析,表2列出了均匀性检验结果。
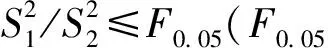
3.4 标准物质的稳定性检验
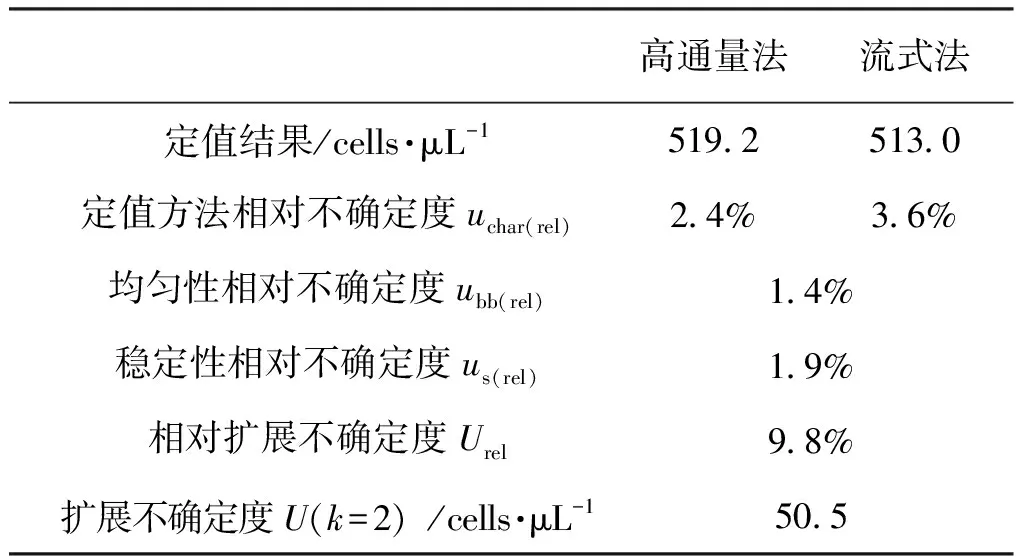
标准物质的稳定性是衡量标准物质的另外一个重要参数。标准物质的长期稳定性与储存条件相关,短期稳定性与运输条件相关。依据JJG 1343—2012《标准物质定值的通用原则及统计学原理》对标准物质候选物进行长期和短期稳定性考察[13]。长期稳定性考察方式为在12个月内周期性每次随机抽取3支样品,采用流式细胞术测试白细胞浓度3次。描绘出特性量值Y与时间X的关系,拟合成一条直线,计算直线斜率b1,并评定稳定性引入的不确定度s(b1)。t0.95,n-2为自由度是n-2和p=0.95(95%置信水平)时的t因子,如果|b1| 表3 标准物质的长期稳定性检验 短期稳定性测试选取了4个温度点4、25、37和60 ℃,不同的时间点进行测试(3、7、11、14、21、31天),每次随机抽取3支样品,每只样品测试3次,采用流式细胞术测试白细胞浓度3次。尿沉渣白细胞计数标准物质短期稳定性考察结果见表4。分析短期稳定性考察数据可知,本研究制备的尿沉渣白细胞计数标准物质样本的短期稳定温度比较宽泛(4~37 ℃),对运输温度条件要求不是非常严格。 表4 标准物质的短期稳定性检验 根据WS-T356—2011《基质效应与互通性评估指南》要求评估标准物质候选物的互通性[14]。用2种测定方法,一种为显微镜检的参考方法,另一种为临床常规全自动尿沉渣检测仪评估方法。其中第二种方法选取了两种原理的代表机型,一种为为显微图像识别原理的迪瑞FUS-2000(评估方法1),另一种流式细胞原理的希森美康UF-5000(评估方法2)。同时对选定的20份新鲜临床尿液样本(各浓度分布均匀)和标准品进行分析,利用2种方法测定临床尿液样本的结果建立数学关系(线性回归),以参考方法测定值为X,以评估方法测定值为Y,采用excel软件进行线性拟合,并采用线性回归模型进行分析。结果表明,尿沉渣白细胞计数标准物质侯选物的细胞浓度值均在95%可信区间内(见图3),说明标准物质候选物中的白细胞与临床样本中的白细胞具有良好的互通性。 图3 标准物质的互通性分析验证 研制的尿沉渣白细胞计数标准物质候选物特性量值的不确定度主要来源于3个方面:定值方法、均匀性和稳定性。后两者引入的不确定度可参考JJF 1342—2012《标准物质定值的通用原则及统计学原理》和相关研究资料[15~20]进行计算。本标准物质候选物采用了两种方法进行定值,因此分别对这2种测量方法的不确定度进行了分析。 该方法可对鞘液流中高速流过的单个细胞进行快速显微拍摄,实现了对研究对象的直接绝对的确认,同时高通量分析测量得到待检测细胞的绝对数量或浓度。通过分析发现,该方法的测量不确定度来源主要包括以下2个方面: (1)测量重复性引入的不确定u1 由表1可知,u1=2.3%。 (2)目标细胞圈门策略引入的不确定度u2 高通量显微成像测量方法利用了流式细胞术的样本采集原理实现高通量测量,因此目标细胞的识别也需要通过相应的光学信号图像进行圈门,圈门初步决定了细胞计数的个数。而常规流式方法中圈门大小主要取决于实验操作者的判断。高通量显微成像测量方法可通过多通道显微图像的辅助显著降低判断的盲目性和主观性。3个操作者分别进行圈门计数,采用独立判断的形式,辅助以显微镜拍照肉眼逐一判断,计算圈门可能引入的不确定度。经统计,u2≈0.8%。 综上,高通量显微成像技术测量方法的合成相对不确定度为: 本研究的另一定值方法是通过有标称数量的标准计数微球作为量值参考,采用流式细胞术同时分析标准物质候选物和标准计数微球,通过计算得到标准物质候选物中白细胞的浓度。其浓度计算公式为: 式中:CRS为待测目标细胞浓度,单位为个每微升(cells/μL);Ncell为获取目标细胞群数量,单位为个(cells);Nball为获取计数标准微球群数量,单位为个;Qball为样本中添加的计数标准微球数量,单位为个;V为待测样本加样体积(不含荧光染料或特异性的荧光染料标记单克隆抗体体积,计数标准微球悬浮液体积等添加物体积),单位为μL;D为样本稀释倍数。 该方法的测量不确定度来源主要包括以下3个方面: (1)测量重复性引入的不确定u1 由表1可知,u1=1.6%。 (2)计数标准微球引入的不确定度u2 通过本研究采用的计数标准微球(BD TrucountTMAbsolute Counting Tubes)使用说明书可得到该批次的量值不确定度u2=2.5%。 (3)目标细胞圈门策略引入的不确定度u3 常规流式方法中圈门大小主要取决于实验操作者的判断,判断的盲目性和主观性会引入测量的不确定度。采用3个操作者分别进行圈门计数,独立判断的形式,计算圈门可能引入的不确定度。经统计,u3≈2.0%。 综上,流式细胞术测量方法的合成相对不确定度为: =0.036 标准物质的不确定度主要来自定值的不确定度uchar,瓶间均匀性ubb,长期稳定性us。定值结果与不确定度来源见表5,表5中高通量法是高通量显微成像法的简称,流式法是流式细胞术测量法的简称。 表5 尿沉渣白细胞计数标准物质的不确定度评定 尿沉渣有形成分的自动化分析是临床检验中常规开展的项目,其测量的准确性和可比性对于提高临床诊疗水平和保证大众健康具有重要的意义。本研究制备的尿沉渣白细胞计数标准物质,原料来源于人血液白细胞,非模拟颗粒。通过超高分辨显微技术与临床样本互通性验证充分证明了其与真实样本中白细胞的形态与生理特性的一致。本研究采用了高通量显微成像法和流式细胞术对标准物质候选物联合定值,既保证了该标准物质的量值可溯源至显微镜检方法,同时又改善了测量的不确定度水平。 本标准物质经验证均匀性和稳定性良好,4 ℃避光可保存12个月,与临床样本具有良好的互通性。通过尿沉渣白细胞计数标准物质的研制,可为我国临床在用的全自动尿沉渣分析仪白细胞测量项目的测量准确性和仪器性能测试提供技术、信息和标准物质服务,这对于我国临床尿沉渣细胞有形成分的分析测量的准确性、可比性和溯源性,提高临床检测分析的质量水平和标准化具有重要意义。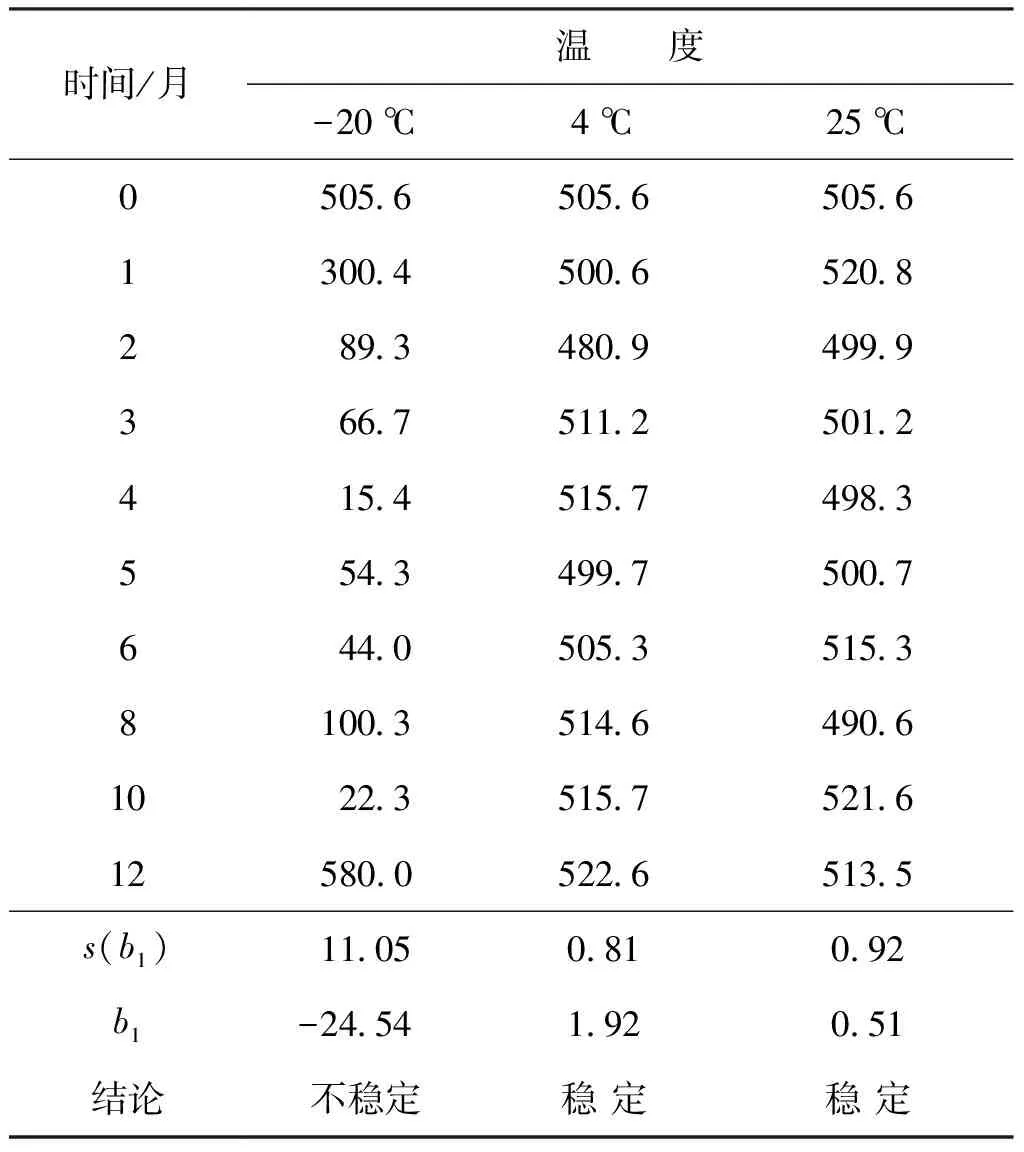
3.5 互通性验证

4 标准物质量值的不确定度评定
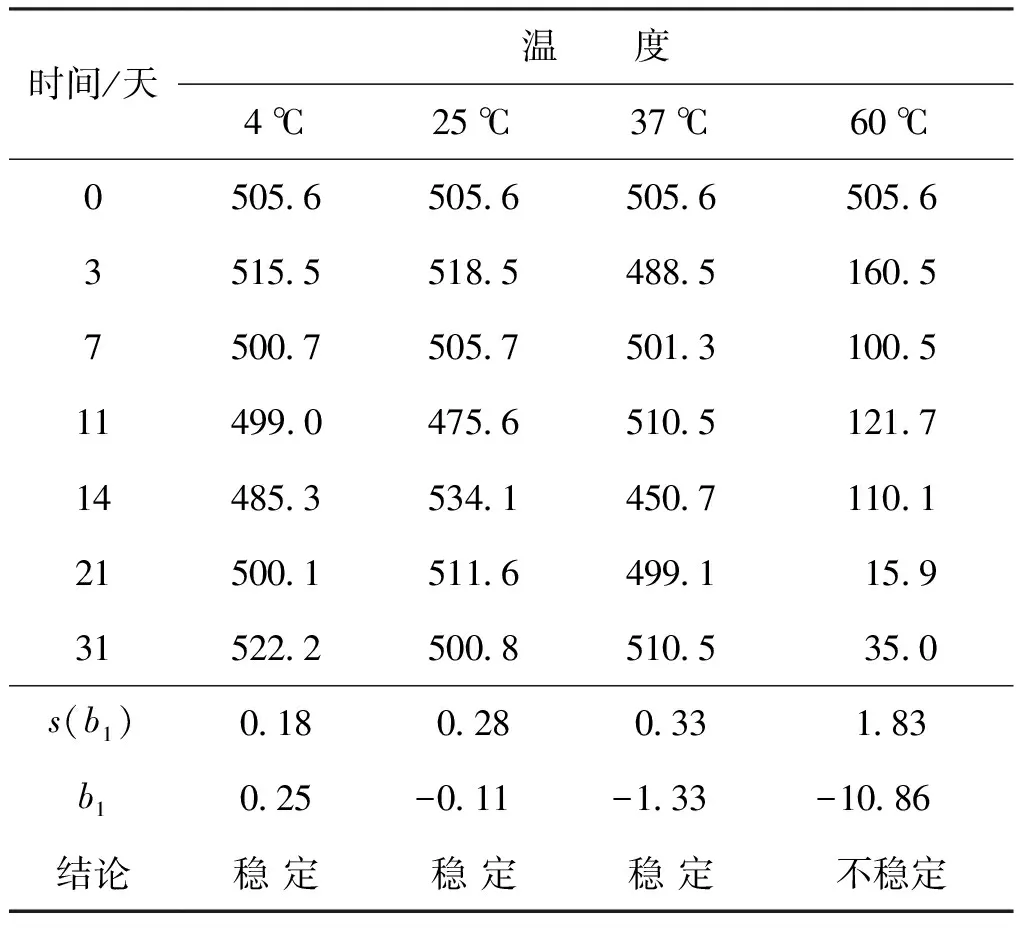
4.1 高通量显微成像测量方法的不确定度评定
4.2 流式细胞术测量方法的不确定度评定
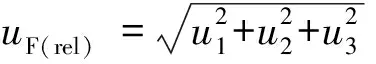
4.3 标准物质候选物的不确定度评定
5 结 论

