绿茶生物炭负载纳米零价铁对地下水中五价钒的去除效果及机理研究
张胤杰 易华炜 谭 笑 林爱军 刘亚修
(1.北京化工大学 化学工程学院,北京 100029;2.杭州环研科技有限公司,杭州 311122)
引 言
钒是地壳中第五大过渡金属,具有熔点高(1 890 ℃)、延展性好、强度大、耐腐蚀性能好等优点[1]。因此,钒作为一种重要的工业原料,被广泛应用于各个领域。但是由于自然淋洗、岩石风化以及钒矿石的提炼加工、化石燃料的燃烧、含钒废弃物的排放等原因,目前地下水中已存在一定程度的钒污染[2-3]。
目前,地下水污染的修复方法主要有原位修复法(如可渗透反应墙(PRB)[7])和异位修复法(如抽出-处理法[8])。异位修复技术具有简单易行和成熟度高的优点,但相较于原位修复法,其存在成本高、能耗大和形成二次污染的可能性大等缺点[9-11]。原位修复法中,PRB技术利用可渗透的反应墙对地下水中的污染物进行阻截和修复,具有占地表面积小、能量需求少、运行和维护费用低和对水文地质条件的影响小等优点,近年来逐渐成为地下水修复技术的研究热点之一[12-14]。PRB技术的关键是选择合适的活性填料,优异的活性填料不仅能减少修复成本,还能提高修复效率,并降低修复过程中可能产生二次污染的风险[15-16]。
生物炭是常用的活性填料之一,具有成本低、环境友好且易于合成的特点。目前,生物炭的制备方法多为利用废弃生物质材料(如秸秆、动物粪便、食物残渣等)进行热解[17-19]。所制备的生物炭具有发达的孔隙结构、较大的比表面积和大量的负电荷,能够吸附各种类型的重金属和有机污染物[20],但对高浓度污染物的去除能力有限[20-22]。对生物炭进行负载改性是提高生物炭对污染物去除能力的一种常用方法[21]。谭笑[22]发现锰改性后的生物炭相较于未改性的生物炭,对Cd(Ⅱ)和As(Ⅲ)的去除容量分别提高了27.2%和54.7%。Fan等[23]制备了纳米零价铁(nZVI)改性的玉米芯生物炭,其对水溶液中V(Ⅴ)的去除容量可达48.5 mg/g。
为了进一步提升生物炭对水溶液中V(Ⅴ)的去除能力以及提高废弃生物质材料的综合利用率,本文以绿茶渣为原料,使用热解法制备了生物炭,采用纳米零价铁对其进行负载改性,并优化了活性填料的制备条件;分析了V(Ⅴ)去除效果的影响因素,探究了吸附作用机理。本文的结果可以为地下水中钒的去除研究提供参考,并为绿茶渣的资源化再利用提供思路。
1 实验部分
1.1 实验材料
绿茶(龙井),杭州市西湖区梅家坞;0.45 μm滤膜(聚醚砜),天津市津腾实验设备有限公司;偏钒酸钠(NaVO3),纯度99%,阿拉丁试剂有限公司;硼氢化钠(NaBH4),纯度98%,伊诺凯科技有限公司;钨酸钠二水合物(Na2WO4·2H2O),纯度98%,毕得医药科技有限公司;磷酸氢二钠(Na2HPO4),分析纯,北京化工厂;无水乙醇,分析纯,天津市富宇精细化工有限公司;盐酸(HCl),分析纯,国药集团化学试剂有限公司;磷酸(H3PO4),分析纯,大茂化学试剂厂;硫酸亚铁(FeSO4)、碳酸钠(Na2CO3)、氯化钠(NaCl)和氢氧化钠(NaOH),均为分析纯,福晨化学试剂有限公司。
1.2 活性填料的制备与制备条件的优化
1.2.1生物炭的制备
将绿茶研磨,过40目筛(筛孔尺寸0.425 mm)。取100 g置于1 L去离子水中,搅拌均匀,在85 ℃下加热1 h,冷却至室温后离心分离,得到绿茶渣固体。将其置于烘箱中于60 ℃干燥48 h,然后破碎至40目,在氮气氛围下在管式炉(SK-G05123K型,天津中环电炉股份有限公司)中分别于300 ℃、500 ℃、700 ℃恒温热解2 h,升温速率为5 ℃/min。冷却后取出,用去离子水和无水乙醇依次洗涤数次,干燥24 h。将研磨干燥后的生物炭过200目筛(筛孔尺寸0.075 mm),备用。所得的生物炭记为BC。
1.2.2生物炭负载纳米零价铁
取5.85 g生物炭加入100 mL FeSO4溶液(0.25 mol/L)中,180 r/min振荡24 h。将浸渍后的混合物倒入三颈烧瓶中,在通氮条件下充分搅拌,加入50 mL无水乙醇,缓慢滴加50 mL NaBH4溶液(1 mol/L),搅拌30 min,离心分离,用去离子水和无水乙醇分别冲洗3次后,于60 ℃真空干燥12 h,备用。所得的负载纳米零价铁的生物炭记为nZVI@BC。
1.2.3活性填料制备条件的优化
分别配制0.25、0.5、0.75、1.0、1.5 mol/L的FeSO4溶液,并以n(NaBH4)∶n(FeSO4)=2∶1相应地调整还原剂NaBH4的用量,按照1.2.2节的方法制备nZVI@BC。在100 mL锥形瓶内,使用NaVO3配制50 mL质量浓度为50.0 mg/L的V(Ⅴ)溶液,加入0.5 g/L(25 mg)由不同浓度FeSO4溶液制备的nZVI@BC(热解温度Tp为700 ℃),固定溶液pH值为3,于25 ℃、180 r/min振荡24 h。静置后取上清液,使用0.45 μm滤膜过滤后,测定V(Ⅴ)去除率。根据V(Ⅴ)去除率筛选出最佳的FeSO4溶液浓度后,分别在不同的热解温度(300 ℃、500 ℃和700 ℃)下制备nZVI@BC,进行热解温度的优化。
1.3 测试与表征
使用扫描电子显微镜(SEM)(ZEISS Gemini 300,卡尔蔡司股份公司)观察样品的微观形貌;使用全自动比表面积分析仪(BET)(ASAP2460,美国麦克仪器公司)测定样品的比表面积和孔径;使用傅里叶变换红外光谱仪(FT-IR)(Bruker ALPHA II,美国布鲁克道尔顿公司)测定样品表面的官能团;使用X射线光电子能谱仪(XPS)(Thermo Scientific K-Alpha,赛默飞世尔科技公司)分析样品的元素组成、化学态和分子结构,激发源为Al Kα射线(0.6 eV),以C 1s(284.6 eV)为基准进行校正;使用X射线衍射仪(XRD)(Ultima IV,日本理学公司)分析样品的元素组成。
1.4 等温吸附试验
分别配制50 mL质量浓度为10、20、40、50、100、200 mg/L的V(Ⅴ)溶液,加入0.5 g/L(25 mg)的nZVI@BC(Tp=300 ℃,c(FeSO4)=1.0 mol/L)。同时配制50 mL质量浓度为15、20、40、80、100 mg/L的V(Ⅴ)溶液,分别加入0.5 g/L(25 mg)的BC(Tp=300 ℃)。将溶液于25 ℃、180 r/min振荡吸附24 h,静置后分别取5 mL上清液,过0.45 μm滤膜,测定V(Ⅴ)去除量。分别使用Langmuir、Freundlich和Sips模型对V(Ⅴ)去除量曲线进行拟合,判断吸附过程。
Langmuir模型为:
式中:Qe为在不同初始质量浓度的V(Ⅴ)下吸附达到平衡时V(Ⅴ)的去除量,mg/g;Qmax为活性填料的最大去除容量,mg/g;Ce为在不同初始质量浓度的V(Ⅴ)下吸附达到平衡时V(Ⅴ)的质量浓度,mg/L;kl为Langmuir方程常数,L/mg。
Freundlich模型为:

Sips模型为:
式中:ks为反应平衡常数,L/mg;ns为非均质系数。
1.5 吸附动力学
配制100 mL质量浓度为50 mg/L的V(Ⅴ)溶液,分别加入0.5 g/L(50 mg)的BC(Tp=300 ℃)和nZVI@BC(Tp=300 ℃,c(FeSO4)=1.0 mol/L)活性填料。于25 ℃、180 r/min振荡吸附,分别在不同时间取5 mL上清液,通过0.45 μm滤膜过滤后测定V(Ⅴ)去除量。使用吸附动力学方程进行拟合,判断吸附动力学过程。
准一级动力学模型为:
ln(Qe-Qt)=lnQe-k1t
式中:Qt为活性填料在t时刻的V(Ⅴ)去除量,mg/g;k1为准一级动力学模型的吸附速率常数,min-1。
准二级动力学模型为:
式中,k2为准二级动力学模型的吸附速率常数,g/(mg·min)。
Elovich模型为:
式中,a和b为Elovich模型吸附参数。
1.6 溶液pH和竞争离子对V(Ⅴ)去除效果的影响
1.6.1溶液pH
配制50 mL质量浓度为50.0 mg/L的V(Ⅴ)溶液,加入0.5 g/L(25 mg)的nZVI@BC(Tp=300 ℃,c(FeSO4)=1.0 mol/L),在pH为2~10的条件下,于25 ℃、180 r/min振荡吸附24 h,静置后分别取5 mL上清液,过0.45 μm滤膜,测定V(Ⅴ)去除率。
1.6.2竞争离子

1.7 V(Ⅴ)去除率和去除量测定
使用磷酸-钨酸钠分光光度法测定溶液中V(Ⅴ)的含量。吸取适量的水样于10 mL比色管中,依次加入1.0 mL用去离子水以1∶1稀释的HCl、1.0 mL用去离子水以3∶1稀释的H3PO4、2.0 mL质量浓度为50 g/L的Na2WO4溶液,用去离子水稀释至刻度,充分摇匀。于35 ℃恒温振荡显色30 min,以水为参比,在420 nm波长处使用紫外可见分光光度计(TU-1900,北京普析通用仪器有限责任公司)测定吸光度。以V(Ⅴ)的质量浓度为横坐标、吸光度为纵坐标,绘制标准曲线,结果如图1所示。拟合优度R2=0.999 06,表明在0.5~30 mg/L的范围内,吸光度与V(Ⅴ)质量浓度之间的线性关系良好。
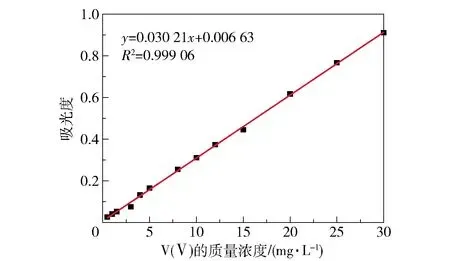
图1 吸光度与V(Ⅴ)质量浓度之间的标准曲线
按照下式计算V(Ⅴ)去除率。
式中:qe为V(Ⅴ)去除率,A0为初始溶液的吸光度,A1为反应后溶液的吸光度。
按照下式计算V(Ⅴ)去除量。
式中:Q为V(Ⅴ)去除量,mg/g;m为活性填料的投加量,g/L。
2 结果与讨论
2.1 活性填料的表征
图2为BC(Tp=300 ℃)与nZVI@BC(Tp=300 ℃,c(FeSO4)=1.0 mol/L)复合活性填料的SEM图。二者的外观为黑色粉末状固体,BC表面较为光滑,并分布有一定的孔道(图2(a)和(b))。nZVI@BC中,负载的nZVI主要分布在BC表面,成串状结构首尾相连,这保证了nZVI的稳定性且不易流失,并能够减少nZVI的团聚情况(图2(c))。同时,一部分nZVI聚集在BC的孔道附近,填充于BC的孔隙结构中,可有效防止部分Fe0被氧化(图2(d))。当nZVI@BC发生部分氧化时,BC表面生成疏松的片状结构,此时Fe0氧化生成了Fe3O4(图2(e)和(f))。

图2 BC和nZVI@BC的SEM图
表1为BC和nZVI@BC的比表面积和孔径。nZVI@BC的比表面积大于BC,这可能是由于氧化生成的Fe3O4在BC表面形成片状结构,增大了材料的比表面积。同时,nZVI@BC的孔径和孔容均大于BC。结果表明,生物炭经负载改性后,其结构有利于增强材料的物理吸附效果。

表1 BC和nZVI@BC的微孔结构参数

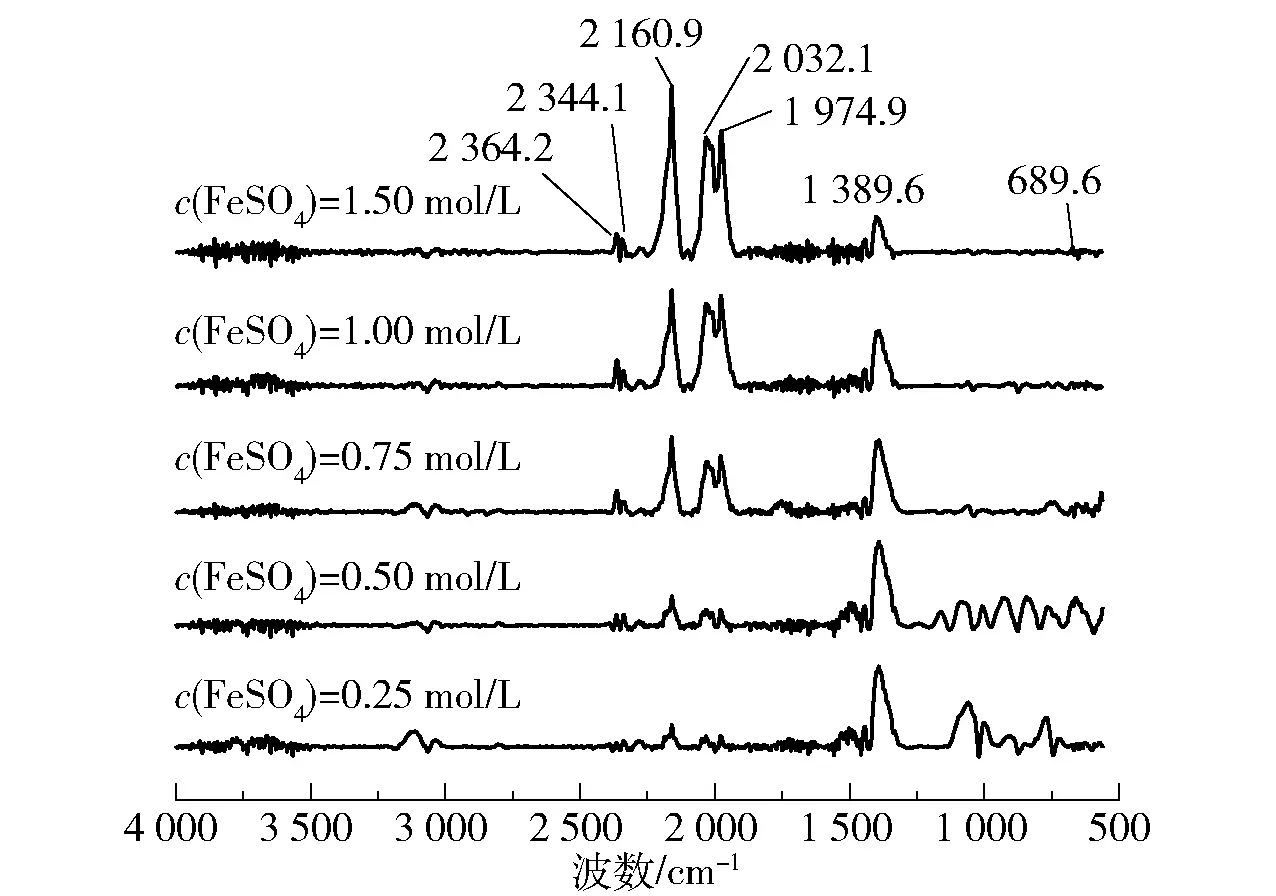
图3 不同浓度FeSO4溶液制备的nZVI@BC的FT-IR谱图
2.2 活性填料制备条件的优化结果
2.2.1FeSO4溶液浓度
图4为生物炭(热解温度Tp=700 ℃)经不同浓度FeSO4溶液改性后对V(Ⅴ)的去除率。c(FeSO4)为0.25 mol/L和0.5 mol/L时,V(Ⅴ)去除率均保持在较低的水平;当0.5 mol/L≤c(FeSO4)≤1 mol/L时,V(Ⅴ)去除率呈线性上升趋势;当c(FeSO4)=1 mol/L时,V(Ⅴ)去除率达到最大值。当负载量在低水平时(c(FeSO4)=0.25 mol/L),在反应过程中活性填料表面的nZVI在短时间内被氧化,并未较好地利用BC的表面[25]。而当c(FeSO4)=1.5 mol/L时,BC作为nZVI的载体可能出现负载饱和,游离的nZVI发生团聚,阻碍了BC的吸附点位;同时,过饱和的nZVI易于氧化,导致活性填料中具有还原活性的组分占比降低,进而出现去除率下降的情况[26]。因此,本文选择1.0 mol/L为最佳的FeSO4溶液浓度。

图4 nZVI@BC的V(Ⅴ)去除率随FeSO4溶液浓度的变化
2.2.2热解温度

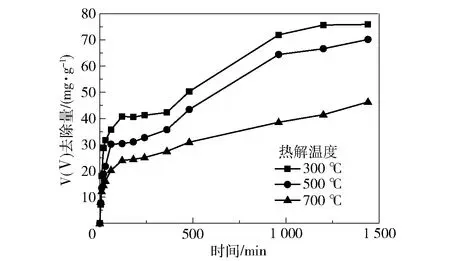
图5 不同热解温度下制备的nZVI@BC的V(Ⅴ)去除量随时间的变化
2.3 等温吸附模型分析
BC和nZVI@BC的等温吸附模型的拟合结果如图6和表2所示。使用Langmuir模型拟合BC吸附反应过程的R2最大(R2=0.83),表明该过程符合Langmuir模型,主要为单分子层吸附,并且其表面的吸附活性位点分布均匀[31]。而nZVI@BC的等温吸附过程更符合Sips模型(R2=0.96),说明材料表面的吸附位点是能量异质的。同时,在Sips模型中ns>1,表明材料发生了化学吸附反应[32]。

表2 等温吸附模型拟合参数

图6 BC和nZVI@BC的等温吸附拟合曲线
2.4 吸附动力学分析
BC和nZVI@BC对V(Ⅴ)的吸附动力学拟合结果如图7和表3所示。在吸附初始阶段,BC对V(Ⅴ)的吸附量快速增加;吸附20 min时,反应出现拐点,吸附速率逐渐减慢,吸附量达到吸附平衡时的67%;当吸附进行至4 h时,吸附基本达到平衡,BC对V(V)的去除量为6.35 mg/g。nZVI@BC在吸附初始阶段同样保持较高的反应速率;吸附20 min时,V(Ⅴ)去除量达15.14 mg/g,吸附速率大于BC;吸附60 min时,吸附出现拐点,吸附速率逐渐减缓,V(Ⅴ)去除率达到吸附平衡时的50%;当吸附6 h时,V(Ⅴ)去除率达到了吸附平衡时的75%;当吸附进行至1 140 min时,吸附趋于平衡,nZVI@BC对V(Ⅴ)的去除量达到71.6 mg/g。
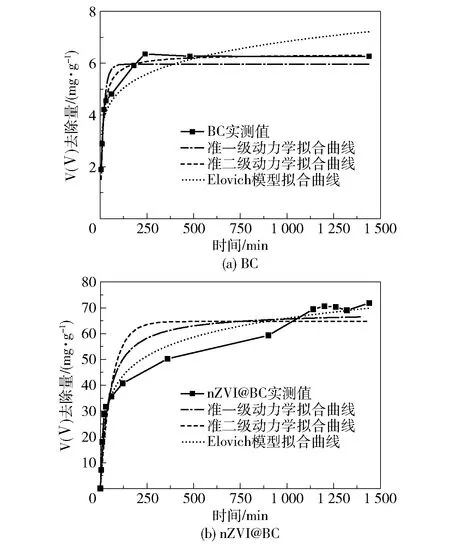
图7 BC和nZVI@BC的反应动力学拟合曲线
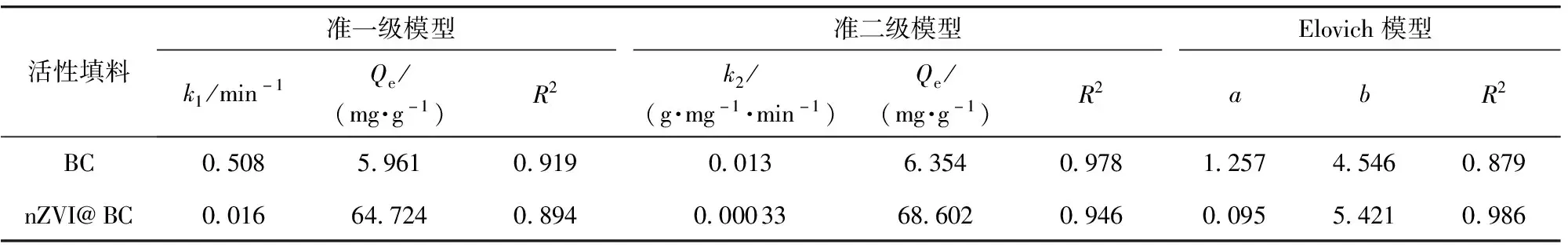
表3 反应动力学模型拟合参数
拟合结果表明,BC的吸附过程更符合准二级动力学过程(R2=0.978),推断该吸附过程的控速步骤为化学反应。而nZVI@BC的吸附过程更符合Elovich模型(R2=0.986),推断该吸附过程以化学吸附为主导,该材料的表面是异质的[33-35]。
2.5 V(Ⅴ)去除效果的影响因素分析
图8为溶液pH值和竞争离子对V(Ⅴ)去除效果的影响。由图8(a)可以看出,当pH=3.0时,V(Ⅴ)去除率最高。由于溶液中含有大量H+,提高了活性填料表面的电子传输效率,因此nZVI能保持高活性,具有极强的还原能力,有利于V(Ⅴ)的还原[36]。当pH>3.0时,随着pH的升高,V(Ⅴ)去除率逐渐降低。这是由于溶液中的OH-能够与游离的Fe2+、Fe3+反应,形成沉淀,降低了活性填料的还原能力。同时,在较高pH下,生物炭表面的电荷趋于负性,不利于V(Ⅴ)在表面的吸附,进而影响材料表面的电子转移效率,导致V(Ⅴ)去除率降低[37]。

图8 溶液pH值和竞争离子对V(Ⅴ)去除效果的影响
2.6 反应机理分析
图9为nZVI@BC在反应前后的XPS谱图。图9(a)中,707 eV和720 eV处的信号峰归为Fe0的结合能,表明nZVI成功负载在BC上;其余信号峰分别对应Fe(Ⅱ)和Fe(Ⅲ),表明BC表面有部分nZVI被氧化。图9(b)中,反应后Fe0对应的信号峰消失,说明在去除V(Ⅴ)的过程中,Fe0起到了关键的作用;反应后Fe(Ⅱ)和Fe(Ⅲ)的信号峰强度增加,说明Fe0发生了氧化还原反应,以Fe(Ⅱ)和Fe(Ⅲ)的形式继续存在于BC表面。分析反应前后材料的元素含量变化(表4),O含量从反应前的35.39%上升至反应后的40.68%,证明材料发生了氧化反应。而Fe含量在反应后有所下降,并出现了V元素,这是因为材料表面的Fe部分溶出,且吸附了一部分被还原的V。
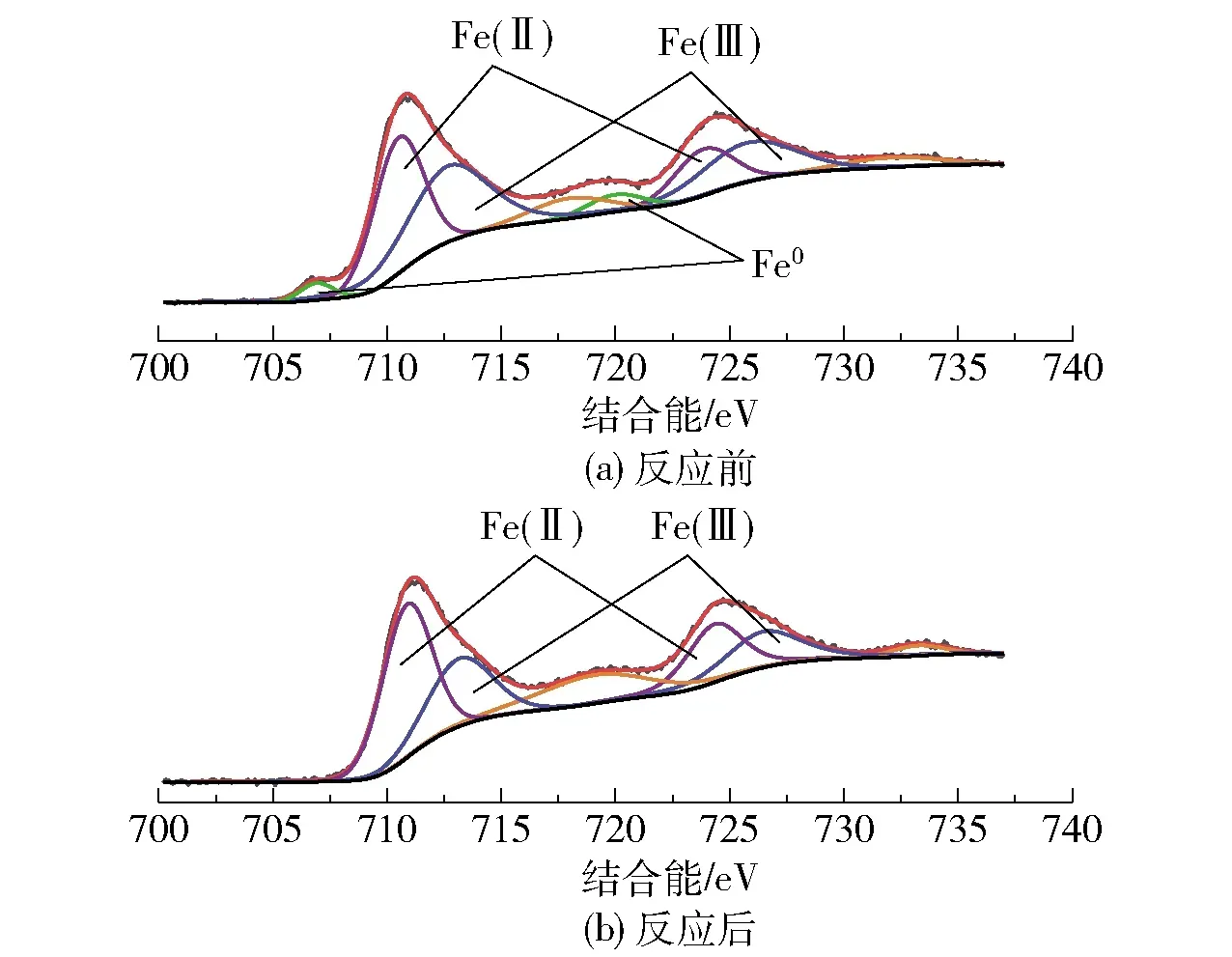
图9 nZVI@BC在反应前后的XPS谱图

表4 nZVI@BC在反应前后的元素含量
图10为nZVI@BC在反应前后的XRD谱图。反应前,Fe0的信号峰极其明显,并伴有铁氧化物(Fe3O4)的信号峰;反应后,Fe0的信号峰基本消失,出现铁氧化物(Fe2VO4)的信号峰。说明Fe0通过氧化还原反应,将溶液中的V(Ⅴ)还原为V(Ⅳ),降低了V的毒性。由此可推断反应过程为BC吸附V(Ⅴ)后,V(Ⅴ)与表面Fe0发生氧化还原反应,最后生成Fe2VO4并解析。
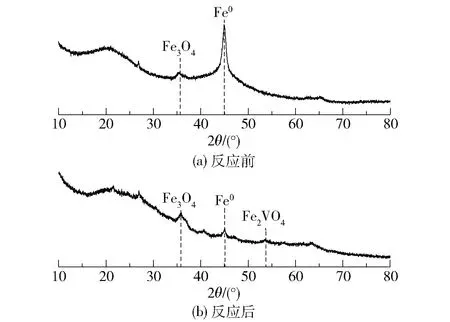
图10 nZVI@BC在反应前后的XRD谱图
值得注意的是,当nZVI@BC在水溶液中进行氧化还原反应时,可构成微型原电池结构。nZVI为阳极,BC为阴极,二者形成微电池回路,在表面形成部分电子与空穴,使溶液中的H+生成新生态氢,并参与氧化还原反应,从而提高V(Ⅴ)的去除效果[39]。
3 结论
本文利用常见的生产废料绿茶渣为生物质原料制备了活性炭,并在其表面负载零价铁,得到一种环境友好的PRB活性填料nZVI@BC,并测定了nZVI@BC对水溶液中V(Ⅴ)的去除效果,所得结论如下:
(1)通过优化nZVI@BC的制备条件,得到最佳的FeSO4溶液浓度为1.0 mol/L,热解温度为300 ℃。在该条件下制备的nZVI@BC在吸附19 h后对V(Ⅴ)的去除量达71.6 mg/g。
(2)溶液pH值对nZVI@BC的V(Ⅴ)去除量具有一定影响,当pH>3.0时,随着pH的升高,V(Ⅴ)去除率逐渐降低。地下水中的共存阴离子与V(Ⅴ)发生竞争吸附,使V(Ⅴ)去除率降低。
(3)nZVI@BC的等温吸附过程符合Sips模型,表明其表面的吸附位点是能量异质的。nZVI@BC的反应动力学过程更符合Elovich模型,表明其在与V(Ⅴ)的反应过程中主要发生化学吸附反应。
(4)nZVI@BC去除V(Ⅴ)的机理主要为物理吸附和化学还原。推断反应过程为:BC吸附V(Ⅴ)后,表面Fe0与V(Ⅴ)发生氧化还原反应,生成Fe2VO4,V(Ⅴ)被还原为V(Ⅳ),从而实现V(Ⅴ)的去除。

