长期无症状高尿酸血症对慢性肾脏病心肾结局的影响
刘伟,吴萌,端靓靓,黄小抗,蔡文娇,王旭
尿酸(uric acid,UA)或尿酸盐是内源性或饮食中的嘌呤核苷酸在体内的代谢终产物,血浆中循环UA 是由黄嘌呤脱氢酶或黄嘌呤氧化酶产生的,尿酸在人体不能进一步代谢,必须通过肾脏或肠道排泄,健康的肾脏消除约70% 的血清尿酸(SUA),大约50%的慢性肾脏病(chronic kidney disease,CKD)病人在肾脏替代治疗之前已经出现高尿酸血症[1-3]。目前仍然不清楚无症状高尿酸血症(hyperuricemia,HUA)是否是心血管疾病的独立危险因素,一些流行病学和观察性研究表明HUA 与心血管事件、高血压和糖尿病相关[4-5]。有研究表明,HUA可预测各种肾病中肾脏疾病和CKD 的进展,UA 值和体质量指数(BMI)与估算的肾小球滤过率(eGFR)下降≥50% 或进入终末期肾病正相关[6]。目前,对于CKD合并无症状HUA 对心肾的长期预后尚缺少大规模的、长时间的研究,本研究的目的在于探讨CKD 无症状HUA是否对心肾的长期预后产生影响。
1 资料与方法
1.1 一般资料选取2016 年1—12 月在安庆市立医院肾内科连续入院的CKD 1~5期148例病人。研究时间从病人住院开始,观察到发生终点事件或到2020 年12 月。其中男76 例(51.4%),女72 例(48.6%),年龄50.2 岁,范围为18~79 岁。高尿酸定义为男性≥420 µmol/L,女性≥380 µmol/L。高血压定义为测量血压:收缩压≥140 mm Hg 或舒张压≥90 mmHg;糖尿病定义为正在接受降糖药物治疗的糖尿病;BMI=体质量(kg)/身高(m2);吸烟与否(既往及现今);eGFR 使用中国人肾病饮食调整(MDRD)方程根据血肌酐水平及年龄计算。已用治疗药物,如他汀类药物、血管紧张素转化酶抑制剂(ACEIs)或血管紧张素受体阻滞剂(ARB);同时记录CKD 的原发病因。排除标准:(1)CKD5期已透析病人;(2)已有痛风发作病史;(3)已经降尿酸治疗病人。病人或其近亲属知情同意,签署知情同意书。本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2 观察指标基线资料包括年龄、性别、SUA、BMI、血压、血糖、血脂、尿蛋白、血白蛋白、肝功能、血肌酐、eGFR、C 反应蛋白(CRP)、引起CKD 的原发病、吸烟史、用药史,终点事件定义为:(1)痛风发作;(2)心脏事件(心源性猝死、心肌梗死);(3)肌酐倍增或进入透析。
1.3 研究方法对病人进行规范治疗。并从其住院开始,不间断地观测其发生各类终点事件的时间。并按入院时尿酸水平将病人分为正常尿酸组和高尿酸组,分别比较两组各项指标并行对心肾预后结局终点的K-M生存分析及COX影响因素分析。
1.4 统计学方法所有数据均采用SPSS 20.0 统计软件进行处理,计量资料符合正态分布以±s表示,组间比较采用两独立样本t检验。 非正态分布的计量资料用中位数(下、上四分位数)表示,即M(P25,P75),组间比较为秩检验。计数资料以例(%)表示,组间比较采用χ2检验。用COX 比例风险回归模型作多因素分析,Kaplan-Meier 方法作生存分析+log-rank检验,并绘制生存曲线。P<0.05为差异有统计学意义。
2 结果
2.1 临床特征比较与CKD正常尿酸组相比,CKD高尿酸组eGFR、总胆固醇、低密度脂蛋白均较低(P<0.05),而收缩压及舒张压均明显高于CKD 正常尿酸组(P<0.05)。年龄、糖尿病史、吸烟史、BMI、用药史两组间差异无统计学意义(P>0.05),见表1。
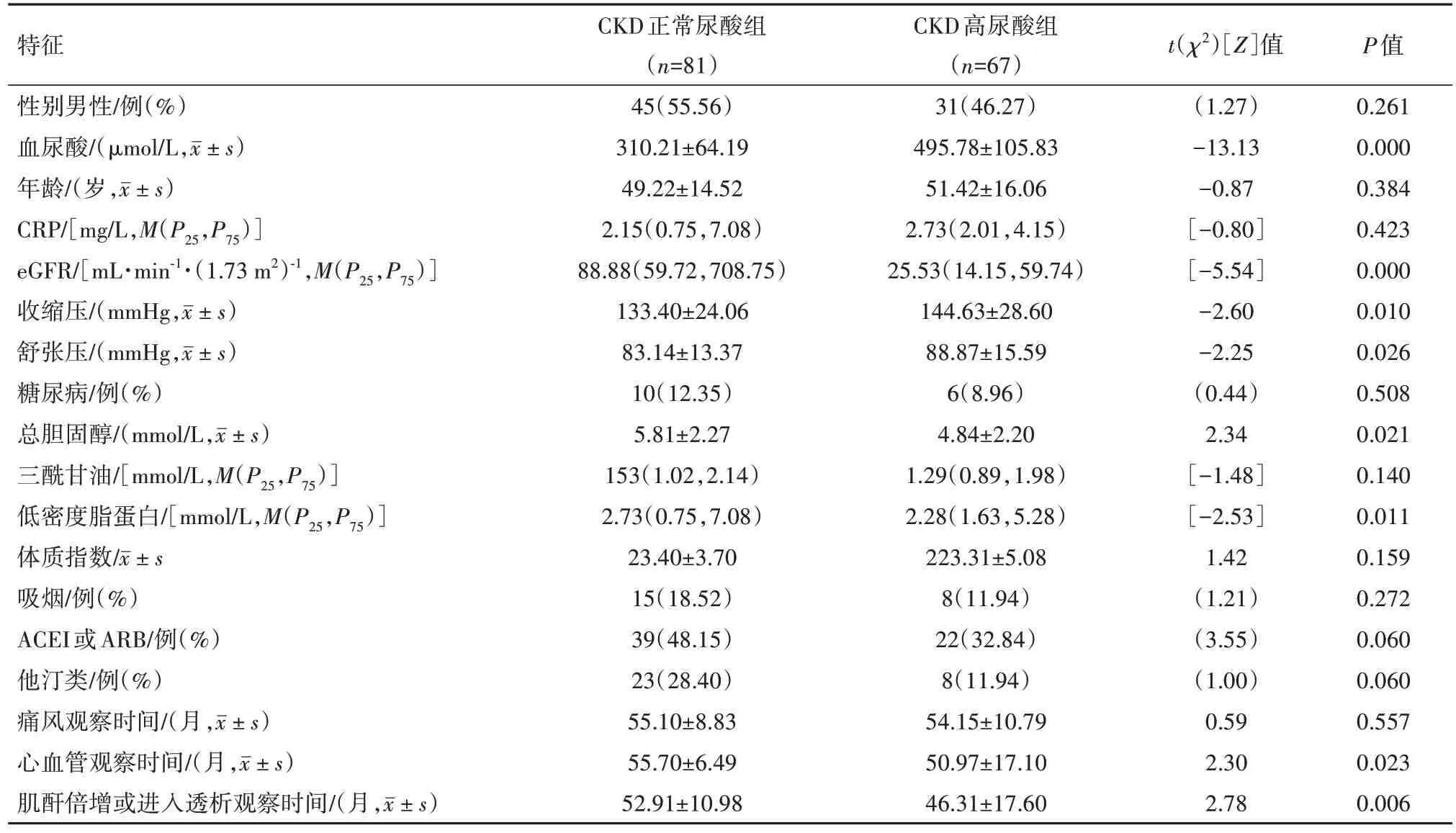
表1 慢性肾脏病(CKD)148例基本特征
CKD 病因中,慢性肾小球肾炎占17.5%,膜性肾病占14.9%,IgA 肾病及糖尿病肾病分别占8.1%,CKD不明病因占23.6%,见表2。
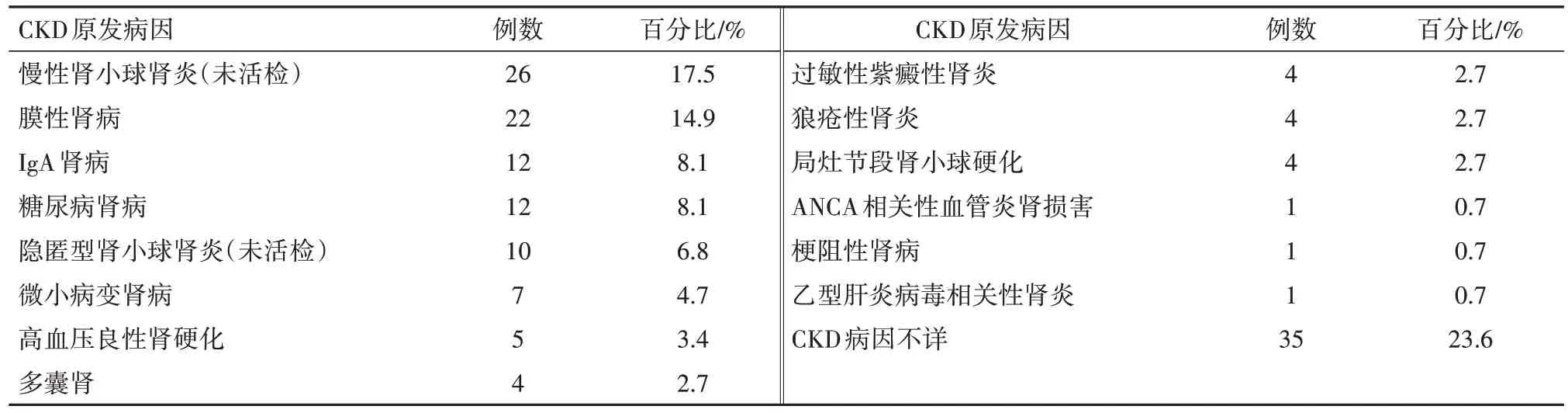
表2 慢性肾脏病(CKD)148例原发病因分析
CKD3、4、5期高于CKD1、2期,差异有统计学意义(F=14.63,P=0.000)。CKD 各期的尿酸分布见表3。
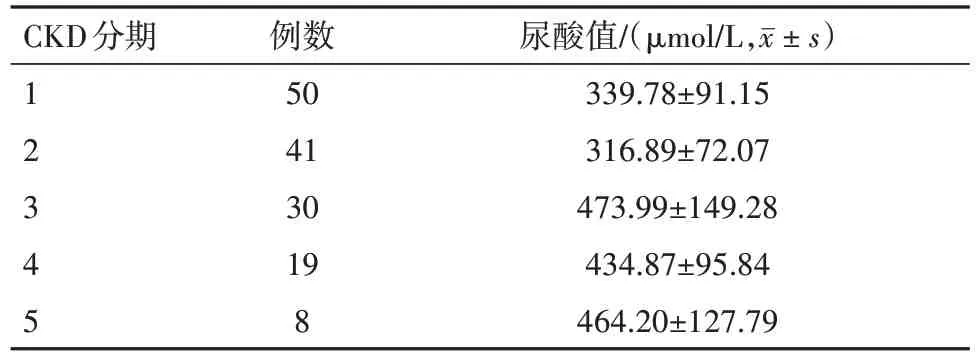
表3 慢性肾脏病(CKD)148例各期尿酸值比较
2.2 高尿酸对病人痛风发作、发生心血管事件、肌酐倍增或进入ESRD 及的影响 148 例病人均获得长期随访,观察时间46.31~55.70个月。其中正常尿酸CKD 组3 例(3.70%)发生痛风急性发作,高尿酸CKD 组4 例(5.97%)发生痛风急性发作;正常尿酸CKD 组3 例(3.70%)发生心血管事件,高尿酸CKD组9 例(13.43%)发生心血管事件;正常尿酸CKD 组12 例(14.82%)出现肌酐倍增或进入ESRD,高尿酸CKD 组31 例(46.27%)出现肌酐倍增或进入ESRD。分别:①以病人痛风发作作为终点事件,Kaplan-Meier 生存分析+log-rank 检验显示:高尿酸CKD 组痛风急性发作与正常尿酸CKD 组病人差异无统计学意义(χ2=0.37,P=0.541);②以病人出现心血管事件作为终点事件,Kaplan-Meier 生存分析+Logrank检验显示:高尿酸CKD 组心血管事件高于正常尿酸CKD组病人(χ2=3.69,P=0.055);③以病人出现肌酐倍增或进入ESRD 作为终点事件,Kaplan-Meier 生存分析+Logrank 检验显示:高尿酸CKD 组肾脏预后明显差于正常尿酸CKD组病人(χ2=16.62,P=0.000)。
2.3 COX 比例风险回归结果回归设计:建立COX 比例风险回归模型,以本研究资料为样本,以心肾长期预后为应变量,赋值1=心肾长期预后不好(出现2.2节所述终点事件),0=否,t=出现终点时间。参考选择表1 中P<0.10 的指标/因素为自变量。各变量赋值参见表4。
回归过程采用逐步后退法,以进行自变量的选择和剔除,设定α剔除=0.10,α入选=0.05。回归结果表明高UA 可作为评估CKD 病人预后的一项独立指标(P<0.05)。此外,年龄、糖尿病、eGFR也具有独立的预后评估意义(P<0.05),见表4。
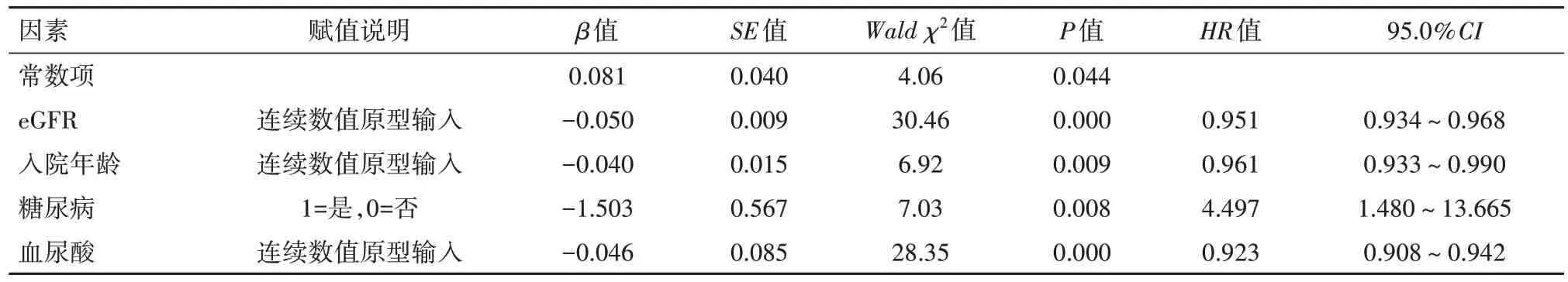
表4 COX回归模型多因素生存分析
3 讨论
无症状HUA 是指血清尿酸浓度升高但既没有出现尿酸盐晶体沉积(例如痛风或尿酸肾病)所导致的症状或体征。与高尿酸血症相关的三种主要晶体沉积相关疾病为痛风、尿酸盐肾病和肾结石,持续性无症状高尿酸血症会增加发生尿酸或尿酸结晶相关临床事件的风险,并且各自的风险至少部分与高尿酸血症的程度和持续时间有关[7-9]。肾脏疾病是高尿酸血症的重要病因,而高尿酸血症也是CKD 最常见的并发症之一。有研究认为,高尿酸可加重肾脏病进展及心脑血管并发症的发生,是导致CKD、心脑血管疾病及代谢性疾病发生、发展的独立危险因素[10]。高尿酸血症可能有助于肾病进展,部分原因是通过刺激传入小动脉血管平滑肌细胞增殖降低肾灌注[11]。也有研究认为,尿酸在肾脏和心血管疾病中没有因果关系,而是一个风险标志物,尿酸如果升高,肾病及心血管疾病风险会更高[12]。
本研究选取CKD1~5 期148 例住院病人,并对心肾终点事件进行长期观察,观察时间46.31~55.70个月。与CKD 正常尿酸组相比,CKD 高尿酸组eGFR 明显较低(P<0.05),而收缩压及舒张压均明显高于CKD正常尿酸组,提示CKD高尿酸组可能更容易肾病进展及更高的心血管疾病风险。Kaplan-Meier生存分析显示高尿酸CKD 组痛风急性发作与正常尿酸CKD 组病人差异无统计学意义(χ2=0.37,P=0.541),正常尿酸CKD组3例(3.70%)发生痛风急性发作,而高尿酸CKD 组4 例(5.97%)发生痛风急性发作。本研究提示,CKD 病人高尿酸并没有增加痛风发生率,CKD 时由于尿酸排泄减少,故伴随肾小球滤过率的减少,尿酸伴随肌酐逐渐升高,这可能与高尿酸血症导致的肾损害发生机制不同,因此对于CKD 伴有无症状HUA 究竟何时启动降尿酸治疗仍有很多争议[13-14]。
本研究中,正常尿酸CKD 组3 例(3.70%)发生心血管事件,高尿酸CKD 组9 例(13.43%)发生心血管事件,高尿酸CKD 组心血管事件高于正常尿酸CKD 组病人(χ2=3.69,P=0.055)。虽然高尿酸CKD组高血压比正常尿酸CKD 组发生率高,但两组糖尿病史、吸烟史、体质指数、用药史两组间差别无统计学意义(P>0.05),而正常尿酸CKD 组血脂比高尿酸CKD 组更高(P<0.05),提示两组可能心血管风险相近,尿酸代谢与血脂、血糖代谢也有密切关联[15]。正常尿酸CKD 组12 例(14.82%)出现肌酐倍增或进入ESRD,高尿酸CKD 组31 例(46.27%)出现肌酐倍增或进入ESRD,高尿酸CKD 组肾脏预后明显差于正常尿酸CKD 组病人(χ2=16.62,P=0.000)。我们的观察结果与既往文献报道类似[16-19],CKD 高尿酸组有更多病人肌酐升高或进入ESRD,但高尿酸与肾病进展是否是因果关系,因为观察性研究性质尚无定论。CKD 高尿酸组eGFR 更低(P<0.05),不能排除基础eGFR 的影响。进一步行COX 回归模型多因素生存分析,结果表明高UA 可作为评估CKD 病人预后的一项独立指标(P<0.05)。此外,年龄、糖尿病、eGFR也具有独立的预后意义(P<0.05)。
本研究提示:(1)CKD 无症状高尿酸与正常尿酸CKD 组比并没有增加痛风发生率;(2)CKD 无症状高尿酸组比正常尿酸CKD 组心血管事件发生率高;(3)CKD 无症状高尿酸组肾脏预后明显差于正常尿酸CKD 组。本研究缺陷在于:(1)样本量小,148例病人尚不能完全反应CKD 病人整体情况;(2)选择偏倚,入选的病人均为同期住院病人,存在一定的选择性偏倚,且未能对其他危险因素进行分层匹配,故可能对研究结果有一定干扰。

