多指标综合评分法结合正交试验优选参枣滴丸的水提工艺
王佳雪,刘渠,2,3,简尚宇,胡涛,2,3,梁生旺,2,3,王淑美,汤丹,2,3,张陆勇
(广东药科大学1.中药学院;4.药学院;5.新药研发中心,广东广州510006;2.国家中医药管理局中药数字化质量评价技术重点研究室,广东广州510006;3.广东省中药质量工程技术研究中心,广东广州510006)
参枣滴丸为本课题组在研中药新药,由广枣、丹参、人参、降香等组成,具有理气止痛、活血化瘀等功效,用于治疗冠心病、心绞痛等病症[1]。研究表明,广枣的主要化学成分包括黄酮类、酚酸类等[2],主要有效成分为没食子酸,可明显改善心肌梗死后心肌纤维化[3]。丹参中含有的主要化学成分为丹参酮ⅡA等丹参酮类脂溶性成分和丹酚酸B 等酚酸类水溶性成分[4],丹酚酸B 对防治动脉粥样硬化有明显作用[5]。人参皂苷和多糖为人参主要有效成分,人参皂苷具有保护和改善心肌缺血的作用[6]。
中药复方的临床运用多为汤剂,课题组前期通过综合考虑参枣滴丸中各成分比例、性质和药理作用,初步确定了参枣滴丸的提取工艺为水煎,本研究以丹酚酸B[7]77、没食子酸[7]45和人参皂苷(Rg1、Re、Rb1)[7]8多组分指标作为评价标准,采用正交试验方法对提取时间、加水倍数和提取次数进行考察,进一步优化参枣滴丸的提取工艺,为其后续研究开发提供参考。
1 仪器与材料
1.1 仪器
岛津LC‑20AT 高效液相色谱仪(日本岛津株式会社);SQP 电子分析天平[赛多利斯科学仪器(北京)有限公司];ME104 电子分析天平[梅特勒‑托利多仪器(上海)有限公司];JJ500电子天平(常熟市双杰测试仪器厂);KQ‑300DZ 超声波清洗机(昆山市超声仪器有限公司);HWS26型电热恒温水浴锅(上海一恒科学仪器有限公司)。
1.2 试剂
甲醇、乙腈(色谱级,瑞典Oceanpak公司);超纯水(屈臣氏集团);冰乙酸(色谱级,上海麦克林生化科技有限公司);磷酸(色谱级,上海阿拉丁生化科技股份有限公司);正丁醇、95%乙醇、甲醇和NaOH(分析级,天津市致远化学试剂有限公司)。
1.3 试药
人参皂苷Rg1对照品(批号:110703‑201832)、人参皂苷Re 对照品(批号:110754‑201827)、人参皂苷Rb1对照品(批号:110704‑201827)、丹酚酸B 对照品(批号:11562‑201716)、没食子酸对照品(批号:110831‑201605)均购于中国食品药品检定研究院;丹参(批号:190101)、人参(批号:181202)、降香(批号:190201)均购于广州至信药业股份有限公司;广枣(批号:190426)购于安徽亳州普润药业有限公司。
2 方法与结果
2.1 指标成分质量分数的测定
选择丹酚酸B、没食子酸和人参皂苷(Rg1、Re、Rb1)为指标成分,参考2020 年版《中国药典》(一部),制定各成分质量分数的测定方法,并进行方法学验证。结果表明,建立的有效成分HPLC 质量分数测定方法满足检测要求。
2.1.1 溶液的制备
供试品溶液的制备:按配方比例称取广枣、丹参、人参、降香药材饮片,加6 倍量水煎煮30 min,过滤,加无水乙醇至70%进行醇沉,过滤,即得丹酚酸B 和没食子酸供试品溶液。将此供试品溶液在60 ℃下旋干去除乙醇,加等量水溶解,等量水饱和正丁醇萃取4次,合并正丁醇层,用1%NaOH溶液洗涤2 次,用正丁醇饱和水洗涤3 次,过滤,滤液于60 ℃旋干,加甲醇定容至5 mL,即得人参皂苷测定用供试品溶液。
对照品溶液的制备:分别精密称取丹酚酸B(8.130 mg)、没食子酸(10.43 mg)和人参皂苷(Rg1、Re、Rb1分别为8.310、8.400、8.100 mg)对照品,置于10 mL量瓶中,分别加入80%甲醇、甲醇、甲醇溶解、定容,分别制成0.813 0 mg/mL 丹酚酸B 对照品溶液、1.043 0 mg/mL 的没食子酸对照品溶液和人参皂苷混合对照品溶液(Rg1、Re、Rb1质量浓度分别为0.207 8、0.210 0、0.202 5 mg/mL)。
阴性样品溶液的制备:除对照药材外,按配方比例称取其他药材饮片,与供试品溶液同法制备,即得阴性样品溶液。
2.1.2 色谱条件
丹酚酸B色谱条件:FeiniGen C18色谱柱(4.6 mm×250.0 mm,5.0 μm),柱温为20 ℃,流动相为乙腈‑0.1%磷酸(体积比22∶78),检测波长为286.0 nm,流速为1.2 mL/min,进样量为10 μL。
没食子酸色谱条件:FeiniGenXPeonyx AQ‑C18色谱柱(4.6 mm×250.0 mm,5.0 μm),柱温为25 ℃,流动相为甲醇‑0.3%冰乙酸(体积比1∶99),检测波长为270.0 nm,流速为1.0 mL/min,进样量为10 μL。
人参皂苷Rg1、Re 和Rb1色谱条件:Agela Tech‑nologies Venusil XBP C18(L)色谱柱(4.6 mm×250.0 mm,5.0 μm),柱温为30 ℃,流动相为乙腈‑0.1%磷酸(梯度洗脱,见表1),检测波长为203.0 nm,流速为1.0 mL/min,进样量为10 μL。

表1 人参皂苷梯度洗脱程序Table 1 The gradient elution procedure of Ginsenoside
2.1.3 方法学验证
2.1.3.1 专属性试验取各指标功效成分的对照品溶液、供试品溶液和阴性对照溶液各进样10 μL,方法专属性考察结果见图1。可见,供试品在与对照品相应位置有对应色谱峰,阴性样品无干扰;丹酚酸B、没食子酸、人参皂苷(Rg1、Re、Rb1)基本上可达到基线分离,分离度>1.5;理论塔板数以没食子酸峰计应不低于3 000,以丹酚酸B 和人参皂苷Rg1峰计应不低于6 000;表明各方法专属性良好。

图1 专属性试验HPLC色谱图Figure 1 HPLC chromatograms of specificity test
2.1.3.2 线性范围以“2.1.1”项对照品溶液为母液,稀释制成一系列对照品溶液,吸取10 μL 进行液相分析。以质量浓度(mg/mL)为横坐标(x)、峰面积为纵坐标(y)绘制标准曲线,进行线性回归分析。
精密吸取1、2、5、8、10、15 μL 丹酚酸B 对照品溶液进行分析,得丹酚酸B 线性回归方程为y=10 007 958.67-43 931.23x,r=1.000,表明丹酚酸B对照品在0.813 0~12.20 μg 范围内与峰面积呈良好线性关系。
取没食子酸对照品溶液适量,加甲醇稀释定容至10 mL,制成质量浓度分别为0.010 43、0.020 86、0.041 72、0.104 3、0.208 6 mg/mL 的一系列溶液,进样分析,得线性回归方程为y=30 039 004.20x,r=0.999 9,没食子酸对照品在浓度0.010 43~0.208 6 mg/mL范围内与峰面积呈良好线性关系。
精密量取人参皂苷Rg1、Re、Rb1对照品溶液适量,加甲醇稀释定容至10 mL,制成系列人参皂苷混合对照品溶液,其中,人参皂苷Rg1质量浓度梯度为0.053 20、0.106 3、0.265 8、0.531 5、0.850 4、1.063 mg/mL,人参皂苷Re质量浓度梯度为0.039 50、0.079 00、0.197 5、0.395 0、0.632 0、0.790 0 mg/mL,人参皂苷Rb1质量浓度梯度为0.040 60、0.081 10、0.202 8、0.405 5、0.648 8、0.811 0 mg/mL。得人参皂苷Rg1回归方程y=3 494 935.74x,r=0.999 9;人参皂苷Re 回归方程y=2 760 475.76x,r=0.999 9;人参皂苷Rb1回归方程y=2 477 157.31x,r=0.999 9。表明人参皂苷Rg1、Re、Rb1分别在质量浓度0.053 20~1.063 mg/mL、0.039 50~0.790 0 mg/mL、0.040 55~0.811 0 mg/mL 范围内与峰面积呈良好线性关系。
2.1.3.3 重复性试验平行制备6 份供试品,精密吸取10 μL 进行液相分析,测得峰面积,求质量分数和RSD值。结果显示丹酚酸B、没食子酸、人参皂苷样品的质量分数分别为24.9、0.97、2.6 mg/g,RSD 值分别为2.44%、1.17%和4.12%(n=6),表明方法重现性良好。
2.1.3.4 精密度试验取已知浓度的供试品溶液,连续进样3 d,每天1 次,记录指标成分的峰面积和RSD 值。结果显示,供试品丹酚酸B、没食子酸、人参皂苷(Rg1、Re、Rb1)峰面积的RSD 值为1.05%、0.79%和1.23%(n=3),表明方法精密度良好。
2.1.3.5 稳定性试验取同一份供试品溶液,分别于0、2、4、8、10、12 h 进样测定,记录6 次进样峰面积和RSD 值。结果显示,丹酚酸B、没食子酸、人参皂苷RSD值为0.47%、0.35%和2.04%(n=6),表明方法稳定性良好。
2.1.3.6 加样回收试验分别取含27 mg 丹参、60 mg 广枣和657 mg 人参生药量的供试品(n=6),对应精密加入丹酚酸B、没食子酸、人参皂苷混合对照品溶液1 mL,加70%乙醇定容至5 mL,摇匀,过滤,精密吸取10 μL 进行液相分析,计算含量、加样回收率及RSD 值(n=6)。结果显示,丹酚酸B 平均加样回收率为97.37%、RSD 值为3.01%,没食子酸平均加样回收率为100.8%、RSD 值为0.43%,人参皂苷(Rg1、Re、Rb1总量)的平均加样回收率为91.31%、RSD值为1.60%,表明方法准确度良好。
2.2 正交试验设计与结果
采用正交试验优选参枣滴丸的水提工艺,按处方比例称取广枣50 g、人参33 g、丹参33 g、降香33 g,以广枣中没食子酸、丹参中丹酚酸B、人参中人参皂苷总含量(Rg1、Re、Rb1总量)为指标成分,以提取时间、加水倍数和提取次数为考察因素,采用L9(34)正交试验表进行工艺考察,因素水平及试验结果详见表2-3。各指标评分权重分别为广枣占0.4、丹参占0.3、人参占0.3,综合评分(Y)=0.4(A-Amin)/(Amax-Amin)+0.3(B-Bmin)/(Bmax-Bmin)+0.3(C-Cmin)/(Cmax-Cmin),其中A 为没食子酸质量分数、B 为丹酚酸B 质量分数、C 为人参皂苷Rg1、Re、Rb1总质量分数。方差分析见表4。
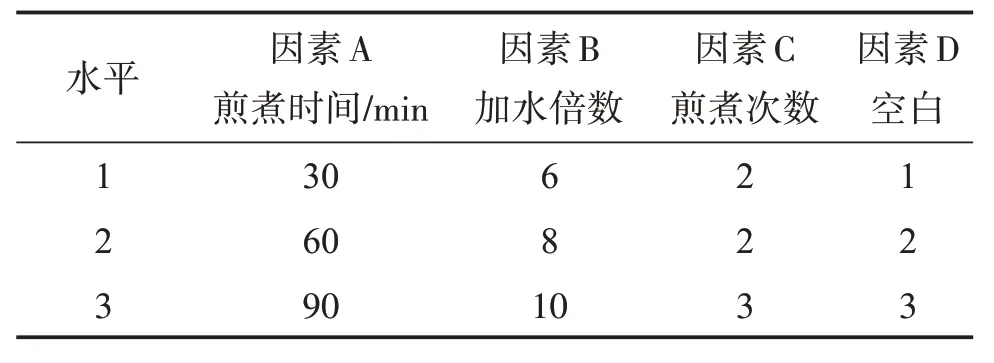
表2 因素水平表Table 2 Factor level table
可见,最佳工艺为A1B2C3,即煎煮时间30 min,8 倍量水,煎煮3 次;C(煎煮次数)对水提工艺的影响最大,但F 值小于F 临界值,表明差异无统计学意义。由于3 个因素的影响均无统计学意义,从工业生产成本和能源节约的角度考虑,最终确定水提工艺为每个因素的初始水平,即:加6倍量水,煎煮2次,每次30 min。
2.3 工艺验证试验
为进一步验证工艺的可行性和合理性,按处方比例称取广枣50 g、人参33 g、丹参33 g、降香33 g,以上述确定的最佳提取工艺条件(6 倍量水,煎煮2 次,煎煮时间30 min),平行试验3 次,每组平行取2 份样品进行检测,检测结果见表5。可见,水提液中的丹酚酸B、没食子酸的质量分数和人参皂苷Rg1、Re、Rb1总质量分数基本稳定且与正交试验数据基本吻合,表明该优选工艺条件可行。
3 讨论
中药复方成分复杂,作用方式多靶点、多层次[8]。若以单一成分指标进行工艺优选,不能保证中药复方整体质量[9];对指标成分进行合理的选择和确定,是优选提取工艺的关键[10‑11]。研究表明,广枣中没食子酸、丹参中丹酚酸B 以及人参中的人参皂苷Rg1、Re、Rb1等成分是治疗心血管疾病的主要有效成分。因此,本研究选择以上成分为指标成分,基于多组分指标和正交试验对参枣滴丸有效成分的提取工艺进行优选,体现了中药复方多成分的整体特点。
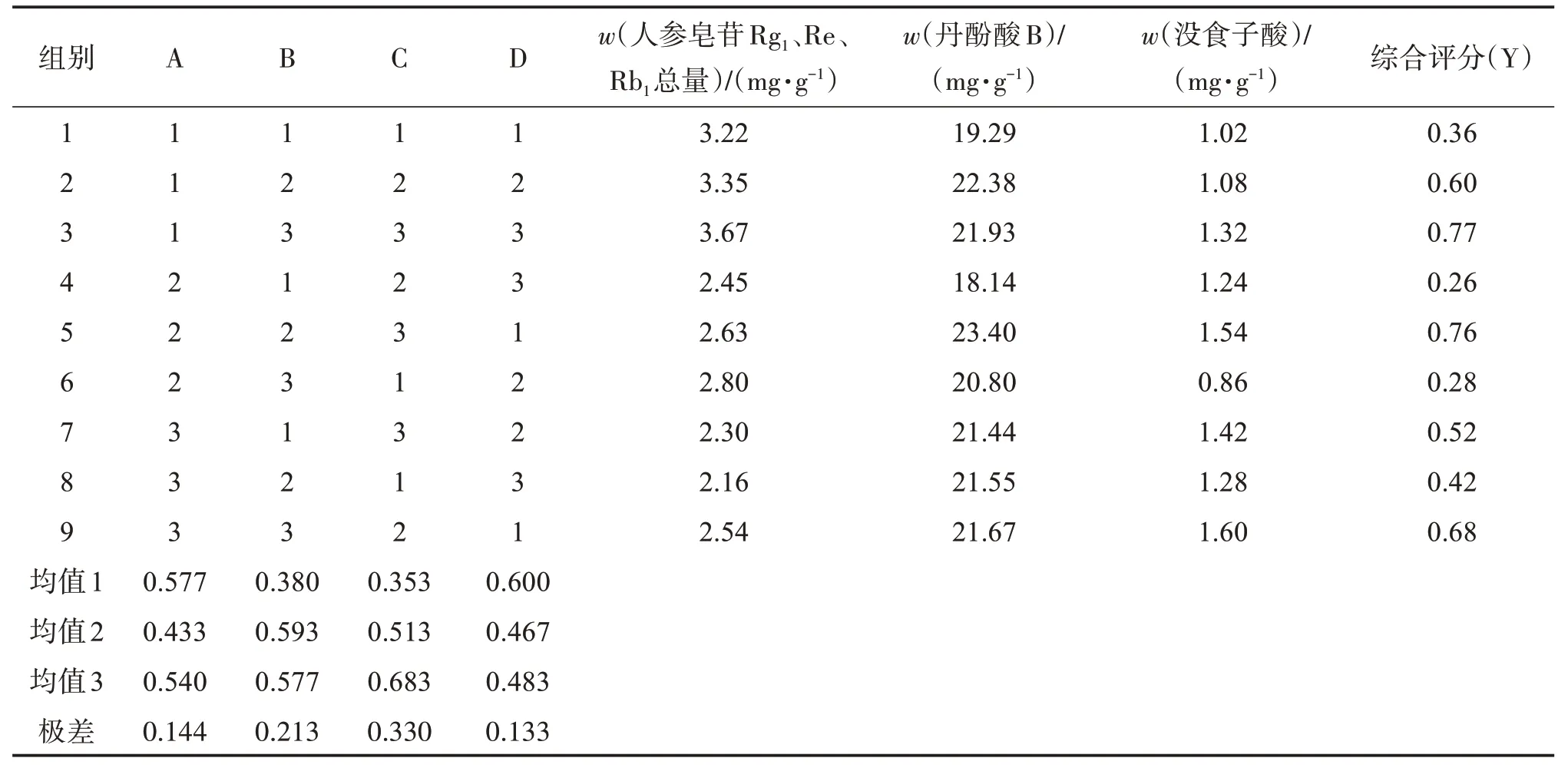
表3 参枣滴丸水提工艺的L9(34)正交试验结果Table 3 The L9(34)orthogonal test results of the water extraction process of Shenzao Dropping Pills
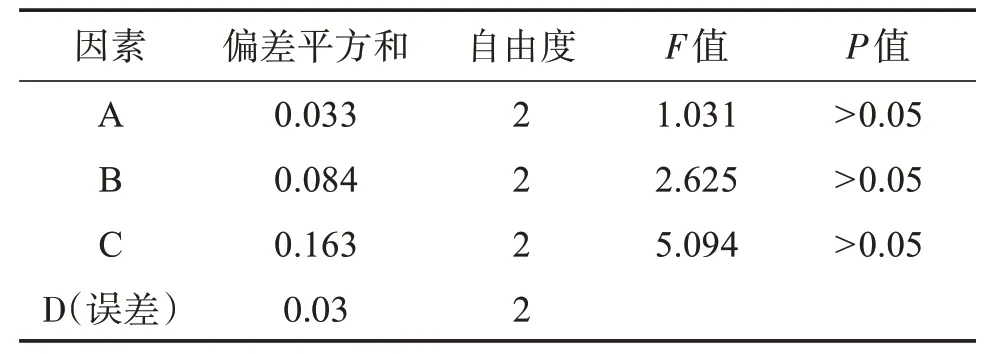
表4 方差分析结果Table 4 The results of variance analysis
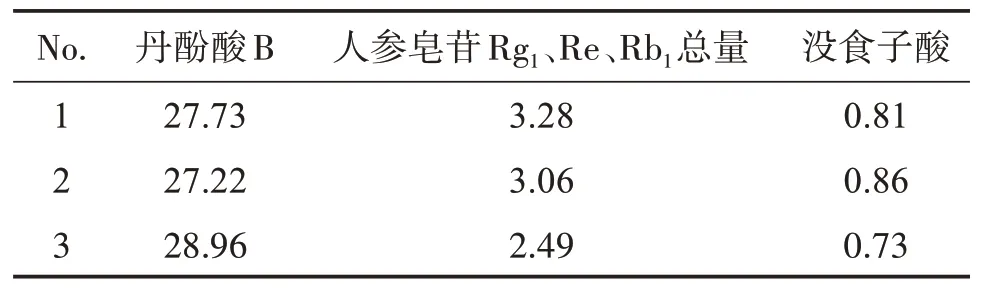
表5 最佳水提工艺验证性试验结果Table 5 Validation test results of the best water extraction process w/(mg·g-1)
本研究基于参枣滴丸方中君臣佐使的组方配伍规律,对广枣中没食子酸、丹参中丹酚酸B以及人参中的人参皂苷(Rg1、Re、Rb1)作为权重指标进行量化[9]。此方中,三味药均为治疗冠心病的要药,广枣为君药,其权重系数设为0.4,丹参活血化瘀,人参大补元气,二者在方中功效均较强,因此权重系数均设为0.3。正交试验设计中,采用Hassan 法,对各指标成分进行归一化处理,因三味药组间指标差值较大,因此用最大最小归一化公式进行计算,即di=(Yi-Ymin)/(Ymax-Ymin)[12]。
综上,本研究优选的参枣滴丸水提工艺为:加6倍量水,煎煮2 次,每次30 min,经验证合理可行,为参枣滴丸的质量控制和后续开发研究提供了依据和参考,并为研究中药复方提取工艺的优化开拓了思路。

