婴儿促纤维增生性星形细胞瘤/节细胞胶质瘤的影像表现
聂磊 时胜利 陈琬 郑彬 苏晓然
婴儿促纤维增生性星形细胞瘤/节细胞胶质瘤(desmoplastic infantile astrocytoma/ganglioglioma,DIA/DIG)十分罕见,迄今全世界报道100 余例[1]。占所有颅内肿瘤的0.5%~1%[2]。国内仅有少量报道,影像表现介绍较少。本研究回顾性收集了9 例经手术病理证实的DIA/DIG 患儿病例,结合国内外以往的相关文献报道,分析研究其影像特点,提高对该病的认识。
1 资料与方法
1.1 一般资料 回顾性收集河南省儿童医院2013年10 月—2020 年12 月行CT 和MRI 检查并经手术病理证实的9 例DIA/DIG 患儿资料。其中,DIA患儿2 例,DIG 患儿7 例;男3 例,女6 例,年龄6~61 个月,中位年龄21 个月。临床表现为呕吐、抽搐、头围增大、四肢活动差、偏瘫等。
1.2 设备与方法
1.2.1 MRI 采用SIEMENS Aera1.5 T MR 扫描设备,头部脊柱联合线圈,扫描范围自颅顶至枕骨大孔。患儿于扫描前接受右美托咪定滴鼻镇静,剂量2 μg/kg 体质量。扫描序列及参数:视野(FOV)220 mm×220 mm,层厚5 mm,层间距1 mm。①T1WI:
TR 284 ms,TE 4.62 ms;②T2WI:TR 4 500 ms,TE 113 ms;③FLAIR T2WI:TR 8 800 ms,TE 115 ms,TI 2 500 ms;④DWI:TR 3 100 ms,TE 104 ms,b=1 000
s/mm2;⑤矢状面T1WI:TR 500 ms,TE 12 ms。增强扫描包括横断面、冠状面、矢状面T1WI 和横断面FLAIR,扫描参数同前。对比剂采用钆喷酸葡胺(马根维显,广州康臣药业有限公司),质量浓度为0.469 g/mL,注射剂量为0.2 mL/kg 体质量,注射流率为0.8 mL/s,经肘静脉推注。
1.2.2 CT 采用PHILIPS Brilliance 64 层CT 设备行头部CT 扫描。扫描参数:管电压120 kV,管电流根据年龄调节(≤3 岁150 mA,4~8 岁200 mA,>8 岁250 mA),层厚5 mm,间距5 mm,螺距0.56。采用滤过反投影算法进行重建,重建层厚及间距均为1 mm。
1.3 影像分析 由2 名分别有16 和24 年诊断经验的影像医师进行影像分析,意见不一时经协商达成一致。记录CT 和MRI 影像上所有肿瘤的分布(额、颞、枕、顶叶)、生长方式(膨胀性、浸润性)、周围水肿情况、囊实性质(囊性、囊实性、实性)、信号特征、强化特点等。
2 结果
2.1 肿瘤的基本特征 9 例患儿肿瘤均为单发,位于颞叶2 个、顶叶4 个、跨脑叶生长3 个(颞顶叶2个、额颞顶叶1 个),其中7 个可见少量瘤周水肿,2个瘤周水肿不明显。肿瘤均呈膨胀性生长,边界清晰,均与脑膜或脑沟接触。其中,囊实性肿瘤8 个,实性肿瘤1 个。囊实性肿瘤的囊壁光整,囊性成分占比明显高于实性;5 个病灶中实性成分偏于肿瘤的浅表位置,3 个在瘤体内分布不均。
2.2 MRI 表现 囊实性肿瘤中囊液呈T1低信号、T2高信号,T2FLAIR 上呈稍高信号,DWI 呈低信号;囊性成分大多(7 个)无分隔,少见(1 个)纤细分隔;实性成分在T1WI、T2WI、T2FLAIR 上均呈等或稍高信号,位置浅表者与脑膜接触并强化明显(图1),分布不均匀者呈轻度强化。另有1 个肿瘤邻近颞部颅板,可见条状DWI 高信号,扩散明显受限(图2),手术证实颅板内侧硬脑膜受侵。单纯实性肿瘤表现为均匀等信号,增强后明显均匀强化,DWI 显示扩散不受限,经免疫组化结果证实为DIG(图3)。

图1 DIG 患儿,女,10 个月15 d。A 图为T1WI 影像,可见右侧颞枕顶叶囊实性占位,实性成分位于右顶叶肿瘤浅表位置。B 图为T1WI 增强影像,囊性部分无强化,实性部分强化显著。
2.3 CT 表现 囊实性肿瘤的囊性成分呈均匀低密度影,实性成分呈等密度影。其中,3 个囊内可见不规则条状钙化,钙化出现在实性成分内或边缘;1 个肿瘤可见邻近的颞骨明显变薄、吸收(图2D)。单纯实性肿瘤1 个,在CT 上表现为类圆形均匀稍高密度影,边界清晰(图3E)。
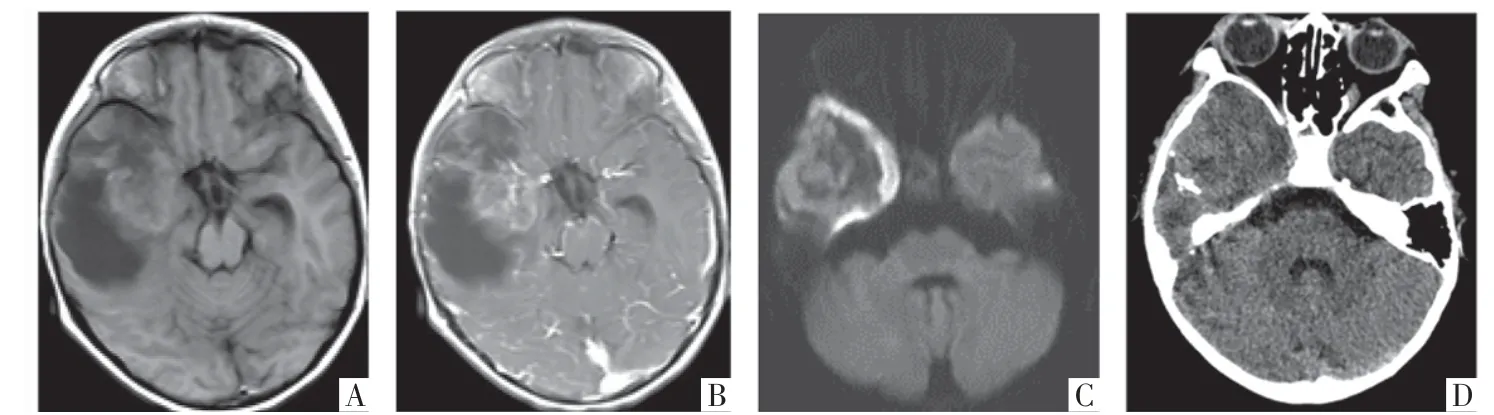
图2 DIG 患儿,男,5 岁1 个月。A 图为T1WI 影像,可见右侧颞顶叶囊实性占位,实性呈等信号,大部分靠近浅表位置。B 图为T1WI 增强影像,可见囊性成分不强化,实性成分轻度强化。C 图为DWI 影像,可见囊性部分呈低信号,实性部分以等信号为主,邻近颞骨颅板下可见条状高信号,考虑颅板受侵蚀。D 图为CT 影像,可见肿瘤内条状、点片状高密度钙化,右侧颞骨局部颅板变薄。
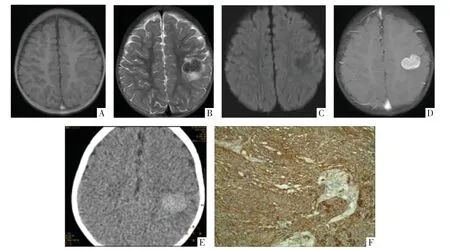
图3 DIG 患儿,女,1 岁4 个月。A 图为T1WI 影像,可见左顶叶类圆形等信号影,位置较深,浅表处与脑膜接触。B 图为T2WI 影像,肿瘤呈较低信号,边界清晰,一侧分叶,周围轻度血管源性水肿。C 图为DWI 影像,可见肿瘤扩散不受限。D 图为T1WI 增强影像,可见肿瘤明显均匀强化。E 图为CT 影像,肿瘤呈均匀稍高密度,CT 值38 HU。F 图为免疫组化,Actin(-),C-D(灶状+),Desmin(-),GFAP(灶状+),Ki-67(10%+),NF(灶状+),P53(10%+),PGP9.5(灶状+),Syn(灶状+),Vimentin(+)。
3 讨论
3.1 DIA/DIG 的命名 1984 年Taratuto 等[3]首次报道了DIA,随后Vandenberg 等[4]首次介绍DIG。DIA和DIG 同为婴儿促纤维增生性肿瘤,两者临床特点及生物学表现极为相似,世界卫生组织(2016)中枢神经系统肿瘤分类将其归类为神经元和混合神经元-胶质瘤,被共同命名为DIA/DIG,归类为Ⅰ级肿瘤[5]。DIA/DIG 通常发生于2 岁以内婴幼儿,少数见于年龄稍大的儿童及成人[6-7]。临床表现多为进行性头围增大、颅压升高症状等,有的可伴发癫发作[8-9]。2010 年,Rangel-Castilla 等[10]提出将DIG 和非婴儿型促纤维增生性节细胞胶质瘤(desmoplastic non-infantile ganglioglioma,DNIG)统称为增生性神经节细胞胶质瘤(desmoplastic ganglioglioma,DG),根据年龄界定具体名称,<5 岁为DIG,≥5 岁为DNIG,而DIG 相对于DNIG 多见。
3.2 DIA/DIG 的影像特点 ①较大的幕上肿瘤,常占据多个脑叶,占位效应明显。②囊实性改变,实性部分位于浅表,与脑膜、脑沟接触且强化明显,当实性分布不均匀时往往强化较轻。③瘤周水肿,DIA/DIG 肿瘤较大但瘤周水肿较轻或无,反映其生长缓慢、良性肿瘤的特点。④钙化,常表现为不规则条状钙化,相对少见。⑤扩散情况,DWI 上常表现为较低信号,符合其良性肿瘤的特点。但本研究显示肿瘤内实性成分分布不均时,会有扩散轻度受限,并且邻近肿瘤的颅骨内板及硬脑膜受到侵蚀同时表现为扩散受限。⑥单纯实性肿块特征,本组1 个肿瘤影像表现为单纯实性肿块,与脑膜、脑沟有接触但面积较小。既往国内鲜有报道DIA/DIG 呈单纯实性表现。曾有研究[11]认为DIA/DIG 表现为单纯实性肿块时,可能是该肿瘤还处在相对的早期时相,随着时间推移肿瘤可转化成囊实性改变。
3.3 DIA/DIG 的病理特点 DIA/DIG 由纤维母细胞为主的结缔组织和神经上皮组织混合组成,神经上皮细胞可以分化为星形细胞和神经元[12]。当肿瘤组织同时有纤维组织和星形细胞,但无神经元细胞时,称为DIA;若同时包括星形细胞和神经元,则称为DIG。病理表现有显著的纤维结缔组织增生,是因为侵犯了软脑膜并刺激软脑膜产生了大量的网状纤维并发生了透明变性[13],也有少数侵犯颅骨内板者,可能是由脑膜纤维母细胞浸润所致[14]。免疫组化提示DIA/DIG 的主要区别在于DIG 有明确的神经元成分,SYN 表达为阳性[15]。
3.4 DIA/DIG 的鉴别诊断 DIA/DIG 需要与胚胎发育不良性神经上皮瘤、幕上室管膜瘤、多形性黄色星形细胞瘤、胶质母细胞瘤、其他类型的中枢神经系统胚胎性肿瘤等相鉴别。胚胎发育不良性神经上皮瘤通常位于半球皮质区,占位效应轻或者无,肿瘤呈脑回样、单囊或多囊表现,边界清晰,“三角征”和瘤内分隔是其特征性征象,增强扫描通常无强化或轻度强化,临床常伴癫 发作。室管膜瘤发生于幕上时多位于深部白质,囊性成分为主,可见出血、钙化,DWI 上扩散有轻度受限,增强后可见环形强化或实性成分不均匀强化。多形性黄色星形细胞瘤多见于颞叶,多数患儿有长期癫史,多表现为伴有壁结节的大囊性肿块,也可表现为单纯囊性或实性,病变中囊液T1WI 及T2WI 均略高于脑脊液。胶质母细胞瘤和其他类型的中枢神经系统胚胎性肿瘤,如非典型畸胎瘤样横纹肌样瘤,其恶性程度高,常见坏死、囊变,DWI 有明显扩散受限。
3.5 小结 DIA/DIG 是一种儿童罕见的幕上良性肿瘤,一般多见于婴幼儿期,影像典型表现为幕上较大的囊实性占位,实性部分浅表且强化明显。本组中有1 个肿瘤为临床较少见的单一实性肿瘤,以往文献虽有讨论,但病例报道较少,本病例为进一步认识此病提供了帮助。

