一种识别Cu2+的罗丹明衍生物的合成及其性质研究
张 杰,戴红亮,郑琦君,覃于鑫,白翠冰,张 琳,李瑞乾,乔 瑞,苗 慧
(阜阳师范大学 化学与材料工程学院,安徽 阜阳 236037)
1 引言
1.1 Cu2+的生物作用
Cu2+对生命活动起着关键的作用[1-3]。Cu2+是生物体活细胞中常见的微量元素离子,参与各种生物酶的形成,例如过氧化物歧化酶、超氧化酶、单胺氧化酶等以及参加生物体内的氧化还原反应[4-6]。Cu2+在生物体内必须确保适宜的浓度,维持细胞正常的各种代谢,反之则会导致机体内会出现一系列问题。例如,细胞里Cu2+的浓度过高会导致细胞内器官损坏,从而导致发生神经性疾病。同时,癌症、心血管疾病、动脉硬化等疾病也与人体内Cu2+失衡有关[7-9]。因此,寻找一种高效,简单的方法去检测Cu2+是十分有意义的。
1.2 Cu2+的检测方法
传统方法经常是使用仪器手段实现了对Cu2+的检测(例如,高效液相色谱、电感耦合等离子体质谱、电化学)。但是这些分析方法存在一些不足,例如仪器昂贵、检测过程繁琐和样品需求量多等[10-12]。因此,找到一种快速,简便的检测环境中和生命体中的Cu2+是十分重要的。近些年以来,Cu2+荧光探针因其突出的优点而引起广泛关注[13-15]。合成得到灵敏度高和选择性好的荧光探针,一直是人们关注的热点之一。
1.3 本课题的设计思路
目前,香豆素类、萘酰亚胺类和氧杂蒽类等[16-18]多类化合物用来检测Cu2+。与其它荧光母体化合物相比,罗丹明类化合物具有独特OFFON 性质、稳定性好等诸多优点[19-22]。基于以上原因,设计合成得到了2-羟基-5-甲基苯甲醛修饰的罗丹明6G 衍生物LX,通过1H NMR 和13C NMR,确定了化合物LX 的结构。结合紫外光谱、荧光光谱和红外光谱,系统研究了化合物LX 与Cu2+之间的相互作用,推测了二者之间作用机理。化合物LX 还可以有效检测线虫体内的Cu2+。
2 实验设备和原料
2.1 实验设备
分析天平(上海赞维衡器有限公司,ZA100R3);紫外可见分光光度计(上海元析仪器有限公司,UV-9000S);低温冷却循环泵(南京肯凡电子科技有限公司,KDC-0506);旋转蒸发仪(上海恩生科技有限公司,ESRE-2010);循环水式真空泵(郑州域达仪器有限公司,SHB-DIII);磁力加热搅拌器(金坛市杰瑞尔电器有限公司,78-1);电热鼓风干燥箱(河南信诺仪器设备有限公司,DHG-9053A);比色皿(宜兴市伟鑫仪器有限公司,JB760-68)。荧光倒置显微镜(上海仪圆光学仪器有限公司,WMF-3690)。
2.2 原料和试剂
罗丹明6G(分析纯,阿达玛斯试剂有限公司),水合肼(分析纯,安耐吉公司),2-羟基-5-甲基苯甲醛(分析纯,安耐吉公司),无水乙醇(分析纯,安耐吉公司),金属离子均为分析纯的氯化盐,使用前未经二次处理。乙腈(色谱纯,阿拉丁公司)。实验过程中的水为去离子水。
3 实验部分
3.1 化合物A 的合成[23]
取罗丹明6G(1.5 g,3 mmol)在乙醇中与乙二胺回流。反应混合物在85℃下回流约8 h。反应完成后,将混合物冷却到室温,过滤产生的沉淀物,用20 mL 冰乙醇洗涤,用真空干燥得到化合物A(图1)。
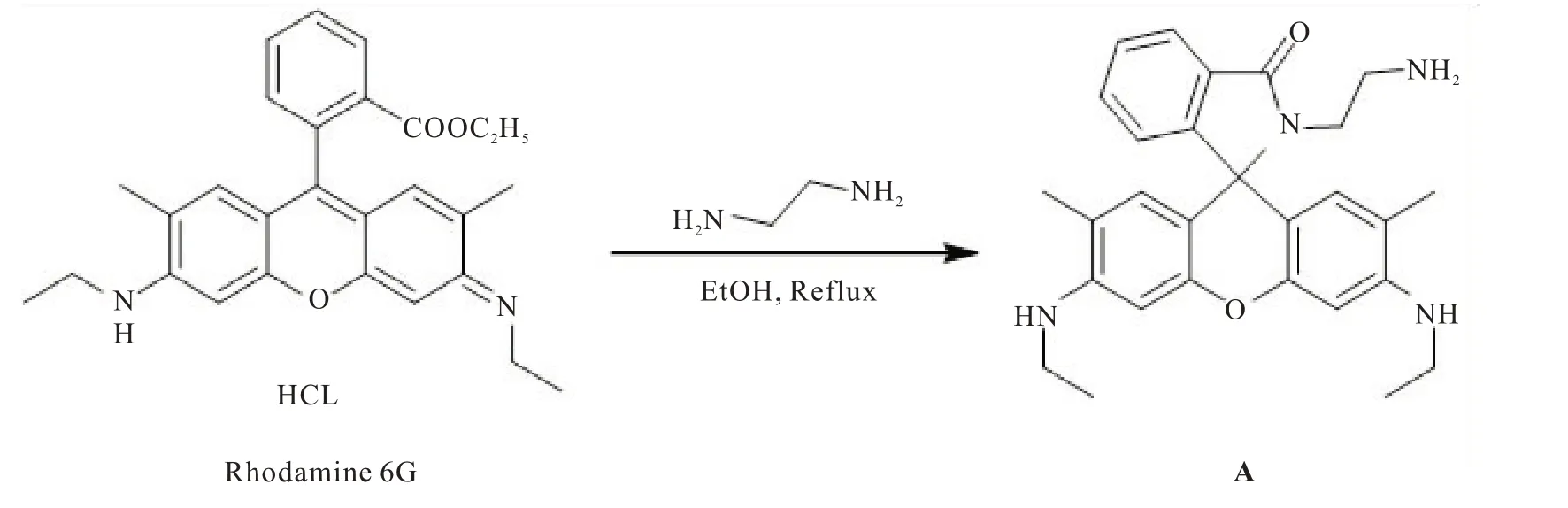
图1 中间体A 的合成路线
3.2 荧光探针LX 的合成
用分析天平称取460 mg(1 mmol)的A 溶解于30 mL 的无水乙醇中,在85℃条件下进行加热回流。称取137 mg(1 mmol)2-羟基-5-甲基苯甲醛(B),加入到反应溶液。随着反应的进行,有大量固体析出。反应结束后,趁热滤出固体,并用冰乙醇洗涤固体三次,得到荧光探针LX(图2)。产率为74.5%。1H NMR (400 MHz,DMSO-d6) δ 12.76 (s,1H),7.91 (s,1H),7.82 -7.73 (m,1H),7.54-7.42(m,2H),7.13-6.94(m,3H),6.72(d,J=8.3 Hz,1H),6.28 (s,2H),6.04 (s,2H),5.09 (t,J=5.4 Hz,2H),3.32 (d,J=6.5 Hz,2H),3.16 (dt,J=19.4,6.4 Hz,6H),2.21 (s,3H),1.80 (s,6H),1.22 (t,J=7.1 Hz,6H).13C NMR (101 MHz,DMSO-d6) δ 167.51,166.54,158.52,153.79,151.49,148.17,133.25,131.89,130.86,128.75,128.13,127.32,124.11,122.84,118.77,118.61,116.58,105.16,96.03,64.55,56.82,37.93,20.38,17.48,14.62.(附录1,附录2)。

图2 荧光探针LX 的合成路线
3.3 金属离子的识别
用乙腈配制浓度为1.0×10-4mol/L 荧光探针LX 和不同的金属离子(NaCl、CuCl2·2H2O、YCl3·7H2O、CoCl2、MgCl2、CeCl3、CdCl2、AgCl、KCl、Ni-Cl2、ZnCl2、HgCl2、FeCl3·6H2O、BaCl2、PbCl2、SrCl2、MnCl2、CaCl2、AlCl3、FeCl2·4H2O)的溶液。分别取荧光探针LX 溶液300 μL 和不同金属离子溶液900 μL,然后定容到3000 μL,单独荧光探针LX稀释到相同浓度(1.0×10-5mol/L)作为对照组依次检测21 组待测溶液的紫外和荧光光谱强度的变化。
3.4 抗干扰实验
其他干扰金属离子(NaCl、YCl3·7H2O、CoCl2、MgCl2、CeCl3、CdCl2、AgCl、KCl、NiCl2、ZnCl2、Hg-Cl2、FeCl3·6H2O、BaCl2、PbCl2、SrCl2、MnCl2、CaCl2、AlCl3、FeCl2·4H2O)被加入到荧光探针LX 对Cu2+的体系中。取荧光探针LX(1.0×10-4mol/L)乙腈溶液300 μL,加入Cu2+(1.0×10-4mol/L)的乙腈溶液900 μL,然后,干扰离子溶液(1.0×10-4mol/L)900 μL 被加入到混合溶液,最后溶液用乙腈稀释定容到3000 μL。
3.5 连续变化法
所测混合溶液的总体积(3000 μL)保持不变,溶液中[Cu2+]/([Cu2+]+[LX])的比例从0.1,0.15,0.2依次递增至0.95。Cu2+的溶液(1.0×10-4mol/L)的体积依次从100 μL,150 μL,200 μL 递增至950 μL,保持时间间隔相同,并测试紫外和荧光强度的变化。
3.6 摩尔法
固定体积为300 μL 荧光探针LX 的乙腈溶液(1.0×10-4mol/L),不同体积的Cu2+乙腈溶液(1.0×10-4mol/L)被依次加入,改变[Cu2+]/[LX]比例从0.0,0.1,0.2,0.3 依次间隔0.1 递增到2.0。溶液被乙腈稀释定容到3000 μL,测定紫外和荧光光谱。
3.7 红外光谱(LX,LX-Cu2+)
称取15 mg 荧光探针LX 和25 mg 的CuCl2·2H2O 溶于20 mL 乙腈溶液,在室温搅拌0.5 小时,溶液在结晶皿中挥发,得固体。测试化合物LX 和LX-Cu2+红外谱图。
3.8 检测水中的Cu2+
通过自制的试纸条,先浸泡在荧光探针LX(1.0×10-4mol/L)溶液中,然后自然晾干备用。把准备好的试纸条依次浸泡在含有Hg2+,Fe3+,Cu2+,Al3+,Fe2+的水溶液中大概1 分钟,然后把试纸条拿出来晾干通过裸眼和紫外灯观察他们的颜色变化。
3.9 在生物体内检测Cu2+
在20℃下,秀丽隐杆线虫与琼脂一起培养。三天后,把秀丽隐杆线虫取出放入96 孔板然后加入LX(0.1 mL,1.0×10-4mol/L,DMSO/H2O=2:8)接着与琼脂脂一起孵育30 分钟,然后,一些线虫加入Cu2+(0.1 mL、2.0×10-4mol/L、H2O)的水溶液,继续培养1 小时。最后线虫用M9(NGM 培养基)洗涤琼脂和残留的物质,然后在荧光倒置显微镜观察荧光成像。
4 结果与讨论
4.1 离子的可视化检测
通过观察溶液中的颜色变化情况,考察荧光探针LX(1.0×10-5mol/L)对各种金属离子的选择性识别能力。从图3 可以看出,当上述金属离子加入LX 溶液中时,只有Cu2+能引起溶液颜色变化。在可见光下显示颜色从无色变为粉红色(图3a),并且在紫外灯下观察到荧光显著增强(图3b),而其它离子则不能引起类似变化。

图3 金属离子响应照片(a:日光下照片,b:365 紫外灯下照片)
4.2 金属离子选择研究
通过光谱可以看出(图4),当Cu2+加入荧光探针LX 的溶液中,探针LX 在525 nm 出现了一个新的吸收峰。利用525 nm 激发溶液,可以观察到在550 nm 处荧光明显增强。而Fe3+、Fe2+、Hg2+、Na+、Y3+、Co2+、Mg2+、Ce3+、Cd2+、Ag+、K+、Ni2+、Zn2+、Ba2+、Pb2+、Sr2+、Mn2+、Ca2+、Al3+则对荧光探针LX 选择性识别Cu2+没有明显影响,这可能是Cu2+的加入使得罗丹明开环。此外,通过其他离子共存实验,进一步得出荧光探针LX 可以专一识别Cu2+并且其它离子并不构成干扰(图5)。
4.3 荧光探针LX 与Cu2+化学计量比
使用摩尔比法和连续变化法确定荧光探针LX 对Cu2+之间的化学计量比。结果发现随着Cu2+浓度的增大荧光探针LX 的吸光度和荧光强度不断的增高,当([Cu2+]/[LX])=1.0 时,Cu2+的浓度增大的同时吸光度和荧光强度无明显变化(图6)。结果表明,荧光探针LX 与Cu2+之间的相互作用比为1:1。固定([LX]+[Cu2+])浓度不变(3.3×10-5mol/L),改变([Cu2+]/([LX]+[Cu2+])比例从0.05增加到0.95,我们发现两条交于一点的不同斜率的直线,刚好对应Cu2+的摩尔分数(0.5)的横坐标。连续变化法的结果与摩尔比法相符合,进一步验证了该结论。上述结果表明,荧光探针LX与Cu2+是1:1 作用的(图7)。

图6 摩尔比法确定荧光探针LX 与Cu2+之间的化学计量比

图7 连续变化法确定荧光探针LX 与Cu2+之间的化学计量比
4.4 荧光探针LX 与LX-Cu2+红外光谱及机理预测
当荧光探针LX 与Cu2+溶液相互作用后,红外光谱发生了改变(图8)。当Cu2+与-OH 发生了配位后,属于-OH 的3460 cm-1处的峰消失,同时当Cu2+加入时探针LX 发生了N-H 健到C=N 健的互变异构出现了一个新的吸收峰1657 cm-1。结合上述荧光探针LX 与Cu2+的化学作用比为1:1的结论,所以我们推测荧光探针LX 与Cu2+的可能的作用方式如图9。

图8 荧光探针LX 和LX-Cu2+的红外光谱图

图9 荧光探针LX 与Cu2+可能的络合机理
4.5 在水中检测Cu2+
为了进一步探索荧光探针LX 的实际应用,我们自制了试纸条来进一步检测水中的Cu2+。根据图10,我们发现LX(1×10-4mol/L)试纸条是无色,但使用Cu2+水溶液浸泡后,肉眼显示为红色,紫外灯下观察到明显荧光增强现象。结果表明,荧光探针LX 可以很好的检测水中的Cu2+,这样使得在金属离子污染检测有很好的应用前景。

图10 试纸条检测水中的Cu2+(从左到右为Hg2+,Fe3+,Cu2+,Al3+,Fe2+,离子溶液为水溶液)
4.6 生物成像
为了进一步探索荧光探针LX 在生物体中的实际应用,我们选取了线虫作为实验的研究对象。从图11 可以看来,线虫自身没有荧光,当和荧光探针LX 培养后依然没有荧光。但是当线虫和荧光探针LX 培养后接着和Cu2+培养,我们发现很明显的绿色和红色的荧光。通过线虫实验,我们进一步得出该荧光探针LX 在生物体中检测Cu2+具有潜在的能力。

图11 线虫的荧光显微镜成像(a)单独线虫的荧光成像图,(b)线虫被LX(1.0×10-4 mol/L,DMSO/H2O=2:8)处理后的荧光图像,(c)用Cu2+(2.0×10-4 mol/L,H2O)处理的负载荧光探针LX 的线虫的荧光图像。从左到右是明场,绿色通道,红色通道
5 结论
本文设计合成得到了一种罗丹明衍生物LX。该化合物能够快速高效并且专一识别Cu2+,与Cu2+之间的络合比为1:1,对Cu2+检出限为1.06×10-8M,可以实现对水中的Cu2+的有效检测。利用荧光成像方法,实现了线虫体内Cu2+的检测。

