酒石酸泰万菌素预混剂在仔猪体内的药代动力学研究
卢 迪,羿 岩,赵宝凯,耿 健,那 璐,闫 琰
(沈阳伟嘉生物技术有限公司,沈阳 110027)
泰万菌素是一种新型大环内酯类抗生素[1],由英国伊科拜克动物保健品有限公司开发,常使用其酒石酸盐。2004年9月9日经欧盟批准用于预防和治疗由猪肺炎支原体[2]引起的猪气喘病、由猪痢疾短螺旋体引起的猪痢疾、由胞内劳森氏菌引起的猪增生性肠炎和由鸡毒支原体引起的鸡支气管感染[3]。目前国内已批准酒石酸泰万菌素预混剂和可溶性粉用于治疗猪、鸡支气管感染和猪血痢短螺旋体以及其他敏感细菌的感染[4]。泰万菌素具有高效、低毒、低残留,能够杀灭革兰氏阳性菌等作用,具有良好的研发和应用前景[5]。本试验研究酒石酸泰万菌素预混剂在仔猪体内的药物动力学特征[6],并将其作为受试制剂与国际市场上的主流产品进行对比分析,以期为新药研发和临床用药提供科学指导[7]。
1 材料与方法
1.1 材料
1.1.1 试验药品 酒石酸泰万菌素预混剂标准品[8](批号:K0691908),中国药品生物制品检定所;酒石酸泰万菌素预混剂(规格:100 g:20 g, 批号:2131301)由沈阳伟嘉生物技术有限公司生产;酒石酸泰万菌素预混剂(规格:100 g:20 g, 批号:2111601)由英国伊科拜克动物保健品有限公司生产[9],非那雄胺标准品(批号:Y0000090),中国药品生物制品检定所。
1.1.2 主要仪器 Exion LC AD Pump,Exion LC AD Solvent Valve,Exion LC AD Degasser,Exion LC AD Controller,Exion LC AD AC Column Oven,Triple Quad 4500MD四级杆质谱仪,Analyst©1.6.3质谱工作站,(美国AB SCIEX公司);QUINTIX125D电子精密天平(Sartorius公司);微型旋涡混合仪(DLAB公司);H2050R高速冷冻离心机(湖南湘仪实验室仪器开发有限公司);超低温冰箱(中科美菱);SG8200HPT超声波清洗器(上海冠特超声仪器有限公司);20、50、100、200、1000 μL移液器(Eppendorf公司)。
1.1.3 主要试剂 甲醇、甲酸、乙腈色谱级购自Sigma-Aldrich公司;纯净水、蒸馏水购自广州屈臣氏食品饮料有限公司。
1.1.4 试验动物 健康一元大白猪12头,28日龄,(公猪),试验前采用耳标标记,编号为:1~12号,平均体重为:7.96±0.5 kg,购自辽宁伟嘉农牧生态食品有限公司种猪场。试验前正常饲养观察1周,每天定时饲喂三次,饲喂不含任何药物的全价日粮(沈阳伟嘉生物技术有限公司提供)。
1.1.5 溶液配制 标准品储备液的配制:精密称取酒石酸泰万菌素预混剂标准品,溶于甲醇中,得到浓度为1.00 mg/mL的储备液,密封后在-20 ℃保存。标准品系列溶液的配制:用纯甲醇稀释储备液成下列酒石酸泰万菌素预混剂系列溶液。标曲系列溶液浓度:C1:20000 ng/mL,C2:10000 ng/mL,C3:4000 ng/mL,C4:2000 ng/mL,C5:1000 ng/mL,C6:400 ng/mL,C7:200 ng/mL,C8:100 ng/mL;质控系列溶液浓度:HQC:16000 ng/mL,MQC:3000 ng/mL,LQC:300 ng/mL。内标品(IS)溶液的配制:精密称取非那雄胺标准品分别溶甲醇中,得到浓度分别为1.00 mg/mL的储备液,密封后在-20 ℃度保存,取内标储备液用纯甲醇稀释成40 ng/mL非那雄胺甲醇溶液,用于样品预处理。
1.2 方法
1.2.1 药物动力学试验设计[10]所有仔猪给药前禁食12 h,给药6 h后恢复正常饮食,对每头仔猪进行称重,并采集血样作为空白对照组。将试验仔猪随机分为两组,每组6头,第一组编号为1~6号,口服灌喂沈阳伟嘉生物技术有限公司的酒石酸泰万菌素预混剂;第二组编号为7~12号,口服灌喂英国伊科拜克动物保健品有限公司的酒石酸泰万菌素预混剂,给药剂量均为125 mg/kg[11]。口服给药后,每头仔猪于0.25、0.5、0.75、1、1.25、1.5、2、2.5、3、4、5、6、8、12、24、36、48、72、96、120、144、168 h前腔静脉采血1 mL左右[12],所采血液均含有抗凝剂肝素钠的试管中室温下静置2 h后3000 r/min离心8 min,分离血浆,取上清液于-20 ℃冷冻保存,待测定[13]。
1.2.2 色谱条件 进样器温度:4 ℃ ,柱温:室温,色谱柱: 纳谱科技C18 3 μm,3.0×50 mm 进样体积:10 μL,流速:0.6 mL/min,流动相A:含有0.1%(V/V)甲酸的水溶液,流动相B:含有0.1%(V/V)甲酸的甲醇溶液(表1)。
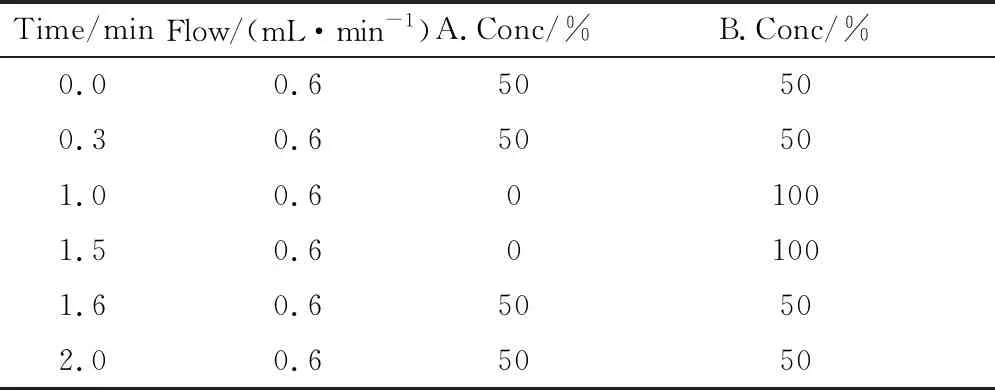
表1 梯度洗脱程序
1.2.3 质谱条件 离子源:电喷雾离子源(ESI),正离子模式检测(POS),源参数:CUR(气帘气):35.00 psi;IS(离子化电压):5500.00 V;TEM(温度):600.00 ℃;GS1(喷雾气):50.00 psi;GS2(辅助加热气):50.00 psi;CAD(碰撞气):7.00 psi;EP(摄入电压):10.00 V;CXP(碰撞室射出电压):6.00 V(表2)。
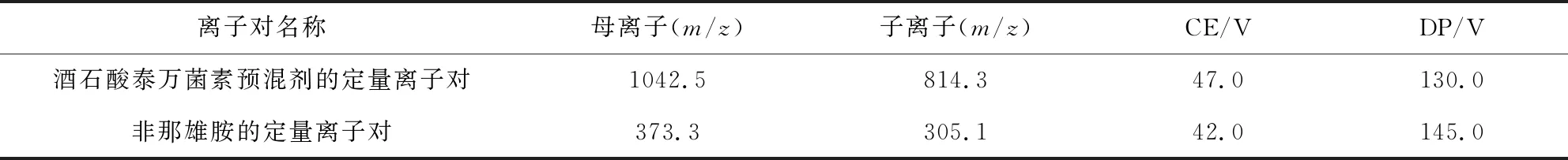
表2 定量离子对
1.2.4 生物样品的处理 取50 μL样品于干净的1.5 mL EP管中,加入100 μL内标(40 ng/mL 非那雄胺甲醇溶液)溶液混匀后,沉淀蛋白,涡旋1 min,15000 r/min离心5 min,取上清液100 μL转移至96孔深孔板,加入300 μL水,涡旋混匀。密封,上机测定。
1.2.5 血浆样品的处理 将血浆样品从-20 ℃冰箱中取出,室温下自然解冻,取10 μL质控标准品溶液于干净的1.5 mL EP管中,加入190 μL空白猪血浆,混匀后,制备成浓度分别为15、150、800 ng/mL的质控的血浆。分别取50 μL样品于干净的1.5 mL EP管中,加入100 μL内标(40 ng/mL 非那雄胺甲醇溶液)溶液混匀后,沉淀蛋白,涡旋1 min,15000 r/min离心5 min,取上清液100 μL转移至96孔深孔板,加入300 μL水,涡旋混匀,密封,上机测定。
1.2.6 标准曲线的建立 分别取10 μL标准品系列溶液于干净的1.5 mL EP管中,加入190 μL空白猪血浆,混匀后,制备成浓度分别为5、10、20、50、100、200、500、1000 ng/mL的标准曲线的血浆。分别取50 μL样品于干净的1.5 mL EP管中,加入100 μL内标(40 ng/mL 非那雄胺甲醇溶液)溶液混匀后,沉淀蛋白,涡旋1 min,15000 r/min离心5 min,取上清液100 μL转移至96孔深孔板,加入300 μL水,涡旋混匀。密封,上机测定。
1.2.7 样品的质量控制 样品的质量控制应符合生物分析规范标准:质控样品每一浓度水平至少>50%以上。
1.2.8 猪血浆中药物浓度测定 将给药后不同时间点获取的血浆,按血浆样品的处理方法处理后进行上机测定数据采集采用Analyst©1.6.3软件;同一序列采集的色谱图使用相同的积分事件进行处理,样品计算峰面积,代入标准曲线回归方程,计算出血浆中样品浓度,对浓度值(待测物与内标浓度的比值)和响应值(待测物与内标浓度的比值)进行线性回归(Y=ax+b),权重因子W=1/X2。
1.2.9 数据分析 采用Excel软件分析处理方法学数据并绘制血浆标准工作曲线及药-时曲线图;药代动力学模型拟合及参数计算采用DAS 2.1.1 药物动力学软件分析。
2 结果与分析
2.1 分析方法的确证 在本研究所建立的方法下,样品保留时间为1.63 min,峰形对称性良好,基线平稳,无明显干扰峰,检测效率高。空白血浆色谱图如图1,空白血浆中添加样品色谱图如图2,给药后血浆中样品色谱图如图3。
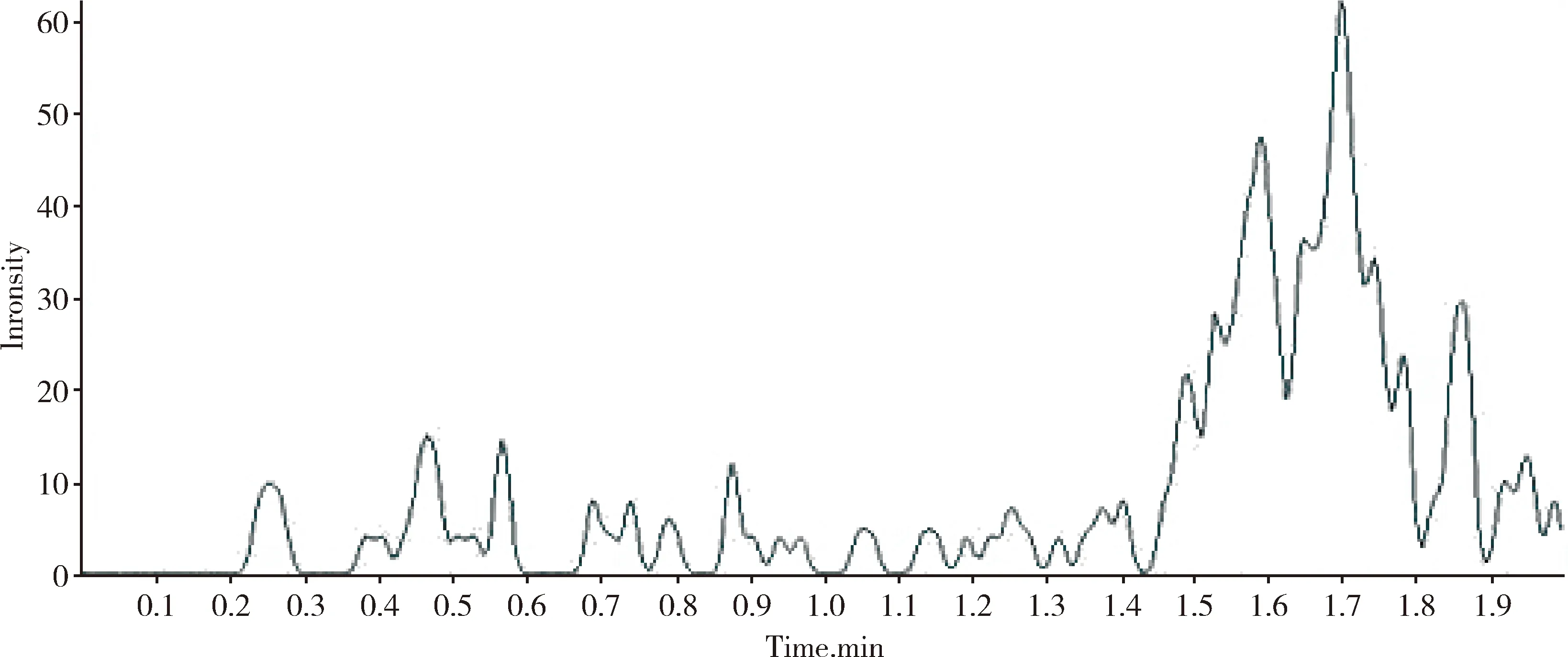
图1 空白血浆色谱图

图2 空白血浆中添加泰万菌素(ng/mL)色谱图
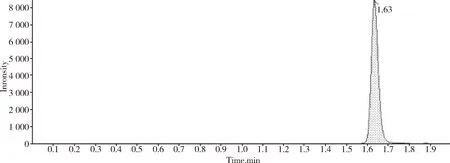
图3 给药后血浆中泰万菌素(ng/mL)色谱图
2.2 血浆标准工作曲线及数据表 标准曲线符合以下生物分析规范标准:校正标样各浓度点的回算浓度应在标示值的±15%以内,定量下限处应该在±20%以内。至少75%且至少6个浓度的校正标样,应满足上述标准。相关系数R值应不小于0.99(表3、图4)。
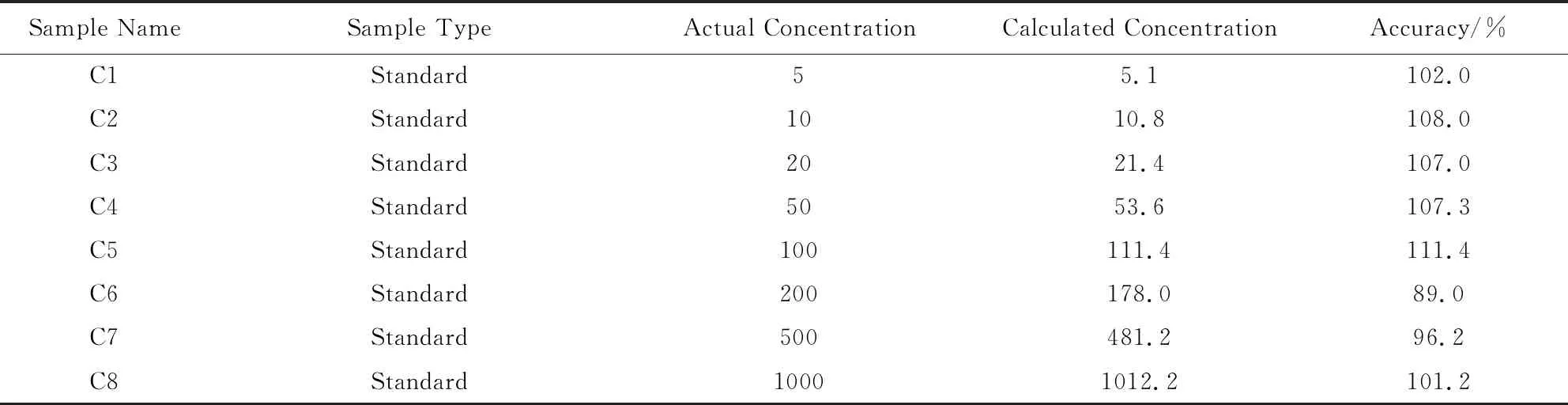
表3 泰万菌素典型回归曲线数据

图4 泰万菌素在血浆中的标准曲线
2.3 样品的质量控制 根据表4的质控数据结果可以看出,质控样品的每一浓度水平都在50%以上,符合规定。

表4 泰万菌素典型质控数据
2.4 药代动力学试验结果 口服酒石酸泰万菌素预混剂血药浓度-时间见表5;口服英国伊科拜克动物保健品有限公司的酒石酸泰万菌素预混剂血药浓度-时间见表6;两组药代动力学参数见表7,两组药-时曲线见图5。
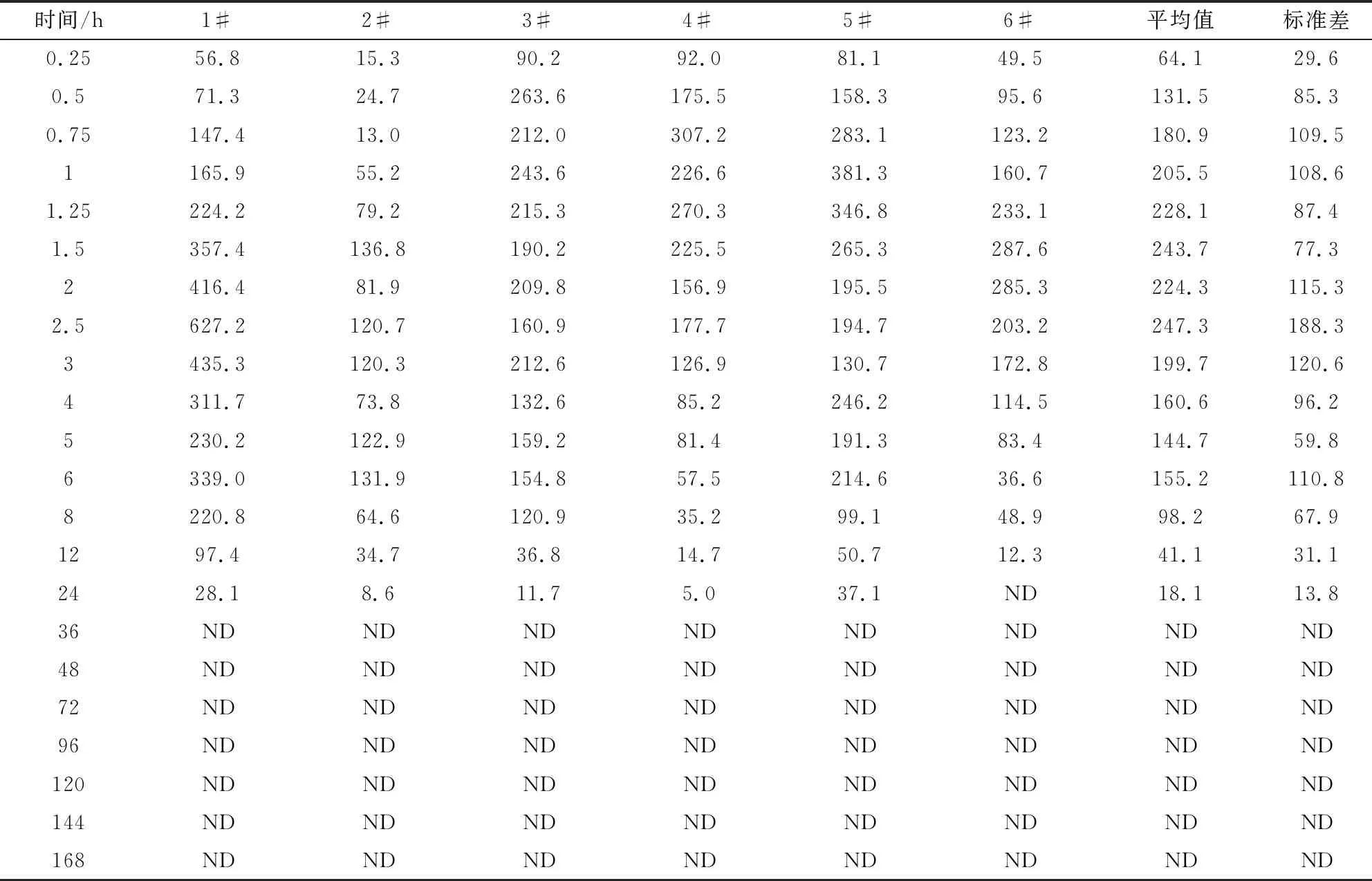
表5 口服酒石酸泰万菌素预混剂随时间变化的血药浓度(ng/mL)
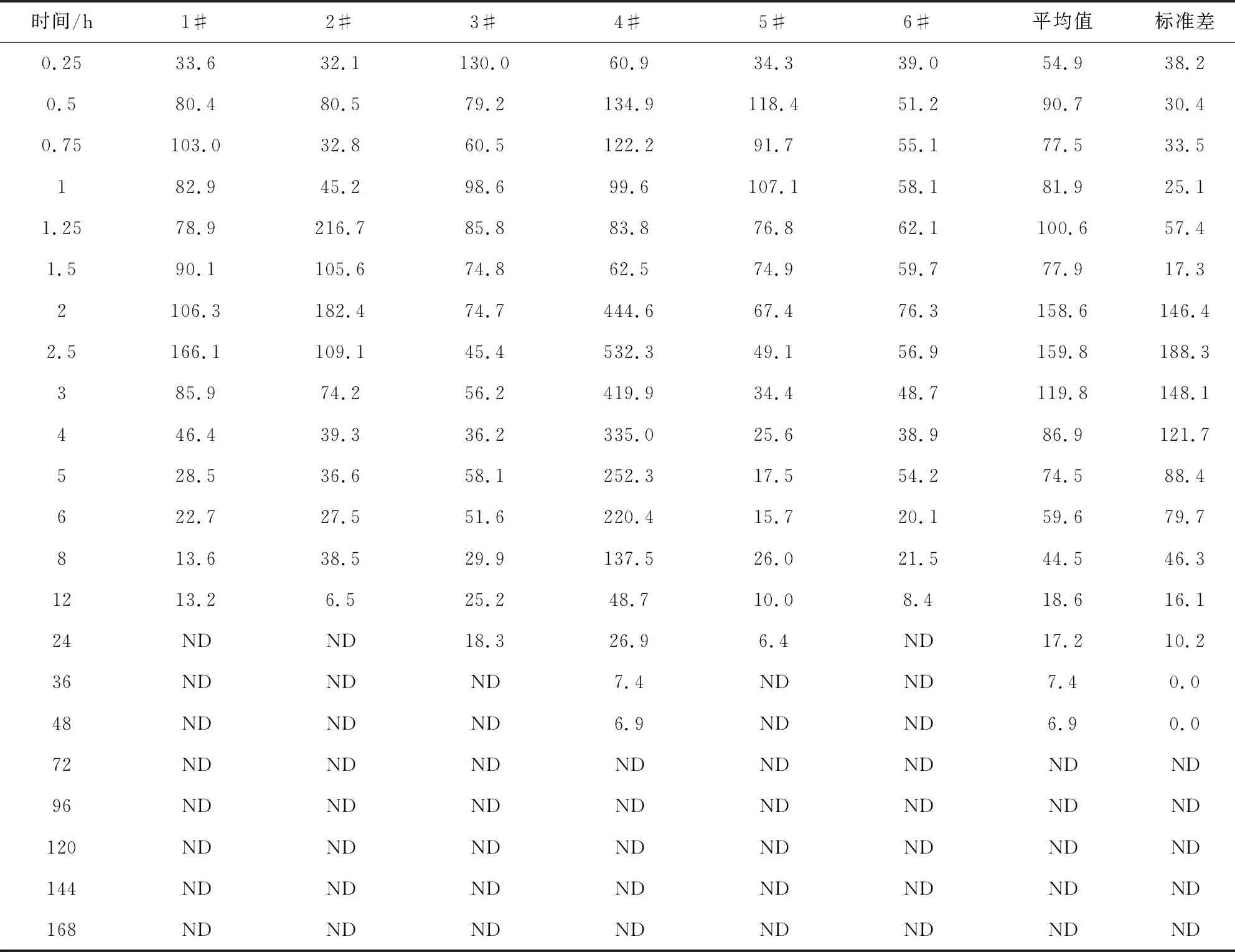
表6 口服英国伊科拜克动物保健品有限公司酒石酸泰万菌素预混剂随时间变化的血药浓度(ng/mL)

表7 药代动力学参数
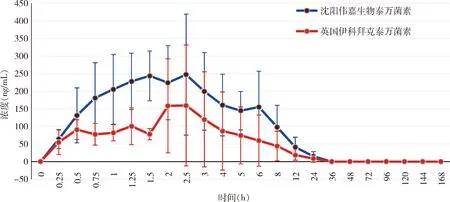
图5 口服酒石酸泰万菌素预混剂药-时曲线
3 讨论与结论
3.1 色谱条件 据朱晓娟等报道[14],目前泰万菌素血药浓度测定法常用高效液相色谱法(HPLC),此方法存在样品处理时间长,灵敏度相对低,线性范围窄等缺点。本研究采用高效液相色谱-质谱法[15]建立了仔猪血浆中泰万菌素的定量分析方法,该方法能缩短样品处理时间,操作方便,灵敏度高,线性范围宽,回收率高且杂质峰少,流动相A采用含有0.1%(V/V)甲酸的水溶液,流动相B采用含有0.1%(V/V)甲酸的甲醇溶液,样品出峰时间稳定,峰形尖锐,与血浆中其余杂质完全分离,对于样品中代谢范围大的代谢化合物能达到很好的检测效果,可应用于泰万菌素在猪体内的药物动力学研究。
3.2 样品处理 为保证血浆样品处理的准确性,本研究采用了40 ng/mL 非那雄胺甲醇溶液为内标,质控标准品溶液制备成浓度分别为15、150、800 ng/mL的血浆,充分沉淀血浆中的蛋白杂质,保证样品提取回收率,有效的提高了检测方法的准确度,减少试验误差保证数据更准确。
3.3 药代动力学特征 本研究用DAS 2.1.1 药动学软件处理两组药代动力学数据,口服沈阳伟嘉生物技术有限公司的酒石酸泰万菌素预混剂在仔猪体内主要药动学参数如下:平均最高血药浓度(Cmax)为247.3 ng/mL,平均药时曲线下面积(AUC)为1899.0 ng/mL·h,平均达峰时间(Tmax)为1 h;口服英国伊科拜克动物保健品有限公司的酒石酸泰万菌素预混剂主要药动学参数如下:平均最高血药浓度(Cmax)为159.8 ng/mL,平均药时曲线下面积(AUC)为986.0 ng/mL·h,平均达峰时间(Tmax)为1.5 h;沈阳伟嘉生物技术有限公司的酒石酸泰万菌素预混剂平均最高血药浓度(Cmax)是参比制剂的1.55倍,平均药时曲线下面积(AUC)是参比制剂的1.93倍,生物利用度是参比制剂的193%。
3.4 科学用药 目前养殖业生产模式的总体发展方向是健康安全养殖,根据中华人民共和国农业农村部第194号公告[16],减抗、限抗将成为养殖新常态。欧洲饲料限抗后对养殖的生产性能影响较大,以猪为例,平均日增重下降,死亡率增加,断奶日龄延迟,现场处方用药的年用量不断增加。当前中国的养殖模式下,断奶仔猪腹泻、保育猪免疫抑制疾病继发细菌感染、育肥猪常见呼吸道与肠道感染以及母猪的产前产后的各种混合感染是养殖过程的主要疾病,过去,饲料中抗菌促生长的药物广泛应用,有效的控制了细菌的定植和增殖,现在,进入健康养殖新时代,其养殖用药的主要原则为科学合理用药与精准用药。养殖过程中不能过度用药,要减少用量,健康养殖是养殖业的发展趋势,健康养殖不是无抗养殖而是科学合理的选择使用兽用抗菌药[17]。泰万菌素是3代大环内酯类广谱抗生素[18],通过一种耐热链球菌转化将泰乐菌素第3位进行乙酰化和第4位进行异戊酰化而获得,对支原体、螺旋体、大部分革兰氏阳性菌和部分革兰氏阴性菌均有较强抗菌活性,泰万菌素已被多项研究证实可抑制PRRSV(猪蓝耳病病毒)的复制,为新一代的兽用抗病毒药物[19]。针对性提高诸如泰万菌素等高端抗生素生物利用度的制剂工艺研发,用以提高药物安全性,加快抗生素的吸收和代谢速度,缩短药物残留时间和休药期,对于健康养殖具有重要意义。平稳的血药浓度,降低波峰波谷现象[20]已成为行业趋向性需求。酒石酸泰万菌素预混剂在仔猪体内的药物动力学研究结果将对其新兽药研发和临床使用提供重要参考[21]。

