紫杉醇脂质体和多西他赛用于乳腺癌新辅助化疗的效果及安全性比较
李红梅
医学研究领域对癌症的研究一直尤为重视,广大医学工作者和专家对于新辅助化疗和恶性肿瘤的探讨也从未停止,并对工作和学术研究中的重点进行大量研究和讨论。有研究发现,对于癌症患者来说,化疗能够杀灭癌细胞,但存在的不良反应使患者承受着较大的痛苦和折磨,严重降低了患者的生活质量[1]。随着对恶性肿瘤相关研究的增多,新辅助化疗或许有望成为治疗乳腺癌等恶性肿瘤疾病的有效方法,并在临床上进行了大量研究和试验[2]。在临床化疗药物中,紫杉醇的使用范围较广泛,可用于乳腺癌和卵巢癌的治疗中,通过使用紫杉醇治疗能够获得较为显著的结果,但是由于紫杉醇的水溶性较差,获取来源较少,因而导致该药物在临床中的广泛应用受到了限制[3]。随着研究的深入,近些年研究发现可以使用脂质体代替紫杉醇,脂质体可以通过人工的方式获得,来源广泛,将其制作成制剂能够增强药物的稳定性,降低药物毒性[4]。我国成功研制了紫杉醇脂质体注射剂,但关于该药物在乳腺癌辅助治疗中的应用临床上的报道较少。因此,本研究选取200例乳腺癌患者进行研究,获得了较好的结果,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年1-12月邳州市人民医院收治的200例乳腺癌患者。纳入标准:(1)符合乳腺癌诊断标准;(2)无其他合并器质性疾病;(3)无心血管疾病;(4)年龄 >18周岁;(5)无乳腺癌手术史。排除标准:(1)化疗不耐受;(2)精神状态异常;(3)对本研究所使用药物过敏。按照电脑随机分组法将患者分为对照组和观察组,每组100例。两组患者均为女性,对照组年龄23~44岁,平均(32.3±3.1)岁;乳腺癌分期:Ⅰ期38例,Ⅱ期54例,Ⅲ期8例。观察组年龄22~45岁,平均(33.2±3.5)岁;乳腺癌分期:Ⅰ期42例,Ⅱ期52例,Ⅲ期6例。两组年龄、癌症分期情况比较,差异均无统计学意义(P>0.05),具有可比性。本研究已获得医院伦理委员会批准,患者自愿加入本研究并签署同意书。
1.2 方法
两组患者均给予对症治疗,包括止吐、抑酸护胃、抗过敏,预防水钠潴留。在化疗前1 d、化疗当天和化疗后1 d给予患者地塞米松(生产厂家:辰欣药业股份有限公司,国药准字H37021898,规格:0.75 mg)0.75 mg,2 次 /d,口服。
对照组采用多西他赛(生产厂家:江苏恒瑞医药股份有限公司,国药准字H20020543,规格:0.5 ml∶20 mg)75 mg/m2、盐酸表柔比星(生产厂家:瀚晖制药有限公司,国药准字H19990280,规格:10 mg)60 mg/m2、环磷酰胺(生产厂家:德国Baxter Oncoiogy Gmbh,进口药品注册证 H20160467,规格:0.2 g)500 mg/m2,静脉滴注,一疗程 21 d,治疗6个疗程。
观察组采用紫杉醇脂质体(生产厂家:南京绿叶制药有限公司,国药准字H20030357,规格:30 mg)代替多西他赛进行治疗,剂量为150 mg/m2。其余与对照组一致。在每个治疗疗程结束之后,患者要进行血常规监测,若出现超过Ⅰ级的骨髓抑制需要皮下注射粒细胞集落刺激因子。
1.3 观察指标及评价标准
(1)两组治疗6个周期后进行效果评估。治疗效果按照RECIST 1.1标准分为:完全缓解(CR)、部分缓解(PR)、稳定病变(SD)和肿瘤进展(PD)4个等级。完全缓解指患者的全部病灶消失,至少维持4周;部分缓解指肿瘤最大径之和缩小≥30%;稳定病变指肿瘤最大径之和缩小不足30%,增大不足20%;肿瘤进展指肿瘤最大径之和增加≥20%[5]。总有效率(ORR)=(CR+PR)/总例数×100%。(2)比较两组的不良反应(中性粒细胞减少、白细胞计数减少、血小板减少、血红蛋白减少、呕吐恶心、腹泻)发生情况。
1.4 统计学处理
采用SPSS 22.0统计学软件进行数据分析,计量资料用(±s)表示,组间比较采用t检验;计数资料用率(%)表示,组间比较采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 两组疗效比较
观察组的治疗总有效率为74.00%,高于对照组的46.00%,差异有统计学意义(P<0.05),见表1。
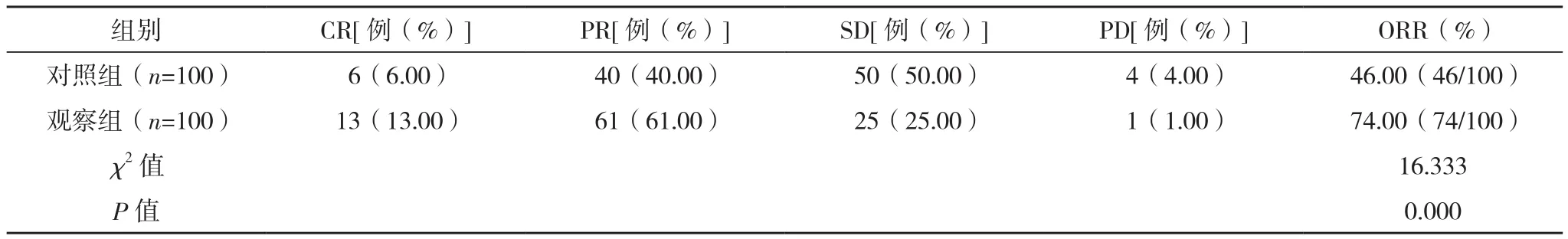
表1 两组疗效比较
2.2 两组不良反应发生情况比较
两组中性粒细胞减少、白细胞计数减少、血小板减少、血红蛋白减少、腹泻、恶心呕吐的发生率比较,差异均无统计学意义(P>0.05),见表2。

表2 两组不良反应发生情况比较[例(%)]
3 讨论
在众多妇科恶性肿瘤疾病中,乳腺癌是一种比较常见的癌症类型。有相关部门对乳腺癌在所有恶性肿瘤中的发病率进行调查发现,每10例恶性肿瘤患者中,就有1例乳腺癌患者,可见其发生率之高,在女性恶性肿瘤疾病中,乳腺癌的发病率仅次于宫颈癌,位居第二[6]。乳腺癌常出现在女性乳腺的上皮组织中,严重危害了女性的生命健康和安全乃至心理健康。关于乳腺癌发生的具体原因,目前临床上还没有给出具体、科学的定论。乳腺癌的早诊断、早治疗能够大大提升女性患者的生存质量和生存时间[7]。新辅助化疗相比传统的手术切除来说更能保证女性乳房外观的完整性,且为很多无法切除乳腺的女性患者带来了一线生机,对女性的生理和心理健康更有意义[8-9]。在乳腺癌化疗中,紫杉醇的使用频率较高,属于临床一线化疗药物,然而紫杉醇存在一些缺点和弊端,例如难以提取,水溶性差,合成难度大等,导致紫杉醇在临床的应用受到明显的限制[10]。多西他赛是一种比紫杉醇水溶性高的半合成紫杉醇类似物,和紫杉醇相比具有更好的水溶性,但总体上来说水溶性依然处于较差的水平,具有半衰期短的特点,在临床上的应用也受到了一定的限制。除此之外,经过临床大量的相关研究发现,患者在长时间使用多西他赛进行干预后出现了较多的副作用和不良反应,例如骨骼肌肉毒性、中性粒细胞减少、外周神经病变等,所以临床上需要寻找更加有效、安全的治疗药物,和别的溶媒相比,脂质性溶液有助于紫杉醇溶解率的提高[11]。聚氧乙烯蓖麻油是传统的紫杉醇溶媒,即使能够有效溶解紫杉醇,但常常伴随着较多不良反应,例如肝肾功能受损、过敏、神经毒性等等。临床上近年来多使用脂质体药物,紫杉醇也受到了临床医生和学者的广泛关注,相关学者还发现,和传统紫杉醇注射液相比,紫杉醇脂质体的安全性更能保障,可降低心脏毒性反应[12]。紫杉醇脂质体的众多优势十分突出,包括性质稳定、可长时间储存、降低不良反应发生率及更高的溶媒安全性。相关学者发现在乳腺癌的术后辅助化疗中,应用紫杉醇脂质体和应用多西他赛及紫杉醇注射液相比,紫杉醇脂质体治疗期间患者的依从性更高,这是由于紫杉醇脂质体对化疗不耐受患者来说,不良反应和副作用低从而减少了患者治疗终止或拒绝治疗的情况[13]。
有研究发现,在乳腺癌的新辅助化疗中,使用紫杉烷类药物或者蒽环类药物效果较好。在乳腺癌新辅助化疗中,紫杉醇发挥了较好的作用,可以通过抑制微管蛋白解离,使微管蛋白聚合并保持良好的稳定性,且能够有效抑制细胞的有丝分裂过程,从而抑制肿瘤细胞的增殖[14]。然而,紫杉烷类药物的缺陷也表现的较为明显,例如水溶性差、不良反应多等。在近些年来,医学技术发展成熟,我国成功研发了紫杉醇脂质体来代替该类药物,改善和弥补了紫杉烷类药物的缺陷,降低了药物的毒副作用,增强了药物的水溶性。紫杉醇脂质体是在紫杉醇外面包括卵磷脂,从而达到增强药物稳定性,延长药物在人体内停留的时间的目的,同时也不会因为使用了溶剂而出现不良反应,安全性较高。在本次研究中,观察组总有效率为74.00%,高于对照组的46.00%(P<0.05),表明在新辅助化疗用于乳腺癌治疗中,紫杉醇脂质体的治疗效果比较明显,随着药物剂量和类型的变化,提升了药物的作用时间和治疗效果,增强了药物对癌细胞的杀伤力,因此能够获得更好的治疗效果。除此之外,比较两组的副作用发生情况发现,观察组发生的不良反应发生率于对照组并无明显差异,说明两组在药物的安全性上差别不大。但本研究的研究条件有限,选取的样本数量较少,范围较窄,所以希望能在日后的研究中扩大样本选取范围和样本数量,深入分析研究结果。
综上所述,在乳腺癌新辅助化疗中应用紫杉醇脂质体对提高治疗效果有较好的帮助,不增加药物不良反应,可促进患者生存期的延长,具有临床借鉴意义。

