苦参碱对胰腺癌吉西他滨耐药细胞化疗敏感性的影响
郭晨博,毛玉宁,张贺,张彩勤,张延英,汪永锋*,师长宏*
(1. 甘肃中医药大学,兰州 730030;2. 空军军医大学实验动物中心,西安 710032)
胰腺癌(pancreatic cancer,PC)是最致命的恶性肿瘤之一,发病率和死亡率分别位于恶性肿瘤的第七位和第六位[1-2],近几年的发病率呈上升趋势[3]。目前手术切除仍是PC患者唯一可能治愈的手段,但由于PC早期缺乏临床症状和体征,直到晚期才被发现,导致手术效果不佳[4]。虽然近几年免疫疗法在PC治疗方面取得了一定进展,但仍然具有一定的局限性,因此化疗依旧是PC治疗的最主要手段之一[5]。吉西他滨(gemcitabine,GEM)是治疗PC的一线化疗药物[6],但是由于对吉西他滨的耐药性,导致治疗效果并不显著,因此急需深入研究吉西他滨耐药的机制,增强其敏感性[7]。近年来研究发现ATP结合盒(ATP binding cassette,ABC)转运体的过表达与肿瘤耐药相关[8]。ABC转运体是一种介导ATP驱动转运的膜蛋白家族[8]。多药耐药蛋白2(the ATP-binding cassette ABC superfamily gmember 2,ABCG2)是ABC膜蛋白家族成员之一,研究发现ABCG2通过降低细胞内药物浓度以显著增加化疗药物耐药性[9],但其在胰腺癌吉西他滨耐药中的作用并不明确,因此将ABCG2作为改善胰腺癌吉西他滨耐药的治疗靶点[9]。
大部分针对特定基因的分子抑制剂只能延迟癌症的进展,癌细胞最终将通过激活替代途径获得对抑制剂的耐药性。与传统的治疗抑制剂相比,中药单体具有低毒性、高安全性的特点,在改善肿瘤细胞耐药性中发挥着重要的作用。研究表明苦参碱具有改善肿瘤耐药的作用。苦参碱(matrine,MT)是从豆科植物苦豆子的根和茎中分离得到的一种天然生物碱[10-11]。具有诱导细胞凋亡和自噬、抑制细胞增殖、侵袭、转移与EMT过程,逆转耐药,细胞周期阻滞等生物学功能,因其高生物活性而被广泛发展为多种制剂[12]。研究发现苦参碱在改善胃癌、结肠癌、乳腺癌、肝癌[13-18]耐药中发挥着重要的作用。目前苦参碱在胰腺癌吉西他滨耐药中的作用并不清楚,并且是否调控ABCG2的表达不明确。本研究旨在研究苦参碱在胰腺癌耐药中的作用,探索其调控机制。
1 材料与方法
1.1 材料
1.1.1 实验动物
20只SPF级雄性BALB/c裸鼠,6 ~ 7周龄,体重22 ~ 25 g,购买自成都药康生物科技有限公司【SCXK(川)2020-034】。环境温度23 ~ 25℃,相对湿度40%,光照/黑暗各12 h,昼夜交替;动物自由摄食和饮水,饲养于空军军医大学实验动物中心SPF级屏障设施中【SYXK(陕)2019-001】。细胞异种移植模型分为对照组、苦参组、吉西他滨组、苦参碱和吉西他滨联合组,每组5只裸鼠。相关动物实验通过空军军医大学实验动物福利伦理委员会批准(IACUC-20220427)。
1.1.2 细胞
人类胰腺癌细胞系AsPC-1购自国家细胞库-ATCC细胞资源中心。
1.1.3 主要试剂与仪器
苦参碱购自上海源叶生物科技有限公司,DMEM培养基和胎牛血清均购自美国Gibco公司;0.05%胰酶购自美国HyClone公司;荧光定量PCR及RNA提取试剂盒等酶标仪(Biotek Take,美国),CCK-8检测试剂盒购自上海七海复泰生物科技有限公司;吉西他滨购自ELI LILLY公司。
酶标仪(Bio Tek,美国),超净工作台(Thermo Fisher Scientific,美国),显微镜(Olympus,日本),普通离心机(安徽中佳科学仪器有限公司,中国),恒温水浴锅(上海三发科学仪器有限公司,中国)。
1.2 方法
1.2.1 细胞培养
AsPC-1细胞用培养基为含有10% FBS及青霉素(100 IU/mL)/链霉素(100 μg/mL)的DMEM,在5% CO2的37℃恒温培养箱中培养。
1.2.2 诱导吉西他滨耐药胰腺癌细胞株
采用96孔板分不同浓度的吉西他滨进行筛选,最终发现AsPC-1细胞系在4 μg/mL浓度的吉西他滨作用下可持续增长,因此选用4 μg/mL吉西他滨持续诱导吉西他滨敏感的胰腺癌AsPC-1细胞株,持续6个月,并观察细胞死亡情况,最终通过CCK-8实验验证其耐药性并将胰腺癌吉西他滨耐药株命名为AsPC-1-GEM。
1.2.3 细胞增殖
通过CCK-8测定法检测细胞增殖。将肿瘤细胞铺在96孔板(3000个细胞/孔)中,在细胞贴壁后加入不同浓度的吉西他滨和苦参碱,培育72 h后加入100 μL培养基/CCK-8混合物(培养基:CCK-8,9∶1)孵育3 h后,测量450 nm处吸光度值,再根据吸光度值算出细胞活力。
1.2.4 实时RT-PCR分析
将AsPC-1细胞和AsPC-1-GEM细胞按照商品化RNA提取试剂盒(总RNA提取试剂盒,TIANGEN,DP419)说明书提取总RNA。用微量酶标仪测定RNA浓度,根据测定结果,将其浓度调整至500 ng/μL。根据TaKaRa试剂盒说明书(PrimeScriptRTMaster Mix,TaKaRa,RR036A)将RNA逆转录为cDNA,反转录条件设置为37℃ 15 min,85℃ 15 s。荧光定量PCR反应按照TaKaRa试剂盒(SYBR Premix Ex Taq Ⅱ,TaKaRa,RR820A)进行荧光定量PCR反应。PCR反应体系(20 μL):SYBR Premix Ex Taq Ⅱ 10 μL,上下游引物各0.5 μL,ROX Reference Dye(50×)0.4 μL,cDNA模板1 μL,ddH2O 7.6 μL。PCR反应条件:95℃预变性30 s,PCR反应95℃ 15 s,60℃ 30 s(荧光测量)40个循环。测各个样本中的Ct值,每组样本检测3次,每次检测均做3个复孔,最终Ct值以平均值表示,扩增的基因有ABCG2,内参为β-actin,相关信息见表1。

表1 引物序列信息Table 1 Primer sequences of genes
1.2.5 免疫印迹分析
将培养瓶中的AsPC-1细胞、AsPC-1-GEM细胞、0.3 mg/mL苦参碱处理72 h的AsPC-1-GEM、0.02 μg/mL吉西他滨处理72 h的AsPC-1-GEM、0.3 mg/mL苦参碱和0.02 μg/mL吉西他滨处理72 h的AsPC-1-GEM的蛋白收集起来用RIPA裂解缓冲液裂解细胞。用BCA试剂(中国Beyotime)检测蛋白浓度。液体配置:电泳液和转膜液配置,通过电泳、转膜、封闭、一抗孵育、二抗孵育、发光,并用相应抗体ABCG2(Proteintech,27286-1-AP)、β-actin(Cell Signaling,8H10D10)进行免疫印迹。最终利用Image J软件对Western Blot结果中各条带灰度值进行半定量分析。
1.2.6 肿瘤细胞异种移植
将Aspc-1-GEM细胞用0.25%的胰酶消化后制备成细胞悬液,用PBS将细胞稀释成每毫升1 × 106接种到6 ~ 7周龄的免疫缺陷裸鼠皮下,每组5只,用游标卡尺测量皮下肿瘤的长度(l)和宽度(w),肿瘤体积(V)计算公式为:V=1/2 ×l×w2。每隔3 d测定1次肿瘤体积,待对照组肿瘤体积接近1000 mm3时,处死裸鼠,并绘制肿瘤生长曲线。
1.2.7 免疫组化
肿瘤组织用4%多聚甲醛固定,石蜡包埋,切片,用二甲苯和梯度乙醇浸泡,再通过高温抗原修复后,内源性过氧化物酶被阻断。用37℃封闭山羊血清10 min。一抗(ABCG2抗体、Abcam,稀释比1∶100)在4℃下孵育过夜。生物素标记的山羊抗兔二抗在室温黑暗中孵育20 min。在3,3’-二氨基联苯胺染色、苏木精、盐酸醇分化、脱水、密封、中性胶密封后,使用Image Pro Plus 6.0软件定量对视野中阳性细胞的比例进行分析。
1.3 统计学分析
采用SPSS 22.0和GraphPad Prism 8.4.0软件进行数据统计学分析,所有实验均重复3次,计量资料以平均值 ± 标准差(± s)表示,组间比较采用独立样本t检验,以P < 0.05为差异具有显著性,P< 0.01为差异极具显著性。
2 结果
2.1 构建胰腺癌吉西他滨耐药细胞株
为了探究胰腺癌细胞耐药性的变化,首先通过4 μg/mL吉西他滨持续诱导吉西他滨敏感的胰腺癌AsPC-1细胞株6个月,构建胰腺癌吉西他滨耐药细胞株,并将其命名为AsPC-1-GEM。采用CCK-8检测不同浓度吉西他滨对AsPC-1和AsPC-1-GEM细胞株的抑制效果,结果显示AsPC-1-GEM株对吉西他滨的敏感性降低,AsPC-1的IC50为10 μg/mL,N为8,AsPC-1-GEM的IC50为110 μg/mL,N为8,比较IC50,发现AsPC-1-GEM的IC50比AsPC-1具有显著性差异(P< 0.01)(图1A,1B)。

图1 构建胰腺癌吉西他滨耐药细胞株Note. A. Analyze the effect of gemcitabine on the pancreatic cancer cell lines AsPC-1 and AsPC-1-GEM by CCK-8. B. Compared with AsPC-1,IC50 of AsPC-1-GEM increased significantly, **P < 0.01. (The same in the following figures)Figure 1 Inducing gemcitabine resistant cell lines by treatment with pancreatic cancer
2.2 苦参碱提高AsPC-1-GEM细胞化疗敏感性
将AsPC-1-GEM细胞分成苦参碱组、吉西他滨组、苦参碱和吉西他滨联用组。CCK-8结果显示,联合组对比其他两组具有显著性差异(图2A)。为了进一步确定,将苦参碱最小有效剂量0.3 mg/mL加入到不同浓度的吉西他滨中,CCK-8结果显示苦参碱最小有效剂量在不同浓度的吉西他滨作用下都具有提高AsPC-1-GEM细胞敏感性的作用(图2B)。故后续实验苦参碱剂量选择为0.3 mg/mL,吉西他滨剂量为0.02 mg/mL。

图2 苦参碱提高了AsPC-1-GEM细胞化疗敏感性Note. A. Analyze the effect of matrine on AsPC-1-GEM cellsby CCK-8. B. Analysis of the effects of matrine and gemcitabine on AsPC-1-GEM cellsby CCK-8.Compared with AsPC-1,***P < 0.001.(The same in the following figures)Figure 2 Treatment with matrine increases the sensitivity of AsPC-1-GEM cells to gemcitabine
2.3 AsPC-1-GEM细胞株ABCG2高表达
通过实时RT-PCR筛选ABC基因,发现ABCG2在AsPC-1和AsPC-1-GEM差异性最大,因此将ABCG2作为研究目标(图3A),再通过文献报道发现ABCG2在胰腺癌吉西他滨耐药中发挥着重要作用[19],因此检测了耐药相关蛋白ABCG2的表达,通过实时RT-PCR和免疫印迹检测发现AsPC-1-GEM对比AsPC-1的ABCG2具有显著性差异(P< 0.01)(图3B)。
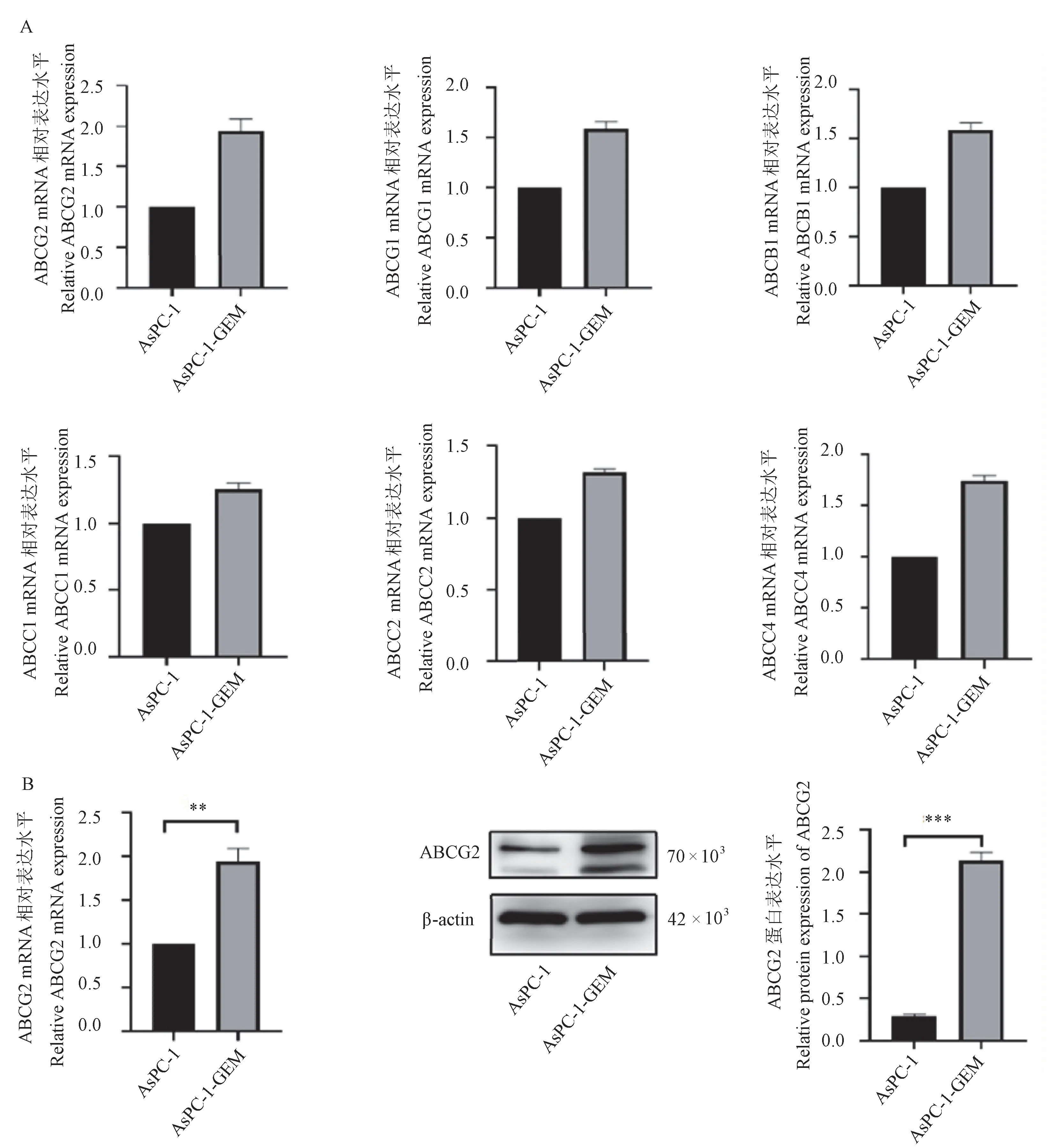
图3 AsPC-1耐药前后ABCG2表达情况Note. A. qRT-PCR screening of expression of individual ABC genes before and after resistance to AsPC-1.B. Analysis ABCG2 expression after AsPC-1 resistance to gemcitabine by Western Blot.Figure 3 Expression of ABCG2 in AsPC-1 cell and AsPC-1-GEM cell
2.4 苦参碱通过降低ABCG2的表达提高AsPC-1-GEM的敏感性
为了探索苦参碱的具体分子作用机制,将AsPC-1-GEM细胞分成溶剂组、苦参碱组、吉西他滨组、苦参碱和吉西他滨联合处理组,Western Blot结果显示苦参碱组、苦参碱和吉西他滨联合处理组对比对照组中的ABCG2具有显著性差异(图4)。

图4 苦参碱降低AsPC-1-GEM细胞中ABCG2的表达Note. The expression of ABCG2 in AsPC-1-GEM cell after treated with matrine was analyzed by Western Blot.Compared with AsPC-1, *P < 0.05.Figure 4 Treatment with matrine reduces the expression of ABCG2 in AsPC-1-GEM cell
2.5 苦参碱降低ABCG2表达可延缓肿瘤生长
为了进一步验证苦参碱在体内的作用,将AsPC-1-GEM细胞以每毫升1 × 106接种到20只裸鼠皮下,监测肿瘤生长情况。待肿瘤长至80 mm3左右时,将其分为溶剂组、苦参碱组、吉西他滨组、苦参碱和吉西他滨组4组处理,苦参碱用量为50 mg/kg[20],1 d 1次,给药方式为腹腔注射,吉西他滨用量为25 mg/kg,1周2次,给药方式为腹腔注射,待溶剂组肿瘤体积接近1000 mm3,处死裸鼠,每3 d测量肿瘤最长直径(l),肿瘤最短直径(w),计算体积。结果显示苦参碱和吉西他滨联合组对比其他三组具有显著性差异(图5A),肿瘤重量也具有显著性差异(图5B),且肿瘤生长缓慢(图5C),裸鼠体重并无显著性差异(图5D),免疫组化发现MT组和联合组对比对照组有显著性差异(图5E)。

图5 苦参碱和吉西他滨联合组可显著延缓体内肿瘤生长Note. A. Tumor growth of AsPC-1-GEM cell xenograft tumor in nude mice. B. The tumor weight AsPC-1-GEM cell xenograft. C. Tumor growth curves of AsPC-1-GEM cell l xenograft tumor in nude mice. D. Body weight changes in nude mice with AsPC-1-GEM cellxenograft tumor. E. Expression of ABCG2.Figure 5 Treatment with matrine and gemcitabine significantly delayed tumor growth
3 讨论
中药单体具有低毒、高安全性的特点,并通过多种途径抑制肿瘤的发生、生长和转移[21-22]。临床实践中发现中药单体可显著增强化疗药物的敏感性,抑制肿瘤的作用[23-24]。苦参是一种传统的中药,具有独特的抗癌作用。苦参碱是苦参的有效成分,近年来发现苦参碱可以通过影响耐药基因从而在肿瘤耐药中发挥着重要作用[25-27],目前苦参碱在胰腺癌吉西他滨耐药中的作用并无文献报道,因此本研究旨在明确苦参碱是否能够提高胰腺癌吉西他滨耐药株敏感性,并探索其相应的机制。
首先选取吉西他滨敏感的人胰腺癌AsPC-1细胞株,采用4 μg/mL吉西他滨持续诱导获得人胰腺癌AsPC-1-GEM耐药株,发现AsPC-1细胞和AsPC-1-GEM在10 000 μg/mL、1000 μg/mL、100 μg/mL、10 μg/mL的吉西他滨作用下的细胞活力的对比发现AsPC-1-GEM细胞活力显著提高,并且AsPC-1-GEM的IC50为110 μg/mL,而AsPC-1细胞的IC50为10 μg/mL,AsPC-1-GEM的IC50比AsPC-1具有显著性差异,从而证实人胰腺癌AsPC-1耐药株建立成功。进一步观察苦参碱在胰腺癌吉西他滨耐药细胞中的作用,图2中CCK-8实验表明苦参碱具有提高胰腺癌细胞的敏感性的作用,分别设置了不同剂量的苦参碱组和不同剂量的吉西他滨组,观察到最小有效剂量0.3 mg/mL的苦参碱可以提高AsPC-1-GEM耐药株对吉西他滨的敏感性,因此后续研究中都是选择0.3 mg/mL的苦参碱进行实验。
研究发现肿瘤耐药与ABCG2相关[27-30],通过文献发现腺癌癌吉西他滨耐药与ABCG2有着密切的关系[31],并在实验中发现在胰腺癌细胞耐药前后ABCG2具有显著性差异,因此本研究将ABCG2和吉西他滨耐药联系起来。通过qRT-PCR和Western Blot实验发现ABCG2在胰腺癌耐药细胞AsPC-1-GEM中高表达,并具有显著性差异,ABCG2可能成为胰腺癌吉西他滨耐药的治疗靶点。将0.3 mg/mL的苦参碱加入到胰腺癌吉西他滨耐药细胞株中,Western Blot实验发现苦参碱具有降低ABCG2的表达的作用,量化结果显示具有显著性差异。进一步将耐药肿瘤细胞移植入裸鼠体内建立异种移植模型,发现苦参碱和吉西他滨联合组肿瘤对比其他三组具有显著性差异;苦参碱和吉西他滨联合组肿瘤的体重对比其他三组具有显著性差异;苦参碱和吉西他滨联合组对肿瘤体积对比其他三组有着明显的抑制作用;通过文献报道吉西他滨为25 mg/kg为安全剂量[32-33],吉西他滨毒性使吉西他滨组和联合组的裸鼠体重均有下降,这也使得肿瘤窗口期不佳,目前苦参碱可以增加吉西他滨敏感性的作用,对吉西他滨毒性的影响较小;通过组化结果发现苦参碱可有效降低ABCG2的表达。因此通过以上实验发现苦参碱通过降低ABCG2的表达,进而提高了胰腺癌耐药细胞的吉西他滨敏感性。
总之,本研究表明,苦参碱具有提高胰腺癌吉西他滨耐药细胞敏感性的作用。体内、体外实验均证实苦参碱可以降低ABCG2的表达,从而提高胰腺癌吉西他滨耐药株敏感性,提示苦参碱可能成为改善胰腺癌耐药的潜在药物。

