内镜下高频电刀与氩离子凝固术联合应用于胃肠息肉治疗中的效果研究
焦胜成 孙增峰 李宾(通信作者)
250115 济南市历城区人民医院内科1,山东济南
250021 山东省立医院消化内科2,山东济南
胃肠息肉属于临床常见的消化系统疾病,虽然此类疾病无典型的症状表现,但存在恶变的可能性[1]。因此积极采取有效的治疗措施清除胃肠息肉十分必要。目前,高频电切术是治疗胃肠息肉的主要方案,具有操作简便、技术成熟、安全性佳等优势,但该技术也存在术后并发症率高、复发率高等问题[2]。氩离子凝固术是一种非接触性电凝固技术,其利用高频单极电流,以电离氩气形成高频能量,引导组织产生凝固效应并变形脱落。为了进一步完善胃肠息肉患者的治疗方案,本研究对65 例胃肠息肉患者应用内镜下高频电刀与氩离子凝固术联合治疗,并与单纯高频电切术对比,观察两种方案的应用效果,现报告如下。
资料与方法
130例研究对象均为2016年6月-2019年5月我院收治的胃肠息肉患者,将其随机分成两组。对照组65 例中男34 例,女31 例;年龄27~73 岁,平均(46.8±7.4)岁;单发息肉48 例,多发息肉17 例;发病部位为结肠32 例,胃部28 例,十二指肠球部5例。研究组65 例中男36 例,女29 例;年龄28~70岁,平均(46.4±7.6)岁;单发息肉49例,多发息肉16例;发病部分为结肠32例,胃部28例,十二指肠球部5 例。两组性别、年龄、发病情况等一般资料比较,差异无统计学意义(P>0.05),具有可比性。患者均签署知情同意书,本研究经伦理委员会批准。
纳入标准:①符合《消化疾病诊疗指南》第3版[3]对胃肠息肉的诊断标准,且经病理检查证实;②心功能与肝肾功能正常。
排除标准:①全身代谢性疾病;②肝肾功能障碍或有心脑血管疾病;③血液疾病;④哺乳与妊娠期女性。
方法:两组术前均禁食水,术前20 min肌注地西泮10 mg+山莨菪碱10 mg。①研究组应用内镜下高频电刀与氩离子凝固术联合治疗:内镜进入病灶处时将息肉周的水分与分泌物去除,暴露息肉。电切输出功率调节至30~90 W,切割与收圈,针对直径过大的息肉给予多次通电切除。氩离子凝固治疗时设置功率为35~45 W,打开氩气瓶阀门,调节流量为1 L/s,以内镜钳在息肉上放置氩气离子束凝固导管,踩踏氩离子凝固档将息肉祛除,也可以进行电切后止血。②对照组采用内镜下高频电切术治疗:内镜、高频电切方法与研究组相同;设置高频电凝输出功率为35~50 W,以内镜钳在息肉上放置圈套器,通电灼除息肉。两组术后均禁食1 d,之后摄入流质饮食,卧床休息,1周内避免剧烈运动,并使用4~8周的胃黏膜保护剂。
观察指标:①对比两组患者1次手术成功率,手术成功即术后3个月复查病灶全部消失,基底凝固变白。②随访1年,对比两组患者复发率。③对比两组术前与术后胃部因子指标的变化,包括血清胃泌素-17(G-17)、胃蛋白酶原Ⅱ(PGⅡ)、胃蛋白酶原Ⅰ(PGⅠ)。④对比两组术后并发症,包括穿孔、出血、腹痛等。
数据统计学:研究数据以SPSS 20.0 软件分析;计数资料以[n(%)]描述,手术成功率、复发率与并发症的组间结果以χ2检验;计量资料以(±s)表示,胃部因子指标的组间结果以t检验;以P<0.05 为差异有统计学意义。
结 果
两组手术的成功与复发率对比:在1次手术成功率比较中,研究组较对照组高,差异有统计学意义(P<0.05);随访1年内复发率,研究组较对照组低,差异有统计学意义(P<0.05)。见表1。
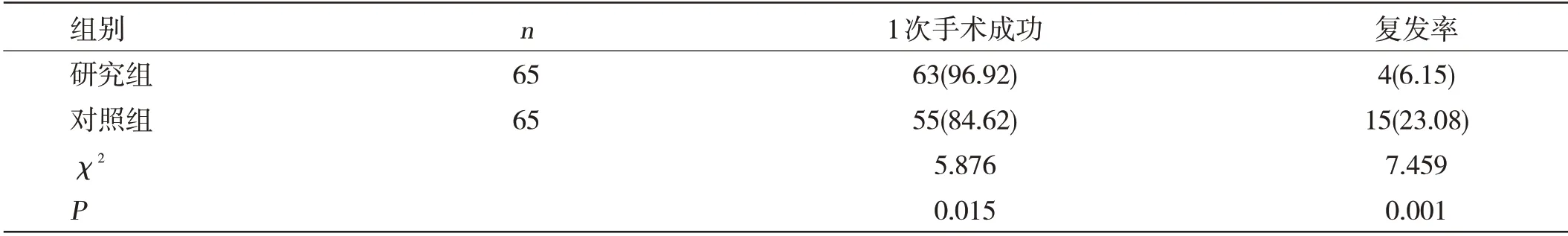
表1 两组1次手术成功率与复发率比较[n(%)]
两组术前与术后胃部因子对比:术前两组各项胃部因子水平比较,差异有统计学意义(P>0.05);术后G-17、PGⅠ指标比较中,研究组均较对照组高,差异有统计学意义(P<0.01);两组PGⅡ水平比较,差异无统计学意义(P>0.05)。见表2。
表2 两组手术前后胃部因子指标水平比较(±s)
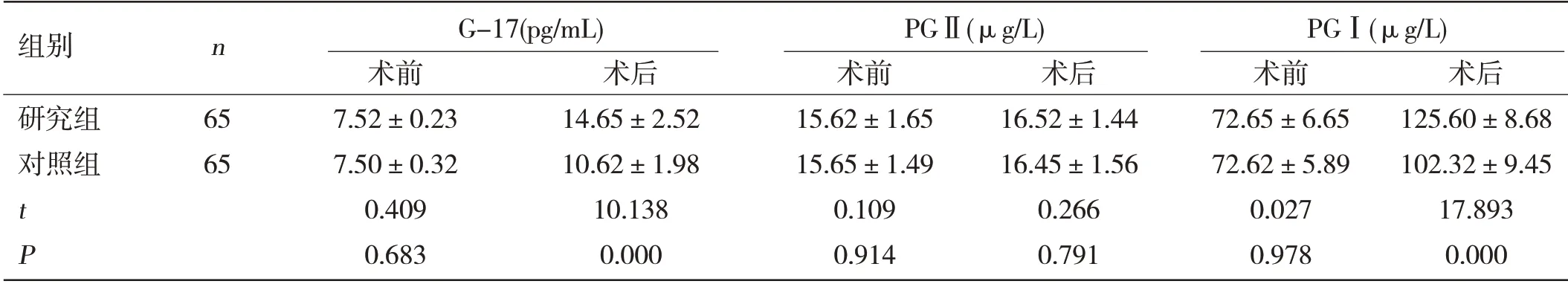
表2 两组手术前后胃部因子指标水平比较(±s)
组别 n G-17(pg/mL) PGⅡ(μg/L) PGⅠ(μg/L)术前 术后 术前 术后 术前 术后研究组 65 7.52±0.23 14.65±2.52 15.62±1.65 16.52±1.44 72.65±6.65 125.60±8.68对照组 65 7.50±0.32 10.62±1.98 15.65±1.49 16.45±1.56 72.62±5.89 102.32±9.45 t 0.409 10.138 0.109 0.266 0.027 17.893 P 0.683 0.000 0.914 0.791 0.978 0.000
两组患者术后并发症发生情况比较:研究组术后发生腹胀3例,腹痛1例;对照组术后发生腹胀5例,腹痛4例,穿孔2例,出血1例。术后并发症发生率比较,研究组(6.15%)较对照组(18.46%)低,差异有统计学意义(P<0.05)。
讨 论
胃肠息肉是常见的消化系统疾病。目前,内镜技术在胃肠息肉的治疗中发挥着重要作用,其中内镜处射频电流、微波、热探头等方案均在临床得到广泛应用[4]。然而,接触性电凝存在探头粘连问题,微波治疗不利于完整的标本采集,而非接触性激光热凝并发症高且价格昂贵,致使临床应用受到局限[5]。高频电切术是一种操作方便、技术成熟的胃肠息肉治疗技术,其通过高频电流电压接触组织产生热量,继而发挥切割、分离组织与止血的目的,对于较大胃肠或带蒂息肉同样适用。然而,高频电切术与组织接触后也易形成热探头粘连,往往需要反复退管对探头进行清理,且组织失活与热凝固深度不利于控制,继而增加了穿孔风险。
氩离子凝固术属于新型电凝治疗技术,具有非接触性特点,其利用特殊装置将氩气离子化能量向组织传递,继而达到治疗组织病变与止血的作用[6]。同时,氩离子凝固术根据电场与气流强度,有效控制穿透深度,通常不超过2~3 mm,所以极大程度地避免了胃肠穿孔等问题。氩离子凝固术属于非接触性操作,探头与组织距离0.3~0.5 cm,且氩离子呈散发状态,可以自动选择到达组织的理想通路,不存在探头粘连情况,且节约了操作时间[7]。此外,氩离子能够形成轴向与侧向传导作用,氩离子束在探头未指向组织表面的情况仍可以规划最佳传导通道,到达病灶组织,且当组织表面过于干燥而失去导电作用时,氩离子还能向导电处导向,直至探头指向部位完全干燥。所以氩离子凝固术不受气流与探头的限制,可以处理任意部位的胃肠息肉。本文研究发现,在1 次手术成功率比较中,研究组较对照组高(P<0.05);随访1年内复发率,研究组较对照组低(P<0.05)。可见,内镜下高频电刀与氩离子凝固术联合应用有效提高了患者的治疗效果,降低复发概率。
PG 是胃蛋白酶前体,主要由泌酸腺形成,并在酸性环境中产生作用。PG 分为PGⅡ与PGⅠ两种类型,其中PGⅡ由十二指肠与黏液颈细胞上部细胞产生,PGⅠ由黏液细胞与主细胞形成,其水平反映了胃泌酸腺细胞的功能与状态,即浓度越高说明胃酸分泌功能越佳[8]。胃G 细胞是胃内分泌的典型开放型细胞,以胃窦部最多,其次为胃底、十二指肠与空肠处。进食时食物使胃出现机械性扩张,壁内神经丛刺激G 细胞分泌促胃液素,并通血液刺激胃底腺分泌。人体中,95%以上有生物活性的胃泌素为α-酰胺化胃泌素,其含有两种异构体,其中80%~90%为G-17,而G-17 作为胃G 细胞标志,可以有效反映出胃黏膜损伤情况与胃功能[9]。本研究发现,术后G-17、PGⅠ指标比较中,研究组均较对照组高(P<0.01)。可见,在高频电刀的基础上应用氩离子凝固术可以有效促进胃黏膜修复,并对肠上皮化生与胃黏膜萎缩等病变具有抑制作用,有效保障了预后。在术后并发症比较中,研究组的并发症发生率为6.15%,较对照组的18.46%低(P<0.05)。两种技术联合应用可以减少单纯高频电刀的操作频率,继而降低相关不良反应,提高治疗的安全性。
综上所述,内镜下高频电刀与氩离子凝固术联合应用于胃肠息肉治疗中效果确切,安全性佳,适于临床推广。

