HPLC法测定卤米松乳膏中有关物质
安明,常珍,吕宁,郎昌野,孙静芬
卤米松是一种强效外用糖皮质激素类固醇药物,具有抗炎、抗过敏、抗增生、收缩毛细血管和止痒等作用。目前临床使用的卤米松主要剂型为乳膏剂,其适应证为对皮质类固醇治疗有效的非感染性炎症性皮肤病,如脂溢性皮炎、接触性皮炎、异位性皮炎、局限性神经性皮炎、湿疹、白癜风、寻常型银屑病和扁平苔藓等。卤米松乳膏因使用方便、起效迅速、疗效显著,而得到广泛的临床应用,并有大量文献报道[1-7]。但卤米松及卤米松乳膏相关的质量研究报道却极少,仅有 1 篇卤米松原料药有关物质研究和 1 篇卤米松乳膏含量测定的文献[8-9],尚未见到对卤米松乳膏有关物质进行系统研究的报道。随着近年来国家药监部门对药品质量控制的加强和质量标准的提高,外用制剂的有关物质研究成为质控重点之一。因此,系统研究卤米松乳膏的有关物质,并建立严格的控制标准,对于保证药品质量和临床用药安全具有重要意义。
本文参照相关文献方法[8,10],建立了卤米松乳膏有关物质检测的高效液相色谱(HPLC)分析方法,并对方法学进行了全面系统的验证。在此基础上,对多个批次的卤米松乳膏自制品进行了有关物质检测,并与原研品进行了比较。
1 材料与方法
1.1 材料
LC-20A 型高效液相色谱仪(包括 LC-20AT型二元高压梯度泵、SIL-20AC 型自动进样器、CTO-20AC 型柱温箱、SPD-20A 型紫外检测器、Labsolution 工作站)为日本岛津公司产品;Ultimate 3000 型高效液相色谱仪(包括集成式四元泵、自动进样器、柱温箱、二极管阵列检测器和变色龙工作站)为美国赛默飞世尔科技有限公司产品;MS105DU 型电子天平为美国梅特勒托利多公司产品。
卤米松乳膏自制品(批号:171201、171202、171203)由湖南明瑞制药有限公司生产;卤米松乳膏原研品(批号:6171131、6171119)为香港澳美制药厂产品;卤米松对照品(纯度:95.9%)、杂质A(纯度:80.48%)、杂质 B(纯度:95.12%)、杂质 C(纯度:97.86%)、杂质 D(纯度:97.37%)、杂质 E(纯度:97.50%)、杂质 F(纯度:96.94%)、杂质 G(纯度:99.02%)、杂质 H(纯度:99.75%)、杂质 I(纯度:99.27%)、杂质 J(纯度:92.41%)、杂质 K(纯度:99.56%)均由湖南明瑞制药有限公司标定;HPLC 级乙腈为美国 Honeywell 公司产品;GR 级冰醋酸为美国阿拉丁公司产品;水为超纯水。
1.2 方法
1.2.1 色谱条件 色谱柱:Agilent ZORBAX SB-C18 色谱柱(4.6 mm × 250 mm,5 μm);流动相:以 0.03% 冰醋酸为流动相 A,乙腈为流动相 B,按表1 所列条件进行梯度洗脱;流速:0.8 ml/min;检测波长:238 nm;柱温:35 ℃;进样体积:20 μl。

表1 卤米松乳膏有关物质检查色谱条件的梯度洗脱程序Table 1 Gradient elution procedure of chromatographic condition for the determination of the related substances in halomethasone ointment
1.2.2 溶液配制 供试品溶液:取卤米松乳膏内容物适量(约相当于卤米松 5 mg),置具塞锥形瓶中,加乙腈:水:冰醋酸(75:25:0.03)10 ml 和氯化钠 0.2 g,60 ℃ 水浴振摇使卤米松溶解,置冰浴中放置 30 min,取出摇匀,放至室温,取上清液3000 r/min 离心 1 min 后,经 0.22 μm 滤膜滤过,取续滤液作为供试品溶液。
对照溶液:精密量取供试品溶液 1 ml,置100 ml 量瓶中,以乙腈:0.03% 冰醋酸溶液(50:50)稀释至刻度,摇匀,作为对照溶液(1.0%)。
灵敏度溶液:精密量取对照溶液 1 ml,置 20 ml量瓶中,以乙腈:0.03% 冰醋酸溶液(50:50)稀释至刻度,摇匀,作为灵敏度溶液(0.05%)。
系统适用性溶液:取卤米松对照品、杂质 A、杂质 C、杂质 F、杂质 G、杂质 J 对照品各适量,精密称定,加乙腈:0.03% 冰醋酸溶液(50:50)溶解并定量稀释制成约含卤米松 0.5 mg/ml、各杂质 2.5 μg/ml 的溶液,作为系统适用性溶液。
1.2.3 测定法 参照高效液相色谱法(《中国药典》2020年版四部通则 0512)试验,采用上述色谱条件,取系统适用性溶液 20 μl 注入液相色谱仪,按卤米松、杂质 G、杂质 J、杂质 F、杂质 C、杂质 A 的顺序依次出峰,上述各峰之间的分离度均应符合要求。取灵敏度溶液 20 μl 注入液相色谱仪,主成分峰高的信噪比应大于 10。再取对照溶液和供试品溶液各 20 μl,注入液相色谱仪,记录色谱图。供试品溶液色谱图中如有杂质峰(扣除相对卤米松保留时间 0.35 倍之前的苯氧基乙醇峰及其他辅料峰),采用加校正因子的自身对照法进行计算,杂质 A、C、F、G、J 峰面积均不得大于对照溶液主峰面积的 0.5 倍(0.5%);其他单个杂质峰面积不得大于对照溶液主峰面积的 0.5 倍(0.5%);各杂质峰面积和不得大于对照溶液主峰面积的 2 倍(2.0%)。供试品溶液色谱图中小于灵敏度溶液中主峰面积的峰忽略不计(0.05%)。卤米松及各杂质结构式见图1,相对校正因子见表2。

表2 卤米松乳膏各有关物质相对校正因子及可接受限度Table 2 Relative correction factor and acceptable limit of various related substances in halomethasone ointment

图1 卤米松及卤米松乳膏中各有关物质结构式Figure 1 Structural formula of halomethasone and various related substances in halomethasone ointment
1.2.4 专属性 卤米松乳膏有关物质标准中,已知杂质规定了杂质 A、杂质 C、杂质 F、杂质 G、杂质 J。专属性试验应考察溶剂、空白辅料对测定有无干扰;卤米松主峰与相邻杂质峰之间,以及各杂质峰相互之间是否能够很好地分离。各溶液配制方法如下:
溶剂1:乙腈:0.03%冰醋酸溶液(50:50)。
溶剂2:乙腈:水:冰醋酸(75:25:0.03)。
空白辅料溶液:取卤米松乳膏自制品处方比例空白辅料约 10 g,精密称定,置 50 ml 具塞锥形瓶中,加 10 ml 溶剂 2 和氯化钠 0.2 g,水浴 60 ℃振摇使卤米松溶解,置冰浴中放置 30 min,取出摇匀,放至室温,取上清液离心 1 min(3000 r/min)后,经 0.22 μm 滤膜滤过,取续滤液,即得。
各杂质对照品贮备液(500 μg/ml):取卤米松杂质 A、杂质 B、杂质 C、杂质 D、杂质 E、杂质 F、杂质 G、杂质 H、杂质 I、杂质 J、杂质 K对照品各约 10 mg,精密称定,分别置不同 20 ml量瓶中,加溶剂 1 溶解并稀释至刻度,摇匀,即得。
混合杂质对照品贮备液 1(10 μg/ml):分别精密量取上述各杂质对照品贮备液(500 μg/ml)各1 ml,置同一 50 ml 量瓶中,加溶剂 1 稀释至刻度,摇匀,即得。
混合杂质对照品贮备液 2(25 μg/ml):分别精密量取上述杂质 A、杂质 C、杂质 F、杂质 G、杂质 J、杂质 K 对照品贮备液(500 μg/ml)各1 ml,置同一 20 ml 量瓶中,加溶剂 1 稀释至刻度,摇匀,即得。
系统适用性溶液:取卤米松工作对照品约10 mg,精密称定,置 20 ml 量瓶中,精密加入 2 ml混合杂质对照品贮备液 1(10 μg/ml),加溶剂 1 溶解并稀释至刻度,摇匀,即得。
自制品溶液:取卤米松乳膏自制品(批号:171201)约 10 g,精密称定,置 50 ml 具塞锥形瓶中,然后按上述空白辅料溶液配制方法操作,即得。
自制品 + 混合杂质对照品溶液(0.5%):取卤米松乳膏自制品约 10 g,精密称定,置 50 ml 具塞锥形瓶中,加 1 ml 混合杂质对照品贮备液 2、9 ml 溶剂 2 和氯化钠 0.2 g,然后按上述空白辅料溶液配制方法操作,即得。
原研品溶液:取卤米松乳膏原研品(批号:6171131)约 10 g,精密称定,置 50 ml 具塞锥形瓶中,然后按上述空白辅料溶液配制方法操作,即得。
自制品自身对照溶液:精密量取自制品溶液1 ml,置 100 ml 量瓶中,加溶剂 1 稀释至刻度,摇匀,即得。
灵敏度溶液:精密量取自制品自身对照溶液1 ml,置 20 ml 量瓶中,加溶剂 1 稀释至刻度,摇匀,即得。
精密量取上述溶液各 20 μl,分别注入液相色谱仪,记录色谱图。
1.2.5 干扰性 干扰性试验应考察供试品溶液色谱图中主峰是否为纯峰,以及高温、强酸、强碱、氧化、光照等破坏条件下降解的供试品溶液相对于未破坏供试品溶液物料平衡率是否在 90% ~ 110%之间,各峰之间是否能够充分分离。空白辅料溶液、自制品未破坏溶液、原研品未破坏溶液配制方法同1.2.4 专属性项下各溶液。
取卤米松乳膏自制品约 10 g,精密称定,平行数份,分别:①置 50 ml 具塞锥形瓶中,置高温120 ℃ 烘箱中,放置 16 h 后取出,冷却至室温(高温破坏);②置 50 ml 石英量瓶中,在 4500 Lx 光照强度下放置 24 h 后取出(光照破坏);③置50 ml 石英量瓶中,在 200 μW/cm2紫外光照强度下放置 24 h 后取出(紫外光照破坏);④置 50 ml具塞锥形瓶中,加入 1 mol/L 盐酸 1 ml,放置24 h 后,立即加入 1 mol/L 氢氧化钠溶液 1 ml 中和(强酸破坏);⑤置 50 ml 具塞锥形瓶中,加1 mol/L 氢氧化钠溶液 1 ml,放置 16 h 后,立即加入 1 mol/L 盐酸 1 ml 中和(强碱破坏);⑥置50 ml 具塞锥形瓶中,加入 30% 双氧水 1 ml,放置 24 h(氧化破坏)。然后,分别按照 1.2.4 专属性项下自制品溶液配制方法操作(其中强氧化破坏样品中加入溶剂 9 ml,强酸和强碱破坏样品中加入溶剂 8 ml,其余破坏样品中均加入溶剂 10 ml),分别作为相应破坏条件的自制品溶液。
原研品和空白辅料各破坏条件溶液的配制方法与自制品相应破坏条件的溶液相同。
精密量取上述溶液各 20 μl,分别注入液相色谱仪,记录色谱图。
1.2.6 线性与范围 取卤米松对照品适量,加溶剂溶解并稀释制成适当浓度的主成分对照品溶液;分别取杂质 A、C、F、G、J、K 对照品,加溶剂溶解并稀释制成系列浓度的各杂质对照品溶液。取各溶液 20 μl,注入液相色谱仪,记录色谱图。以浓度 C(μg/ml)为横坐标,以峰面积 A 为纵坐标,进行线性回归,求出线性方程。
1.2.7 定量限与检测限 取上述线性与范围项下各溶液,以溶剂逐步稀释,精密量取 20 μl,注入液相色谱仪,记录色谱图,按峰高约为基线噪音10 倍和 3 倍分别作为定量限(S/N ≥ 10)和检测限(S/N ≥ 3)。
1.2.8 精密度
⑴重复性:按照专属性项下方法分别配制自制品溶液和自制品自身对照溶液。按照专属性项下空白辅料溶液配制方法,仅将其中 10 ml 溶剂 2 替换为 1 ml 混合杂质对照品贮备液 2(25 μg/ml)+9 ml 溶剂 2,制得混合杂质对照品溶液。分别精密量取上述溶液各 20 μl,分别注入液相色谱仪,记录色谱图。以 6 份自制品溶液中杂质含量(采用加校正因子的自身对照法计算)的 RSD 考察方法的重复性。
⑵中间精密度:不同操作人员采用不同仪器于不同日期照重复性项下方法进行自制品溶液(6 份)和自制品自身对照溶液的配制。以 12 份自制品中杂质含量(采用加校正因子的自身对照法计算)的 RSD 考察方法的中间精密度。
1.2.9 准确度 按“1.2.8 精密度”中“重复性”项下方法,配制混合杂质对照品溶液。向卤米松乳膏自制品中分别加入“1.2.4 专属性”项下所述混合杂质对照品贮备液 2(25 μg/ml)适量,按自制品溶液配制方法操作,制备成含各已知杂质限度量的 50%、100%、150% 浓度的溶液,作为回收率供试品溶液。分别精密量取该回收率供试品溶液各 0.5 ml,置 50 ml 量瓶中,加溶剂稀释至刻度,摇匀,作为回收率自身对照溶液。
精密量取上述溶液各 20 μl,分别注入液相色谱仪,记录色谱图。按加校正因子的自身对照法计算回收率。
1.2.10 溶液稳定性 照专属性项下方法配制自制品溶液,于室温条件下放置,在 0、4、8、12、24、36、48 h 分别量取 20 μl,注入液相色谱仪,记录色谱图。以各已知杂质、单杂、总杂含量变化及杂质峰个数考察自制品溶液稳定性。
1.2.11 耐用性
⑴校正因子耐用性:考察了更换不同色谱柱(色谱柱 1、2、3)以及微调柱温(33、35、37 ℃),流速(0.75、0.8、0.9 ml/min),检测波长(236、238、240 nm),流动相初始比例(流动相 A:B 分别为63:37、65:35、67:33)等条件,对校正因子结果的影响。
⑵方法耐用性:考察了更换不同色谱柱(色谱柱 1、2、3)以及微调柱温(33、35、37 ℃),流速(0.75、0.8、0.9 ml/min),检测波长(236、238、240 nm),流动相初始比例(流动相 A:B 分别为63:37、65:35、67:33)等条件,对系统分离情况和杂质检测结果的影响。
1.2.12 样品有关物质检测 采用上述经过验证的有关物质检查方法,对卤米松乳膏 3 批自制品和 2 批原研品进行检测。
2 结果
2.1 专属性
由专属性试验结果(图2 和表3)可知:溶剂和空白辅料对测定无干扰;主峰与相邻杂质峰之间,以及各已知杂质峰与相邻峰之间均能很好分离;灵敏度溶液中,主成分峰高信噪比 > 10;自制品中检出杂质 C、杂质 F 和杂质 J;原研品中检出杂质 C、杂质 F 和杂质 G;自制品中加入混合杂质对照品后,相应杂质位置检出杂质峰。结果表明,自制品与原研品杂质谱基本一致,本方法专属性良好。
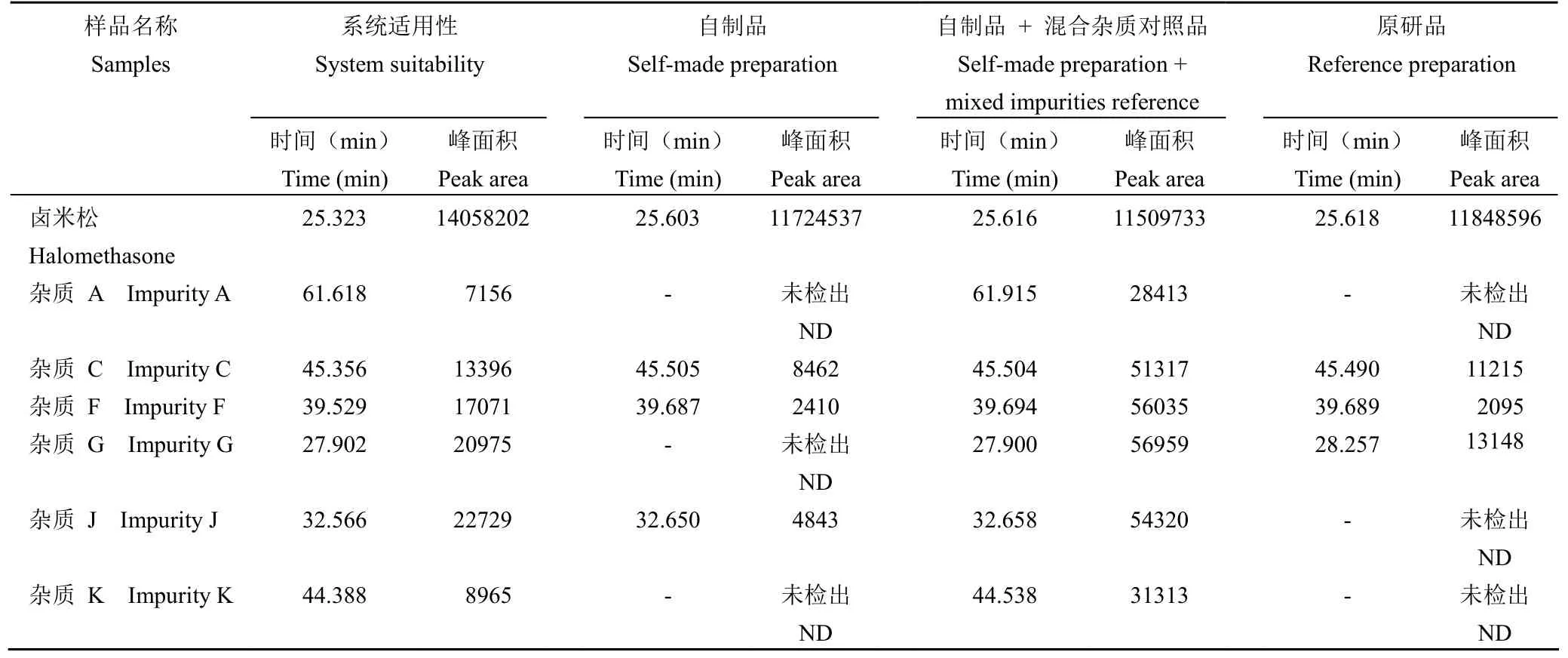
表3 卤米松乳膏有关物质检查专属性试验结果Table 3 Results of specificity test of halomethasone ointment

图2 卤米松乳膏有关物质检查专属性试验色谱图(A:溶剂 1;B:空白辅料溶液;C:系统适用性溶液;D:灵敏度溶液;E:自制品溶液;F:自制品+混合杂质对照品溶液;G:原研品溶液)Figure 2 Chromatograms of specificity test of halomethasone ointment (A: Solvent 1; B: Blank excipient solution; C: System suitability solution; D: Sensitivity solution; E: Self-made preparation solution; F: Self-made preparation + mixed impurities reference solution; G: Reference preparation solution)
2.2 干扰性
由干扰性测定结果(代表性图谱见图3)可知,空白辅料在各条件下破坏后,对测定无干扰。各破坏条件下的自制品和原研品经二极管阵列(PDA)检测器测定主峰纯度,均为单一峰。自制品和原研品对强酸破坏基本稳定,对强碱破坏极不稳定,在其他破坏条件下不稳定。具体如下:
高温破坏条件下,自制品杂质 G、J、F、C、其他单个最大杂质和总杂质均有所增加;原研品杂质 G、F、C 及总杂质有所增加。光照破坏条件下,自制品和原研品的杂质 G、F 及总杂质均稍有增加。紫外光照条件下,自制品杂质 A 和总杂质有所增加;原研品杂质 F、A 和总杂质有所增加。强酸破坏条件下,自制品仅总杂质稍有增加;原研品仅杂质 G 和总杂质稍有增加。强碱破坏条件下,自制品和原研品杂质 G、J、F 均稍有增加,均出现新的未知杂质峰(自制品在 RRT 0.54 和 RRT 0.56 处,原研品在 RRT 0.55 和 RRT 0.57 处),总杂质均明显增加。氧化破坏条件下,自制品杂质J 稍有增加,原研品总杂质稍有增加。
破坏前后物料平衡率计算结果表明,各破坏条件下,破坏前后物料守恒(物料平衡率在 93.9% ~103.4% 之间)。可见,本方法干扰性符合相关规定。
由于空白辅料在各破坏条件下对测定无干扰,原研品与自制品在各破坏条件下结果类似,因此图3中仅列出自制品未破坏和各破坏条件下色谱图。
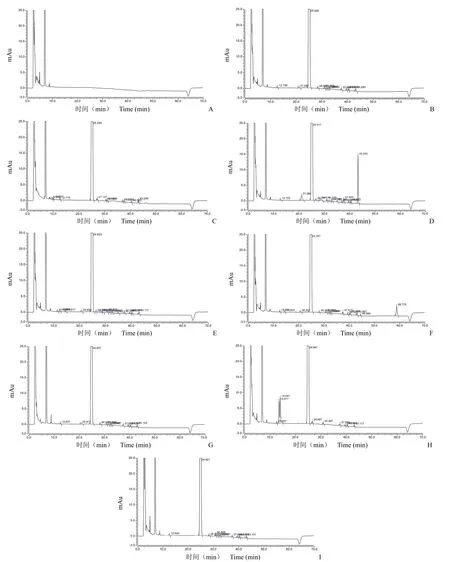
图3 卤米松乳膏有关物质检查干扰性试验色谱图(A:空白辅料溶液;B:自制品溶液;C:原研品溶液;D:高温破坏;E:光照破坏;F:紫外光照破坏;G:强酸破坏;H:强碱破坏;I:氧化破坏)Figure 3 Chromatograms of interference test of halomethasone ointment (A: Blank excipient solution; B: Self-made preparation solution; C: Reference preparation solution; D: High temperature damaged; E: Light damaged; F: Ultraviolet light damaged; G:Strong acid damaged; H: Strong alkali damaged; I: Strong oxidants damaged)
2.3 线性与范围
线性与范围测定结果见表4。主成分卤米松有两个线性方程,其中方程 1 对应有关物质检测时供试品浓度的线性,方程 2 对应限度浓度范围的线性。
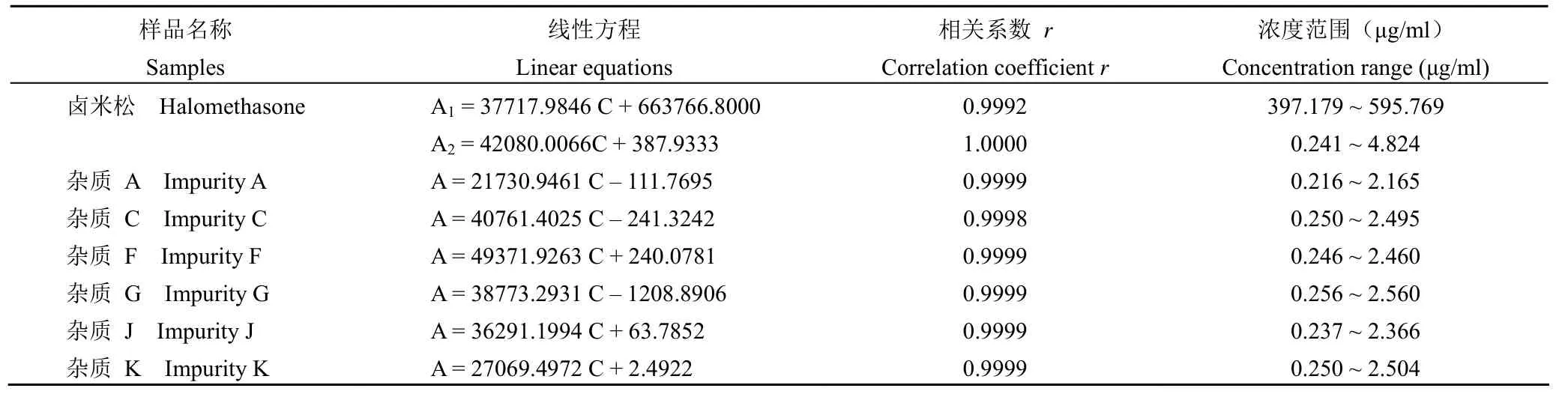
表4 卤米松及各有关物质线性方程Table 4 Linear equation of halomethasone and various related substances by HPLC
结果表明,主成分卤米松与各已知杂质(杂质A、C、F、G、J、K)在上述浓度范围内,浓度与峰面积线性相关系数r均 ≥ 0.9992,各杂质和主峰的截距/限度浓度峰面积均 < 10%,各峰响应因子RSD 均 < 10%。因此各杂质浓度与峰面积线性关系均良好。
2.4 定量限与检测限
由表5 可见,0.0032% 的杂质 A、0.0013% 的杂质 C、0.0009% 的杂质 F、0.0019% 的杂质 G、0.0017% 的杂质 J、0.0018% 的杂质 K 均能被有效检出;卤米松的检测限相当于供试品溶液主成分浓度的 0.003%,表明 0.003% 的未知杂质能被有效检出。可见卤米松及各杂质检测限完全满足卤米松乳膏有关物质检查标准限度的要求。
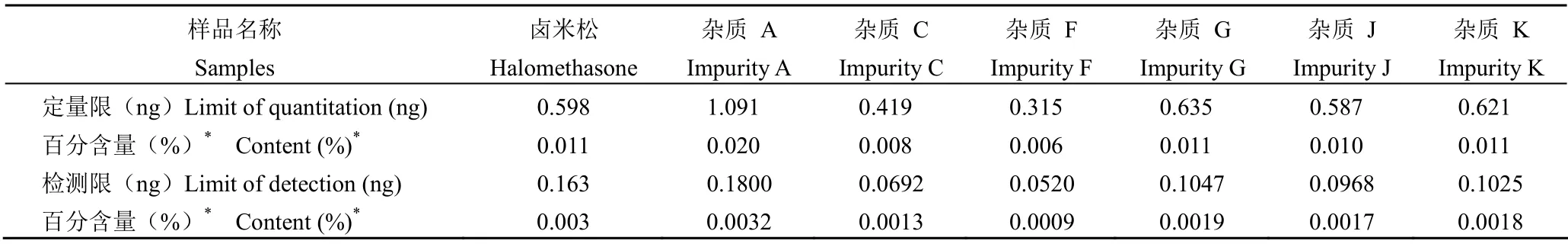
表5 卤米松及各有关物质定量限和检测限Table 5 Limit of quantitation and detection of halomethasone and various related substances by HPLC
2.5 精密度
2.5.1 重复性 卤米松乳膏有关物质重复性结果表明:6 份自制品中均未检出杂质 G 和杂质 K,均在 RRT 约 1.64 处检出最大单杂,检出的已知杂质 A、C、F、J、最大单杂及总杂含量的 RSD 分别为 4.48%、3.19%、2.20%、1.59%、6.90%、2.42%,均小于 10%。可见本方法重复性良好。
2.5.2 中间精密度 卤米松乳膏有关物质中间精密度结果表明:12 份自制品中均未检出杂质 G 和K,均在 RRT 约 1.64 处检出最大单杂;检出的已知杂质 C、F、J、最大单杂及其总杂含量的 RSD 分别为 2.61%、3.71%、3.36%、5.29%、3.04%,均小于 10.0%;杂质 A 含量 RSD 为 17.23%,极差小于限度的 20%(限度为 0.5%)。表明本方法中间精密度良好。
2.6 准确度
准确度结果(表6)表明:在 50%、100% 和150% 限度浓度下,制剂中各杂质回收率均在 92% ~105% 之间;各浓度下各杂质回收率 RSD 均小于5.0%。可见本方法各杂质回收率较高,准确度良好。
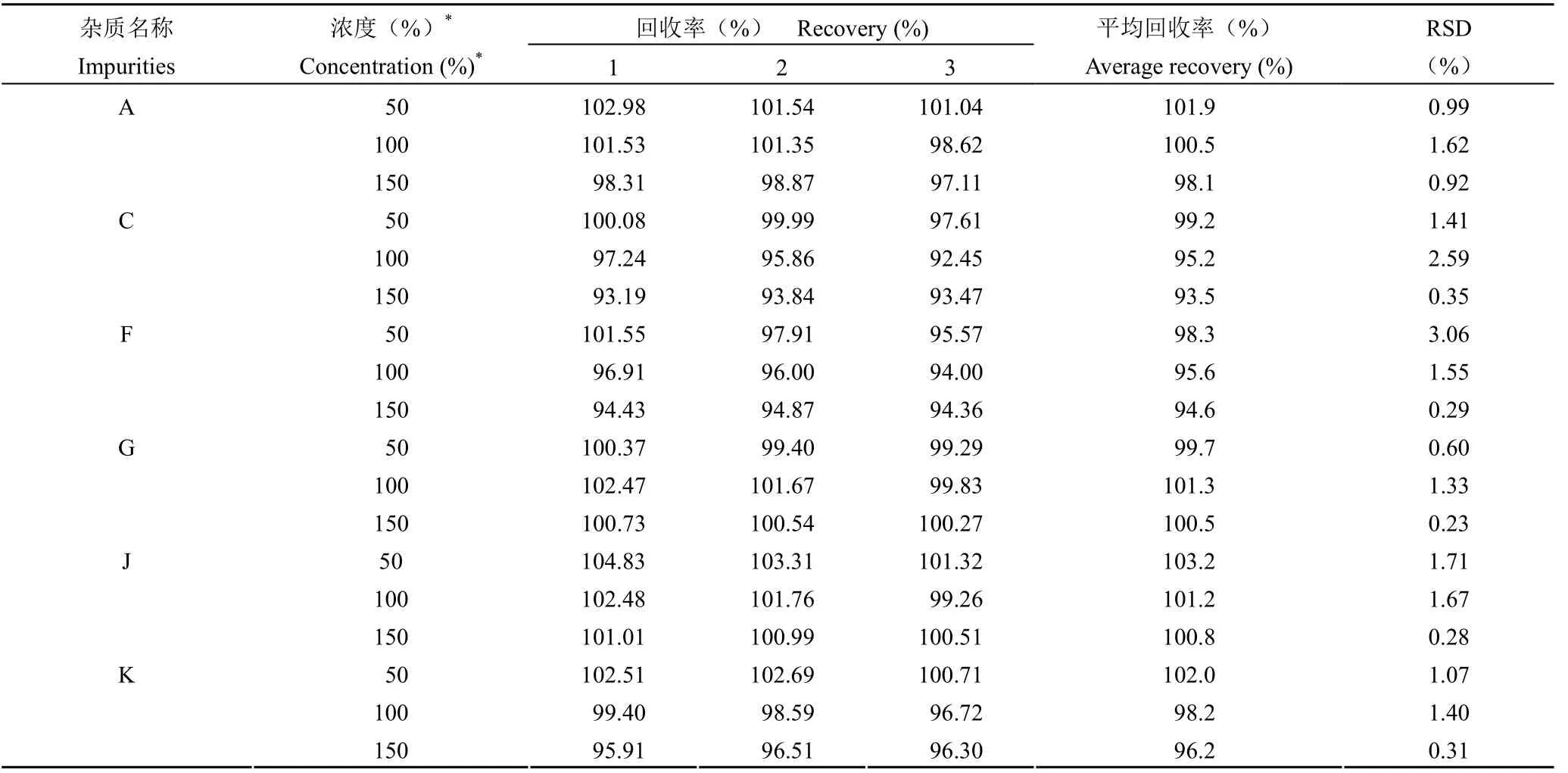
表6 卤米松乳膏有关物质检查准确度结果Table 6 Accuracy of various related substances in halomethasone ointment by HPLC
2.7 溶液稳定性
溶液稳定性结果表明,室温条件下放置 48 h,各时间点自制品溶液中各杂质均无明显变化,均未检出杂质 G 和杂质 K,杂质 A、C、F、J、最大单杂和总杂含量的 RSD 分别为 8.21%、1.47%、2.27%、0.82%、8.39%、2.95%,均小于 10%,说明室温条件下放置溶液稳定性良好。
2.8 耐用性
2.8.1 校正因子耐用性试验结果 更换色谱柱以及微调柱温、流速、检测波长、流动相初始比例的条件下,各已知杂质和主成分卤米松的浓度与峰面积线性关系均良好;不同条件下各杂质校正因子的RSD 均小于 10.0%。结果表明本方法校正因子耐用性良好。
2.8.2 方法耐用性试验结果 更换色谱柱以及微调柱温、流速、检测波长、流动相初始比例的条件下,系统适用性溶液中各峰间分离度均大于 1.5,系统适用性试验耐用性良好;供试品中均未检出杂质 G 和杂质 K,检出的已知杂质 A、C、F、J 和最大单杂及总杂含量 RSD 均小于 10%;在微调柱温和流动相比例后,杂质的相对保留时间稍有变化,因此,在质量标准中采用杂质对照品配制系统适用性溶液进行杂质的定位。结果表明本方法耐用性良好。
2.9 样品有关物质检测
对卤米松乳膏 3 批自制品和 2 批原研品进行有关物质检测,结果见表7。
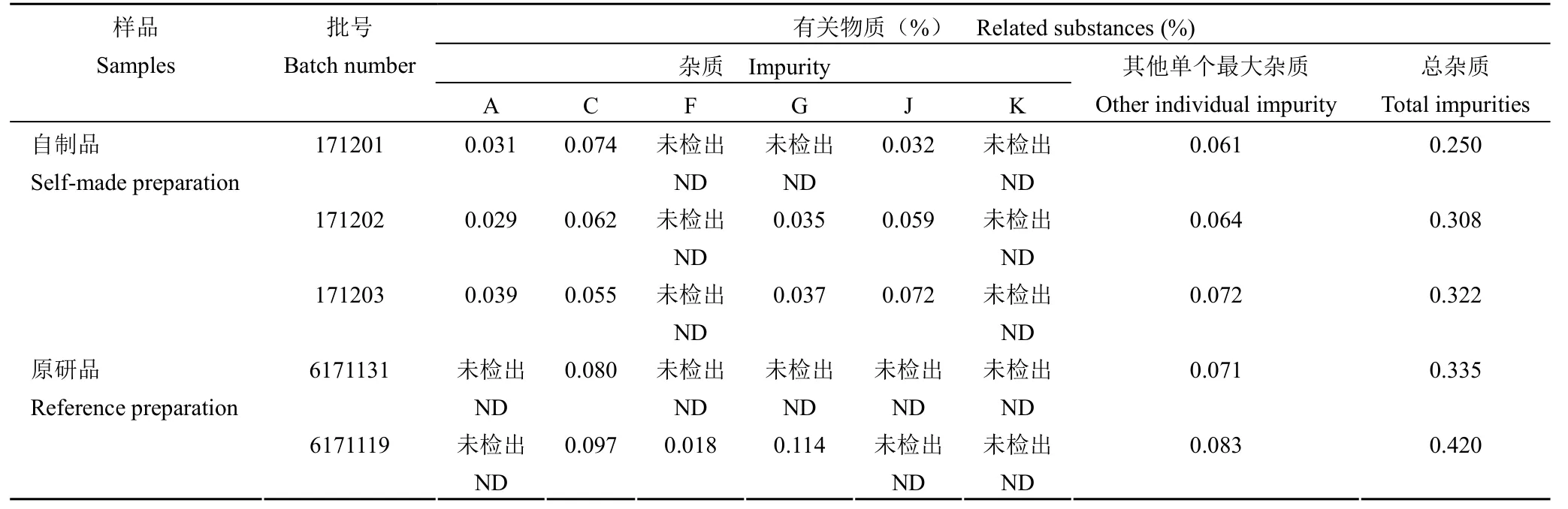
表7 卤米松乳膏有关物质检查结果Table 7 Result of the related substances in halomethasone ointment
由上述结果可知,卤米松乳膏自制品和原研品杂质谱基本一致,各批次自制品和原研品中各已知杂质、其他最大单个杂质和总杂质含量均在规定限度内,说明各批次样品有关物质均符合所订质量标准的规定。
3 讨论
本文参考了卤米松乳膏国家药品标准有关物质项下对单个杂质及总杂质的限度规定,并结合自制卤米松乳膏所用原料药的合成路线、结构特点以及制剂处方工艺条件和降解路径,对卤米松乳膏的杂质谱进行了全面系统的研究。在此基础上,进一步完善了卤米松乳膏有关物质检测条件,建立了本文所述的有关物质检查方法。
国家药品标准中卤米松乳膏有关物质项下,并未规定已知杂质采用自身对照法计算杂质含量;而本研究中对多个已知杂质进行了规定,且采用加校正因子的自身对照法计算各已知杂质含量,使杂质定量更为准确。
本研究中干扰性试验显示卤米松乳膏自制品和原研品在强碱、高温、光照及氧化条件下均不稳定,可降解出杂质 A、C、F、G、J,因此将这几种已知杂质纳入卤米松乳膏有关物质标准中。杂质K 为卤米松原料药的工艺杂质,在卤米松乳膏干扰性试验和影响因素试验中并未降解产生,因此,虽在方法学验证中对其进行研究,但未将其纳入制剂质量标准中。此外,卤米松原料药的工艺杂质还包括杂质 D(中间体 2)、杂质 B(中间体 2 的工艺副产物)、杂质 E(中间体 3)、杂质 H(氟米松)、杂质 I(中间体 1),这些杂质在卤米松乳膏干扰性和影响因素试验中均不会降解产生,且在原料药质量标准中已进行规定,因此卤米松乳膏有关物质方法中不再进行相关研究,仅在方法学验证过程中的系统适用性溶液中加入,以确保制剂中如果引入这些工艺杂质,在所建立的色谱条件下能够有效分离并检出。
综上所述,本文建立了卤米松乳膏有关物质检查的 HPLC 法,并进行了全面系统的方法学验证。结果表明,该法专属性良好,干扰性符合相关规定,各已知杂质浓度-峰面积之间的线性关系良好,方法精密度、准确度和耐用性均良好,可用于简便、快速、准确地检测卤米松乳膏中的有关物质。
采用该法对卤米松乳膏 3 批自制品和 2 批原研品进行了有关物质检查,结果表明,自制品和原研品杂质谱基本一致,自制品中各已知杂质、单个未知杂质和总杂质均低于质量标准规定的限度。

