超声引导下射频消融术与开放性手术治疗甲状腺良性大结节的疗效比较
汪 涛 李志民
(1 厦门大学附属第一医院杏林分院普外科,福建省厦门市 361022;2 厦门大学附属第一医院肝胆胰血管外科,福建省厦门市 361000)
全球范围内甲状腺结节的发病率呈逐年上升趋势,其超声检出率高达65%[1]。目前对甲状腺结节的处理方式有开放性手术、腔镜切除术及热消融术。对于甲状腺良性大结节(最大径≥3 cm),常采用甲状腺腺叶全切除术及甲状腺次全切除术治疗,但术后患者甲状腺功能减退的发生率高,颈前瘢痕残留且严重影响美观。腔镜手术虽可达到良好的美容效果,但皮下创伤大,而且对甲状腺大结节的处理要求术者有娴熟的腔镜操作经验。研究显示,热消融术对甲状腺结节尤其是中小结节具有良好的治疗效果及操作安全性[2-3],但对甲状腺大结节进行热消融治疗可能面临更多的出血、疼痛、神经损伤等并发症,治疗效果亦缺乏长期的临床观察。此外,美国甲状腺协会于2015年推出的《成人甲状腺结节与分化型甲状腺癌诊治指南》[4]明确提出,不建议将射频消融术(radiofrequency ablation,RFA)作为常规使用的非手术方法治疗甲状腺良性结节。但鉴于热消融术对甲状腺中小结节具有良好的治疗效果,本研究回顾性分析采用超声引导下RFA及传统开放性手术治疗甲状腺良性大结节的手术情况、操作安全性、术后24个月结节变化及结节复发情况,探讨RFA在甲状腺良性大结节中的临床应用价值。现报告如下。
1 资料与方法
1.1 一般资料 选取2016年3月至2020年1月在厦门大学附属第一医院杏林分院经超声检查诊断为甲状腺良性大结节(最大径≥3 cm)的148例患者作为研究对象。根据治疗方式将其分为观察组(采用超声引导下RFA治疗)76例、对照组(采用传统开放性手术治疗)72例。纳入标准:(1)符合美国甲状腺协会2015年《成人甲状腺结节与分化型甲状腺癌诊治指南》[4]中甲状腺结节的诊断标准;(2)甲状腺结节最大径≥3 cm;(3)超声和细针穿刺细胞学检查显示为良性甲状腺结节;(4)有颈部异物感、疼痛、压迫感等主观症状。排除标准:(1)病理检查提示恶性病变;(2)合并重要器官的器质性病变;(3)出凝血功能障碍;(4)甲状腺功能异常;(5)对侧声带功能障碍。两组患者均充分了解治疗方式并自主选择治疗方案。观察组男21例、女55例,年龄22~70 (42.8±10.6)岁,结节最大径3.3~5.9(3.9±0.7)cm;对照组男20例、女52例,年龄 25~68(43.2±10.3)岁,结节最大径3.2~5.6(3.8±0.6)cm。两组患者的年龄、性别、结节最大径差异均无统计学意义(均P>0.05),具有可比性。
1.2 仪器设备 GE Logic7彩色超声诊断仪(购自美国通用电气公司);7.5~12 MHz高频探头;韩国STARmed公司射频治疗仪(型号:VRS01);18-07S-10F型单针单极式射频消融针,规格为18 G,针长度为7 cm,射频针消融裸区长度为1.0 cm。
1.3 手术方法
1.3.1 术前准备 常规进行甲状腺彩超、血常规、生化、凝血功能、甲状腺功能、心电图、颈部CT等检查以评估全身情况。所有患者术前均签署知情同意书,观察组患者术前禁食4 h,对照组按全麻进行术前准备。
1.3.2 观察组 患者取仰卧位,头后仰,肩部垫枕,充分暴露颈部。常规消毒,将2%利多卡因和生理盐水以1 ∶2混合,对穿刺部位的皮肤、皮下和甲状腺周围进行局部麻醉。根据结节所在部位,从颈外侧或峡部进针,将射频电极插至病灶,以“移动消融”[5]的方式从肿物边缘向深部连续移动射频针,初始功率为30 W,以5 W/min的速率增加功率,最高功率为55 W,分多层面及多点消融,待高回声区完全覆盖结节边缘时结束消融。操作中采用液体隔离带法、杠杆撬离法规避可能出现的损伤风险,即避免对邻近喉返神经、气管、颈总动脉等重要组织造成损伤。难以一次完全消融的大体积结节,术后1~3个月复查甲状腺彩超,待结节缩小后进行二次消融。术后禁食4 h,常规颈部冰敷,监测生命体征,应用止血药物。
1.3.3 对照组 患者取仰卧位,行全身麻醉。自胸骨颈静脉切迹上缘做一5~6 cm弧形切口,依次切开皮下组织、颈阔肌,游离皮瓣,充分暴露甲状腺,根据甲状腺结节的位置、大小、数目,采用甲状腺腺叶次全切除术或甲状腺全切除术治疗。采用超声刀或高频电刀分离甲状腺周围组织,暴露甲状腺背侧与气管食管沟,分离、结扎甲状腺上下动脉及上中下静脉,注意保护喉返神经与甲状旁腺,将结节及一侧腺叶完整切除,或保留甲状腺背侧腺体组织及包膜,术后常规负压引流。
1.4 观察指标 (1)手术情况:比较两组患者的术中出血量、手术时间、住院时间、术后2周的疼痛评分。其中术后疼痛评分采用视觉模拟评分法(visual analogue scale, VAS)评估,即将疼痛划分为10个等级,0分为无痛,10分为最严重的疼痛,患者根据数字对应的疼痛等级自行评分,评分越高提示疼痛越剧烈。(2)术前、术后3个月甲状腺激素水平:包括血清游离三碘甲状腺原氨酸(FT3)、血清游离四碘甲状腺原氨酸(FT4)、促甲状腺激素(thyroid-stimulating hormone, TSH)。(3)术后3个月内的并发症发生情况:包括出血或血肿、甲状腺功能减退、恶心呕吐、感染,以及声音嘶哑、呛咳等喉返神经损伤表现等。(4)手术满意度:术后3个月采用自制的调查表对患者的手术满意度进行调查,内容包括手术切口情况(瘢痕、疼痛、肿胀)、主观症状改善情况(异物感、咽部不适、压迫感等)、生命活动状况(包括饮食、睡眠、体力活动等)、焦虑抑郁等精神状态。得分≥90分为满意,80~89 分为基本满意,<80分为不满意。手术满意率=(满意+基本满意)例数/总例数×100%。(5)记录观察组术后1、6、12、24个月结节体积及术后24个月结节复发情况,计算结节体积缩小率(volumereduction ratio,VRR),VRR=[(消融前体积-随访时体积)/消融前体积]×100%。
1.5 统计学方法 采用SPSS 22.0统计学软件进行数据分析。计量资料以均数±标准差(x±s)表示,组间比较采用独立样本t检验,组内治疗前后比较采用配对t检验;计数资料以例数(n)和百分比(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 手术情况比较 观察组患者的手术时间、住院时间均短于对照组,术中出血量少于对照组,术后2周的VAS评分低于对照组,差异均有统计学意义(均P<0.05)。见表 1。

表1 两组患者的手术情况比较 (x±s)
2.2 血清甲状腺激素水平比较 术前,两组患者的血清FT3、FT4、TSH水平差异均无统计学意义(均P>0.05);观察组患者术后3个月的血清FT3、FT4、TSH水平与术前差异均无统计学意义(均P>0.05),对照组术后3个月的血清FT3、FT4水平均较术前及观察组低、血清TSH水平均较术前及观察组升高,差异均有统计学意义(均P<0.05)。见表2。
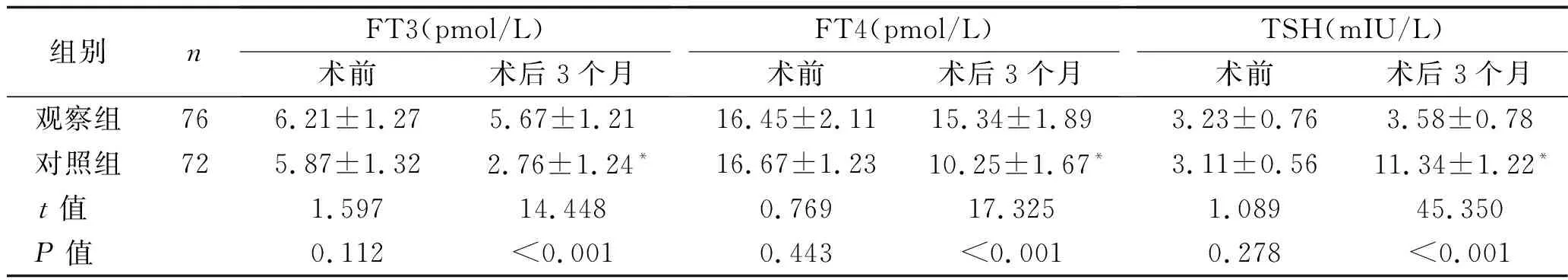
表2 两组患者术前、术后3个月的血清甲状腺激素水平比较 (x±s)
2.3 术后并发症发生情况 观察组术后发生不良反应5例,并发症总发生率为6.58%。其中声音嘶哑1例,于术后2个月内自行恢复;穿刺部位出血/血肿2例,予局部压迫、冰敷1周后消散;恶心呕吐2例,术后自行缓解。对照组发生不良反应18例,并发症总发生率为25%。其中术后甲状腺功能减退7例,予左甲状腺素钠片治疗后,定期复查,血清FT3、FT4、TSH水平均正常;声音嘶哑2例,3个月内自行恢复;出血/血肿3例、恶心呕吐4 例、感染1例、呛咳1例,予止血药、伤口换药、对症处理后均于1个月内恢复。观察组患者的术后并发症总发生率低于对照组,差异有统计学意义(P<0.05)。见表3。
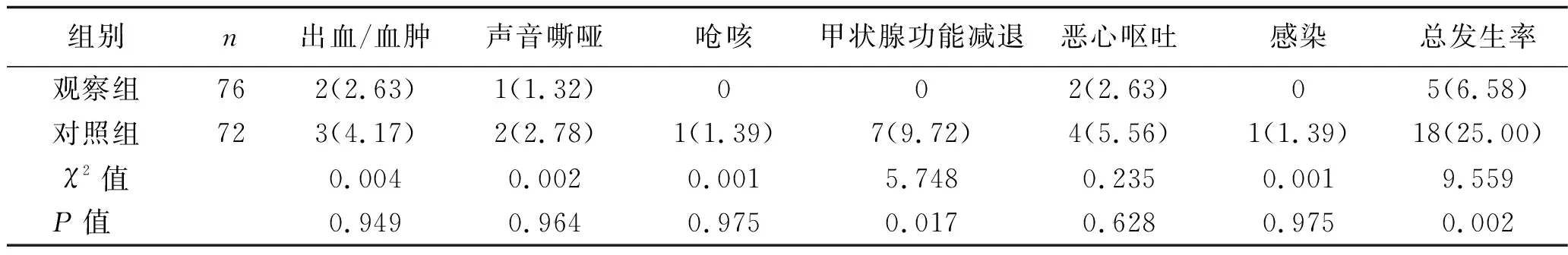
表3 两组患者术后3个月内的并发症发生情况比较 [n (%)]
2.4 手术满意度比较 观察组患者对手术满意35例、基本满意38例,手术满意率为96.05%(73/76);对照组患者对手术满意30例、基本满意31例,手术满意率为84.72%(61/72)。观察组患者的手术满意率高于对照组,差异有统计学意义(χ2=5.542,P=0.019)。
2.5 观察组结节体积的变化情况 观察组患者术后1、6、12、24个月,结节的最大径逐渐缩短、体积逐渐缩小,结节消失数逐渐增多、VRR逐渐增大,其中术后24个月的VRR高达 (90.51±2.93)%。见表4。
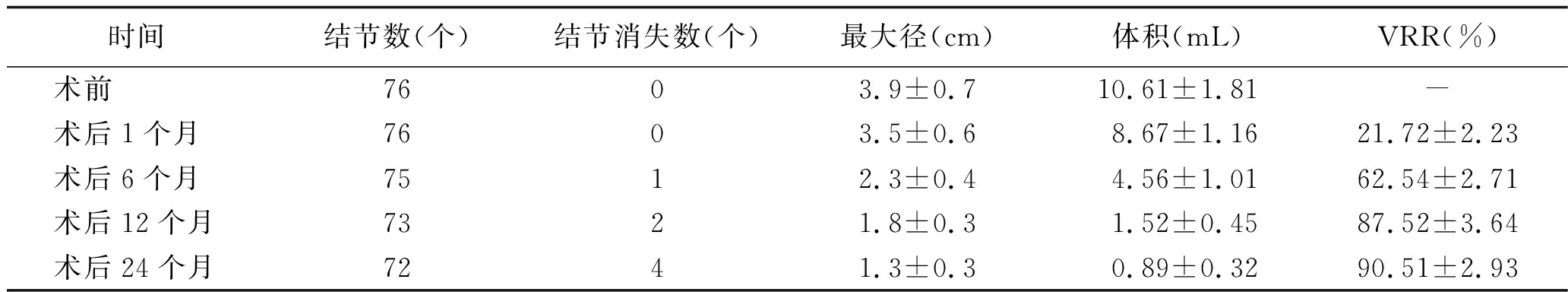
表4 观察组患者手术前后结节体积的变化 (x±s)
2.6 结节复发情况 术后随访24个月,观察组复发3例(3.9%),对照组复发2例(2.8%),两组患者的甲状腺结节复发率差异无统计学意义(χ2=0.004,P=0.951)。与患者充分沟通后由其自主选择手术方式,两组复发患者均成功行超声引导下RFA治疗。
3 讨 论
RFA是一种利用热量使肿瘤组织发生凝固性坏死,从而达到缩小肿瘤体积和改善临床症状的治疗方法,具有恢复快、可重复、美观且甲状腺功能损伤小等优点。2006年RFA首次被应用于甲状腺良性结节的治疗中,在随后10余年的临床实践中,RFA治疗引起了广泛的关注和讨论,其治疗甲状腺良性结节的安全性、有效性逐步得到证实及认可[6],RFA的适应证也从甲状腺良性结节向低风险恶性肿瘤、良恶性肿瘤复发病灶拓展[7-8]。2018年推出的《甲状腺良性结节、微小癌及颈部转移性淋巴结热消融治疗专家共识》[9]使甲状腺结节热消融的适应证及操作流程更加规范。
相关文献报道,热消融治疗对甲状腺中小良性结节的效果较好,采用热消融治疗甲状腺中小良性结节后VRR为93.4%,复发率仅为5%[10]。甲状腺良性大结节目前多采用手术治疗,手术治疗的优势是可以直观、彻底地清除病灶,但其带来的手术创伤、术后瘢痕及高龄患者伴随的基础疾病仍让不少患者心存顾虑而拒绝手术。RFA治疗具有微创、美观的特点,易被患者接受,但甲状腺大结节在消融过程中也面临很多的风险及并发症,加之目前尚缺乏远期效果观察,限制了其在临床上的应用。笔者所在科室对甲状腺大结节进行RFA治疗时主要采用以下方法规避风险:(1)水隔离带法,即在甲状腺和周边器官的潜在间隙注入生理盐水,可分离甲状腺与颈前肌群,并推开大血管、食管、神经,从而阻止射频治疗过程中的热传导;(2)杠杆撬离法,即在射频消融时通过上抬或下压针尖使结节远离周围重要结构,加大安全距离;(3)囊性或囊实性肿物可先抽吸部分囊液使其体积缩小后再进行消融。大肿物消融时间长,部分患者无法耐受,且消融后炎症反应及穿刺部位血肿可能会对周围组织产生压迫,甚至有窒息风险,可在首次消融后,待结节体积缩小再进行二次或多次消融。本研究中观察组有3枚结节的最大径≥5.2 cm,均进行二次消融治疗。在临床操作中可采取个体化治疗方案,联合使用以上3种方法或具有更高的安全性。
本研究结果显示,观察组患者的手术时间及住院时间均短于对照组,术中出血量少于对照组,术后疼痛评分和并发症总发生率均低于对照组(均P<0.05),这提示,相较于传统开放性手术,超声引导下RFA对机体的损伤更小,恢复更快,具有微创的优点。其原因可能为:(1)RFA一般在局麻下操作,根据患者的情况在手术前后应用镇痛、镇静药物,因而患者均可较好地耐受手术操作,无明显不适;(2)RFA的热凝固可以对穿刺针道及病灶进行有效止血,术后亦无须放置引流管,对机体的影响更小;(3)射频操作全程在彩超引导下进行,可精准对靶病灶进行消融,避免了血管、气管等周围脏器损伤;(4)操作时与患者进行实时交流,利于患者及时反馈疼痛、恶心等不适,且术者可以观察其声音有无改变,以调整治疗方案。本研究中,观察组患者的手术满意度高于对照组(P<0.05),这可能是因为RFA术后患者疼痛轻微,术后24 h即可出院,其精神状况、睡眠、活动等方面均较对照组改善,因而RFA治疗更符合快速康复的理念[11]。
本研究对患者术后的甲状腺功能进行监测,结果显示观察组患者手术前后的血清FT3、FT4、TSH 水平均无统计学意义(均P>0.05),对照组术后血清 FT3、FT4 水平均较术前低、血清TSH 水平较术前高,这提示RFA对甲状腺功能的影响较小。而对照组甲状腺功能减退发生率高于观察组(P<0.05),这可能是因为甲状腺大结节采取患侧甲状腺腺叶全切除术或次全切除术治疗,对于合并双侧多发结节的患者,甚至需行甲状腺全切除术治疗,从而导致术后患者的甲状腺功能减退发生率高。而RFA只对病灶进行消融,可最大限度地保留正常甲状腺组织,从而保留甲状腺功能,避免患者需长期服用甲状腺激素药物,因而甲状腺功能减退的发生率相对较低。研究显示,影响RFA术后甲状腺结节体积缩小的主要因素有结节的大小、位置、性质及血流灌注情况,甲状腺结节的初始体积越大,其坏死物质被免疫系统吞噬的速度越慢,体积缩小的速度也越慢[12-15]。本研究中,术后1、6、12、24个月,观察组结节最大径逐渐缩短、体积逐渐缩小,结节消失数逐渐增多、VRR逐渐增大,其中术后24个月的VRR高达(90.51±2.93)%,但低于相关研究[10]报道的结节VRR(93.4%),考虑与本研究纳入的均为大体积结节,术后坏死物质吸收较缓慢有关。本研究结果还显示,5.2%(4/76)的结节在术后24个月内完全消失,主要为囊性、囊实性结节,提示囊性成分的结节具有更好的VRR,与国外文献[13]报道的结果相似。本研究中,观察组术后甲状腺结节复发率为3.9%,复发率较低,且与对照组差异无统计学意义(P>0.05),显示出RFA对甲状腺良性大结节具有较好的临床治疗效果。
在RFA治疗甲状腺良性大结节的过程中,需要把握以下几点:首先,术前详细了解肿物的位置及其与重要结构的关系,设计合理的穿刺路线,采用移动消融法、水隔离带法、杠杆撬离等方法,以避免对周围组织结构造成损伤,对大结节不宜追求一次性完全消融。巨大胸骨后甲状腺肿或大部分甲状腺结节位于胸骨后方应列为RFA禁忌,但对无法耐受手术及麻醉者,也可考虑分次消融[16]。其次,患者充分知情并具有微创治疗意愿,术前与其进行良好的沟通,告知其RFA的原理及术后结节变化过程,以及可能会出现症状改善不明显、结节复发、中转开放性手术等,且术后需定期复查随访,以取得患者更好的配合。
综上所述,采用超声引导下RFA治疗甲状腺良性大结节微创、安全、有效,其治疗效果与开放性手术相当,但对甲状腺功能的影响更小,具有较好的临床推广价值,可为甲状腺良性大结节患者提供除手术外的另一种可选择的治疗方案。

