经皮冠状动脉介入治疗术后替格瑞洛及其代谢物浓度测定LC-MS方法的建立和应用
秦 军,王 楠,相 芳,初晓玲,李 祥,陈 群,初晓倩
0 引 言
随着社会生活条件的日益提高,急性冠状动脉综合征(acute coronary syndrome,ACS)也逐渐呈年轻化的趋势,其中高血压、糖尿病、血脂异常以及炎症等均是导致ACS发病的危险因素[1]。当动脉粥样硬化不稳定斑块破裂或侵蚀导致的冠状动脉内急性血栓形成,成为多数ACS发病的基础[2],血小板激活在其中起着重要作用[3]。有效的抗血小板治疗成为预防ACS血栓事件的重要手段。近年来,P2Y12受体抑制剂联合小剂量阿司匹林(75~150 mg)被认为是ACS患者经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)时的标准治疗方法[4]。氯吡格雷受基因多态性影响,常产生氯吡格雷抵抗,继而引起心血管不良事件风险增加[5]。替格瑞洛作为一种可逆的、直接作用的P2Y12受体抑制剂,用于降低ACS患者的血栓事件(心肌梗死、中风)风险,具有比氯吡格雷更快、更强、更一致的特点,而不增加总体大出血率[6-7]。PLATO研究后,国内外指南推荐替格瑞洛作为急性冠状动脉综合征(ACS)患者首选的P2Y12血小板抑制剂。
临床观察发现,目前中国ACS患者PCI术后替格瑞洛的常规给药剂量可能偏高,存在一定的用药风险,但尚缺乏相应的循证医学证据。有研究表明,替格瑞洛血药浓度与出血事件成正相关[8]。ACS患者往往存在高龄、女性、肾功能不全、贫血、低BMI、合用口服抗凝剂等出血风险因素[9],用药风险进一步加大,临床需要关注替格瑞洛的用药安全性,目前国内有关ACS患者替格瑞洛血药浓度及其与人群特征关系的研究较少。因此,本研究旨在建立ACS患者PCI术后定量测定替格瑞洛血浆浓度的LC-MS/MS方法并观察其特征分布,为临床建立可靠的监测方法,为替格瑞洛的安全、有效应用打下基础。
1 资料与方法
1.1 研究对象本研究为随机单中心研究,研究对象为2020年9月至2022年1月东部战区总医院秦淮医疗区确诊为ACS以及需要植入药物洗脱支架的患者120例。所有受试者在参与前均提供书面知情同意书,并得到医院伦理委员会批准(批准号:81YY-KYLL-19-13),且研究是根据临床实践协调准则国际会议和赫尔辛基宣言进行的。入组标准:①确诊为ACS以及使用替格瑞洛的患者;②规律使用替格瑞洛的患者。排除标准:①对阿司匹林、替格瑞洛等药物不耐受的患者;②急性心衰或心源性休克、心律失常的患者;③活动性消化道溃疡、严重感染、恶性肿瘤的患者;④血液系统疾病、出血性疾病或有出血倾向的患者;⑤在研究过程中服药依从性差,包括酒精滥用、精神疾病、药物依赖的患者;⑥孕妇或者哺乳期妇女;⑦因合并其他疾病,预期生存期不超过 1 年的患者.
1.2 方法学的建立和浓度测定
1.2.1 血样的采集符合入组要求的患者,入院后口服治疗剂量替格瑞洛药(90 mg,1天2次),达到稳态后(约3~5个半衰期,约30~50 h),于下次服药前1 h左右采集静脉血,2 h内分离血浆并转移至EP管内,-80 ℃保存,并由本单位完成浓度测定及数据采集。
1.2.2 替格瑞洛及其他心血管药物LC-MS/MS方法学的建立①试剂(规格,厂家,批号):空白血清(NA,东部战区总医院秦淮医疗区,NA),甲醇(MS级,Fisher,201603),乙腈(HPLC级,Fisher,196024),甲酸(MS级,Fisher,193068),纯水(MS级,Honeywell,DY616)。②标准品名称(纯度,来源,批号):替格瑞洛(97%,TRC,2-AGE-110-1);替格瑞洛-d7(96%,TRC,4-AKT-180-5);去羟乙氧基替格瑞洛(98%,TRC,27-MJC-49-1);去羟乙氧基替格瑞洛-d7(99.75%,TRC,3-MSI-60-2);药品信息:替格瑞洛片90 mg/片(商品名:倍林达,厂家:阿斯利康制药有限公司,批号:2005047、2007087、200834及2009063)。③仪器(型号,厂家):液相色谱-三重四极杆串联质谱仪(ACQUITY HPLC-MS-Class,Waters corporation),高速冷冻离心机(Heraeus FRESC021,日立(日本)),纯水仪(Unique-R10,锐思捷(厦门)纯化技术公司),涡旋混合仪(G560E,美国Scientific Industries),移液器(2-20、10-100、20-200、100-1000 μL,Thermo),电子天平(XSR205(十万分之一),METTLER TOLEDO),超声波清洗机(SB-3200DTD,宁波新芝生物科技公司),医用保存箱(2~8 ℃)(MPR-312DCN-PC,Panasonic Appliances Cold(大连)),低温保存箱(-20 ℃)(DW-YL270,美菱生物医药(安徽)),超低温保存箱(-70 ℃)(MDF-U54V,Panasonic Healthcare(上海)),量筒(100、500 mL,博美、金正)。④色谱条件:流动相A:0.1% 甲酸水溶液;流动相B:乙腈;流速:0.4 mL/min;柱温:40 ℃;色谱柱:Kinetex 2.6 μm XB C18,50mm×3 mm。⑤质谱条件:质谱离子源参数,Capillary(V):3000(ESI+)4000(ESI-);Nozzle Voltage(V):200(ESI+)500(ESI-);Gas Temp(℃):300;Gas Flow(L/min):7;Nebulizer(psi):45;Sheath Gas Temp(℃):300;Sheath Gas Flow(L/min):11。⑥检测对象:替格瑞洛(Ticagrelor,TIC)、去羟乙氧基替格瑞洛(Deshydroxyethoxy Ticagrelor,DHTIC)。⑦标准溶液的配制。标准溶液的配制:精密称取各药物标准品适量,精密称取纯度分别为97%及98%的替格瑞洛和活性代谢物,加入1.808和0.979 mL的溶剂,涡旋均匀得到浓度分别为2 mg/mL和1 mg/mL的化合物储备液。分别准确移取母液浓度2000 μg/mL的替格瑞洛及浓度1000 μg/mL的其活性代谢物10 μL,各自加入80%乙腈溶液443 μL,充分混匀得到0.5 mL浓度分别为40 000及20 000 ng/mL混合标溶液(S0)。内标溶液的配制:精密称取纯度分别为96%的TIC-d7及99.75%的DHTIC-d7,加入0.959 mL和0.998 mL溶剂,涡旋均匀得到浓度分别为0.5 mg/mL和1.0 mg/mL的药物同位素内标储备液。准确移取体积为5 μL的TIC-d7及DHTIC-d7的内标储备液,分别加入80%乙腈溶液440 μL,充分混匀得到2种0.5 mL浓度均为1500 ng/mL的10倍内标SI溶液,使用时用乙腈稀释10倍,可得到浓度均为150 ng/mL的2种内标工作液。
1.3 血浆样品的处理用移液器准确移取待测标本50 μL于标记好的1.5 mL EP管中,加入20 μL 内标工作溶液(IS-1),加入180 μL乙腈,涡旋均匀;振荡5 min,14 800 r/min,4 ℃离心5 min,转移EP管中的上清液80 μL待进样,进样量为3 μL。
1.4 相关参数考察分别对样品的特异性、回收率、准曲线制备及定量下限测定、基质效应、批内、批间精密度试验、准确度试验、稳定性试验进行考察,确保符合样本定量检测的要求。

2 结 果
2.1 方法学考察
2.1.1 特异性在实验所采用的色谱条件下,DHTIC、DHTIC-d7、TIC、TIC-d7各目标药物及同位素内标出峰时间分别为3.5、3.48、3.51、3.51 min。目标化合物和内标峰形良好,无杂峰干扰测定,基线平稳。本方法具有较高的特异性,能准确测定血浆中的替格瑞洛及其活性代谢物的浓度,灵敏度较高。
2.1.2 标准曲线及定量下限TIC归方程为Y=0.022615X+0.008650(R2=0.99922869);DHTIC直线回归方程为Y=0.028250+0.028721(R2=0.99920823);目标物在合适范围内呈良好的线性关系。另外,各药物在在血浆中的定量下限见表1。
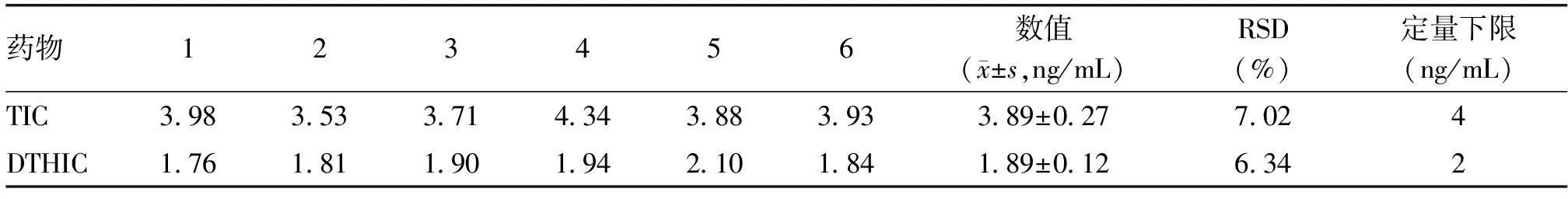
表1 替格瑞洛及其活性代谢物的定量下限(n=6)
2.1.3 回收率试验(绝对回收率)及基质效应不同浓度的2种药物其回收率均在80%~110%之间,其相对标准偏差(RSD%)均小于10%,符合回收率的实验标准。不同浓度的各种药物(高、中、低)内标归一化的基质因子平均值,结果发现活性代谢物在5、100、800 ng/mL及150 ng/mL内标中其ME平均值均在合理范围内,替格瑞洛在10、200、1600 ng/mL及内标150 ng/mL中其ME平均值也均在合理范围内。
2.1.4 精密度与准确度以高、中、低3个浓度对连续5批次各药物样品的批件和批内RSD进行考察,结果显示各药物样品批内及批间RSD均在15%以内,该实验结果符合生物样品分析方法的要求。见表2。
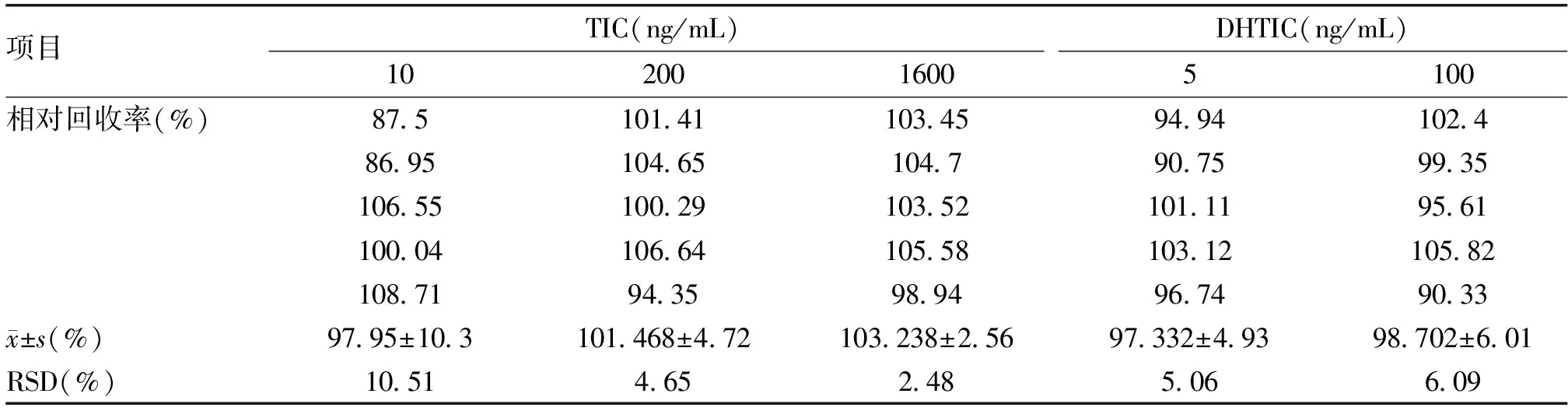
表2 不同浓度对连续5批次各药物样品HPLC-MS/MS法的批内、批间精密度考察
2.1.5 稳定性考察不同浓度的2种药物(高、中、低)样品立刻进样,室温放置6 h,4 ℃冰箱放置24 h,以及-80 ℃条件下反复冻融下测定,RE值均在合理范围之内,表明2种药物在上述条件下均保持稳定。见表3。
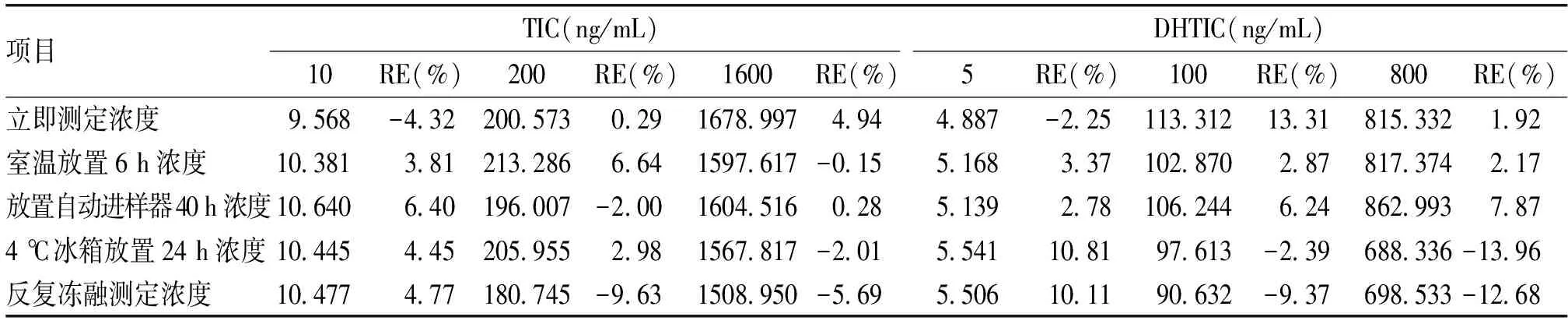
表3 人体血浆中替格瑞洛及其活性代谢物稳定性
2.2 临床特征
2.2.1 患者基本资料入组120例行经皮冠状动脉介入治疗术的急性冠脉综合征患者根据性别将其分组,纳入年龄、体重、心血管危险因素、临床分型、合并用药等临床资料,统计分析发现2组患者在年龄(P=0.001)、吸烟(P=0.000)、饮酒(P=0.000)、PCI术后(P=0.000)及合并用地尔硫卓(P=0.004)方面差异有统计学意义。
2.2.2 替格瑞洛及活性代谢物稳态谷浓度在不同年龄段的分布特征和相关性通过上述LC-MS/MS方法学的建立,并根据WHO对年龄段的划分,对入组患者药物稳态谷浓度进行监测并分析了浓度与年龄之间的相关性,结果发现替格瑞洛及其活性代谢物3组之间浓度差异无统计学意义(P=0.078),但替格瑞洛谷浓度在≤50岁与>60岁2组之间差异具有统计学意义(P=0.041)。同时也发现随着年龄的增长,替格瑞洛血药浓度与年龄呈正比。见表4。
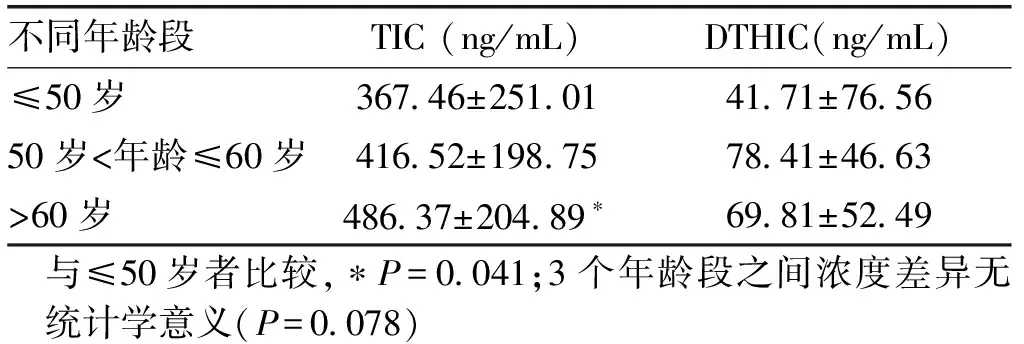
表4 不同年龄段之间的替格瑞洛及其活性代谢物谷浓度的差异性
3 讨 论
根据相关研究报道,替格瑞洛及ARC-124910XX的离子扫描模式正、负离子模式均有[10-11]。实验前期,我们比对了目标物在正负离子模式下的响应,发现在正离子模式下存在干扰峰而最终选择负离子扫描模式;另外本实验参考了柯东升等[12]研究,发现采用0.1%甲酸-乙腈为流动相保留时间,峰形等均良好。本研究成功建立了测定临床心血管抗血小板药物替格瑞洛的LC-MS/MS法。经考察,该方法准确度高,稳定且简便。
一项亚洲人群ACS患者的荟萃分析结果显示[13],相比于氯吡格雷的双联抗血小板方案,虽然替格瑞洛致命性出血的发生率没有差异,却显著增加了其他出血事件(如非致命性大出血、轻微出血等)的风险。除增加出血风险外,队列研究发现[14],接受PCI并服用替格瑞洛长达1年的ACS患者中,呼吸困难风险也有显著增加。
本研究对入组患者的基本资料分析发现,2组患者(以性别分组时)在年龄、吸烟、饮酒、PCI术后及合并用药等方面可能存在差异性。另外,在对年龄进行分段研究发现替格瑞洛血药浓度随着年龄增加而增加,且在≤50岁与>60岁2组之间存在显著性差异,表明年龄段与谷浓度可能存在相关性,且呈正相关,但仍需进一步的临床研究。一项对40名健康人群的研究发现[15],接受200 mg替格瑞洛后,年龄≥65岁患者较年轻者AUC和Cmax分别增加52%和63%;女性比男性患者的AUC和Cmax分别高37%和52%,证实了年龄、性别对药代动力学/药效学(PK/PD)的影响;因所有入组患者血小板聚集抑制率均达标,因此研究者认为年龄、性别对疗效影响没有临床意义。这可能与替格瑞洛本身抑制血小板聚集功能较强有关,但其样本量较少,且PK/PD的差异性与出血、呼吸困难等不良反应的相关性还有待研究。既往研究显示替格瑞洛出血风险增加,与女性、年龄>75岁,同时使用非甾体类抗炎药(NSAIDs)和抗栓药物有关[16]。REPLACE-2研究显示[17],女性患者是PCI术后发生出血事件的独立危险因素,机制尚未完全明了,可能与微血管病变、血管相关并发症以及相对于低体重指数的过度抗凝有关。
本研究通过对120例PCI术后ACS患者的血浆样本进行分析,建立了ACS患者PCI术后血浆中替格瑞洛及其代谢物HPLC—MS/MS测定法,方法稳定且符合生物样品定量分析要求,并成功应用于临床。从血药浓度监测的结果证实了替格瑞洛谷浓度与不同人群特征之间可能存在相关性,这不仅丰富了替格瑞洛在中国冠心病患者人群中的研究,对指导ACS患者抗血小板药物的个体化治疗和开展有效性、安全性临床研究提供了一定的参考价值。

