激光联合口服普萘洛尔治疗小儿血管瘤的疗效观察
黎胜苗 黄敏燕 罗春芬 於林军
小儿血管瘤是临床上常见的一种以血管内皮细胞过度增殖为主要特征的良性肿瘤,具有进展性发展趋势,在新生儿中发病率为1.1%~2.6%[1]。小儿血管瘤好发于头、面、颈部,部分瘤体生长迅速可引起患儿局部功能障碍,创面破溃出血亦可引发皮炎、瘢痕等并发症[2]。普萘洛尔是一种非选择性竞争性β 受体阻断剂,可通过降低多种血管生成因子表达抑制血管生成,临床上用于治疗小儿血管瘤[3~5]。激光辅助药物治疗血管瘤可有助于提高治疗效果,其中激光对于消退期血管残留及部分溃疡性血管瘤具有较好的辅助治疗作用[6]。本次研究旨在探讨两种不同的激光辅助治疗方案对小儿血管瘤的治疗效果,以期为临床治疗提供参考。现报道如下。
1 资料与方法
1.1 一般资料 选取2018 年2 月至2020 年7 月期间温州医科大学附属台州医院收治的103 例血管瘤患儿,其中男性40 例、女性63 例;年龄1~9个月,平均年龄(4.65±1.45)个月,血管瘤面积为(9.15±2.35)cm2;血管瘤部位:头颈部52 例、躯干32 例、四肢19 例。纳入标准为:①符合《血管瘤和脉管畸形诊断和治疗指南》[7]中小儿血管瘤的诊断标准,经临床特征及超声检查确诊;②年龄1 个月~1 岁;③血管瘤厚度<3 mm;④本次研究经院方伦理委员会批准,且患者家属均知情同意。排除标准为:①深度、混合型血管瘤者;②入院前接受过相关药物治疗或激光治疗者;③合并严重器质性病变者;④瘢痕体质者;⑤存在普萘洛尔禁忌证者。按照随机数字表法分为观察组和对照组,观察组52 例,其中男性19 例、女性33 例;年龄1~8 个月,平均(4.53±1.52)个月;血管瘤面积为(9.56±2.43)cm2;血管瘤部位:头颈部28 例、躯干15 例、四肢9 例。对照组51 例,其中男性21 例、女性30 例;年龄1~9 个月,平均(4.77±1.33)个月;血管瘤面积为(8.73±2.21)cm2;血管瘤部位:头颈部24 例、躯干17 例、四肢10 例。两组患者的一般临床资料比较,差异均无统计学意义(P均>0.05)。
1.2 方法
1.2.1 观察组先给予药物治疗再进行激光治疗:先给予普萘洛尔(由江苏亚邦爱普森药业生产)口服治疗,1.5~2 mg·kg-1·d-1,分早晚2 次服用,初始剂量为0.75~1 mg·kg-1·d-1,根据患儿服药后的情况阶梯式增加药物剂量,之后根据患儿体重变化情况调整药物剂量,直至瘤体不因继续服药而消褪时逐渐减量停药。然后采用585 nm/1064 nm 双波长激光系统行激光治疗,根据患儿年龄、皮损程度、瘤体深度等多种因素调节激光能量密度及脉宽,本次研究所用595 nm 激光能量密度为8~12 mJ/cm2,脉宽0.5~3 ms,1064 nm激光能量密度为20~50 J/cm2,脉宽5~15 ms,配备Cynergy 动态冷却设备,治疗时将激光垂直对准皮损处,治疗后用冰袋冰敷20~30 min并以红霉素软膏涂于患处,治疗后1 周内避免阳光照射,以减少疼痛、红肿、水疱等不良反应发生。每月治疗1 次,全程治疗需要1~5 次。
1.2.2 对照组药物和激光治疗同时进行,药物和激光治疗方法同观察组,疗程同观察组。
1.3 观察指标 ①临床指标:评估两组患儿治疗前及治疗结束后6 个月血管瘤面积、瘤体厚度,记录两组患儿血管瘤治疗时间。②血流动力学指标:采用B 超检测两组患儿治疗前及治疗结束后6 个月的血流峰值及阻力系数。③不良反应:治疗期间,统计两组患儿腹泻、食欲不振等不良反应发生情况,并记录皮肤色素沉着、水疱生成状况。
1.4 临床疗效评价标准 Ⅰ级:瘤体缩小或颜色消退≤25%;Ⅱ级:瘤体缩小或颜色消退>25%且≤50%,Ⅲ级:瘤体缩小或颜色消退>50%且≤75%;Ⅳ级:瘤体缩小或颜色消退>75%,其中Ⅳ级及以上为显效,Ⅱ~Ⅲ级为有效,Ⅰ级为无效[8]。
1.5 统计学方法 采用SPSS 22.0 统计学软件处理数据。计量资料以均数±标准差()表示,两独立样本比较采用独立样本t检验,同组治疗前后比较采用配对t检验;计数资料比较采用χ2检验。设P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗结束后6 个月临床疗效见表1

表1 两组治疗结束后6 个月临床疗效比较/例(%)
由表1 可见,治疗结束后6 个月,观察组患者的临床有效率明显高于对照组,差异有统计学意义(χ2=3.98,P<0.05)。
2.2 两组治疗前后临床指标比较见表2
由表2 可见,治疗前,两组患者的瘤体面积及瘤体厚度比较,差异均无统计学意义(t分别=1.81、1.77,P>0.05),治疗结束后6 个月,观察组患者的瘤体面积及瘤体厚度明显均低于对照组,差异均有统计学意义(t分别=6.75、9.53,P均<0.05),观察组患者的治疗时间明显短于对照组,差异有统计学意义(t=7.76,P<0.05)。
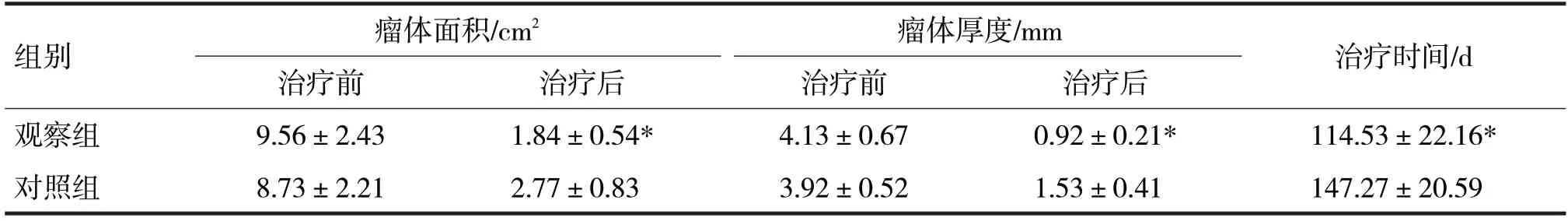
表2 两组治疗前后临床指标比较
2.3 两组患者治疗前后血流动力学指标比较结果 见表3

表3 两组治疗前后血流动力学指标比较
由表3 可见,治疗前,两组血流峰值和阻力系数比较,差异均无统计学意义(t分别=0.98、0.61,P均>0.05);治疗结束后6 个月,观察组血流峰值明显低于对照组,阻力系数明显高于对照组,差异均有统计学意义(t分别=3.08、2.09,P均<0.05)。
2.4 两组不良反应比较见表4
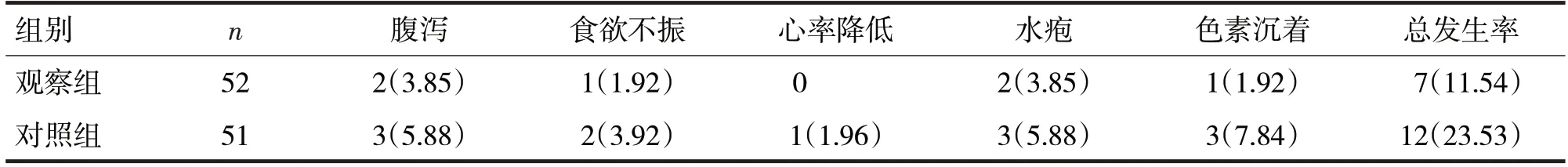
表4 两组不良反应比较/例(%)
由表4 可见,两组患者的不良反应发生率比较,差异无统计学意义(χ2=1.73,P>0.05)。
3 讨论
小儿血管瘤是指患儿出生一年内快速增殖的一种良性血管肿瘤,其发病机制尚不明确,普遍认为其与患儿全身或局部缺氧、血管内皮因子异常生成、胎儿及围生期因素促进血管异常生成相关[9]。半数以上的血管瘤可自行消退,但部分增殖期血管瘤可对患儿器官功能及成长发育产生影响,如不给予积极有效的治疗可引发纤维组织和脂肪组织沉积,使局部皮肤呈现不同程度的萎缩、瘢痕、色素沉着,对患儿容貌产生不利影响[10]。
本次研究采用595 nm、1064 nm 双波长激光治疗血管瘤患儿,符合国际治疗标准,治疗效果较好且安全性较高。不同波长脉冲激光的介质各异,可以是染料或Nd:YAG,其发出的激光可优先被氧合血红蛋白吸收,通过光热效应使血红蛋白受热凝固,促使增生血管封闭萎缩,进而达到治疗目的[11]。目前国内外主要采用585 nm、595 nm、1064 nm波长激光治疗小儿血管瘤,治疗过程中几乎不损伤皮肤,且周期性冷却处理可减少病变部位热损害,安全性较高[12]。普萘洛尔是治疗心血管疾病的常用药,可用于心绞痛、高血压、心率失常等多种心血管疾病的治疗,其主要通过去甲肾上腺素能神经递质或肾上腺素类药物竞争β 受体发挥抑制作用[13]。2008 年普萘洛尔首次被提出应用于治疗婴幼儿血管瘤后其临床应用逐渐被推广,药物安全性较高,临床应用以来未见严重不良反应及致死病例报道,目前已成为眼周等多个高风险部位血管瘤的首选治疗药物。普萘洛尔治疗小儿血管瘤的药物作用机制尚不明确,有报道表明,其可能是通过促进血管收缩,减少血管生长因子的生成、促进血管内皮细胞凋亡等机制促进血管瘤消退[14]。
本次研究结果显示,治疗后观察组患者的血流动力学改善程度更为明显,提示其增生血管消退更为明显,表明普萘洛尔对小儿血管瘤具有较好的治疗效果,且在一定用药范围内药物安全性良好。这是因为长期使用普萘洛尔治疗小儿血管瘤疗效虽好但存在不良反应,而降低普萘洛尔用药剂量可在一定程度上减少不良反应[15],目前国内外应用普萘洛尔治疗小儿血管瘤剂量范围为1~3 mg/kg,本次研究所用剂量为1.5~2 mg·kg-1·d-1,符合国内外用药标准,结果显示,观察组临床疗效更高,治疗结束后6 个月瘤体面积及厚度均明显小于对照组(P均<0.05),提示增殖期采用普萘洛尔治疗可有效抑制血管增生,而激光照射对血管损伤深度有限,因而在治疗前期采用激光配合治疗的效果并不明显,经过一段时间的药物治疗,患儿瘤体体积及深度均明显减小,此时血管瘤处于消退期,配合激光治疗可有助于加快血红蛋白凝固,促进血管萎缩,因而后期联合治疗效果更好,而对照组临床疗效低于观察组的原因在于,前期激光治疗皮损处血管瘤可减缓皮损愈合,延长色素消退时间,故而疗效欠佳。在不良反应方面,本次研究结果显示观察组不良反应总发生率为11.54%,对照组为23.53%,两组不良反应发生率比较无明显差异(P>0.05),提示普萘洛尔治疗小儿血管瘤较为安全,其中观察组腹泻、食欲不振、心率降低发生率稍低,可能是由于观察组用药周期较短,而对照组则治疗全程均服用普萘洛尔,因而观察组不良反应发生率更小;而观察组水疱、色素沉着发生率较低主要是由于进展期未采用激光治疗因而导致的皮损较小,故而色素沉积较少。
综上所述,口服普萘洛尔可有效控制小儿血管瘤增长,促进消退,但不宜长期服用,在符合停药指征时及时停药并配合激光治疗有助于提高临床疗效,降低不良反应。本次研究仍有不足,首先样本量较小,且为单中心研究,随访观察时间亦不够长,未来开展大样本的多中心研究,或可得出更有价值的结论。

