慢性心力衰竭急性加重伴发肺动脉栓塞的危险因素分析
王海霞,王江挺,盛益,郑易,胡海雷,岑镇波
慢性心力衰竭(CHF)临床表现为渐进性心肌结构或功能重塑,是导致心血管疾病患者住院的主要原因,其致死率和致残率较高,严重影响患者的生活质量和预后。肺动脉栓塞(PE)是一种较常见的综合征,是由于内源性或外源性栓子堵塞肺动脉或其分支引起的肺循环障碍的临床病理生理综合征[1]。当这两种疾病同时存在时,医生容易忽视另一个诊断,而病情发展则会进一步损害呼吸功能和心功能,使病情加重[2]。此外,两种情况并存可能形成恶性循环,对治疗决策有重大影响。本研究以320 例CHF急性加重(AECHF)且行CT肺动脉造影检查的患者作为研究对象,探讨AECHF伴发PE 的危险因素,报道如下。
1 资料与方法
1.1 一般资料 选取2014 年1 月至2020 年12 月在浙江省慈溪市人民医院因AECHF 就诊,且行CT 肺动脉造影(CTPA)检查的320 例患者,其中男246例,女74 例;年龄55~88 岁,平均(71±10)岁;纽约心脏病协会(NYHA)心功能Ⅱ~Ⅳ级。按是否伴发PE(CPTA 检查显示肺动脉主干或分支阻塞或充盈缺损)分为观察组(AECHF伴发PE患者29例)和对照组(单纯AECHF患者281例)。
1.2 方法 收集两组患者一般资料,包括性别、年龄、体质量指数(BMI)、吸烟史、既往病史[高血压、心房颤动、糖尿病、冠心病、脑卒中、慢性阻塞性肺疾病、恶性肿瘤(患肿瘤状态并且未接受根治性治疗)、深静脉血栓(VTE)、手术/骨折(近期2 个月内发病的骨折或接受过非局麻手术)等]、卧床≥3d(白天卧床时间≥50%,且生活不能自理)及深静脉置管情况。于入院后抽取研究对象静脉血,检测D 二聚体、血N末端B型脑钠肽(NT-proBNP)等,并完善不吸氧下血气分析检查。
1.3 统计方法 采用SPSS 17.0 统计软件进行分析,计量资料以均数±标准差表示,采用t 检验;计数资料比较采用检验;影响因素分析采用多因素Logistic回归分析。P<0.05 为差异有统计学意义。
2 结果
2.1 一般情况 两组年龄,性别比,吸烟史、高血压、糖尿病、冠心病、脑卒中、肺部感染、慢性阻塞性肺病、深静脉置管史、手术/骨折及肿瘤史占比等差异均无统计学意义(均P>0.05);两组卧床时间≥3 d、有心房颤动病史及VTE的占比差异均有统计学意义(均P<0.05)。见表1。
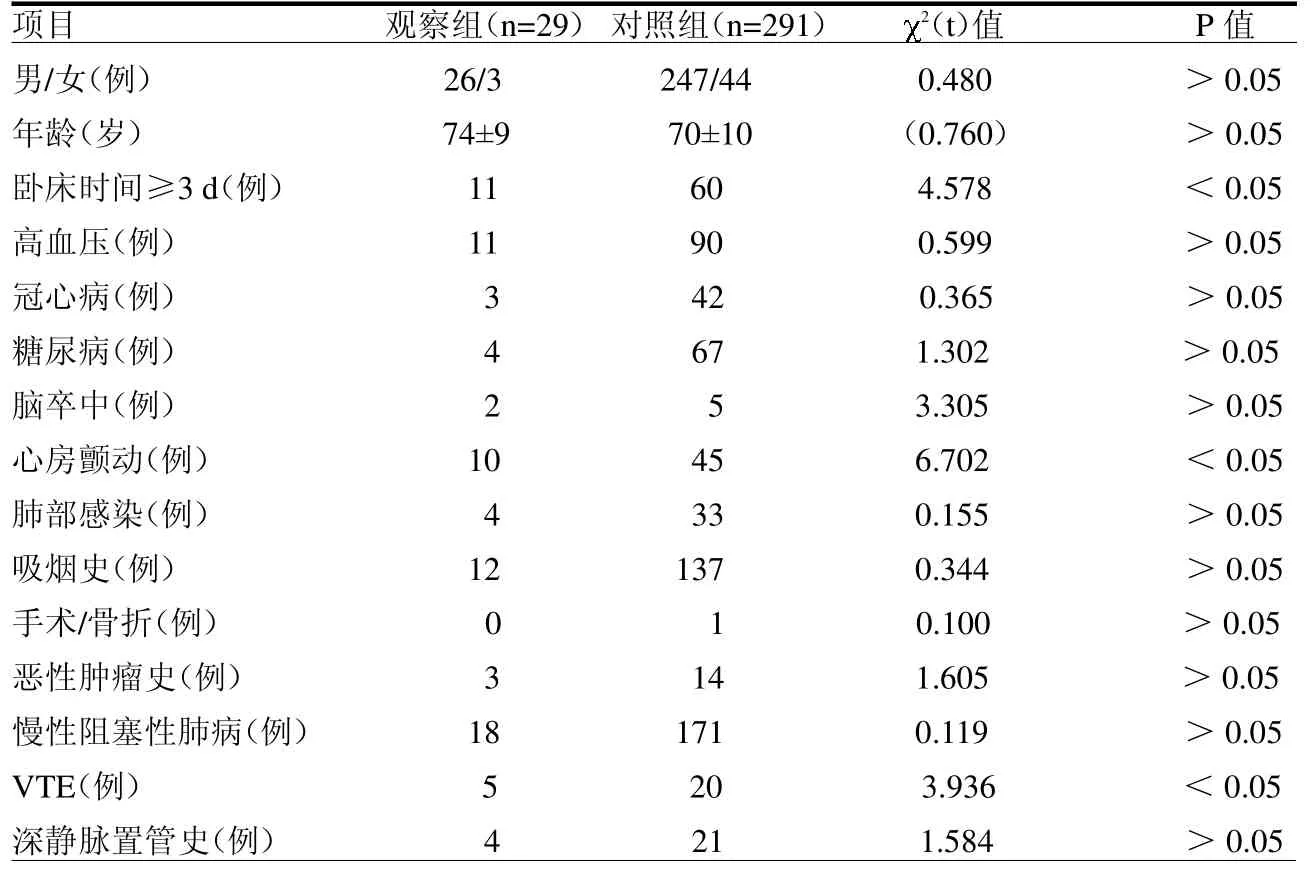
表1 两组临床资料比较
2.2 两组临床检查结果比较 观察组D 二聚体≥1 000 ng/ml、D 二聚体≥2 000 ng/ml、NT-proBNP≥1 000 pg/ml、肺动脉压≥50 mmHg、动脉血氧分压(PaO2)≤60 mmHg 占比均高于对照组(均P<0.05);两组二氧化碳分压(PaCO2)≥50 mmHg,NT-BNP≥500pg/ml 占比差异均无统计学意义(均P>0.05)。见表2。
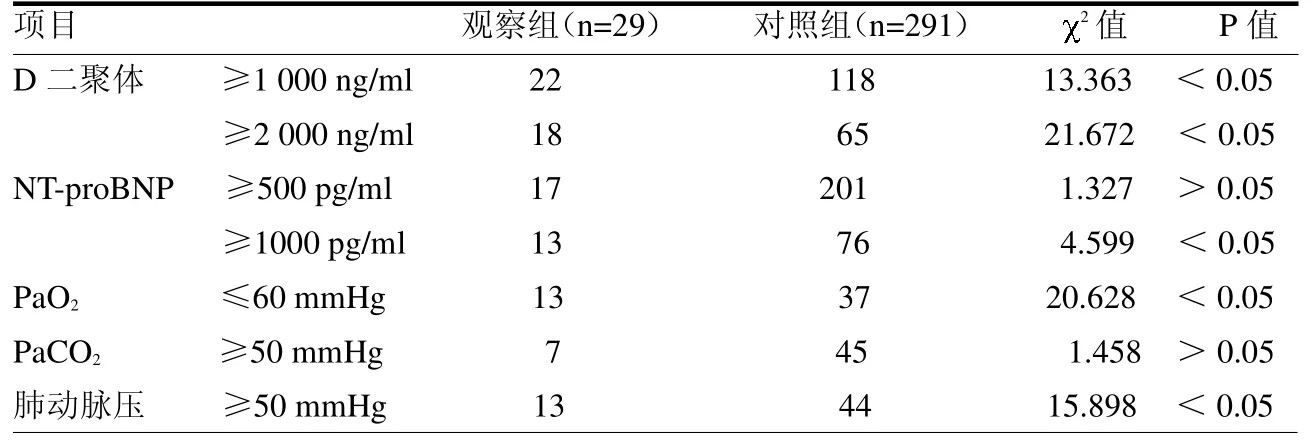
表2 两组临床检查结果比较 例
2.3 CHF伴发PE的危险因素分析 连续卧床≥3 d、D二聚体≥2 000 ng/ml、肺动脉压≥50 mmHg、PaO2≤60 mmHg 为AECHF 伴发PE 的危险因素(均P<0.05)。见表3。

表3 CHF 伴发PE 危险因素的Logistic 多元回归逐步向前法分析
3 讨论
CHF 与PE 不仅临床表现相似,而且拥有许多相同危险因素和病理生理机制[3]。高血压、血脂异常、糖尿病、肥胖、吸烟、不健康的饮食、压力及雌激素疗法等都会对内皮功能、炎症和高凝性产生不利影响,可能促进动脉粥样硬化血栓的发生(导致心肌梗死和HF)和动脉血栓形成(导致PE)[4]。心力衰竭患者普遍存在静脉血流瘀滞、内皮损伤、血液高凝状态及活动减少等情况。心力衰竭患者的PE 发生率和病死率几乎是非心力衰竭患者的两倍,这种风险会随着心功能的下降而增加。有研究发现,射血分数降低的心力衰竭患者静脉血栓栓塞的风险增加[4]。室壁运动异常、心腔内血流瘀滞及心输出量下降等均可能激活凝血系统并导致纤维蛋白形成。住院CHF 患者PE 或深静脉血栓(DVT)发生率为4%~14%,而LVEF<30%及左室舒张末内径>50mm 患者栓塞发生率是其相应患者的5~5.5 倍[5],心脏功能衰竭本身是发生PE 的重要原因。本研究320 例AECHF 患者中伴发PE 29例,发病率为9.06%,由此可见AECHF伴发PE 发生率较高,应引起重视。
本研究显示,伴发PE 的AECHF 患者与单纯AECHF患者在卧床≥3d、心房颤动、深静脉置管病史、血NT-proBNP≥1 000 pg/ml、血D 二聚体水平≥1 000 ng/ml,PaO2≤60 mmHg,肺动脉压≥50 mmHg 的占比差异均有统计学意义(均P<0.05)。多因素分析显示卧床时间≥3d、D 二聚体≥2 000 ng/ml、肺动脉压≥50 mmHg 及PaO2≤60 mmHg 是AECHF伴发PE 的独立危险因素(均P<0.05)。老年和呼吸系统疾病等因素使得CHF患者易伴发PE,这可能是因为他们更易出现心房颤动及心房血栓,但心房颤动是否能够作为PE 的发病因素仍然存在争论[6-7]。本研究显示在AECHF 中心房颤动不是一个独立的伴发PE 的危险因素。NT-proBNP 主要是由心室分泌,具有排钠、利尿、扩张血管和抑制肾素-血管紧张素-醛固酮系统的作用。左心功能不全、右心功能不全及全心功能不全患者血NT-proBNP 水平均会升高。一般来说,合并PE 的CHF 患者心功能Ⅲ~Ⅳ级比例明显升高。本研究发现AE CHF 伴发PE 的患者总体上NT-proBNP水平升高更明显,>1 000 pg/ml 占比高于对照组(P<0.05),但多因素分析未能提示其为独立危险因素。这可能是由于NT-proBNP 在CHF 和PE 中均常见升高,对PE的发生没有很强的阳性预测值,也不能改变临床治疗决策[8]。本研究显示,当D 二聚体≥2 000 ng/ml 时,AECHF 伴发PE 风险明显增加。PE 后,肺内血流侧向分流,当堵塞导致的血流损失超过分流代偿时,就会出现肺动脉压升高甚至肺水肿,肺内通气血流比值失衡,导致出现低氧血症。
综上所述,CHF 患者如存在连续卧床≥3 d、D-二聚体≥2 000 ng/ml、肺动脉压≥50 mmHg、PaO2≤60 mmHg 时,应考虑伴发PE的可能,需给予CTPA检查和积极治疗。

