TyG指数对老年大动脉粥样硬化型脑卒中患者预后的预测价值
谢 翼 高修银 李 雷 姬 燕
急性缺血性脑卒中(acute ischemic stroke,AIS)是由于大脑动脉突发堵塞所造成供血部位脑组织坏死的神经系统疾病,起病急、进展快,易致残、致死,临床预后康复情况与患者的生存质量紧密相关。老年患者大多是慢性疾病共存状态,机体的代偿能力也已下降,极易发生AIS,目前AIS已成为我国老龄化人口中严重的健康问题[1]。大动脉粥样硬化(large-artery atherosclerotic stroke,LAA)型是临床最常见的脑卒中类型,动脉粥样硬化(atherosclerosis,AS)是AIS的病理生理基础,糖脂代谢紊乱是AS的重要发病机制,甘油三酯葡萄糖指数(triglyceride-glucose index,TyG 指数)是综合了糖脂代谢的指标,目前已有研究表明TyG 指数可作为AS的生物学指标,且与缺血性脑卒中疾病相关[2]。为提高 AIS 患者的生存质量,改善患者的预后情况,本研究探讨TyG指数对老年LAA型AIS患者预后的预测价值。
对象与方法
1.研究对象及分组:回顾性搜集2019年7月~2020年6月于笔者医院神经内科住院治疗的老年LAA型AIS患者396例患者的病史及临床检查资料。对患者出院后进行电话或门诊跟踪随访12个月,依据改良 Rankin 量表(mRS)评分综合判定其预后情况,以mRS 评分≤2分为预后良好,共217例,mRS 评分>2分为预后不良,共179例。纳入标准:(1)AIS的诊断符合《中国急性缺血性脑卒中诊治指南2018》[3]诊断标准。(2)纳入患者的头颈部 CTA提示颈动脉或颅内大动脉狭窄≥50%。(3)就诊时距离发病 7天以内。(4)患者年龄大于60岁。(5)签署知情同意书。排除标准:(1)颅内出血、感染、占位等其他神经系统疾病。(2)住院期间进行溶栓或血管内治疗。(3)伴有各系统严重疾病。(4)疑似家族性高甘油三酯血症[TG≥500mg/dl(5.65mmol/L)]。(5)资料信息收集有缺失或失访的患者。
2.研究方法:收集患者的等病史资料,所有患者于清晨采集空腹静脉血,进行实验室检查,所有患者入院后3天内完成头颈部 CTA及头颅 MRI 检查。计算TyG指数=ln[空腹甘油三酯(mg/dl)×空腹葡萄糖(mg/dl)/2][4]。所有患者跟踪随访12 个月,记录患者是否合并肺炎、脑卒中复发及严重残疾的情况。
结 果
1.预后不良组与预后良好组之间的一般资料比较:预后不良组与预后良好组之间患者的糖尿病史、FPG、HbA1c、NIHSS评分、TyG 指数相较于预后良好组患者,差异有统计学意义(P<0.05),详见表1。
表1 预后不良组、预后良好组临床资料比较
2.高TyG指数组与低TyG指数组之间的一般资料比较:根据TyG指数的中位数分为两组,即高TyG指数组199例(TyG指数≥8.828)和低TyG指数组197例(TyG指数<8.828)。结果显示高TyG指数组男性患者多,合并有高血压、糖尿病、冠心病的人数多,FPG、TC、TG、HDL-C、HbA1c、NIHSS评分及mRS评分相较于低TyG指数组,差异有统计学意义(P<0.05),详见表2。
表2 高TyG指数组与低TyG指数组临床资料比较
3.Spearman相关性分析:TyG 指数与老年LAA型AIS患者预后mRS评分呈正相关(r=0.304,P=0.000)。
4. 高TyG指数组与低TyG指数组随访12 个月内是否合并肺炎、脑卒中复发及严重残疾的情况比较:高TyG指数组患者合并肺炎、脑卒中复发及严重残疾的发生率较低TyG指数组高(P<0.05),详见表3。
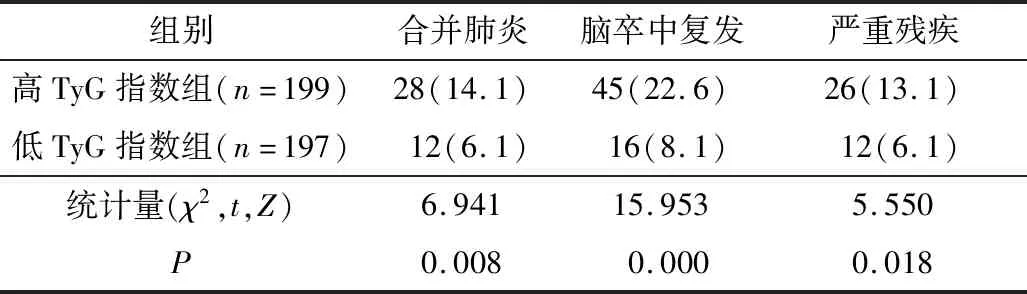
表3 不同TyG指数组12 个月内不良事件发生比较[n(%)]
5.老年LAA 型 AIS患者预后的Logistic回归分析:将单因素分析中有意义的作为自变量, 预后良好及不良作为因变量,Logistic回归分析显示HbA1c、NIHSS评分、TyG指数均为影响老年 LAA 型 AIS患者预后的独立危险因素(P<0.05),详见表4。

表4 影响老年LAA型AIS患者预后的多因素Logistic回归分析
6. TyG指数预测老年 LAA 型 AIS患者预后不良的价值:ROC分析TyG指数预测老年LAA 型 AIS 患者预后不良的曲线下面积(AUC)为0.724(95% CI: 0.674~0.775),敏感度为79.97%,特异性为63.1%,阈值为8.757,详见图1。
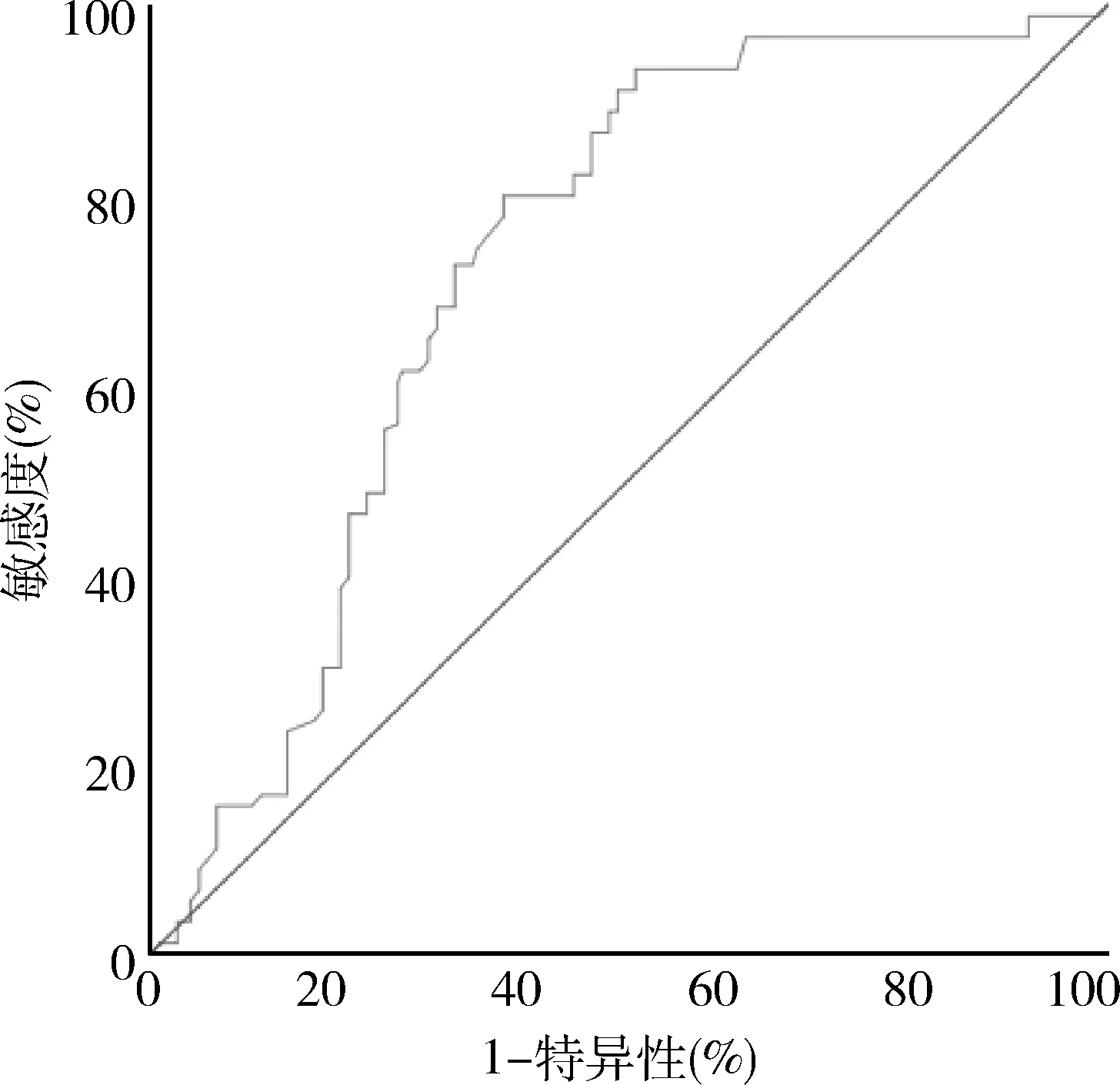
图1 TyG指数预测老年LAA 型 AIS患者预后不良的ROC曲线参数
讨 论
随着人们饮食和生活习惯的改变,脑卒中的高危因素(糖尿病、高血压、冠心病、动脉粥样硬化)在人群中普遍存在,AIS的不良预后增加了患者的生活及心理负担[5]。有研究表明,中老年急性缺血性脑卒中患者相较于青年患者,高血压、糖尿病、高胆固醇血症等发生率更高[6]。临床上通常根据病因对AIS患者进行分型,经典的TOAST分型已被广泛应用,具有较高的可信度和实用性,其中大动脉粥样硬化型即LAA型AIS是临床常见的类型[7]。
有研究表明,老年急性缺血性脑卒中患者,其病因构成以大动脉粥样硬化为主,随着年龄的增长,血管逐渐老化,动脉粥样硬化的血管弹性减弱而脆性增加,其侧支循环的构建能力也日益减弱[8]。动脉粥样硬化是一个复杂的过程,涉及许多机制,例如炎症、脂质蓄积和胰岛素抵抗。进展过程主要包括动脉壁上脂质条纹的积累,逐步发展成动脉粥样斑块,斑块破裂后可能引起不同部位的阻塞[9]。
TyG指数是FPG和TG的复合性指标,已被证实是一种简便的胰岛素抵抗标志物[10]。众所周知,胰岛素抵抗(insulin resistance,IR)通过促进血小板活化、触发内皮细胞功能障碍、促进炎症过程的表达以及其所引起的糖脂代谢调节的紊乱促进了AS的形成和发展[11, 12]。Lambrinoudaki 等[13]在对473例非糖尿病绝经后女性的研究中指出,TyG 指数与颈动脉内膜中层厚度(carotid intima media thickness,cIMT)相关,cIMT是AS存在和进展的广泛使用的替代标志物[14]。研究发现TyG指数可预测普通人群出现缺血性脑卒中的风险,同时与AIS神经系统恶化、脑卒中复发风险、重症脑卒中院内病死率相关[15~17]。本研究针对老年LAA型AIS患者探讨TyG指数与其不良功能预后是否存在关联,结果提示TyG指数可作为预测老年LAA 型 AIS 预后的指标,且TyG指数与mRS评分呈正相关,同时TyG指数是影响老年LAA 型 AIS 患者预后的危险因素,表明TyG指数可作为一个衡量患者预后的检测指标。
此外,本研究在对患者进行12 个月的随访,结果发现TyG指数与老年LAA 型 AIS 患者不良事件的发生率显著相关,可以预测患者脑卒中复发,这与Zhou等[16]结果一致。Kim等[18]研究显示,在糖尿病患者中,TyG指数与系统性炎症指标高敏感性 C 反应蛋白(hs-CRP)显著相关,提示TyG指数亦可反映全身的炎症水平,脑卒中相关性肺炎是AIS常见的感染并发症,本研究提示TyG指数与患者是否合并脑卒中相关性肺炎相关,这为临床上鉴别AIS患者感染情况提供了简便的检测指标。
综上所述,TyG指数通过影响动脉粥样硬化的进程进而影响患者的预后,与老年LAA型AIS患者预后相关,是其预后不良的危险因素,具有预测患者预后不良的临床价值,同时,本研究还发现,TyG指数与AIS患者脑卒中复发、脑卒中相关性肺炎以及严重残疾等不良事件的发生显著相关,可作为非侵入性临床标志物,尽早识别高危的老年LAA型AIS患者,继而进行积极干预,以期减轻公共卫生负担的社会价值。本研究存在样本量较小、随访时间不足等问题,因此在后续研究中应进行多中心研究,延长随访时间,同时应该动态监测TyG指数。

