不同剂量每周顺铂方案在鼻咽癌同步放化疗中的疗效观察*
张 杰,彭海波,李鹏程,姜鹤群
成都医学院第一附属医院 肿瘤科(成都 610500)
鼻咽癌是我国常见的头颈部恶性肿瘤,其主要的治疗方式为放化疗。对于局部晚期的鼻咽癌患者,同步放化疗是目前优选的治疗方案[1-2]。在同步放化疗的方案中,含顺铂方案是公认的优选方案,其中以高剂量顺铂3周方案为美国国立综合癌症网络(nationcal comprehensive cancer network,NCCN)推荐的临床实践指南[3]。在中国临床肿瘤学会发布的指南中,也推荐以顺铂为主的治疗方案。由于高剂量顺铂方案(3周方案)对患者强度较大,可接受整个治疗方案的患者较少,有相关研究[4-5]也采用每周顺铂方案。但在每周顺铂方案的实施过程中,采用指南推荐的顺铂40 mg/m2/周方案,患者亦很难完整耐受整个治疗流程,影响治疗效果。因此探索适合患者的顺铂剂量十分重要,本研究拟比较不同剂量的每周顺铂方案的疗效与不良反应,现报道如下。
1 资料与方法
1.1 临床资料
选取2011年6月至2016年1月在成都医学院第一附属医院肿瘤科收治的88例Ⅲ期及Ⅳa期鼻咽癌患者为研究对象,以随机数字表法分为顺铂剂量20 mg/m2/周组(A组)与顺铂剂量30 mg/m2/周组(B组)。纳入标准:1)经病理学诊断明确的鼻咽部鳞癌的初治患者;2)既往无肿瘤疾病治疗史;3)年龄<65岁,体能状况评分<2分;4)治疗前分期为Ⅲ期或Ⅳa期;5)重要器官功能正常(特别是肝肾功能),听力正常,无使用顺铂的禁忌;6)按实体瘤的疗效评价标准(response evaluation criteria in solid tumors, RECIST)患者存在可测量病灶;7)理解治疗安排,同意按要求治疗及完成随访。排除标准:既往有肿瘤治疗史;无法按计划完成治疗的患者。A组年龄(55.14±6.08)岁,B组年龄(55.82±6.66)岁,两组年龄、性别、体能评分等基本资料比较,差异无统计学意义(P>0.05),具有可比性(表1)。
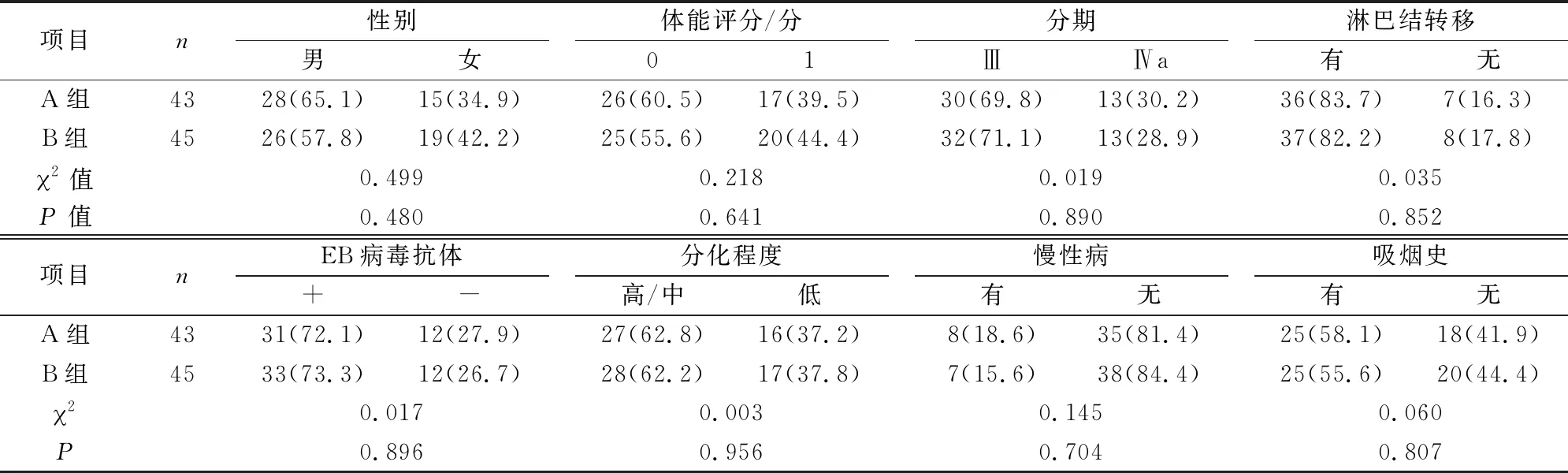
表1 两组基本资料比较[n(%)]
1.2 治疗方案
所有患者均采用同步放化疗序贯辅助化疗的治疗方式。放疗方案:适形调强放射治疗,计划靶区70 Gy,采用常规分割(2.0 Gy/次,1次/d,5次/周,共7周)。同步化疗方案:两组均采用每周1次的方式进行,共7次。同步放化疗结束后,患者进行PF方案(顺铂75 mg/m2, D1+5-FU 1 000 mg/m2,D1-4, 24 h维持,每4周重复)辅助化疗,共3周期,化疗期间常规给予抑酸、止吐等药物处理。患者治疗结束后,根据其病情变化酌情进行后续治疗或进入随访期。剂量调整方案:如出现Ⅰ、Ⅱ度化疗相关不良反应,给予对症处理,恢复后继续原方案治疗,下周期预防性使用升高白细胞的药物。出现Ⅲ度不良反应时,给予相应处理后,在相应时间内恢复的化疗按原计划继续。在无法按期恢复的患者中,延后2 d恢复者,则按原计划进行;延后2 d仍未恢复者,此周化疗暂停,下周化疗方案减量25%继续进行;再次出现Ⅲ度不良反应者化疗终止,放疗继续。出现Ⅳ度不良反应者,化疗终止,对症处理后单纯放疗。放疗相关不良反应的处理:出现Ⅰ、Ⅱ度不良反应时给予对症处理;出现Ⅲ度及以上不良反应时,放化疗均暂停,恢复后继续原方案治疗;出现Ⅳ度不良反应,所有治疗均需暂停,待恢复后再继续治疗。系统治疗后完成全身检查,进行疗效评价,无明显阳性病灶者进入随访期,如有颈部阳性淋巴结残留者考虑颈部淋巴结清扫后进入随访期。
1.3 观察不良反应及相应处理
按常见不良反应事件评价标准(common terminology criteria for adverse events, CTCAE)对不良反应(包括治疗中及随访期内的所有不良反应)进行分级。对各级不良反应按照CTCAE 4.0版进行记录并及时处理,如出现某一不良反应但程度不同时,以分级较重的记录。出现Ⅲ、Ⅳ度不良反应的患者,参考上述剂量调整方案进行处理。
1.4 随访
所有随访由专人负责,以电话及门诊随访的方式进行。随访期内进展的患者,按NCCN指南[6]推荐的方案进行后继治疗。终止随访日期为2020年1月,所有患者均完成随访。本研究随访时间为(19~94)(52.89±19.23)个月。
1.5 疗效评价标准及观察目标
所有患者治疗前行基线评估,完善血液学检查及必要的影像学检查。在治疗过程中定期复查基线评估的观察指标。每3个月进行心功能评估,每半年行骨扫描1次。随访期的患者,每3个月进行1次血液学及影像学复查。按照RECIST 1.1版进行疗效评价,其评价分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)及进展(progressive disease,PD)。观察目标:主要观察终点为比较两组按计划完成同步化疗次数、不良反应及疾病进展时间(disease-free survival, DFS)及总生存期(overall survival, OS)。次要观察终点为比较两组治疗有效率(response rate, RR)、疾病控制率(disease-control rate, DCR)。
1.6 统计学方法

2 结果
2.1 两组完成同步化疗次数比较
A组完成化疗次数为(5.40±1.12)次(95%CI:5.05~5.75),B组为(4.31±1.11)次(95%CI:3.98~4.64),A组化疗次数较B组多,两组比较差异有统计学意义(t=4.581,P<0.001)。
2.2 两组RR、DCR比较
以同步放化疗结束后、辅助化疗之前复查的结果进行短期疗效评估,A组CR 33例,PR 6例,SD 2例,PD 2例。B组CR 37例,PR 5例,SD 2例,PD 1例。A组RR为 90.70%,B组RR为93.33%,两组RR比较差异无统计学意义(2=0.209,P=0.648)。A组DCR为95.35%,B组DCR为7.78%,两组DCR比较差异无统计学意义(2=0.394,P=0.530)。
2.3 两组DFS比较
A组1、3年无疾病进展率分别为100.0%、72.4%,DFS为14~77(60.66±4.17)个月, 95%CI:52.49~68.82。B组1、3年无疾病进展率分别为100%、78.3%,DFS为17~68(57.63±3.01)个月,95%CI:51.74~63.52。两组DFS比较,差异无统计学意义(2=0.250,P=0.617)(图1)。
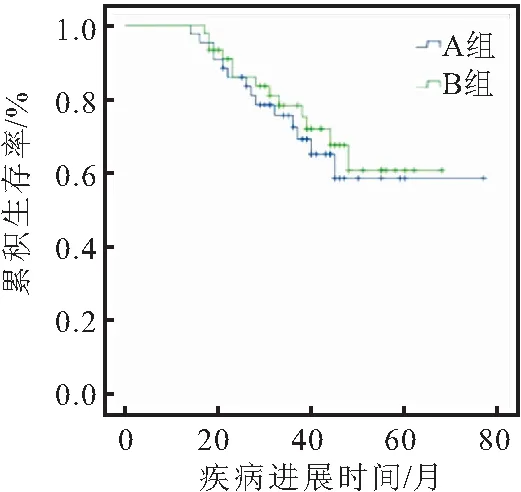
图1 两组DFS比较
2.4 两组OS比较
A组1、3、5年总生存率分别为100.0%、86.0%、70.8%;OS为33~92(77.16±3.76)个月,95%CI:69.79~84.54。B组1、3、5年总生存率分别为:100.0%、86.5%、70.7%,OS为23~96(82.78±3.91)个月,95%CI:75.12~90.43。两组OS比较,差异无统计学意义(2=0.054,P=0.817)(图2)。

图2 两组OS比较
2.5 两组不良反应比较
Ⅰ/Ⅱ度便秘:A组15例,B组26例,两组比较差异有统计学意义(P<0.05)。出现化疗相关Ⅲ/Ⅳ度不良反应例数:A组11例(25.6%),B组26例(57.8%),两组比较差异有统计学意义(P<0.05)。Ⅲ/Ⅳ度白细胞降低例数:A组8例,B组17例,两组比较差异有统计学意义(P<0.05)。两组其余不良反应(包括放疗相关不良反应)比较,差异无统计学意义(P>0.05)(表2~3)。
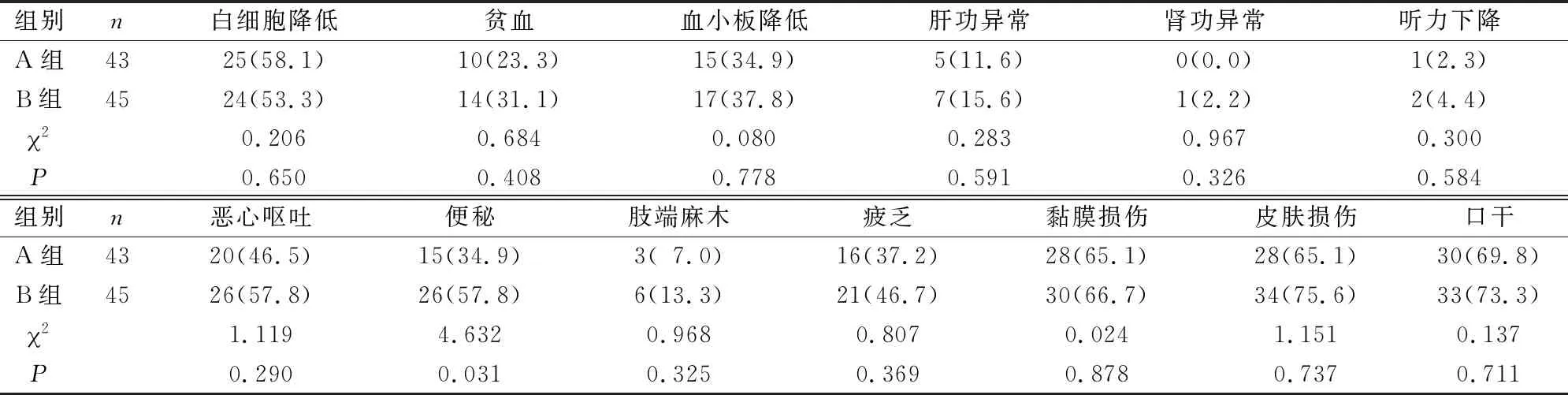
表2 两组Ⅰ/Ⅱ度不良反应比较[n(%)]

表3 两组Ⅲ/Ⅳ度不良反应比较[n(%)]
3 讨论
在NCCN指南中,含顺铂方案是鼻咽癌的标准同步放化疗方案。多项单纯同步放化疗的研究[1-2,7-9]表明,同步放化疗可使鼻咽癌患者在治疗中获益,特别是以顺铂为基础或单药顺铂方案。在顺铂为基础的方案中,每周方案在多项研究[1,4-5,10]中得到应用。本研究在治疗初期也采用与上述方案相同的顺铂剂量(40 mg/m2,1次/周,共7次),结果几乎没有患者可耐受此方案连续3周及以上的治疗。有学者[11-13]曾对不同剂量的顺铂方案进行了临床研究,但不同剂量间疗效是否有差异仍需进一步研究。因此,本研究旨在比较不同的同步化疗剂量对患者的近期疗效、远期疗效及不良反应之间的差别,为寻找高效的单药顺铂剂量提供相关依据。
本研究结果显示,不同的顺铂单药剂量与患者完成总的同步化疗周数相关,A组大部分患者能接受5次及以上的治疗周数,而B组大部分患者仅能接受4次。同时,B组出现中重度不良反应的例数明显比A组多,因为顺铂属于细胞周期非特异性药物,治疗剂量的增加与不良反应的增多有相关性。B组出现便秘的不良反应较A组多,其原因是使用5-HT3受体拮抗剂治疗顺铂导致的恶心呕吐时所致。此外,本研究设计的顺铂剂量,两组放疗不良反应(黏膜损伤、皮肤损伤、口干)比较,差异无统计学意义(P>0.05),这与Beckmann等[4]研究报道的顺铂导致黏膜相关不良反应增加的情况不一致。与其他研究[4-5]结果相比较,本研究的DFS及OS 结果更优。究其原因,主要系上述研究纳入的病例为头颈部多部位恶性肿瘤患者,本研究主要是针对鼻咽癌患者,而鼻咽癌在头颈部恶性肿瘤中的治疗效果较好所致。在横向与鼻咽癌的相关研究进行比较时,本研究与Kong等[14]在各项近期或远期疗效观察的结果较一致。
本研究仍有不足之处,1)本研究未设立指南推荐的标准剂量组(40 mg/m2/周),仅与其他文献的相应剂量组的结果进行了比较。因入组病例及治疗单位等多种原因的影响,导致结果可能存在偏倚。所以,仍应针对此剂量进行对照研究以进一步评估患者的近期、远期疗效。2)本研究纳入的研究病例较少,这主要是因为单中心的临床观察无法保证足够的病例数,且并未进行分层分析,不能对顺铂剂量与某些因素治疗的关系进行进一步评估。
综上所述,本研究结果表明,在同步放化疗中,采用单药顺铂的方案可行有效,单药顺铂每周方案剂量为20 mg/m2时患者更易接受完整的治疗疗程,且较30 mg/m2的剂量未降低治疗效果。本研究下一步应在增加样本量的同时,设定标准剂量组进行对比,以期得到更多临床数据。

