独立三维剂量验证在鼻咽癌容积调强放射治疗计划中的应用
刘致滨,石锦平,李盈辉,张利文,谢秋英,滕建建,常元智
佛山市第一人民医院(中山大学附属佛山医院)肿瘤放射物理科,广东佛山 528000
前言
鼻咽癌是中国华南地区最常见的肿瘤之一,放射治疗已经成为鼻咽癌最主要的治疗手段[1-2]。容积调强放射治疗(VMAT)技术通过动态旋转形式,同步连续调节机架角度、多叶准直器(Multileaf Collimator,MLC)的形状和剂量率,以更多的自由度高效地实现了靶区的剂量适形度同时又保护了周围正常组织,在临床治疗上应用越来越广[3]。鼻咽癌特殊的解剖学特点和周围危及器官的剂量限制,使得计划设计难度大大增加。同时靶区边缘剂量梯度大,各射野内注量分布不均,导致计划产生较多的窄条射野。鼻咽癌VMAT 计划实施的复杂性和高效性对计划的验证提出了新的挑战。近年来三维剂量验证已成为主要的验证手段,可以在患者影像信息上重建三维剂量分布,根据剂量体积直方图(Dose Volume Histogram, DVH)对靶区和危及器官做出针对性评价,并指出剂量偏差的具体位置,给予更多的信息判断误差对临床治疗产生的影响。因此本研究研究独立三维剂量验证在鼻咽癌VMAT 计划中的可行性,并寻找鼻咽癌VMAT 计划验证的最佳γ通过率阈值,为独立三维剂量验证的应用奠定一定的基础。
1 资料与方法
1.1 临床资料
随机选取2019年5月~12月在佛山市第一人民医院接受VMAT的31例鼻咽癌患者为研究对象。年龄33~76岁,中位年龄55岁。
CT扫描后图像通过网络传输至Varian Eclipse计划系统工作站。结合磁共振成像(MRI)等影像勾画出靶区和正常组织。勾画的靶区有原发肿瘤区的计划靶区PGTVnx、转移淋巴结肿瘤区的计划靶区PGTVnd、亚临床病灶高危靶区和低危靶区的计划靶区分别为PTV1和PTV2。危及器官主要勾画脊髓、脑干、左右腮腺等。
1.2 治疗计划设计
在Eclipse 13.5 计划系统上设计VMAT 计划,Varian Trilogy 加速器上执行。采用6 MV 光子线,设置为两条全弧,分别为逆时针方向179°~181°(准直器角度15°)和顺时针方向181°~179°(准直器角度345°)。PGTVnx、PGTVnd、PTVl 和PTV2 的处方剂量分别为70、68、62和54 Gy,分33次完成。
1.3 三维剂量验证
将31 例VMAT 计划的RT Plan、RT Structure、RT Dose和CT图像传输至Compass系统中。IBA公司的Compass三维剂量验证系统,可由内置算法的筒串卷积(Collapsed Cone Convolution,CCC)算法模型对治疗计划系统(Treatment Planning System,TPS)的计划进行独立计算,得到独立三维剂量分布(Computed Dose Distribution,CDD)。也可采用MatriXX 探测器阵列实际测量得到加速器的剂量在患者CT 影像的重建三维剂量分布(Reconstructed Dose Distribution,RDD),对治疗计划及治疗实施的准确性进行验证[4]。分别对独立三维剂量分布与治疗计划系统分布(CDD-TPS)和重建三维剂量分布与治疗计划系统分布(RDD-TPS)进行γ 通过率比较。对于靶区和正常组织的γ 值,γ<1 表示为通过,阈值选择的是3%/2 mm、10%。
1.4 剂量学差异
Compass 系统内置的CCC 算法模型计算得到的独立三维剂量与治疗计划系统相比较,选取相应的靶区和危及器官的绝对百分剂量差异来进行研究。其中绝对百分剂量差异=本研究中评价的剂量学参数有靶区的最大剂量D2%、平均剂量Dmean、最小剂量D98%;危及器官比较脊髓D1%、左右腮腺的Dmean以及脑干D1%和Dmean。
1.5 统计学分析
所有数据均采用SPSS 20.0 统计学软件进行分析,两组间指标比较采用配对t检验,P<0.05 为差异有统计学意义。应用Bland-Altman 法检验两种验证方法的一致性,95%一致性界限来评估一致性效果。使用受试者工作特征(Receiver Operating Characteristic,ROC)曲线来确定最佳γ 通过率阈值。
2 结果
2.1 γ通过率
由表1可知,CDD-TPS的Body(体轮廓)、PGTVnx、PGTVnd、PTV1、PTV2、脑干、脊髓、左右腮腺的γ通过率平均值为93.32%~99.38%,RDD-TPS相应的γ通过率平均值为92.33%~99.09%。两种验证方式的γ通过率平均值均在90%以上。CDD-TPS与RDD-TPS相比较,在Body、PGTVnd、PTV1和PTV2的γ通过率差异有统计学意义(P<0.05),而PGTVnx、脑干、脊髓和左右腮腺的γ通过率均无统计学意义(P>0.05)。
表1 鼻咽癌治疗计划三维剂量验证的γ通过率(n=31,%,± s)Tab.1 Gamma passing rate of treatment plans of nasopharyngeal carcinoma(NPC)in three-dimensional dose verification(n=31,%,Mean±SD)

表1 鼻咽癌治疗计划三维剂量验证的γ通过率(n=31,%,± s)Tab.1 Gamma passing rate of treatment plans of nasopharyngeal carcinoma(NPC)in three-dimensional dose verification(n=31,%,Mean±SD)
所选结构CDD-TPS RDD-TPS P值Body PGTVnx PGTVnd PTV1 PTV2脑干脊髓左腮腺右腮腺93.32±1.47 94.08±3.42 95.18±3.63 94.88±2.55 95.55±2.02 99.38±0.71 97.77±2.26 98.79±1.80 98.62±1.48 95.02±1.58 92.63±3.88 92.33±4.47 92.71±3.45 92.55±2.22 97.85±2.73 99.09±1.33 98.28±2.61 98.54±1.60 0.001 0.148 0.003 0.005 0.002 0.060 0.051 0.348 0.823
2.2 Bland-Altman一致性分析
Bland-Altman方法常用于两种方法在同一个体上的测量结果进行一致性评价。本研究应用Bland-Altman方法检验CDD-TPS和RDD-TPS两种验证方法的一致性。以每个测量点两种方法测量结果的均值为横坐标,其差值为纵坐标绘制均值-差值散点图,计算得到95%一致性界限,观察界限内测试点来评估一致性效果[5]。31例鼻咽癌计划共有279个测试点。统计结果显示:两种测量方法γ 通过率均值为86.21%~100.00%,平均(95.81±3.10)%;差值-14.4%~14.28%,平均(1.17±3.93)%。Bland-Altman分析结果:差值检验提示两种方法在三维剂量验证测量时存在统计学差异,差值的95%一致性界限为-6.56%~8.90%。在279个点中位于一致性界限置信区间范围外的有13个,占比4.66%(13/279)。从图1可以看出,CDD-TPS和RDD-TPS两种验证方法有95.34%的测试点落在一致性界限内,因此可认为两种验证方法之间具有较好的一致性,从而验证了独立三维剂量验证应用于鼻咽癌VMAT计划中是可行的。

图1 CDD-TPS和RDD-TPS γ通过率的均值-差值散点图Fig.1 Mean-difference scatter plot of gamma passing rates in CDD-TPS and RDD-TPS
2.3 最佳阈值的确定
ROC 曲线是临床评价诊断试验的重要工具,它是二元分类模型,以假阳性(1-特异性)为x轴、敏感性(真阳性)为y 轴绘制而成的曲线,曲线下面积(Area Under the Curve,AUC)显示诊断判别阳性和阴性的能力。通过寻找最佳阈值,使得敏感性和特异性达到平衡,减少漏判和误判的发生[6]。31例鼻咽癌治疗计划从DVH中剂量学参数获得绝对百分剂量差异,一旦计划中任意一个参数出现绝对百分剂量差异>5%,该计划将被视为临床上不可接受的计划。共有8 例为临床可接受计划,其余23 例均为不可接受计划,见表2。
利用图2和表2,可生成VMAT 计划中5 种不同结构的AUC,根据AUC 值来评价哪种结构参数作为γ 通过率的评价指标效果最好,约登系数(即敏感性+特异性-1)最大时确定最佳γ 通过率阈值。结果如表3所示。在Body、PGTVnx、PGTVnd、PTV1 和PTV2 5 种结构中,选取PTV2 将得到最大的AUC 值(0.946),其中最大约登系数为0.826,对应的γ通过率最佳阈值为95.41%。

图2 鼻咽癌治疗计划中5种不同结构的ROC曲线Fig.2 Receiver operating characteristic curves of 5 different kinds of structures in NPC plan

表2 鼻咽癌治疗计划剂量学参数的绝对百分剂量差异(n=31,%)Tab.2 Absolute percentage dose difference in dosimertric parameters of NPC plan (n=31,%)
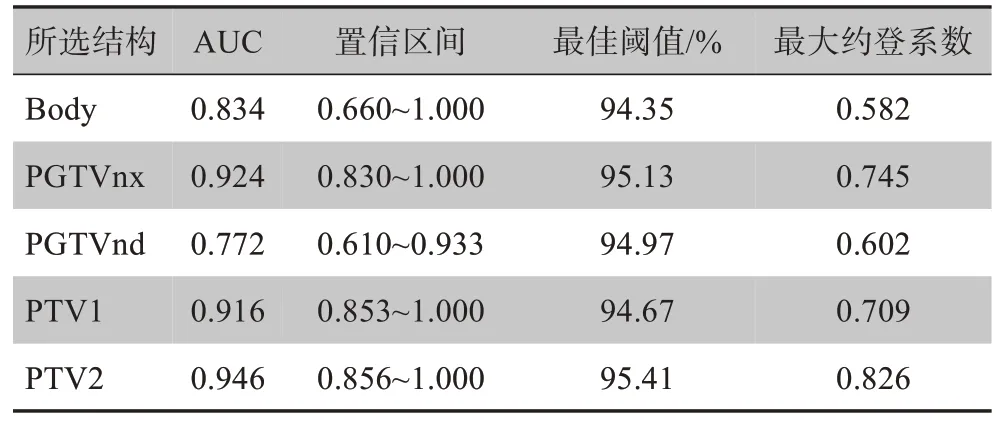
表3 鼻咽癌治疗计划中5种结构ROC曲线确定的最佳阈值参数Tab.3 The optimal threshold parameters determined by the ROC curve of 5 kinds of structures in NPC plan
3 讨论
精确放射治疗对于放射治疗计划的质控要求非常严格。传统的二维剂量验证通过将治疗计划移植到模体内进行测量,比较所选取层面上计划系统计算和实际测量之间的差异,获得二维平面的剂量信息。但是单一平面的剂量验证无法判断患者计划是否与机器照射得到的测量剂量相一致,而且没有具体的解剖信息,不能清晰看到偏差出现的位置,对临床的指导意义有限。Compass 三维验证系统可以弥补传统的二维剂量验证的不足,并能给出与患者解剖结构相关的体积剂量误差、γ 通过率、误差的位置等信息,有利于临床的评估。
本研究基于Compass 的三维剂量验证进行治疗前的独立三维剂量验证工作,目前国内外已有相关的文献对独立三维剂量验证进行了研究。Jeong 等[7]应用Compass 进行前列腺癌VMAT 计划的三维剂量验证,分别将独立三维剂量和三维剂量重建的剂量分布进行了比较,结果显示所有结构的γ 失败率在2 mm/2%标准中小于8%,而在3 mm/3%标准中则小于1%。刘潇等[8]验证了Mobius 3D 在宫颈癌IMRT计划中进行独立三维剂量验证的可行性,可提高计划验算的准确性。赵涵铱等[9]基于日志文件的三维独立剂量验证系统在IMRT 质控中的可行性研究表明该系统可快速进行临床计划的验证,为治疗提供安全可靠的技术。
本研究结果显示,在3%/2 mm、10% 标准下CDD-TPS 和RDD-TPS 的γ 通过率平均值在90%以上。从得到的绝对百分剂量差异数据来看,PGTVnx的D98%、脊髓的D1%、左右腮腺的Dmean差异平均值均大于3%。Eclipse 计划系统常采用各向异性分析算法(Anisotropic Analytical Algorithm,AAA),而Compass采用的是CCC 算法,不同算法之间的差异造成较大的百分剂量偏差从而导致临床上不可接受计划的增多。PGTVnx 主要是原发肿瘤区,存在较多空腔且临近高密度骨[10]。AAA在对组织异质性的敏感性上低于CCC 算法[11-13]。陈华等[14]研究空腔边缘剂量CCC算法和AAA 的准确性,与蒙特卡罗算法相比CCC 算法和AAA 均高估了剂量,CCC 算法计算精确性优于AAA,但误差依然存在。腮腺由于比较靠近皮肤,且部分处于低剂量区域,因此Dmean误差较大,最大误差可达9.7%。这与柏朋刚等[15]研究结果类似。
TG218 号报告建议:3%/2 mm 的γ 通过率通用容差限值≥95%,通用干预限值≥90%[16-17]。本研究使用治疗计划DVH 中剂量学参数的差异和γ 通过率作为标准,结合ROC 曲线确定最佳γ 通过率阈值。AUC值能综合反映ROC 曲线的特性,表示试验标准中阳性和阴性诊断结果分布的重叠程度,反映了诊断试验价值的高低。当数值为0.5~0.7时,诊断价值较小,分类的准确性不高;0.7~0.9 时,诊断价值中等,分类准确性较好;0.9 以上时,诊断价值较高,分类的准确性很高[18]。从表3的数据来看,5种不同结构中PTV2的AUC 值最大(其值为0.946),适合选取PTV2 用于诊断γ 通过率,其阈值为95.41%,此时敏感性和特异性比例趋于平衡。如果选用常规的γ 通过率限值95%,其敏感性基本不变,但是特异性降低,增加了可接受计划被误判的机会。刘礼东等[19]研究宫颈癌VMAT计划验证中γ通过率的最佳阈值,全局3%/3 mm和2%/2 mm 标准下最佳阈值分别为98.3% 和87.05%,在3%/3 mm 标准下最佳阈值相对于常规阈值的全局γ 敏感性可达0.93,得到显著提升,提高了阻止不可接受计划通过的能力,也降低了可接受计划误判的可能。闫慧芳等[20]研究基于日志文件分析PerFRACTION 系统的敏感度和特异度,利用PerFRACTION 系统测量工具对头颈VMAT 计划的γ通过率进行ROC 曲线分析,在敏感度和特异度均较高的情况下,获得3%/2 mm 标准下头颈VMAT 计划对应的最佳γ通过标准分别是96.32%,为头颈VMAT计划的QA 提供了更为精确的通过标准,实现精准放疗。
综上所述,独立三维剂量验证可作为计划系统计算准确性的检验,同时在不影响临床治疗的情况下,可快速地对计划进行治疗前的验证。最佳阈值有助于计划的筛查,对于独立三维剂量验证γ 通过率低于最佳阈值的计划,可结合实测的重建三维剂量分布,不仅可以筛选出明显错误的计划,还可以减轻物理师的验证工作量。独立三维剂量验证可以快速地为患者提供治疗前治疗计划计算准确性的检验,为放疗计划准确的实施提供安全、有效的技术保障。

