闭孔疝临床诊疗分析:附5例报告
杨永光,陈伟峰,邓春梅,陈伟策,张艺,陈明,林满洲
(广东医科大学附属医院肝胆胰、疝腹壁外科,广东湛江524001)
闭孔疝是一种罕见的腹壁疝,发病率仅为0.05%~2.2%[1]。因其缺乏特异性的临床表现,且多以急性肠梗阻为急诊,临床的漏诊及误诊率较高;又因其易发生肠管嵌顿、坏死,故患者病死率较高。如何尽早诊断并及时手术是处理闭孔疝的关键[2]。本文旨在通过回顾性分析广东医科大学附属医院肝胆外科于2011年1月—2021年1月收治的5 例闭孔疝患者临床资料,在随访60 个月的基础上,结合文献复习报告如下,以提高闭孔疝的诊治水平。
1 资料与方法
1.1 一般资料
本组闭孔疝病例5 例(4 例患者,1 例女性患者半年内先后被诊断为左、右侧闭孔疝),其中女4 例,男1 例;年龄61~87 岁,中位年龄(73.6±10.6)岁;BMI(18.2±1.1)kg/m2;发病部位右侧2 例,左侧3 例;除1 例行右侧腹股沟疝探查发现合并同侧隐匿闭孔疝外,其余均以腹痛,不明原因肠梗阻就诊,收治专科3 例,胃肠外科首诊术中会诊2 例;患者临床资料见表1。术前完善CT 检查明确诊断3 例,术中诊断2 例,患者术前CT 资料(图1)。患者术前查体均未扪及体表包块。
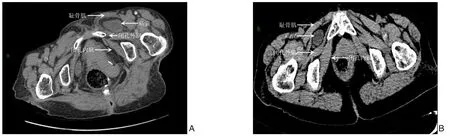
图1 患者术前盆腔CT Figure1 Preoperative pelvic CT

表1 5例闭孔疝的临床资料Table 1 Clinical data of 5 cases of obturator hernia
1.2 治疗方法
入院完善相关检查,排除手术禁忌后,1 例择期外,其余均行急诊手术。手术方式:开腹闭孔疝修补术3 例,2 例行腹腔镜下闭孔疝修补术。其中1 例行剖腹探查:肠嵌顿松解肠切除,3-0 Prolene关闭缺损;同例患者,先因左侧闭孔疝行剖腹探查肠嵌顿松解Prolene 续缝合关闭缺损,半年后又因右侧闭孔疝行肠嵌顿松解联合右侧闭孔疝无张力修补;2 例行腹腔镜腹膜前闭孔疝修补术(TAPP), 术中嵌顿肠管及回纳后肠管后闭孔(图2)。
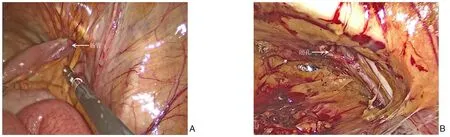
图2 闭孔疝患者术中情况Figure 2 Intraoperative situation of patient with obturator hernia
2 结 果
2.1 手术结果
本组患者术中均明确诊断为闭孔疝,左侧3 例,右侧2 例;疝内容物均为小肠,行小肠切除1 例。修补方式中,2 例行直接缝合,1 例患者行开放修补无张力修补术,2 例行腹腔镜补片修补。手术时间40~120 min,平均77.8 min。
2.2 术后结果
术后1 例患者因感染性休克ICU 死亡,4 例病例(3 例患者)治愈出院,住院时间4~10 d,平均7.4 d。出院患者术后均随访,随访时间1~5年,中位数(3.0±2.2)年,随访期间患者均无闭孔疝复发。
3 讨 论
闭孔疝是指腹腔脏器经髋骨闭孔向股三角区(由腹股沟韧带、内收长肌内缘和缝匠肌内缘组成)突出的一种临床罕见的隐匿性腹外疝。疝内容物可为小肠、结肠、网膜、卵巢及输卵管等[3-4]。闭孔是人体中最大的孔,由耻骨上下支与坐骨围成,位于骨盆的前侧壁,其外侧为髋关节、股骨干,内侧为耻骨弓、会阴、股薄肌,下方为耻骨支,外形呈三角形[5]。闭孔是盆腔通至大腿的孔道,正常情况下指尖大小,内有少量脂肪覆盖。闭孔管是一纤维骨性组织,长2~2.5 cm,有内、外2 个口。管内有闭孔神经及血管穿行。闭孔疝位于耻骨肌的深层,股三角区的下端,在闭孔肌的上方,耻骨肌和内收长肌之间。闭孔疝发生除因股三角区潜在薄弱裂隙闭孔管的存在以外,还与老年人盆腔组织退化,多次妊娠和腹内压增加等因素有关[6]。由于闭孔无伸展性固闭孔疝极易发生嵌顿和绞窄,小肠嵌顿最为常见,70%以上闭孔疝以急性肠梗阻首诊,本组5 个病例有4 例(4/5)以急性腹痛来就诊。
流行病学调查发现,闭孔疝好发于亚洲女性,尤以体型消瘦多产的老年女性多见,常称“老太太疝”[7-8],文献报道其男女发病率比为1∶6[9],多与女性闭孔管较男性宽大、平直有关。由于左侧有乙状结肠遮挡,故闭孔疝以右侧疝、单发疝多见,双侧占总闭孔疝发病率为6%[10]。而本组患者左、右侧发病比例为3∶2,1 例患者前后发现闭孔疝1/5。
闭孔疝缺乏特异性的临床表现及体征。70%以上的患者表现为不明的病因急性肠梗阻,当疝囊底部浅,疝内容物可自行复位,表现为反复发作的腹痛[11]。当肠管嵌顿不能回位时,则会出现“痛、呕,闭,胀等”急性机械性肠梗阻的症状。肠管缺血发生坏死、穿孔时,则出现急性腹膜炎、休克的症状及体征。又因闭孔神经位于闭孔的外侧壁,当发生嵌顿时疝内容物压迫神经,会出现闭孔神经分布区从腹股沟部和大腿内侧放射到腘窝的刺激性疼痛、感觉异常或麻木,临床称为Howship-Romberg(HR)征。患者多呈屈髋位,当咳嗽、髋伸直或旋转活动时疼痛加重,患侧下肢屈曲、内收、内旋时疼痛减轻。本组患者仅1 例患者自述有股内侧向下肢放射痛表现。HR 征其敏感性仅有15%~50%[12],且易于骨关节炎易混淆,诊断率低于盆腹腔CT 检查[13]。
闭孔疝术前诊断困难,误诊率60%~100%,主要原因包括:闭孔疝发病率低,临床医师对此病认知甚少,经验不足;加之患者体征特异性不明显误诊率较高[14]。自Meziane 等[15]于1983年首次报道了CT 诊断闭孔疝后,CT 变成为诊断闭孔疝的金标准,其准确率可达90%。此外,多层螺旋CT 不仅可以诊断,也有助于预测肠管嵌顿高危因素、判断有无小肠缺血及肠穿孔诊断[15-16]。CT 疝囊多显示低密度的软组织影,其最常位于为耻骨肌和闭孔肌肉之间、其次闭孔外肌上、下肌束之间,闭孔内、外肌之间最少见。本组5 例中3 例术前行CT检查并明确诊断,1 例胃肠外科会诊术中诊断,1 例术前诊断右侧腹股沟疝术中发现合并右侧闭孔疝。CT 上股疝与闭孔疝影像特点不同,股环的边界,内侧界为腔隙韧带,后界为耻骨梳韧带,前界为腹股沟韧带,外侧界为股静脉内侧的纤维隔。若软组织块在耻骨上支的上方,髂静脉内侧突出则为股疝。若软组织块从耻骨上支的下方,闭孔内肌表面突出来的,考虑诊断闭孔疝。此外,也有应用彩色多普勒超声诊断闭孔疝临床报道[17]。
闭孔疝是一种高致命性疾病,患者常因延误诊断、手术干预延迟及合并肠坏死,导致围手术期病死率高达70%[18]。闭孔疝一旦诊断建议尽早手术,根据有无肠管嵌顿分为急诊手术或择期手术[11,19]。
对于入院评估肠管无坏死的闭孔疝患者,可尝试手法复位后,再行择期手术[20]。手术入路包括传统剖腹探查入路,经腹膜外入路和经腹腔镜入路手术等[21]。修补方式包括直接缝合和补片修补。此外,也有关于借助超声引导下行手法复位后,再行择期行经股入路闭孔疝修补术,以提高围手术期手术的安全性[22-23]。经腹正中剖腹探查是治疗闭孔疝最常见传统的方法。然而随着外科微创技术发展,使用经腹腹膜前修补(TAPP)治疗闭孔疝的报道越来越多[24-25]。鉴于闭孔疝嵌顿肠管多为部分肠管或局部肠管壁,我们认为对于可以耐受气腹,且腹胀较轻的患者,腹腔镜探查与开放手术相比,其具备以下优势:⑴具备更大视野,可全面探查腹腔,可探查有无合并隐匿疝或复合疝;⑵术野更清晰,容易暴露神经血管,减少副损伤;⑶对于肠切除患者可以完全腹腔镜下完成或行加行腹部小切口脱出腹腔后完成肠切除;⑷方便腹腔的冲洗;⑸腹腔干扰小术后胃肠恢复快、进食早、切口感染率低及住院时间短优点[26-27]。但对于下腹部既往有手术史,或肠根阻晚期腹胀严重者,存在肠管副损伤及延长手术时间的弊端,建议慎重选择腹腔镜探查。术中在松解疝环时注意切开方向,避免损伤外上方走形的闭孔血管及闭孔神经,同时术中建议将腹膜外脂肪一并拉出闭孔,以减少因其导致压迫闭孔神经导致相关症状及体征。
对于行闭孔疝合并肠管嵌顿的患者,是否放置补片相关指南未做明确说明。文献[28]报道对于腹腔感染不重的患者,可在充分冲洗腹腔、放置腹腔引流并与患者沟通下可以放置补片,推荐大网孔轻量补片或生物补片修补以增强修补效果。
本组5 例患者中,1 例行单纯修补,1 例患者行肠切除后闭孔疝单纯修补术,其余3 例均放置补片,术后未见补片感染。有研究[29]表明闭孔疝手术行补片修补的患者的3年复发率显著低于直接缝合。单纯行腹膜关闭仅适用于对肠坏疽继发手术区域严重污染的闭孔疝进行紧急缝合,或用于当发现对侧有隐匿性小闭孔疝时的修补。在组患者中,1 例术后转至ICU 因感染性休克、多器官功能衰竭,其余4 例均痊愈出院,随访期间均无复发。
综上所述,对于体型消瘦、有多次生育史的老年女性患者,若出现不明原因的小肠梗阻症状,应考虑有闭孔疝的可能,建议尽早完善腹盆腔CT以明确诊断。对于诊断明确的患者,建议尽早手术治疗。患者条件允许建议腹腔镜探查并修补。依据术中具体情况,选择使用补片以增强修补效果。

