电外科设备临床评价用动物模型研究进展
韦禹帆,钟钰婷,李席如
(1.南开大学医学院,天津 300071;2.解放军医学院,北京 100853;3.解放军总医院第一医学中心普通外科,北京 100853)
0 引言
电外科设备(electrosurgical unit,ESU)是指利用高频电能达到对组织进行切割、分离、止血、消融等手术目的的设备,包括高频电刀、氩气刀、等离子刀和超声刀等,被广泛应用于各种外科手术中。随着新型能量模态的不断发展,将不同能量形式进行结合,可有效提升ESU 的有效性和安全性,但其带来的组织热损伤、对大血管较差的封闭效果以及对神经的损伤等仍是待解决和优化的问题。围手术期注册护士协会的相关数据显示,每年大约有4 万名患者因ESU 导致烧伤[1]。目前,ESU 应用于血管封闭时,只能对≤7 mm 的中小动静脉进行有效封闭,探究如何实现对大血管的有效凝血以及血管封闭效果的影响因素也成为未来的重要课题。此外,ESU 造成的医源性神经损伤也是外科领域重要的问题之一,其热扩散作用可能造成神经轴突和髓鞘的破裂,导致患者术后产生神经麻痹、水肿甚至吸入性肺炎等并发症。
目前,尚无一款经济实用、切割止血效果较好且对周围组织热损伤较小的ESU。临床前动物试验有助于探索和优化ESU,构建离体模型和动物模型,模拟ESU 在人体各组织器官中的切割、止血以及对神经损伤的影响,评估其有效性和安全性。这对于ESU的研发和改进,减少术中出血、缩短手术时间以及减少术后并发症等具有重要的应用价值和临床意义。本文对ESU 临床评价用动物模型的构建方法和评估ESU 有效性和安全性的指标等进行综述,分析其优缺点,并对未来的发展趋势进行展望。
1 动物切割凝血模型
通过构建动物切割凝血模型,可评估ESU 对皮肤和其他器官组织的游离、切割凝血效果以及安全性。随着医疗技术的不断创新和人类对美的追求标准的提升,术后的疤痕修复效果以及其大小、长度等因素也被考虑到手术成功与否的评估标准内。目前,设备刀头局部温度高,对皮肤热损伤大,疤痕形成明显,临床上暂无可直接应用于皮肤切割的ESU。因此构建动物切割凝血模型,用以评估ESU对皮肤的切割凝血效果以及术后的疤痕修复效果具有重要意义。
1.1 模型构建
1.1.1 皮肤创伤愈合模型
猪由于其在生理、解剖结构以及免疫系统上,尤其是表皮、真皮层等皮肤结构组成方面与人体相似,成为了理想的动物实验对象。Bateman 等[2]构建了猪侧腹皮瓣创伤模型,在一个皮瓣区域内直观地对比切口和正常皮肤以评估切口愈合情况。但猪侧腹皮瓣创伤模型对动物的创伤较大且易造成伤口感染,降低试验精准性,因此Scott 等[3]构建了动物背侧垂直创伤切口模型,进一步优化了切口设计。该模型适用于狗等体型细长的动物,切口之间的间距较大,避免了相互影响。皮肤切口愈合过程中存在水肿、炎症和瘢痕形成等情况,动物模型也在逐渐完善以进行不同愈合时间点相关指标的评估。Loh 等[4]构建了皮肤创伤愈合模型,分别在第0 天、第21 天、第28 天、第35 天和第42 天在猪背侧作全层皮肤切口,从而得到不同愈合期创伤切口。不同皮肤愈合观察期的试验设计模拟了临床皮肤切口的愈合过程,对评估术后疤痕修复效果具有重要意义。Wu 等[5]则构建了象限切口模型,使切口以评估指标为标准得以直观分类,但猪皮肤组织未得到充分利用。本研究以猪为研究对象对皮肤创伤愈合模型进行了总结(如图1 所示),但创伤切口大小及间距也需根据具体试验方案调整。皮肤创伤愈合模型是目前应用较为广泛的皮肤模型,可实现不同疤痕愈合期时间点的切口观察,且对皮肤利用度较高。但目前尚无标准化皮肤创伤愈合模型的构建方法,包括模型中愈合期时间点、动物试验部位、切口深度的不同选择等,降低了不同研究间的可比性。

图1 猪皮肤创伤愈合模型
1.1.2 组织器官切割凝血模型
动物组织器官切割凝血模型主要分为离体模型和活体动物模型2 种。离体模型对ESU 的有效性和安全性进行初步探究,活体动物模型模拟其在人体内的应用过程,为临床应用提供证据和前提。ESU 被广泛应用于临床各专科领域中,基于不同应用情景和组织器官,临床评价用动物模型的构建方法也愈丰富。
ESU 因其能有效降低出血量并减少手术时间而被广泛应用于开放性或腔镜下的肝脏及胆囊切除术中。根据ESU 不同的临床应用情景,本文总结了多种动物肝脏切割凝血模型(如图2 所示)。Macdonald等[6]构建了肝脏组织创伤切口模型,切口设计简单有效,且可同时评估ESU 的切割和凝固止血作用。氩离子凝固术可用于器官或组织大面积渗血的处理,Glowka 等[7]比较了氩气刀和氦气刀对肝脏的凝血作用,构建离体肝组织灌注模型并利用钛模具标准化凝血区进行活体猪实验,模拟临床应用情景,适用于非接触型器械的凝血效果评估。Carus 等[8]评估了ESU在微创腔镜手术中对肝脏组织的作用效果,应用脉冲器官灌注训练器在猪离体肝肝组织上进行试验,并对不同ESU 凝固止血效果进行后续的评估分析。目前,对于ESU 在部分复杂且切割凝血方式多样化手术中的应用,如肝叶切除术等,仍难以进行探索和客观的量化评估,未来动物肝脏切割凝血模型的设计应与临床术式相符合。
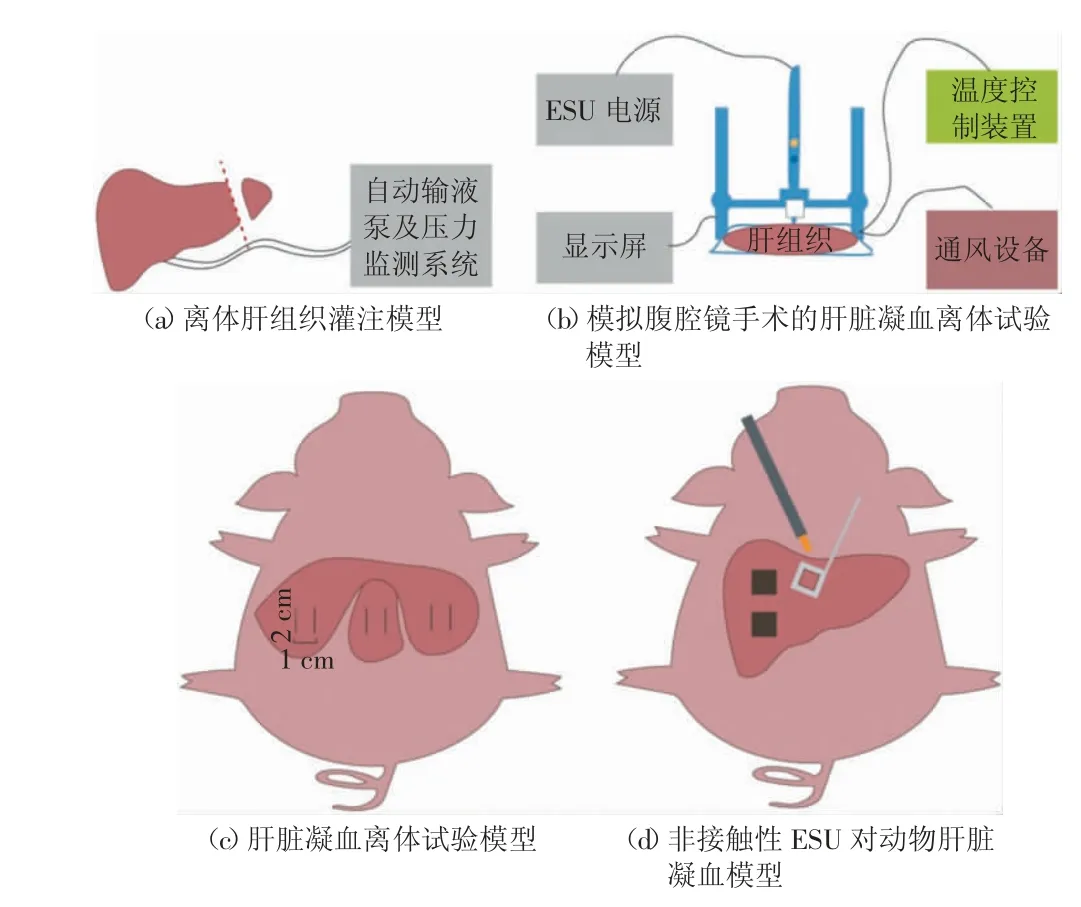
图2 动物肝脏切割凝血模型
ESU 工作时局部温度较高,可能造成皮下脂肪的液化坏死。Applewhite 等[9]通过构建皮肤及皮下组织块切割凝血模型,在组织块的皮下与脂肪交界处横向进行切割凝血,评估超声刀对皮下脂肪的组织热损伤程度。一些骨科和脊柱手术应用ESU 解剖骨骼肌以暴露手术部位,但热损伤影响创伤愈合,导致患者术后疼痛甚至功能受损。Usas 等[10]利用C57BL/6鼠,在其左右两侧腓肠肌中部做50%宽度、100%深度的切口后缝合并分别于术后1、2、4、8 周时间点收集腓肠肌标本,评估ESU 对肌肉组织的损伤程度。通过构建皮下脂肪和肌肉切割凝血模型评估ESU对组织损伤的程度,有助于ESU 的优化,从而减少患者术后脂肪液化坏死、肌肉疼痛及运动功能受损等并发症的发生。
1.2 评价指标
ESU 在切割凝血过程中,失血量、手术烟雾的产生、对组织的急性热损伤程度以及疤痕形成相关指标等均是其重要的评价指标。
1.2.1 热损伤程度
ESU 对组织热损伤程度的影响因素包括使用方法、设备类型及工作时间和相应的功率。局部温度是反映组织热损伤程度和ESU 热扩散较直观的指标。在皮肤创伤愈合模型中,测量局部温度主要通过利用高清晰度热像仪记录每个设备激活期间的热分布并形成热分布图。在组织器官切割凝血模型中,还可以利用T 型热电偶探头插入周围组织,并将探头与温度记录软件相连进行记录分析[9]。Kadesky 等[11]的研究表明,高功率超声切割后在胆管和主动脉等重要结构附近可通过组织学检查发现肉眼未见的热损伤。组织学水平上,ESU 刀头的局部高温使皮肤组织失去正常结构,组织细胞破裂融合成片状,纤维肿胀变宽,发生玻璃样变,形成凝固坏死区。ESU 对组织的侧向热损伤程度主要就是通过对伤口进行组织学切片染色处理,光镜下测量组织凝固坏死深度进行评估的。
1.2.2 疤痕形成相关指标
疤痕是创伤后皮肤修复和愈合过程中引起的正常皮肤组织的外观形态和组织病理学的改变,其愈合过程分为局部炎症反应期、细胞增殖分化及肉芽组织形成期和组织重建期3 个阶段。ESU 因其合并侧向热损伤往往造成周围组织的缺血坏死甚至碳化,对疤痕修复不利。
目前,常用以监测皮肤疤痕物理特征的参数包括颜色、表面积、深度和柔韧性等(如图3 所示[12])。皮肤颜色异常是疤痕患者的常见症状,可通过色度计确定反射光强度并利用光吸收模式来量化色素沉着,以及通过激光多普勒测定血流灌注和血管分布。皮肤疤痕表面积是评估疤痕形成较为直观的指标,包括透明示踪或摄影方法等。而疤痕深度则是为了量化总体疤痕体积。皮肤疤痕柔韧性的测量主要包括压力、吸引、扭转和张力等参数。柔韧性较好的疤痕可与正常皮肤一起滑动和拉伸,发挥正常的生理功能,增加患者疤痕愈合的满意度。Lucas 等[13]的研究显示,创伤早期的炎症反应能促进组织和疤痕修复,而创伤后期炎性细胞过度浸润则会影响愈合效果,测定炎症细胞浸润程度(如T 淋巴细胞、巨噬细胞等)可反映创伤切口愈合情况。

图3 皮肤疤痕物理特征的参数测量示意图[12]
1.2.3 其他相关指标
动物切割凝血模型中,失血量是评估凝血效果最直观的指标之一。失血量可以通过滤纸直接放置于创伤伤口处60 s,并将滤纸扫描为数字图像格式定量分析得到。手术烟雾是ESU 高温灼烧组织导致蛋白质不完全燃烧而产生的混合物。Karjalainen 等[14]通过定制手术切割和烟雾浓度标准化平台结合低压电子冲击器,对ESU 在猪各种组织器官中应用时产生的烟雾进行颗粒分析和评估,以期减少ESU 在应用过程中产生的烟雾,在清晰手术视野等方面得到优化和提升。
2 血管封闭模型
目前,越来越多的血管封闭器械应用于腔镜手术中,促进了腔镜手术的发展,可对中小动静脉进行有效封闭,临床上大血管的封闭仍以缝合结扎及应用止血夹等方法为主,探究如何实现对大血管的有效凝血封闭以及血管封闭效果与血管其他特性有无关联也是未来的重要课题之一。
2.1 模型构建
离体模型是对ESU 血管封闭有效性的初步探索,目前以采集动物脾、胃、肠系膜及颈动静脉试验为主,利用不同血管封闭器械进行凝血封闭并评估血管最大破裂压力等指标[15-16]。此外,离体模型简单方便,也可进行血管封闭性能影响等机制层面的探究。Wyatt 等[17]通过改变猪离体颈总动脉用于血管封闭的大小和形态,并以弹性蛋白染色程度评估封闭质量,提出双极血管封闭设备可封闭<5 mm 的血管,且其凝血效果与血管形态无关。但实施动物体内试验仍然是必要的,其优点包括可设置观察期、进行体内环境支持下的动态指标评估及模拟临床情境等。Diamantis 等[18]利用ESU 对新西兰大白兔的胃短动静脉凝血,并设置了不同长度的观察期,通过剖腹探查,记录胃组织受损程度、腹腔游离液体量等参数和术后穿孔等并发症,比较了4 种血管封闭器械的凝血效能。Schuld 等[19]利用猪肠系膜动静脉评估2 种不同ESU 的凝血效果并通过动态热成像评估了其热性能。而Crispi 等[20]则构建了猪体内血管封闭模型,评估切割不同血管时和切开后10 min 2 个时间点,在正常血压和药物诱导动脉高压2 种状态下超声刀的血管封闭效果,模拟了其在体内的应用,术中情况如图4(a)所示。但Crispi 等[20]的研究模型构建的局限性在于观察时间较短且无法评估动物术后状态。Kraemer 等[21]通过2 个阶段手术,弥补了其观察期短、评估指标不足等问题。
2.2 评价指标
Newcomb 等[16]通过使用输液泵向血管内注入恒定流速的生理盐水,持续监测血管内压力,记录血管破裂前的最大压力,评估ESU 的血管封闭效果,如图4(b)所示。Katsuno 等[22]在此基础上设计了靛蓝-胭脂红染色生理盐水输液装置,最大破裂压力即从血管残根处观察到的彩色生理盐水渗漏点处的压力,可直观评价ESU 止血效能,该装置示意图如图4(c)所示。有研究显示血管胶原蛋白、弹性蛋白与血管最大破裂压力有关,可能对血管封闭效果具有预测作用[23]。此外,电极压力也是影响封闭质量的重要因素之一。Chen 等[24]通过在双极血管封闭器械手柄上安装一个压阻式力传感器,测量操作者对手柄施加的力以评估手柄压力与血管最大破裂压力之间的关系。
此外,对于局部温度测量和热损伤程度的评估,除前文所提及的方法外,马森染色和天狼猩红染色2 种特殊染色技术可以对组织切片中血管胶原蛋白和肌纤维可视化,尤其是变性的热损伤区,这使得热损伤程度的评估更加精准和直观,典型血管热封闭的马森染色切片图像如图4(d)所示[21]。此外,还有研究针对ESU 血管封闭过程中凝血效果、组织粘连程度、横断效果等设计了评分量表,以提高评估的精准性和客观性[25]。
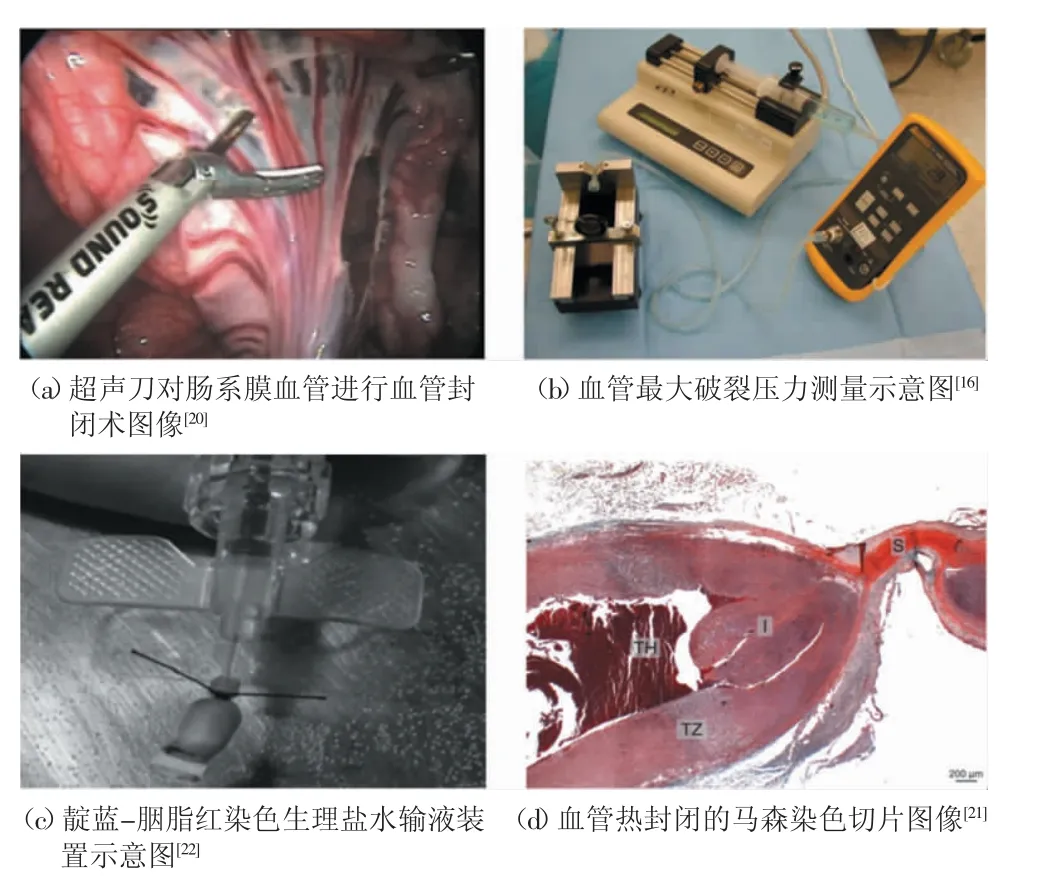
图4 血管封闭模型及其评价指标测量图
3 神经损伤模型
ESU 因其较好的切割止血和血管封闭效果而得到广泛应用,但医源性神经损伤使其在神经周围组织的应用仍具有一定的限制,如前列腺切除术、脑外科手术、头颈外科手术和脊柱手术等。
3.1 模型构建
神经损伤模型目前研究较少,大部分动物模型的构建仍以甲状腺手术模型为主。甲状腺切除术等术中应用ESU 可能会引起暂时性喉返神经麻痹甚至损伤。鼠的坐骨神经走行方式、大小与人体喉返神经相似,是较合适的喉返神经损伤模型实验动物。超声刀由于依靠机械能完成切割作用,无电流通过组织,对周围组织热损伤较小[26]。为探究超声刀对神经热损伤和功能作用的影响程度,Carlander 等[27]构建了鼠的坐骨神经刺激模型并在手术前后进行肌电图检测。Chen 等[28]通过实行假手术的方式对坐骨神经刺激模型进行了完善,经大腿后外侧入路暴露坐骨神经,并于距坐骨神经不同距离的股二头肌表面激活器械、进行切割或实行假手术,手术前后诱发神经复合动作电位以检测神经电生理功能。Chen 等[28]的研究考虑到ESU 应用距离对神经的影响,得到了ESU 应用时的安全距离,这一发现有助于规范临床电刀的操作,减少患者术后并发症的产生。由于鼠坐骨神经与人体之间仍具有差异,犬、猪等大型动物也可应用于神经损伤模型的构建[9]。Yang 等[29]利用超声刀和LigaSure 对犬模型进行甲状腺手术,术中距喉返神经不同距离激发ESU,通过监测肌电图及组织学观察甲状腺组织形态和喉返神经超微结构,评估犬模型甲状腺手术中应用止血能量外科设备的可行性。
3.2 评价指标
动物神经损伤模型评估指标主要包括对神经的热损伤检测、功能检测以及形态学观察3 个方面。热损伤的检测包括局部温度测量和组织学检测,后者通过对神经节段进行HE 染色,观察神经血管和炎症细胞变化。功能检测主要通过记录肌电图电位进行评估[30]。形态学上通过病理学检查,光镜下观察神经轴突、髓鞘形态,并参考卡兰德等级评分以评估其损伤程度[31]。
4 各模型构建方法优缺点分析
构建ESU 临床评价用动物模型,通过热损伤程度、失血量等指标对ESU 的有效性和安全性进行评估,有助于探索新型能量模态、优化能量转化方式及参数,减少组织损伤、神经损伤并提升止血效能,为ESU 的优化和改进提供重要线索和证据支持。但目前的动物模型构建方法也存在一定问题:(1)尚无标准化动物模型设计。既往动物模型的构建方法多种多样,各具侧重和创新,利弊共存,但尚未标准化,降低了不同研究间的可比性。(2)与临床应用的差异。活体动物模型可为临床应用提供前提,但无法满足多样化的临床手术情景需求,需提高动物模型和临床应用一致性,根据不同临床应用情景提供相应的模型构建方案。(3)尚未形成统一的ESU 动物模型评价体系。部分评价指标具有主观性和差异化,如热损伤凝固坏死区域的判定、血管有效封闭的标准及神经损伤程度的分级等。且仍有部分性能无法通过客观有效的评价方法和数据描述,如ESU 应用过程中所产生烟雾的性质、量的测定及切割组织的流畅度等,均是动物模型构建和评价过程中亟待解决和优化的问题。
5 结语
电外科是一个正蓬勃发展、研究不断更新的领域。ESU 可实现切割、分离、止血、消融等手术目的,除本文提及的高频电刀、超声刀等传统ESU 外,一些新型能量器械也逐渐应用于临床各领域手术中,如等离子电刀、激光刀等。ESU 的探索和优化过程仍需大量的离体和活体动物模型试验,以减少组织热损伤、出血和神经麻痹等问题。而随着电外科领域的不断发展,手术机器人、编程软件自动化样本切除装置及影像学检测等手段减少了人为操作带来的误差和偏倚,提高了实验精准性[32-35]。未来ESU 临床评价用动物模型的发展应与人工智能、计算机信息自动化等技术相结合,将动物模型设计标准化的同时形成统一的评价体系,应更加满足临床实际应用的需求,促进ESU 的不断优化和改进。

